文档内容
广东仲元中学 2020 学年第二学期期中考试
高一年级化学必修第一册、第二册模块试卷
本卷共20小题,满分100分,考试时间75分钟
相对原子质量: H-1 C-12 N-14 0-16 Na-23 Al-27 S-32 CI-35.5
第一卷(选择题,共44分)
一、选择题。(本题共16小题,共44分。第1-10小题,每小题2分:第11-16题,每小题4
分。在每小题给出的四个选项中,只有一项是符合题目要求)
1. 下列叙述错误的是
A. 酒精的主要成分是乙醇,其在水溶液或熔融状态下不能导电,因此属于非电解质
的
B. 乙烯可用于制备聚乙烯塑料、乙醇等,是重要 化工原料,因此乙烯的产量是衡量一个国家石油化工
发展水平的标志
C. 我国西气东输的气体天然气主要成分是甲烷,由于甲烷燃烧放出大量的热,其产物无污染,因此属于
一种可再生的清洁能源
D. 酸雨对环境危害巨大,形成酸雨的主要原因是含硫、含氮物质的排放。
2. 下列表示物质结构的化学用语正确的是
A. 空间充填模型 可以表示甲烷分子,也可以表示四氯化碳分子
B. 乙烯C H 的结构简式:CHCH
2 4 2 2
C. 乙醇的结构式是
D. NH 的电子式:
3
3. 物质类别和核心元素的价态是学习元素及其化合物性质的重要认识视角。如图是某元素的“价类二维图”,
其中单质b是黄色固体,f、h均为正盐,且焰色都是黄色。下列说法不正确的是A. d能使品红溶液褪色
B. a和c反应可以生成b
C. e的浓溶液可用铝槽车运输
D. h的水溶液呈碱性
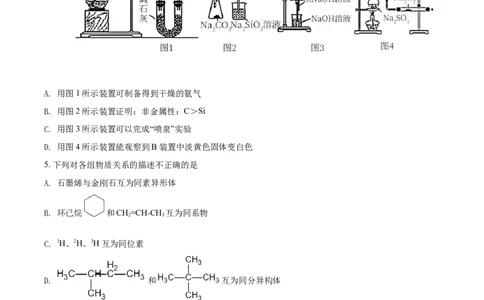
4. 下列有关实验装置进行的相应实验,不能达到实验目的的是
A. 用图1所示装置可制备得到干燥的氨气
B. 用图2所示装置证明:非金属性:C>Si
C. 用图3所示装置可以完成“喷泉”实验
D. 用图4所示装置能观察到B装置中淡黄色固体变白色
5. 下列对各组物质关系的描述不正确的是
A. 石墨烯与金刚石互为同素异形体
B. 环已烷 和CH=CH-CH 互为同系物
2 3
C. 1H、2H、3H互为同位素
D. 和 互为同分异构体
6. 下列各反应中属于加成反应的是
①CH=CH +H O CHCHOH
2 2 2 3 2
②H+Cl 2HCl
2 2
③CHCH=CH+H CHCHCH
3 2 2 3 2 3④5CH=CH +12KMnO +18H SO →10CO↑+28H O+6KSO +12MnSO
2 2 4 2 4 2 2 2 4 4
⑤2CHCHOH+2Na→2CH CHONa+H ↑
3 2 3 2 2
A. ①②③ B. ②③⑤ C. ①④ D. ②③④
7. 下列实验能达到预期目的是
选项 实验内容 实验目的
A 加热盛有浓硫酸和碳的试管 探究浓硫酸的脱水性
B 向FeSO 溶液中加入KSCN溶液 检验FeSO 部分变质
4 4
C 向某未知溶液中加入BaCl 溶液后,再加入稀硝酸,观察沉淀的生成 检查是否含有SO
2
D 向某未知溶液中加入NaOH固体,加热,在管口用湿润的红色石蕊试纸检验 检验是否含NH
A. A B. B C. C D. D
8. 下列现象及解释均正确的是
A. 向氯化铝溶液中滴加过量氨水后,无白色沉淀产生:AI3++4NH·H O=AlO +4NH +2H O
3 2 2
B. 浓盐酸与MnO 反应有黄绿色气体产生:MnO +4HCl(浓) Mn2++2Cl—+Cl↑+2H O
2 2 2 2
C. 水晶手镯接触石灰水会被腐蚀:SiO+Ca(OH) =CaSiO +H O
2 2 3 2
D. 不用铜盆盛放食醋:2CHCOOH+Cu=Cu2++2CH COO—+H ↑
3 3 2
9. 下列关于天然橡胶( )的叙述中,不正确的是
A. 天然橡胶是天然高分子化合物
B. 天然橡胶不能燃烧
C. 天然橡胶能使酸性高锰酸钾溶液褪色
D. 天然橡胶含有双键,能发生加成反应
10. 类比是研究物质性质的常用方法之一,可预测许多物质的性质,但类比是相对的,不能违背客观事实。
下列各种类比推测的说法中正确的是
.
A 加热条件下,已知 Fe与S能直接化合生成FeS,推测Cu与S可直接化合生成Cu S
2
B. 已知Mg加入CuSO 溶液中 Mg+ Cu2+= Cu + Mg2+,推测 Na加入到CuSO 溶液中2Na + Cu2+= Cu+2Na
4 4
C. 加热条件下,已知足量Cu与浓硫酸反应只生成SO ,推测足量铝与浓硫酸反应也只生成SO
2 2D. 已知足量Fe与稀硝酸反应生成Fe(NO ),推测点燃时足量Fe与Cl 反应生成FeCl
3 2 2 2
11. 某烃的结构简式如下图,下列说法中正确的是
A. 该烃的命名是邻二甲苯
B. 该烃不能发生加成反应
C. 该烃苯环上的一氯代物共有4种
D. 分子中最多有14个原子处于同一平面上
12. 下列说法错误的是(设N 为阿伏伽德罗常数的值)
A
A. 1mol C HCl分子中其共价键数目为7N
2 5 A
B. 100g质量分数为46%的乙醇(C HO)水溶液含氧原于数目为4N
2 6 A
C. 3.4g氨气中含有N—H键的数目为0.6N
A
D. 50mL 18.4mol/L浓硫酸与足量铜充分反应,生成SO 分子的数目为0.46N
2 A
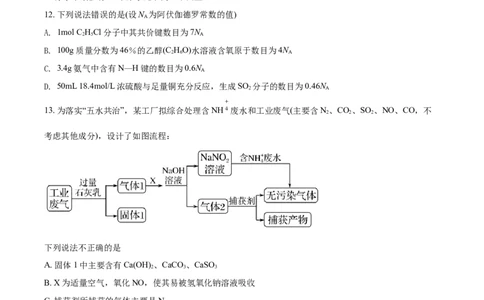
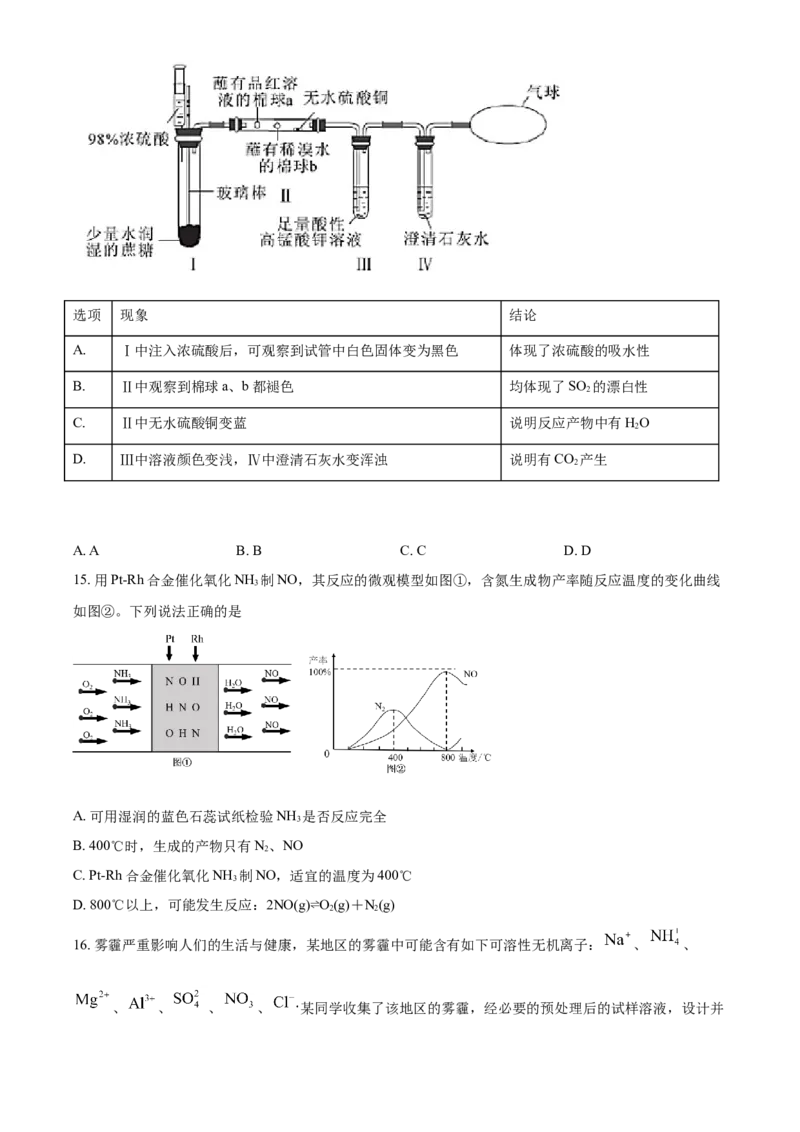
13. 为落实“五水共治”,某工厂拟综合处理含NH 废水和工业废气(主要含N、CO、SO 、NO、CO,不
2 2 2
考虑其他成分),设计了如图流程:
下列说法不正确的是
A. 固体1中主要含有Ca(OH) 、CaCO 、CaSO
2 3 3
B. X为适量空气,氧化NO,使其易被氢氧化钠溶液吸收
C. 捕获剂所捕获的气体主要是N
2
D. 处理含 NH 废水时,发生反应的离子方程式为 NH +NO =N ↑+2H O
2 2
的
14. 某同学设计了蔗糖与浓硫酸反应 改进装置,并对气体产物进行检验,实验装置如图所示。下列结论
中正确的是( )选项 现象 结论
A. Ⅰ中注入浓硫酸后,可观察到试管中白色固体变为黑色 体现了浓硫酸的吸水性
B. Ⅱ中观察到棉球a、b都褪色 均体现了SO 的漂白性
2
C. Ⅱ中无水硫酸铜变蓝 说明反应产物中有HO
2
D. Ⅲ中溶液颜色变浅,Ⅳ中澄清石灰水变浑浊 说明有CO 产生
2
A. A B. B C. C D. D
15. 用Pt-Rh合金催化氧化NH 制NO,其反应的微观模型如图①,含氮生成物产率随反应温度的变化曲线
3
如图②。下列说法正确的是
A. 可用湿润的蓝色石蕊试纸检验NH 是否反应完全
3
B. 400℃时,生成的产物只有N、NO
2
C. Pt-Rh合金催化氧化NH 制NO,适宜的温度为400℃
3
D. 800℃以上,可能发生反应:2NO(g)⇌O(g)+N(g)
2 2
16. 雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下可溶性无机离子: 、 、
、 、 、 、 某同学收集了该地区的雾霾,经必要的预处理后的试样溶液,设计并完成了如下实验:
已知: ,根据以上的实验操作和现象,该同学得出的结论
不正确的是
A. 试样中肯定存在 、 、 和
B. 试样中一定不含
C. 试样中可能存在 、
D. 该雾霾中可能存在 、 和
第二卷(非选择题,4大题,共56分)
17. 1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字
母分别代表某一化学元素。
(1)元素c代表的元素是(写元素符号)_______
(2)请写出元素e在元素周期表中所在的位置_______
(3)请画出元素f的简单离子结构示意图_______。请写出单质f与d的最高价氧化物对应水化物的离子反
应方程式_______。
(4)元素a和b能构成最简单的有机化合物(用结构式表示)_______。请写出元素a和b构成的最简单有机
化合物与i单质发生的第一步化学反应方程式_______。(5)元素h的最高价氧化物对应的水化物呈_______(酸性、中性或碱性);请写出元素h的最高价氧化物
对应的水化物与单质b的化学反应方程式_______。
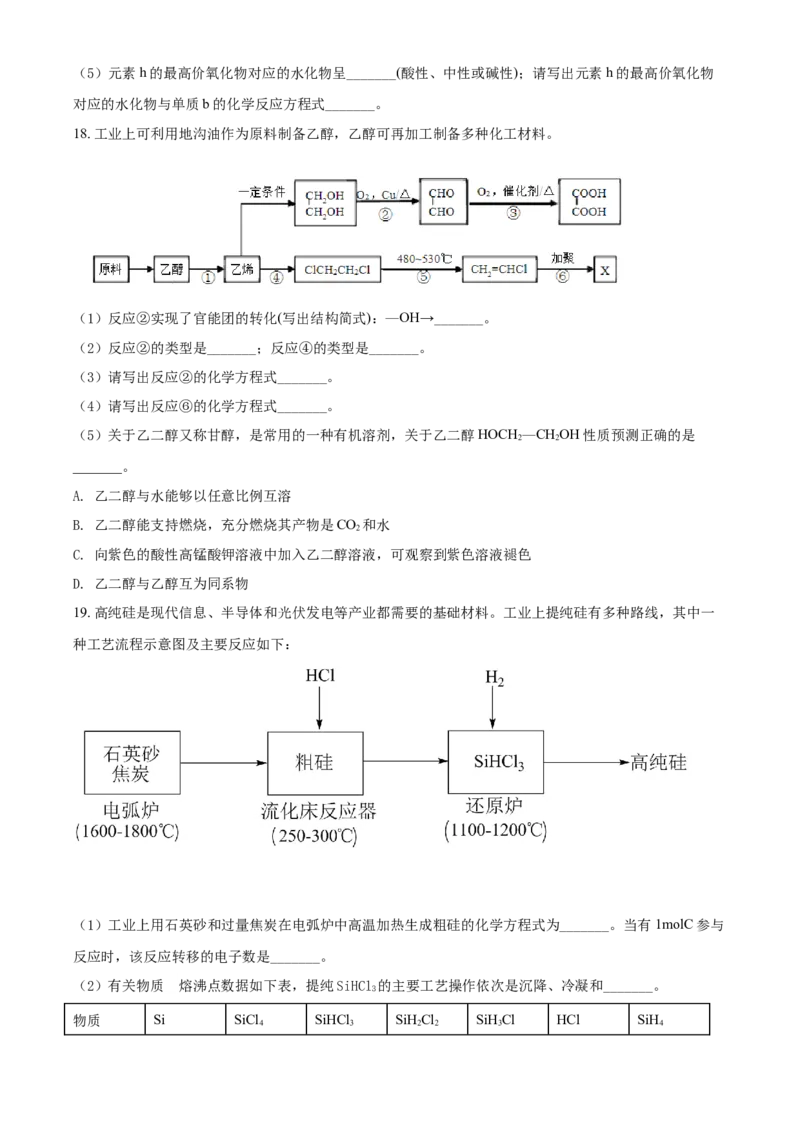
18. 工业上可利用地沟油作为原料制备乙醇,乙醇可再加工制备多种化工材料。
(1)反应②实现了官能团的转化(写出结构简式):—OH→_______。
(2)反应②的类型是_______;反应④的类型是_______。
(3)请写出反应②的化学方程式_______。
(4)请写出反应⑥的化学方程式_______。
(5)关于乙二醇又称甘醇,是常用的一种有机溶剂,关于乙二醇HOCH —CHOH性质预测正确的是
2 2
_______。
A. 乙二醇与水能够以任意比例互溶
B. 乙二醇能支持燃烧,充分燃烧其产物是CO 和水
2
C. 向紫色的酸性高锰酸钾溶液中加入乙二醇溶液,可观察到紫色溶液褪色
D. 乙二醇与乙醇互为同系物
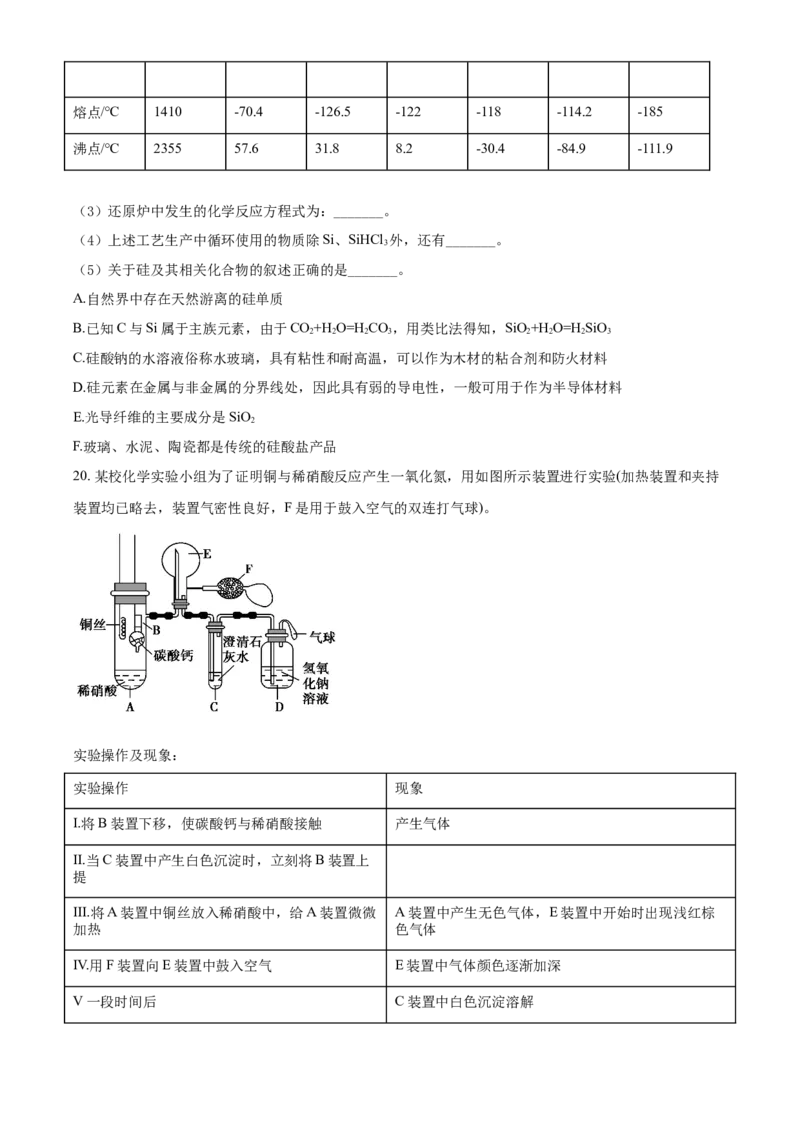
19. 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一
种工艺流程示意图及主要反应如下:
(1)工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为_______。当有 1molC参与
反应时,该反应转移的电子数是_______。
(2)有关物质 的熔沸点数据如下表,提纯SiHCl 的主要工艺操作依次是沉降、冷凝和_______。
3
物质 Si SiCl SiHCl SiHCl SiHCl HCl SiH
4 3 2 2 3 4熔点/℃ 1410 -70.4 -126.5 -122 -118 -114.2 -185
沸点/℃ 2355 57.6 31.8 8.2 -30.4 -84.9 -111.9
(3)还原炉中发生的化学反应方程式为:_______。
(4)上述工艺生产中循环使用的物质除Si、SiHCl 外,还有_______。
3
(5)关于硅及其相关化合物的叙述正确的是_______。
A.自然界中存在天然游离的硅单质
B.已知C与Si属于主族元素,由于CO+H O=HCO,用类比法得知,SiO+H O=HSiO
2 2 2 3 2 2 2 3
C.硅酸钠的水溶液俗称水玻璃,具有粘性和耐高温,可以作为木材的粘合剂和防火材料
D.硅元素在金属与非金属的分界线处,因此具有弱的导电性,一般可用于作为半导体材料
E.光导纤维的主要成分是SiO
2
F.玻璃、水泥、陶瓷都是传统的硅酸盐产品
20. 某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持
装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。
实验操作及现象:
实验操作 现象
I.将B装置下移,使碳酸钙与稀硝酸接触 产生气体
II.当C装置中产生白色沉淀时,立刻将B装置上
提
III.将A装置中铜丝放入稀硝酸中,给A装置微微 A装置中产生无色气体,E装置中开始时出现浅红棕
加热 色气体
IV.用F装置向E装置中鼓入空气 E装置中气体颜色逐渐加深
.
V一段时间后 C装置中白色沉淀溶解试回答下列问题:
(1)操作I中产生气体的化学式为_______。操作I的目的是_______。D装置的作用是_______。
(2)C装置中白色沉淀的化学式是_______。操作II中当C装置中产生白色沉淀时立刻将B装置上提的原
因是_______。
(3)操作III中A装置中产生无色气体的化学方程式是_______。
(4)E装置内气体颜色逐渐加深的原因是_______。
(5)操作V现象产生的原因是(用两个化学方程式说明)_______,_______。