文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”考后提升卷(江西卷)
高三化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ca 40 Co 59
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.2023年10月26日11时14分,神舟十七号载人飞船点火升空成功发射,我国航天航空事业再次迎来飞
速发展。下列有关说法错误的是
A.太阳电池翼采用的碳纤维框架和玻璃纤维框架均为无机非金属材料
B.返回舱降落回收过程中使用了芳纶制作的降落伞,芳纶是有机高分子材料
C.飞船舱体外壳部件材料是铝合金材料制成,主要是利用了其密度大、硬度大的特性
D.新型火箭燃料煤基航天煤油主要由不同馏分的烷烃、芳香烃和烯烃类的碳氢化合物组成
2. 是一种液态化合物,其与水反应的化学方程式为: ,下列说法错误
的是
A. 的结构式为 B.氯离子的结构示意图为
C.键角: D. 与 的空间结构相同
3.某兴趣小组以活性白土为催化剂进行乙醇脱水制备乙烯的实验,装置如图所示(夹持装置已略去)。下列
说法正确的是
A.实验时,冷凝水从a口进b口出
B.加快圆底烧瓶中乙醇的汽化速率,有利于提高乙醇的转化率更多全科试卷,请关注公众号:高中试卷君
C.溴的四氯化碳溶液褪色,不能说明生成了乙烯气体
D.当有4.6g乙醇汽化时,具支试管中收集到2.0g液体,则乙醇的转化率约为93%
4.过二硫酸钾( ,其中S为 价)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶
液制备。它在100℃下能发生分解反应: (未配平),设 为阿伏加德罗常
数的值,下列说法正确的是
A. 中含有非极性共价键的数目为
B. 分解,生成 的分子数为
C.标准状况下, 含有的原子数为
D. 溶液中的离子总数为
5.下列实验目的对应的实验操作正确的是
选
实验目的 实验操作
项
A 证明活泼性:Na > Cu 将少量Na投入CuSO 溶液中,观察是否产生红色固体
4
证明酸性:HSO >
2 3
B 将SO 通入漂白粉溶液,观察是否变浑浊
2
HClO
C 证明HSO 具有氧化性 将少量稀硫酸滴入NaSO 溶液,观察是否产生刺激性气味的气体
2 4 2 2 3
D 证明淀粉已水解完全 取适量淀粉水解液,滴入几滴碘水,观察溶液是否变蓝
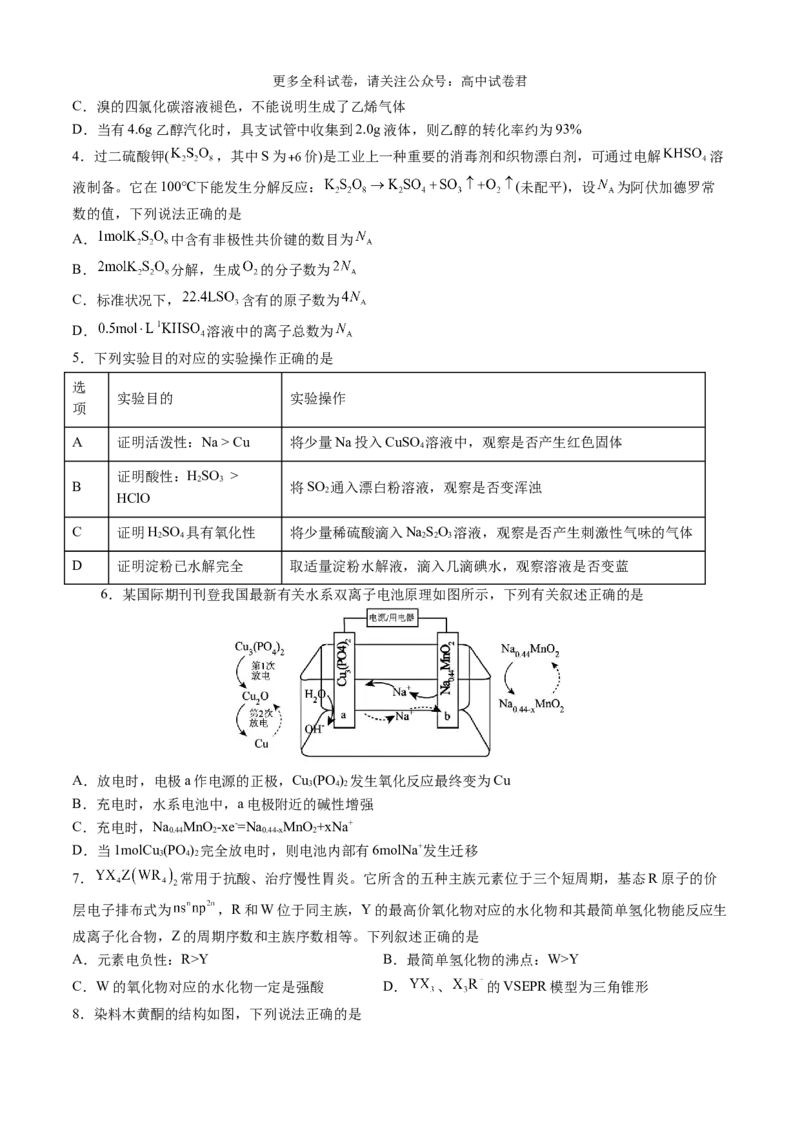
6.某国际期刊刊登我国最新有关水系双离子电池原理如图所示,下列有关叙述正确的是
A.放电时,电极a作电源的正极,Cu (PO ) 发生氧化反应最终变为Cu
3 4 2
B.充电时,水系电池中,a电极附近的碱性增强
C.充电时,Na MnO -xe-=Na MnO +xNa+
0.44 2 0.44-x 2
D.当1molCu (PO ) 完全放电时,则电池内部有6molNa+发生迁移
3 4 2
7. 常用于抗酸、治疗慢性胃炎。它所含的五种主族元素位于三个短周期,基态R原子的价
层电子排布式为 ,R和W位于同主族,Y的最高价氧化物对应的水化物和其最简单氢化物能反应生
成离子化合物,Z的周期序数和主族序数相等。下列叙述正确的是
A.元素电负性:R>Y B.最简单氢化物的沸点:W>Y
C.W的氧化物对应的水化物一定是强酸 D. 、 的VSEPR模型为三角锥形
8.染料木黄酮的结构如图,下列说法正确的是更多全科试卷,请关注公众号:高中试卷君
A.分子式为C H O
15 9 5
B.经核磁共振氢谱测定,分子中存在4种官能团
C.1mol该物质与足量溴水反应,最多可消耗4mol Br
2
D.1mol该物质与足量H 反应,最多可消耗8molH
2 2
9.某学习小组进行了如下实验:
下列说法正确的是
A.键角: 中的∠H-O-H大于 中的∠H-N-H
B.步骤①的实验现象说明了 和 的结合能力比 和 的强
C.步骤②的实验现象说明了 的氧化性强于
D.工业上常利用上述转化实现空气中氧气的分离与提纯
10.常见的塑料包括PS(聚苯乙烯)、亚克力(聚甲基丙烯酸甲酯)、PC( )、
PET( )等。下列说法正确的是
A.PS的单体存在顺反异构体
B.亚克力的单体中共面的原子最多有10个
C.PC和PET均可通过缩聚反应生成
D.PET的单体分别与苯甲酸、甘油互为同系物
11.周期表中VIA族元素及其化合物应用广泛。 、 、 是氧元素的3种核素,可以形成多种重要
的化合物。亚硫酰氯 为黄色液体,其结构式为( ),遇水发生水解。工业上可电解
HSO 与 混合溶液制备过二硫酸铵 ,过二硫酸铵与双氧水中都含有过氧键(-O-
2 4
O-)。硝化法制硫酸的主要反应为: 。SO 和SO
2 3
都是酸性氧化物,是制备硫酸的中间产物。下列有关
,下列说法正确的
A.该反应中反应物的总能量低于生成物的总能量
B.反应达平衡后,分离出少量SO ,正反应速率加快
3
C.其他条件不变,平衡后继续充入NO ,平衡常数将减小
2
D.该反应中消耗22.4LNO ,转移电子的数目为2×6.02×1023
2
12.乙二胺四乙酸(EDTA)是一种常用的配位试剂,可以与金属离子形成稳定的配合物。在水质分析中,
EDTA常用于测定水中钙、镁含量。EDTA滴定法测定有机物中钙含量的基本步骤如下:更多全科试卷,请关注公众号:高中试卷君
①EDTA标定
称取0.1000gEDTA,溶于100mL去离子水中,取10.00mL0.1mol·L-1标准CaCl 溶液,加入3滴甲基橙溶液
2
作指示剂,用配制的EDTA溶液滴定,终点时,消耗EDTA溶液体积为 。
②钙提取
称取一定质量的有机物,用酸性KMnO 溶液氧化有机物,将有机物中的金属经萃取、反萃取到水中得到提
4
取液。
③杂质掩蔽及调pH
用掩蔽剂将提取液中除钙之外的金属掩蔽,防止对钙含量测定造成干扰;根据选择的指示剂变色范围,将
提取液的pH调到11.3。
④EDTA滴定
取20.00mL提取液,加入钙黄绿素为指示剂,钙与钙黄绿素生成能发出绿色荧光的配合物,在黑色背景下
用标定后的EDTA溶液滴定,终点时,消耗EDTA溶液体积为 。
上述过程中,EDTA与钙反应时物质的量之比均为1:1。
对于上述实验,下列说法正确的是( )
A.量取标准CaCl 溶液时,选用规格为10mL的量筒
2
B.实验室中萃取、反萃取时,使用的主要仪器为长颈漏斗
C.提取液中钙含量为
D.EDTA滴定时,溶液绿色荧光消失即可判定滴定终点
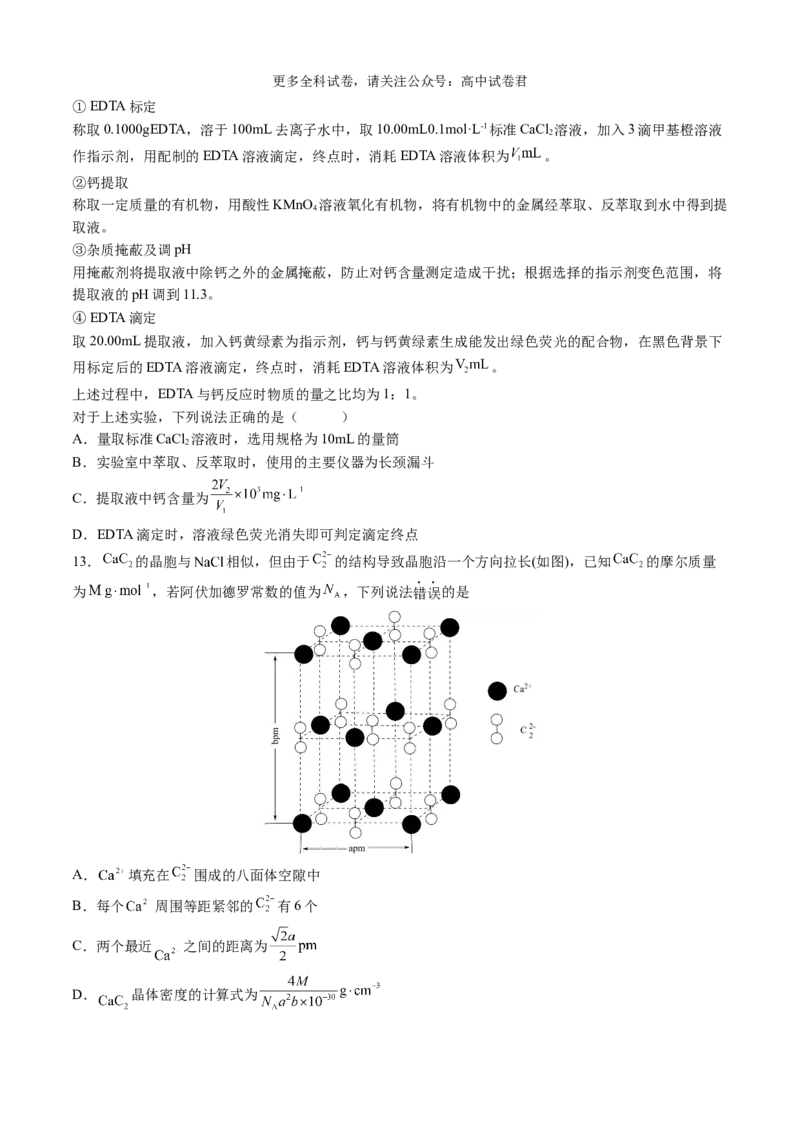
13. 的晶胞与 相似,但由于 的结构导致晶胞沿一个方向拉长(如图),已知 的摩尔质量
为 ,若阿伏加德罗常数的值为 ,下列说法错误的是
A. 填充在 围成的八面体空隙中
B.每个 周围等距紧邻的 有6个
C.两个最近 之间的距离为
D. 晶体密度的计算式为更多全科试卷,请关注公众号:高中试卷君
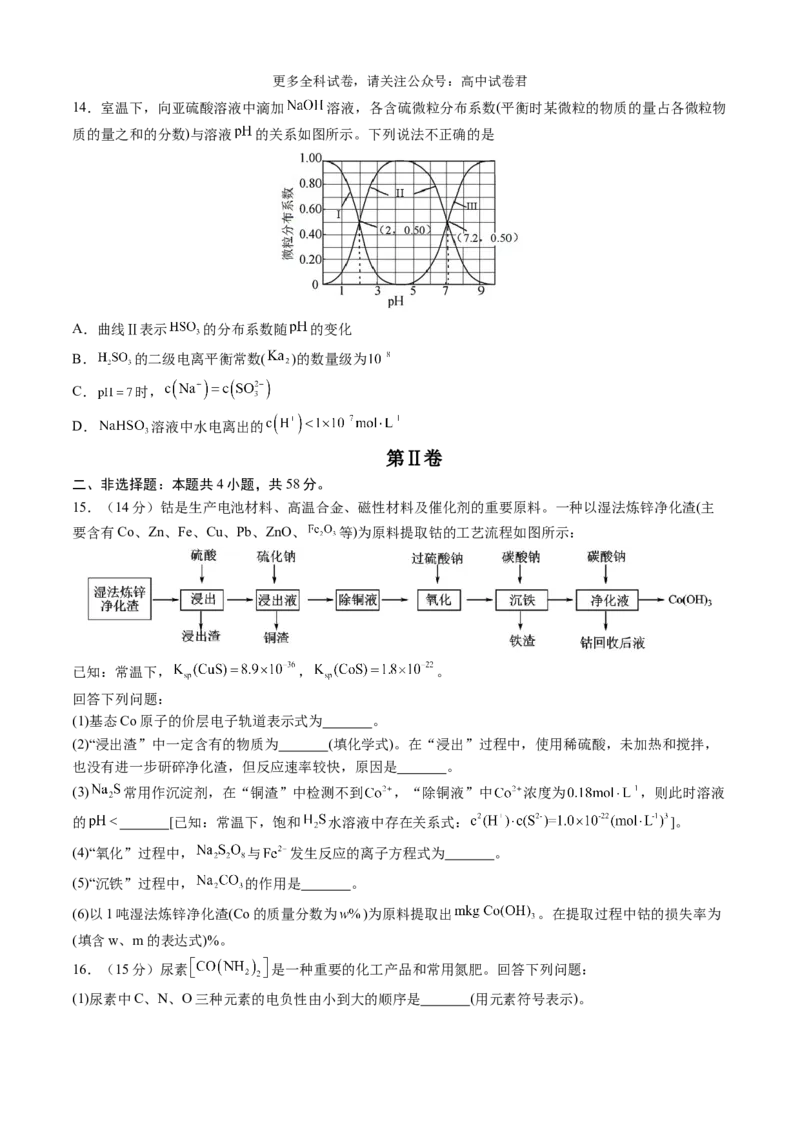
14.室温下,向亚硫酸溶液中滴加 溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物
质的量之和的分数)与溶液 的关系如图所示。下列说法不正确的是
A.曲线Ⅱ表示 的分布系数随 的变化
B. 的二级电离平衡常数( )的数量级为
C. 时,
D. 溶液中水电离出的
第Ⅱ卷
二、非选择题:本题共4小题,共58分。
15.(14分)钴是生产电池材料、高温合金、磁性材料及催化剂的重要原料。一种以湿法炼锌净化渣(主
要含有Co、Zn、Fe、Cu、Pb、ZnO、 等)为原料提取钴的工艺流程如图所示:
已知:常温下, , 。
回答下列问题:
(1)基态Co原子的价层电子轨道表示式为 。
(2)“浸出渣”中一定含有的物质为 (填化学式)。在“浸出”过程中,使用稀硫酸,未加热和搅拌,
也没有进一步研碎净化渣,但反应速率较快,原因是 。
(3) 常用作沉淀剂,在“铜渣”中检测不到 ,“除铜液”中 浓度为 ,则此时溶液
的 [已知:常温下,饱和 水溶液中存在关系式: ]。
(4)“氧化”过程中, 与 发生反应的离子方程式为 。
(5)“沉铁”过程中, 的作用是 。
(6)以1吨湿法炼锌净化渣(Co的质量分数为 )为原料提取出 。在提取过程中钴的损失率为
(填含w、m的表达式)%。
16.(15分)尿素 是一种重要的化工产品和常用氮肥。回答下列问题:
(1)尿素中C、N、O三种元素的电负性由小到大的顺序是 (用元素符号表示)。更多全科试卷,请关注公众号:高中试卷君
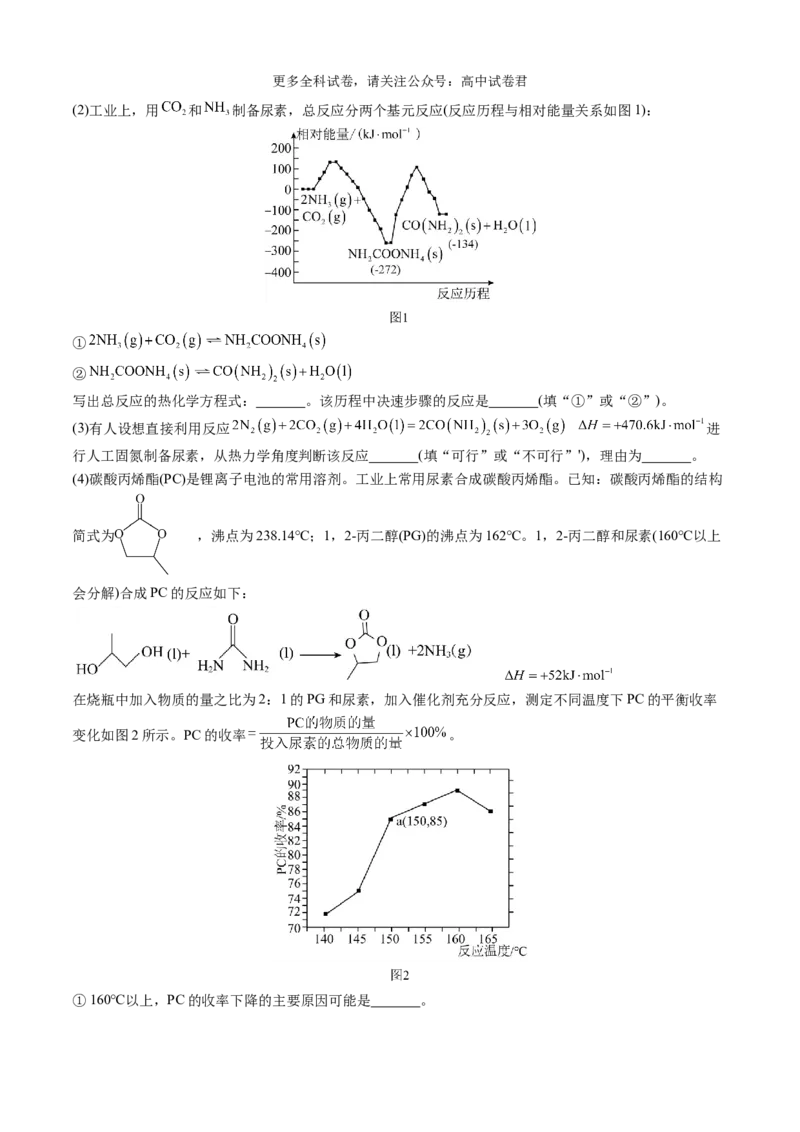
(2)工业上,用 和 制备尿素,总反应分两个基元反应(反应历程与相对能量关系如图1):
①
②
写出总反应的热化学方程式: 。该历程中决速步骤的反应是 (填“①”或“②”)。
(3)有人设想直接利用反应 进
行人工固氮制备尿素,从热力学角度判断该反应 (填“可行”或“不可行”'),理由为 。
(4)碳酸丙烯酯(PC)是锂离子电池的常用溶剂。工业上常用尿素合成碳酸丙烯酯。已知:碳酸丙烯酯的结构
简式为 ,沸点为238.14℃;1,2-丙二醇(PG)的沸点为162℃。1,2-丙二醇和尿素(160℃以上
会分解)合成PC的反应如下:
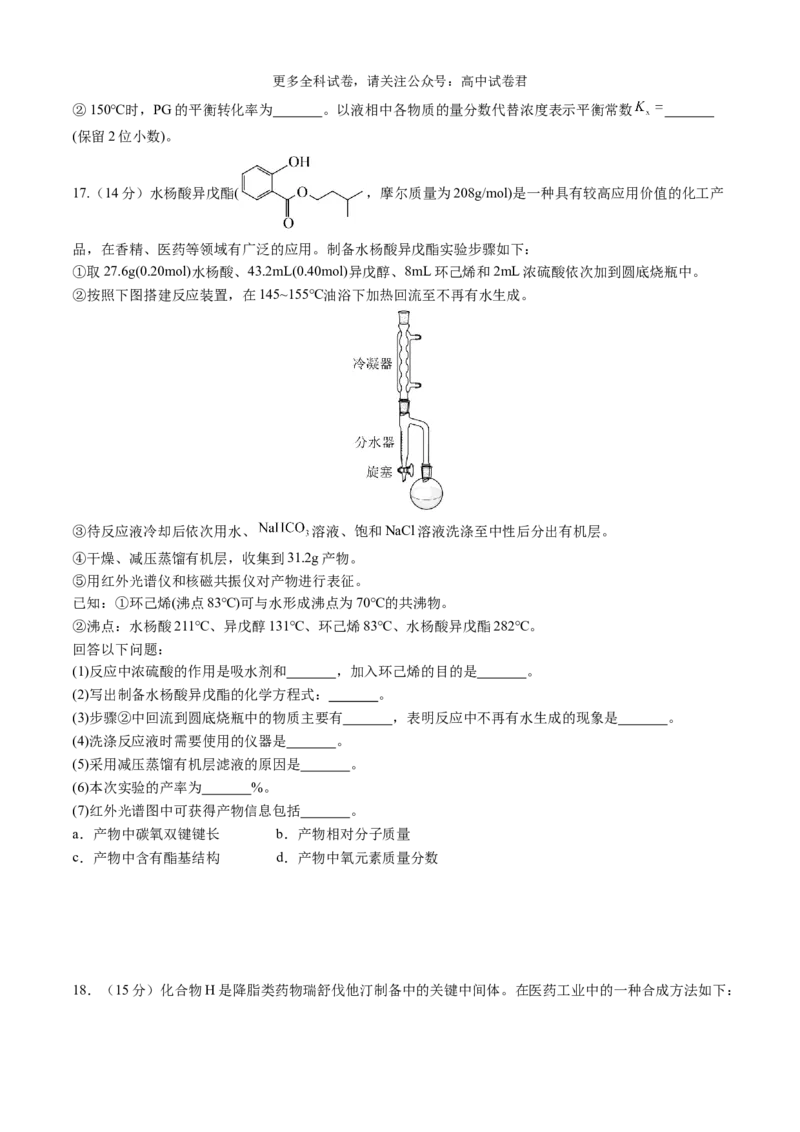
在烧瓶中加入物质的量之比为2:1的PG和尿素,加入催化剂充分反应,测定不同温度下PC的平衡收率
变化如图2所示。PC的收率 。
①160℃以上,PC的收率下降的主要原因可能是 。更多全科试卷,请关注公众号:高中试卷君
②150℃时,PG的平衡转化率为 。以液相中各物质的量分数代替浓度表示平衡常数
(保留2位小数)。
17.(14分)水杨酸异戊酯( ,摩尔质量为208g/mol)是一种具有较高应用价值的化工产
品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
①取27.6g(0.20mol)水杨酸、43.2mL(0.40mol)异戊醇、8mL环己烯和2mL浓硫酸依次加到圆底烧瓶中。
②按照下图搭建反应装置,在145~155℃油浴下加热回流至不再有水生成。
③待反应液冷却后依次用水、 溶液、饱和NaCl溶液洗涤至中性后分出有机层。
④干燥、减压蒸馏有机层,收集到31.2g产物。
⑤用红外光谱仪和核磁共振仪对产物进行表征。
已知:①环己烯(沸点83℃)可与水形成沸点为70℃的共沸物。
②沸点:水杨酸211℃、异戊醇131℃、环己烯83℃、水杨酸异戊酯282℃。
回答以下问题:
(1)反应中浓硫酸的作用是吸水剂和 ,加入环己烯的目的是 。
(2)写出制备水杨酸异戊酯的化学方程式: 。
(3)步骤②中回流到圆底烧瓶中的物质主要有 ,表明反应中不再有水生成的现象是 。
(4)洗涤反应液时需要使用的仪器是 。
(5)采用减压蒸馏有机层滤液的原因是 。
(6)本次实验的产率为 %。
(7)红外光谱图中可获得产物信息包括 。
a.产物中碳氧双键键长 b.产物相对分子质量
c.产物中含有酯基结构 d.产物中氧元素质量分数
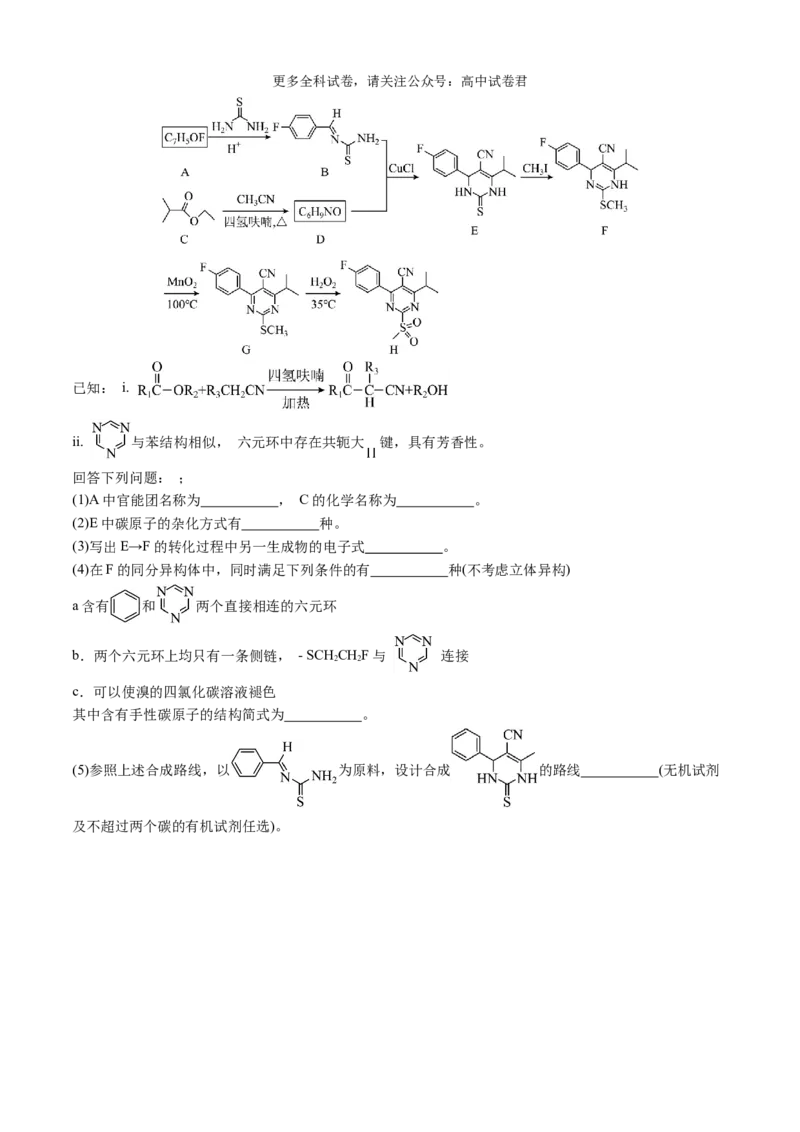
18.(15分)化合物H是降脂类药物瑞舒伐他汀制备中的关键中间体。在医药工业中的一种合成方法如下:更多全科试卷,请关注公众号:高中试卷君
已知: i.
ii. 与苯结构相似, 六元环中存在共轭大 键,具有芳香性。
回答下列问题: ;
(1)A中官能团名称为 , C的化学名称为 。
(2)E中碳原子的杂化方式有 种。
(3)写出E→F的转化过程中另一生成物的电子式 。
(4)在F的同分异构体中,同时满足下列条件的有 种(不考虑立体异构)
a含有 和 两个直接相连的六元环
b.两个六元环上均只有一条侧链, - SCHCHF与 连接
2 2
c.可以使溴的四氯化碳溶液褪色
其中含有手性碳原子的结构简式为 。
(5)参照上述合成路线,以 为原料,设计合成 的路线 (无机试剂
及不超过两个碳的有机试剂任选)。