文档内容
人教版A版(2019)第一章第三节 氧化还原反应 第1课时
氧化还原反应
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.处处留心皆知识,生活中的下列事实,不涉及到氧化还原反应的是
A.小苏打用作食品膨松剂 B.铁钉生锈 C.火法炼铜
D.食物腐败变质
2.下列变化过程中,属于还原反应的是
A.HCl→Cl B.Na→Na+ C.CO→CO D.Fe3+→Fe
2 2
3.下列反应既是离子反应又是氧化还原反应的是
A. 通入烧碱溶液中
B.稀盐酸与铁锈反应
C.CO与 反应制备Fe
D. 溶液中加入稀
4.CO 加氢转化为燃料是实现CO 减排的一个重要策略。我国科学家在调控CO 加氢
2 2 2
反应的选择性方面取得新进展,其过程的示意图如下。下列分析不正确的是
A.该过程中,H 分子中非极性键发生断裂
2
B.CO 的电子式为
2
C.该反应中CO 作氧化剂
2
D.该反应的化学方程式为CO+4H CH+2H O
2 2 4 2
5.下列变化过程中,必须加入氧化剂才能实现的是( )
A.KMnO →MnO B.Fe→Fe2+
4 2
C.Cl→Cl- D.CO→CO
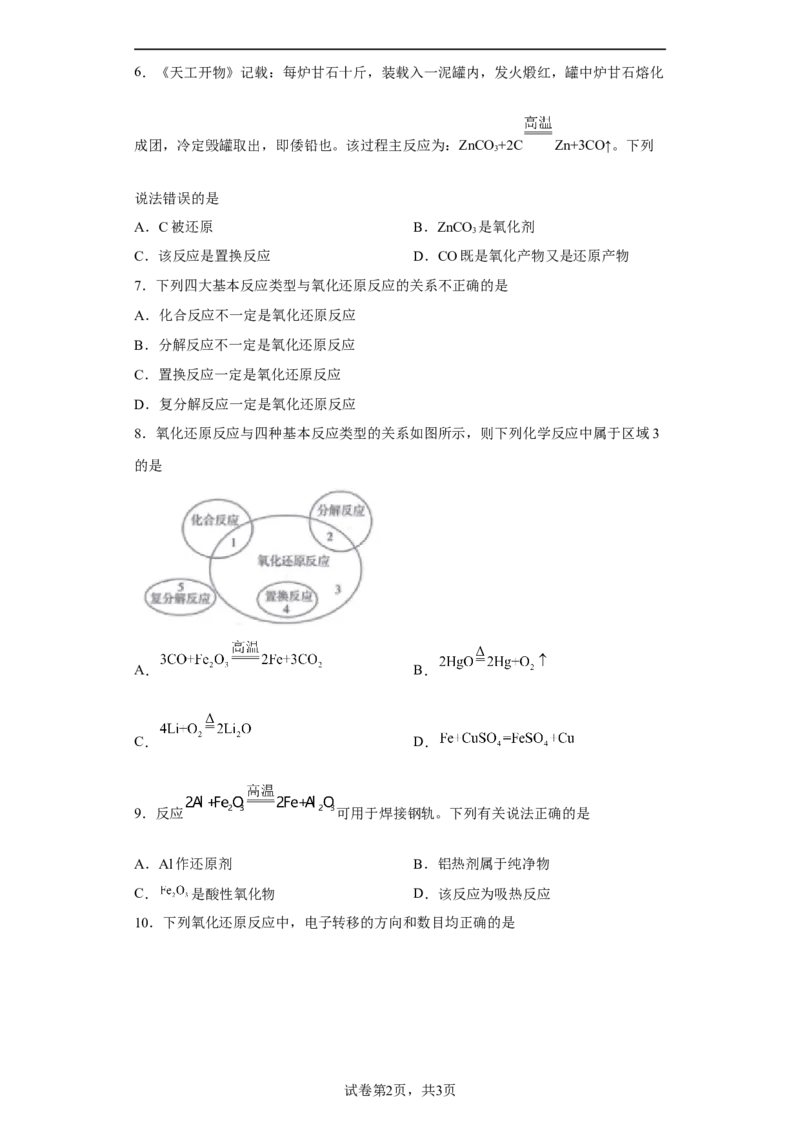
2 26.《天工开物》记载:每炉甘石十斤,装载入一泥罐内,发火煅红,罐中炉甘石熔化
成团,冷定毁罐取出,即倭铅也。该过程主反应为:ZnCO +2C Zn+3CO↑。下列
3
说法错误的是
A.C被还原 B.ZnCO 是氧化剂
3
C.该反应是置换反应 D.CO既是氧化产物又是还原产物
7.下列四大基本反应类型与氧化还原反应的关系不正确的是
A.化合反应不一定是氧化还原反应
B.分解反应不一定是氧化还原反应
C.置换反应一定是氧化还原反应
D.复分解反应一定是氧化还原反应
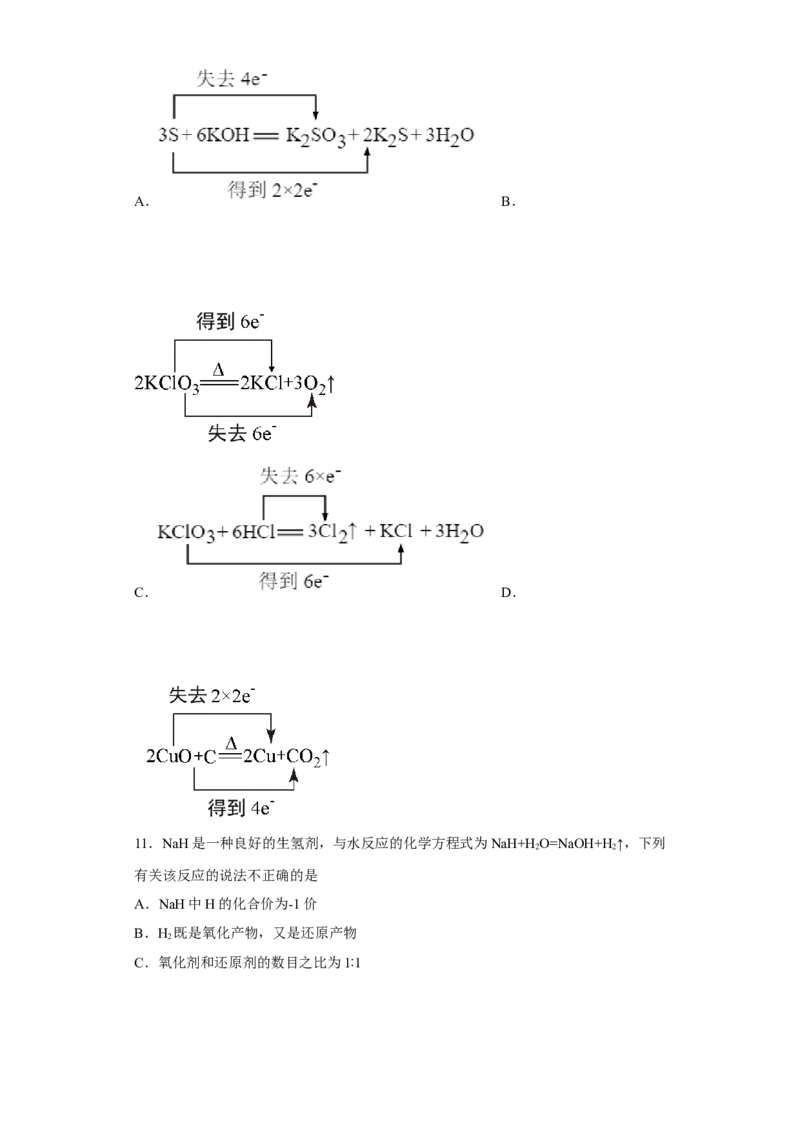
8.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应中属于区域3
的是
A. B.
C. D.
9.反应 可用于焊接钢轨。下列有关说法正确的是
A.Al作还原剂 B.铝热剂属于纯净物
C. 是酸性氧化物 D.该反应为吸热反应
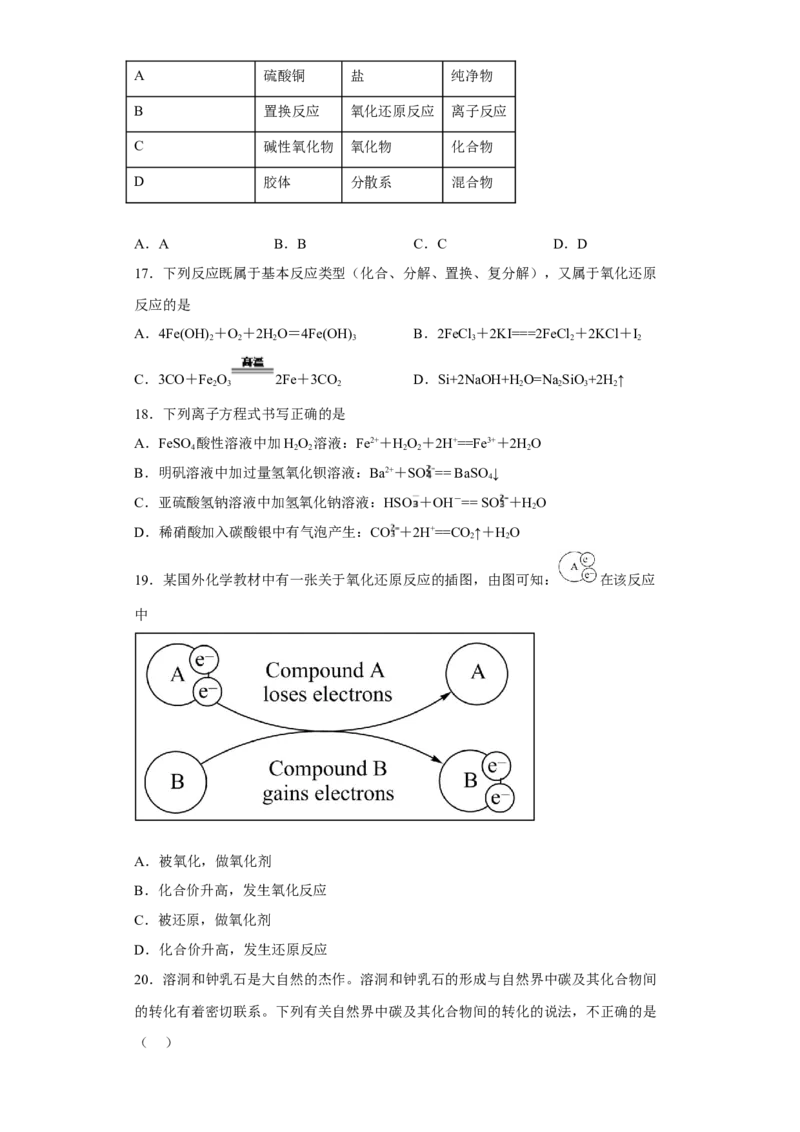
10.下列氧化还原反应中,电子转移的方向和数目均正确的是
试卷第2页,共3页A. B.
C. D.
11.NaH是一种良好的生氢剂,与水反应的化学方程式为NaH+H O=NaOH+H ↑,下列
2 2
有关该反应的说法不正确的是
A.NaH中H的化合价为-1价
B.H 既是氧化产物,又是还原产物
2
C.氧化剂和还原剂的数目之比为1∶1D.电子转移的方向和数目可以表示为:
12.下列离子方程式书写正确的是
A. 与稀硝酸反应:
B. 溶液与溴水反应:
C. 溶液与过量 溶液反应:
D.铁与稀硝酸反应:
13.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
2FeCl +Cu=2FeCl +CuCl 。该反应利用了铜的
3 2 2
A.氧化性 B.还原性 C.稳定性 D.导电性
14.下列反应既属于离子反应,又属于置换反应的是
A.FeCl 溶液中加入Fe粉 B.Ba(OH) 溶液中滴入NaSO 溶液
3 2 2 4
C.FeCl 溶液腐蚀印刷电路铜板 D.Zn片放入盐酸中
3
15.三元催化剂可催化汽车尾气中污染性气体转化为无污染气体,其反应如下:
,下列说法中正确的是
A.CO是氧化剂
B.每生成 共转移2mol电子
C.氧化产物和还原产物的物质的量之比为
D.每产生标准状况下 共转移0.08mol电子
16.下列各组物质或概念之间,不符合如图所示关系的是
X Y Z
例 氧化物 化合物 纯净物
试卷第4页,共3页A 硫酸铜 盐 纯净物
B 置换反应 氧化还原反应 离子反应
C 碱性氧化物 氧化物 化合物
D 胶体 分散系 混合物
A.A B.B C.C D.D
17.下列反应既属于基本反应类型(化合、分解、置换、复分解),又属于氧化还原
反应的是
A.4Fe(OH) +O+2HO=4Fe(OH) B.2FeCl +2KI===2FeCl +2KCl+I
2 2 2 3 3 2 2
C.3CO+Fe O 2Fe+3CO D.Si+2NaOH+H O=Na SiO+2H ↑
2 3 2 2 2 3 2
18.下列离子方程式书写正确的是
A.FeSO 酸性溶液中加HO 溶液:Fe2++HO+2H+==Fe3++2HO
4 2 2 2 2 2
B.明矾溶液中加过量氢氧化钡溶液:Ba2++SO == BaSO ↓
4
C.亚硫酸氢钠溶液中加氢氧化钠溶液:HSO +OH-== SO +HO
2
D.稀硝酸加入碳酸银中有气泡产生:CO +2H+==CO ↑+HO
2 2
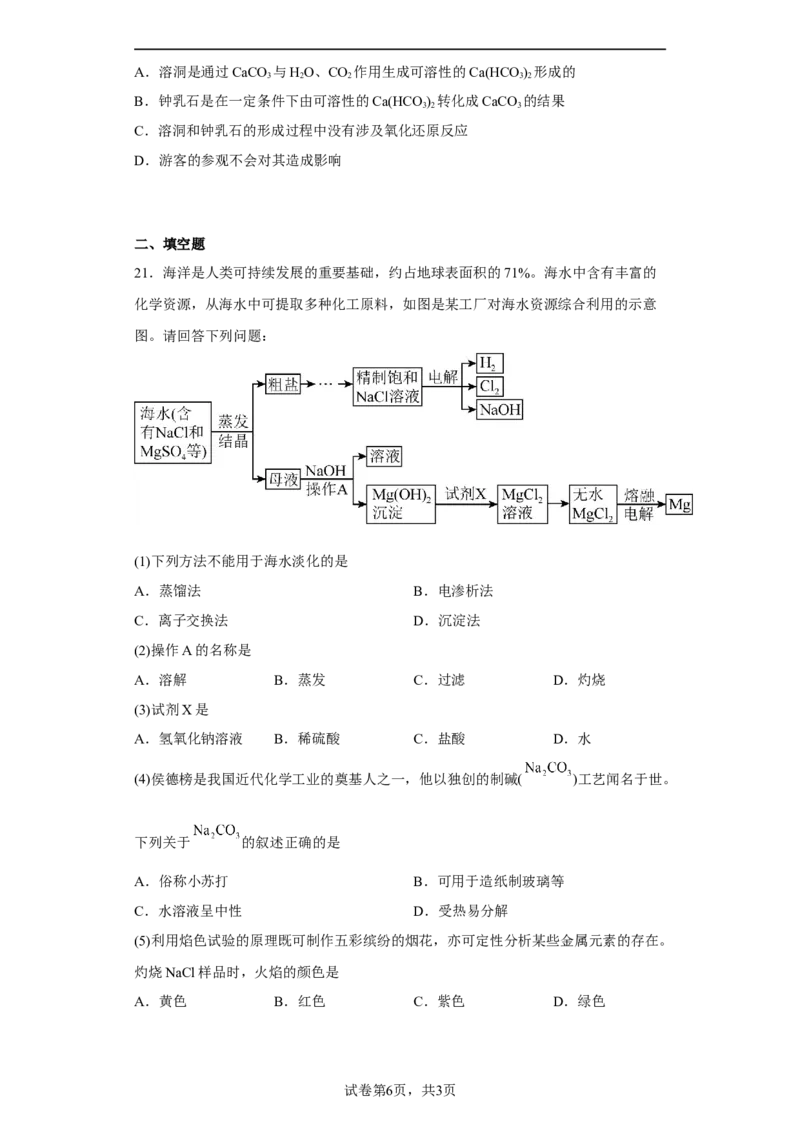
19.某国外化学教材中有一张关于氧化还原反应的插图,由图可知: 在该反应
中
A.被氧化,做氧化剂
B.化合价升高,发生氧化反应
C.被还原,做氧化剂
D.化合价升高,发生还原反应
20.溶洞和钟乳石是大自然的杰作。溶洞和钟乳石的形成与自然界中碳及其化合物间
的转化有着密切联系。下列有关自然界中碳及其化合物间的转化的说法,不正确的是
( )A.溶洞是通过CaCO 与HO、CO 作用生成可溶性的Ca(HCO ) 形成的
3 2 2 3 2
B.钟乳石是在一定条件下由可溶性的Ca(HCO ) 转化成CaCO 的结果
3 2 3
C.溶洞和钟乳石的形成过程中没有涉及氧化还原反应
D.游客的参观不会对其造成影响
二、填空题
21.海洋是人类可持续发展的重要基础,约占地球表面积的71%。海水中含有丰富的
化学资源,从海水中可提取多种化工原料,如图是某工厂对海水资源综合利用的示意
图。请回答下列问题:
(1)下列方法不能用于海水淡化的是
A.蒸馏法 B.电渗析法
C.离子交换法 D.沉淀法
(2)操作A的名称是
A.溶解 B.蒸发 C.过滤 D.灼烧
(3)试剂X是
A.氢氧化钠溶液 B.稀硫酸 C.盐酸 D.水
(4)侯德榜是我国近代化学工业的奠基人之一,他以独创的制碱( )工艺闻名于世。
下列关于 的叙述正确的是
A.俗称小苏打 B.可用于造纸制玻璃等
C.水溶液呈中性 D.受热易分解
(5)利用焰色试验的原理既可制作五彩缤纷的烟花,亦可定性分析某些金属元素的存在。
灼烧NaCl样品时,火焰的颜色是
A.黄色 B.红色 C.紫色 D.绿色
试卷第6页,共3页(6)氯碱工业的反应原理: ,该反应的反应类
型属于
A.复分解反应 B.置换反应 C.氧化还原反应 D.分解反应
22.《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶端分
许,名曰发烛。”《资治通鉴》中记载:“陈宣帝太建九年,齐后妃贫苦,至以卖烛
为业。”文中的“发烛”就是原始的火柴。已知KCr O 用于工业中制造火柴头。
2 2 7
KCr O+HCl(浓)→KCl+CrCl +Cl↑+H O(未配平)
2 2 7 3 2 2
(1)___(填元素名称)元素被氧化,__(填化学式,下同)是氧化剂。
(2)__是氧化产物,__发生氧化反应。
(3)参加反应的盐酸,表现了__性质。(填“还原性”“氧化性”或“酸性”)
(4)该反应中每生成3分子Cl 转移电子个数为__个。
2
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目___。
23.储氢纳米碳管研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大
量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应的化学方程式如下:
回答下列问题:
(1)该反应中,KCr O 表现出___________(填“氧化性”或“还原性”),KCr O 发生
2 2 7 2 2 7
了___________(填“氧化反应”或“还原反应”)。
(2)H SO 在该反应中表现出___________
2 4
A.只有酸性 B.只有氧化性 C.酸性和氧化性 D.酸性和还原性
(3)该反应中,还原反应得到的生成物是___________(填化学式)。
(4)每生成1molH O,该反应转移了___________mol电子。
2参考答案:
1.A
【详解】A. 小苏打(碳酸氢钠),受热后分解出二氧化碳气体,使馒头膨松,不涉及氧化
还原反应,A符合题意。
B. 铁钉生锈,单质铁转化为三氧化二铁,有元素化合价升降,属于氧化还原反应,B不符
合题意。
C. 火法炼铜的化学方程式为Cu S+O 2Cu +SO ,有元素化合价升降,属于氧化还原反
2 2 2
应,C不符合题意。
D. 食物腐败过程发生缓慢氧化,有元素化合价的升降,属于氧化还原反应,D不符合题意。
2.D
【详解】A、.HCl→Cl 中氯元素化合价升高,属于氧化反应,A项错误;
2
B、Na→Na+中钠元素化合价升高,属于氧化反应,B项错误;
C、CO→CO 中碳元素化合价升高,属于氧化反应,C项错误;
2
D、Fe3+→Fe中铁元素化合价降低,属于还原反应,D项正确;
答案选D。
3.A
【详解】A. 通入烧碱溶液中,在溶液中反应,生成NaCl和NaClO,又是氧化还原反
应,A符合题意;
B.稀盐酸与铁锈反应,生成氯化铁和水,属于复分解反应,是离子反应,不是氧化还原
反应,B不符合题意;
C.CO与 反应制备Fe,不在溶液中,不是离子反应,C不符合题意;
D. 溶液中加入稀 ,生成NaSO 、CO、HO,是离子反应,不是氧化还原
4 2 2
反应,D不符合题意;
故选A。
4.B
【详解】A.化学变化是旧键断裂新键形成的过程,该过程中,H 分子中非极性键发生断
2
裂,A正确;
B.CO 中中心原子碳原子和每个氧原子形成2对共用电子对达到8电子稳定结构,电子式
2为 ,B错误;
C.该反应中CO 得到电子发生还原反应生成甲烷,作氧化剂,C正确;
2
D.该反应中二氧化碳和氢气在催化剂作用下生成甲烷和水,化学方程式为CO+4H
2 2
CH+2H O,D正确;
4 2
故选B。
5.B
【详解】A.KMnO →MnO ,该转化中锰元素化合价降低了,加热KMnO ,无需加入还原
4 2 4
剂就能实现,故A错误;
B.Fe→Fe2+,该转化中铁元素的化合价升高,必须加入氧化剂才能实现,故B正确;
C.Cl→Cl-,该转化中氯元素化合价降低了,需加入还原剂才能实现,故C错误;
2
D.CO→CO ,该转化中无化合价变化,不属于氧化还原反应,故D错误;
2
答案选B。
6.A
【详解】A.反应中C的化合价由0价升高为+2价,故C被氧化,A错误;
B.反应中ZnCO 的C的化合价由+4降低为+2价,Zn的化合价由+2价降低为0价,故
3
ZnCO 被还原,是氧化剂,B正确;
3
C.该反应是一种单质和一种化合物反应生成新的单质和新的化合物,故属于置换反应,C
正确;
D.CO中的C的化合价既有由0价转化为+2价的,也有由+4价转化为+2价,故CO既是
氧化产物又是还原产物,D正确;
故答案为:A。
7.D
【详解】A.化合反应不一定是氧化还原反应,如CaO与水反应生成氢氧化钙,是化合反
应,反应中没有化合价的变化,不是氧化还原反应,故A正确;
B.分解反应不一定是氧化还原反应,如碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,
属于分解反应但没有化合价的变化,不是氧化还原反应,故B正确;
C.置换反应中反应物为单质和化合物,生成物为另一种单质和另一种化合物,则单质的
答案第2页,共2页化合价一定发变化,一定是氧化还原反应,故C正确;
D.复分解反应一定不存在元素化合价的变化,一定不是氧化还原反应,故D错误;
综上所述答案为D。
8.A
【分析】区域1既是化合反应又是氧化还原反应,区域2既是分解反应又是氧化还原反应,
区域3既不是四种基本反应类型,又是氧化还原反应,区域4既是置换反应又是氧化还原
反应,区域5是复分解反应,不是氧化还原反应。
【详解】A. 是氧化还原反应,但不属于四种基本反应类型,A
属于区域3,A符合题意;
B. 既是分解反应又是氧化还原反应,属于区域2,B不符合题意;
C. 既是化合反应又是氧化还原反应,属于区域1,C不符合题意;
D. 属于置换反应,属于区域4,D不符合题意;
故选A。
9.A
【详解】A.Al化合价升高,为还原剂,A正确;
B.铝热剂是铁粉和氧化铝的混合物,B错误;
C.氧化铁与酸反应生成盐和水,是碱性氧化物,C错误;
D.铝热反应为放热反应,D错误;
故选A。
10.A
【详解】A.在该反应中S元素化合价由反应前S单质的0价变为反应后KSO 中的+4价,
2 3
化合价升高4价,失去电子4e-;S元素化合价由反应前S单质的0价变为反应后KS中
2
的-2价,化合价降低2价,得到电子2e-,化合价升降最小公倍数是4,根据氧化还原反应
中得失电子数目相等,等于元素化合价升降总数,可知反应中转移电子数目为4e-,所以
KSO 的系数是1,KS的系数是2,S的系数是3,根据K原子守恒可知KOH系数是6,
2 3 2
最后根据H元素守恒,可知HO的系数是3,故该反应的电子转移方向和数目都符合事实,
2A正确;
B.在该反应中Cl元素化合价由反应前KClO 中的+5价变为反应后KCl中的-1价,化合价
3
降低6价,得到电子6e-;O元素化合价由反应前KClO 中的-2价变为反应后O 中的0价,
3 2
化合价升高2×2=4价,失去电子4e-;化合价升降最小公倍数是12,所以根据氧化还原反应
中得失电子数目相等,等于元素化合价升降总数,可知反应中转移电子数目为12e-,电子
转移数目不符合反应事实,B错误;
C.在该反应中KClO、KCl中的Cl原子发生电子转移都变为Cl。Cl元素化合价由反应前
3 2
KClO 中的+5价变为反应后Cl 中的0价,化合价降低5价,得到电子5e-;Cl元素化合价
3 2
由反应前HCl中的-1价变为反应后Cl 中的0价,化合价升高1价,失去电子e-;化合价升
2
降最小公倍数是5,以根据氧化还原反应中得失电子数目相等,等于元素化合价升降总数,
可知反应中转移电子数目为5e-,图示的电子转移方向及数目均不符合反应事实,C错误;
D.在该反应中Cu元素化合价由反应前CuO中的+2价变为反应后Cu单质中的0价,化合
价降低2价,得到电子2e-;C元素化合价由反应前C单质中的0价变为反应后CO 中的+4
2
价,化合价升高4价,失去电子4e-;元素化合价升降最小公倍数是4,所以根据氧化还原
反应中得失电子数目相等,等于元素化合价升降总数,可知反应中转移电子数目为4e-,图
示的电子转移方向不符合反应事实,D错误;
故合理选项是A。
11.D
【分析】在反应NaH+H O=NaOH+H ↑中,NaH中H的化合价为-1价,HO中H的化合价
2 2 2
为+1价,只有H元素的化合价发生变化,氢气既是还原产物又是氧化产物,结合化合价的
变化判断电子的转移。
【详解】A.NaH中Na的化合价为+1价,则H的化合价为-1价,故A正确;
B.反应中只有H的化合价发生变化,氢气既是氧化产物也是还原产物,故B正确;
C.H元素的化合价由-1价升高为0,可知NaH为还原剂,水中H元素的化合价降低,水
为氧化剂,则氧化剂和还原剂的物质的量之比为1∶1,故C正确;
D.反应中转移电子数为1,正确的为 ,故D错
误;
答案第4页,共2页故选D。
12.B
【详解】A.碳酸钙与稀硝酸反应生成硝酸钙、二氧化碳和水,且碳酸钙不溶于水,在书
写离子方程式中不拆开,反应的离子方程式为 ,故A错
误;
B.硫酸亚铁溶液与溴水反应生成硫酸铁和溴化铁,反应的离子方程式为
,故B正确;
C.氢氧化钠溶液与过量的草酸溶液反应生成草酸氢钠和水,反应的离子方程式为
,故C错误;
D.铁与稀硝酸反应生成硝酸铁、一氧化氮和水,不能生成氢气,反应的离子方程式为
,故D错误;
故选B。
13.B
【详解】由反应2FeCl +Cu=2FeCl +CuCl 可知Cu的价态升高,被氧化,Cu作还原剂,故
3 2 2
该反应利用了铜的还原性,B正确;
答案选B。
14.D
【分析】属于离子反应,一般应在溶液中进行,且有离子参加;一种单质与一种化合物反
应生成另一种单质和另一种化合物的反应属于置换反应;
【详解】A.铁和铁离子生成亚铁离子,有铁离子参加属于离子反应,生成物中没有单质,
不是置换反应,A错误;
B.钡离子和硫酸根离子生成硫酸钡沉淀,为离子反应,该反应属于复分解反应,B错误;
C.铜和铁离子生成铜离子和亚铁离子,有离子参加属于离子反应,生成物中没有单质,
不是置换反应,C错误;
D.锌和氢离子生成锌离子和氢气,有离子参加属于离子反应,符合置换反应定义为置换
反应,D正确;
故选D。15.D
【详解】A.CO中碳元素化合价从+2价升高到+4价,失去2个电子,CO是还原剂,A错
误;
B.氮元素化合价从+2价降低到0价,得到2个电子,因此每生成 共转移4mol电
子,B错误;
C.二氧化碳是氧化产物,氮气是还原产物,氧化产物和还原产物的物质的量之比为 ,
C错误;
D.每产生标准状况下 即0.02mol氮气,共转移0.02mol×4=0.08mol电子,D正
确;
答案选D。
16.B
【详解】A.盐是指由金属离子和酸根离子组成的化合物,硫酸铜是由硫酸根离子和铜离
子构成的盐,盐是化合物,是纯净物,A正确;
B.置换反应一定是氧化还原反应,但氧化还原反应不一定属于离子反应,如氢气还原氧
化铜是置换反应,是氧化还原反应,但不是离子反应,B错误;
C.氧化物依据组成元素分为金属氧化物和非金属氧化物,依据性质分为酸性氧化物、碱
性氧化物、两性氧化物、不成盐氧化物、过氧化物等,则碱性氧化物属于氧化物,氧化物
是指由两种元素组成的化合物中,其中一种元素是氧元素,所以氧化物是化合物,C正确;
D.分散系包括溶液、胶体、浊液三种,胶体属于分散系,而分散系都是由两种以上的物
质组成,因此分散系属于混合物,D正确;
故合理选项是B。
17.A
【详解】根据定义,多变一为化合反应;一变多为分解反应;一种单质与一种化合物生成
另一种单质和另一种化合物的反应是置换反应;两种化合物相互交换成分生成另外两种化
合物的反应的复分解反应,有元素化合价变化的反应为氧化还原反应。4Fe(OH) +O+
2 2
2HO=4Fe(OH) 属于化合反应、氧化还原反应,故A正确;2FeCl +2KI===2FeCl +2KCl
2 3 3 2
+I 属于氧化还原反应,不属于基本反应类型,故B错误;3CO+Fe O 2Fe+3CO
2 2 3 2
属于氧化还原反应,不属于基本反应类型,故C错误;Si+2NaOH+H O=Na SiO+2H ↑属于
2 2 3 2
答案第6页,共2页氧化还原反应,不属于基本反应类型,故D错误。
18.C
【详解】A. 两端电荷没有配平,A错误;B.少量氢氧化钡:2Al3+ + 3SO 2- + 3Ba2+ + 6OH-
4
= 2Al(OH) ↓+ 3BaSO↓+ 3H2O,过量氢氧化钡:Al3+ + SO 2- + Ba2+ + 4OH- = AlO - +
3 4 4 2
BaSO↓+ 2H O,B错误;C. 反应正确,两端平衡,C正确;D. 碳酸银难溶解于水,不能
4 2
拆分写成CO ,D错误。故选择C。
19.B
【详解】由图示可知,反应为:A2-+B=B2-+A,反应中A的化合价有-2价变为0价,化合价
升高被氧化,发生氧化反应,作还原剂,故答案为:B。
20.D
【详解】A.溶洞是通过碳酸钙与空气中的二氧化碳和水作用生成可溶性的碳酸氢钙形成
的,反应的方程式为:CaCO +H O+CO=Ca(HCO ),故A正确;
3 2 2 3 2
B.钟乳石是在一定条件下碳酸氢钙分解产生碳酸钙的结果,反应的化学方程式为:
Ca(HCO ) CaCO +H O+CO↑,故B正确;
3 2 3 2 2
C.上述两个反应中没有元素化合价的变化,不属于氧化还原反应,故C正确;
D.大量游客的进入会释放出更多的二氧化碳,使溶洞中二氧化碳的含量增大,会对溶洞
和钟乳石造成影响,故D错误;
故答案选D。
21.(1)D
(2)C
(3)C
(4)B
(5)A
(6)C
【分析】海水(含有NaCl和MgSO )蒸发结晶得到粗盐和母液,母液中含有硫酸镁,加入氢
4
氧化钠溶液生成氢氧化镁沉淀和硫酸钠溶液,过滤得到氢氧化镁沉淀,氢氧化镁沉淀中加
入盐酸生成氯化镁溶液,得到无水氯化镁,电解得到镁。
(1)海水淡化的方法有蒸馏法、电渗析法、离子交换法等,故选D。(2)分离溶液和沉淀的方法为过滤,故选C。
(3)根据分析可知,试剂X为盐酸,故选C。
(4)A.小苏打为碳酸氢钠,不选;B.碳酸钠可用于造纸制玻璃等,选;C.碳酸钠水溶液呈
碱性,不选;D.受热难分解,不选,故选B。
(5)Na的焰色实验现象为黄色,故选A。
(6)该反应中H、Cl的化合价都有变化,属于氧化还原反应,故选C。
22. 氯 KCr O Cl HCl 还原性、酸性 6
2 2 7 2
【详解】(1)反应中部分氯元素的化合价由-1价升高到0价,被氧化;KCr O 中铬元素
2 2 7
的化合价由+6价降低到+3价被还原,KCr O 作氧化剂;故答案为:氯;KCr O;
2 2 7 2 2 7
(2)HCl Cl,氯元素化合价升高,发生氧化反应,Cl 为氧化产物;故答案为:Cl;
2 2 2
HCl;
(3)14个HCl分子参加反应,有6个HCl分子体现还原性被氧化,生成3个Cl 分子,另
2
外8个HCl分子起酸的作用,故答案为:还原性、酸性;
(4)部分氯元素的化合价由-1价变到0价,故生成3分子Cl 转移电子个数为3 2 [0-
2
(-1)]=6;故答案为:6。
(5)生成3mol氯气,转移6mol电子,配平上述反应,并用单线桥表示出该反应电子转移
的方向和数目为: 。
23.(1) 氧化性 还原反应
(2)A
(3)
(4)1.5
【分析】(1)
答案第8页,共2页该反应中, 中Cr的化合价降低, 作氧化剂,具有氧化性, 被还
原,发生还原反应,故答案为:氧化性;还原反应;
(2)
与Cr、K原子反应生成盐,且化合价未变,在该反应中 表现酸性,故A正确,
故答案为:A;
(3)
中Cr的化合价降低,发生了还原反应,则还原反应得到的生成物是 ,故
答案为: ;
(4)
根据反应方程式: ,可知
每生成 时,转移 电子,则每生成 ,反应转移
电子,故答案为:1.5。答案第10页,共2页