文档内容
人教版(2019)高一必修第一册 第三章 铁 金属材料 第二
节 金属材料 专题一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下表中物质的用途与所对应性质不相符的是
选项 物质 用途 性质
A 铁、铬(18%)、镍(8%)合金 制作医疗器材、厨具 不易生锈
B 氨水 用于消除燃煤烟气中的二氧化硫 可与酸性氧化物反应生成盐和水
C 抗坏血酸(维生素C) 水果罐头中的抗氧化剂 还原性
D 氢氟酸 用于刻蚀玻璃 HF属于强酸,能与硅酸盐反应
A.A B.B C.C D.D
2.下列关于合金的叙述中正确的是
A.合金是由两种或多种金属熔合而成的
B.日常生活中用到的五角硬币属于铜合金
C.合金在任何情况都比单一金属性能优良
D.低碳钢比中碳钢强度高
3.下列硫化物中不能直接用金属单质和硫单质反应制得的是( )
A.FeS B.CuS C.ZnS D.MgS
4.下列关于合金的说法中,正确的是
A.常见的一些合金的硬度比其成分金属的大,是因为合金中原子的排列比纯金属中
更规整
B.储氢合金是一类能够大量吸收H,并与H 结合成金属氢化物的材料
2 2
C.合金的熔点一定比各成分金属的低
D.在我国使用最早的合金是生铁
5.最近科学家冶炼出纯度高达99.9999%的铁。你估计它不会具有的性质是
A.硬度比生铁低 B.与4mol/L的HCl反应时速率比生铁
快
C.在冷的浓硫酸中可钝化 D.在潮湿的空气中不易生锈
6.国庆70周年阅兵式,大量新式武器新鲜出炉且都为中国制造,制造这些“国之重
器”的材料多为合金。下列关于合金的说法不正确的是A.合金在工业上的用途比纯金属更广
B.合金的硬度一般比它的成分金属大
C.合金的熔点一般比它的成分金属高
D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能
7.下列化学方程式与事实相符且书写正确的是( )
A.炼铁高炉中生成铁:3C+2Fe O 4Fe+3CO ↑
2 3 2
B.铝放入稀硫酸中:Al+H SO =AlSO+H ↑
2 4 4 2
C.向氢氧化钠溶液中加入硫酸铜溶液:2NaOH+CuSO =Cu(OH) ↓+Na SO
4 2 2 4
D.向小苏打中滴加稀硫酸: NaCO+H SO =Na SO +H O+CO↑
2 3 2 4 2 4 2 2
8.许多成语中都蕴含化学原理,下列有关解释不准确的是
成语 化学原理
A 沙里淘金 利用金的密度较大的性质将黄金从沙中淘洗出来
B 刀耕火耨 放火烧去野草,用余灰肥田,还可降低土壤碱性
C 百炼成钢 通过多次锻炼,使生铁中碳杂质降低到钢的标准
金属元素在燃烧时显示的不同焰色,又叫焰色反
D 火树银花
应
A.A B.B C.C D.D
9.b g某金属与足量的稀硫酸反应,生成该金属的三价正盐和a g氢气。该金属的相对
原子质量为
A. B. C. D.
10.现有质量均为54g的铝粉两份,分别与1L浓度均为3mol∙L-1的盐酸和氢氧化钠溶
液反应,产生的氢气的体积比为
A.1∶1 B.1∶2 C.1∶3 D.2∶3
11.200℃时,11.6g由CO 和水蒸气的混合物与足量的NaO 充分反应后,固体质量增
2 2 2
加了3.6g,则原混合气体的平均摩尔质量为g/mol
A.5.8 B.11.6 C.46.4 D.23.2
12.下列离子方程式对应的化学方程式正确的是
A.H++OH﹣═H O CHCOOH+NaOH═CH COONa+H O
2 3 3 2
B.Ba2++SO2﹣═BaSO ↓ Ba(OH)+H SO ═BaSO ↓+2H O
4 4 2 2 4 4 2
C.CO2﹣+2H+═CO ↑+H O CaCO +2HCl═CaCl +CO ↑+H O
3 2 2 3 2 2 2
D.3Cu+8H++2NO﹣═3Cu2++2NO↑+4HO 3Cu+8HNO (稀)═3Cu(NO )
3 2 3 3
试卷第2页,共3页+2NO↑+4HO
2 2
13.下列反应离子方程式正确的是
A.钠和水反应:Na+2HO=Na++2OH-+H ↑
2 2
B.NaHCO 溶液中加过量Ca(OH) 溶液:Ca2++2OH-+2HCO -=CaCO ↓+CO2-+2H O
3 2 3 3 3 2
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO 2-=BaSO ↓+H 0
4 4 2
D.向NaAlO 溶液中通入过量CO:AlO-+CO +2H O=Al(OH) ↓+HCO -
2 2 2 2 2 3 3
14.下列关于金属铝的叙述中,说法不正确的是
A.铝的化学性质很活泼,但在空气中不易锈蚀
B.铝是比较活泼的金属,在化学反应中容易失去电子,表现出还原性
C.铝箔在空气中受热可以熔化,且发生剧烈燃烧
D.铝箔在空气中受热可以熔化,但由于氧化膜的存在,熔化的铝并不滴落
15.铁和铁合金是生活中常见的材料,下列说法正确的是
A.纯铁的熔点低于铁合金 B.纯铁和铁合金都能导电、传热
C.纯铁的硬度和强度都高于铁合金 D.不锈钢是铁合金,只含金属元素
16.下列说法都正确的是
① 生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
② 江河入海口三角洲的形成通常与胶体的性质有关
③ “钡餐”中使用的硫酸钡是弱电解质
④ 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤ 常用的自来水消毒剂有氯气和HO,两者都含有极性键
2 2
⑥ 水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
A.①②③④ B.①②④⑥ C.①②⑤⑥ D.③④⑤⑥
17.下列有关物质的鉴别或检验错误的是
A.用激光笔照射区别食盐水和蛋白质溶液
B.向溶液中滴入铁氰化钾溶液,可检验溶液中是否存在Fe2+
C.将红色石蕊试纸伸到集气瓶口可检验瓶里是不是氨气
D.向溶液中滴入足量稀盐酸后再滴入氯化钡溶液,可检验溶液中是否存在SO
18.下列物质中,不能使酚酞溶液变红的是
A.NH B.NaSiO C.NaHCO D.Al(OH)
3 2 3 3 3
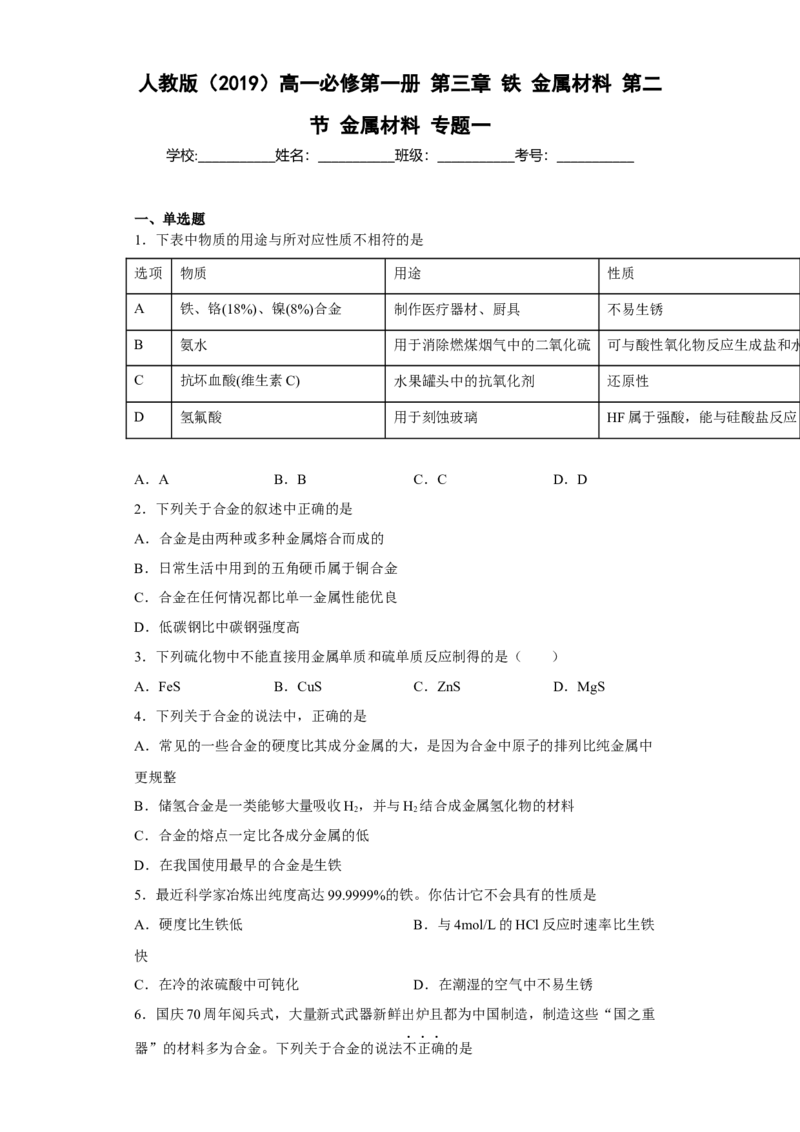
19.某兴趣小组在实验室通过镁粉和空气中的氮气制备氮化镁(可与水发生反应),其装
置如下图所示。已知:维生素C具有较强的还原性。下列说法错误的是A.装置①③中盛放的分别是NaOH溶液和浓硫酸B.装置②的作用为吸收空气中的
O
2
C.实验开始时应先通空气再点燃酒精灯 D.装置⑤中碱石灰可以替换为NaCl
二、填空题
20.现有以下物质:①NaCl固体;②液态CO;③液态氯化氢;④汞;⑤固体
2
BaSO;⑥蔗糖;⑦酒精;⑧熔融的NaCO,请回答下列问题:
4 2 3
(1)以上物质中能导电的是________;
(2)以上物质属于电解质的是________;
(3)以上物质属于非电解质的是_______;
(4)以上物质溶于水后形成的溶液能导电的是______;
(5)属于盐的有________;
(6)写出⑧溶于水中的电离方程式_____;
(7)分离胶体和溶液常用的方法叫__________;
(8)等质量的O 和O 所含原子个数比为______;
2 3
(9)设N 为阿伏加德罗常数的数值,若ag某气体中含有的分子数为b,则c g该气体在
A
标准状况下的体积是___________。(用含有N 的式子表示)
A
三、计算题
21.将70克过氧化钠和氧化钠的混和物跟98克水充分反应后,所得氢氧化钠溶液的
质量百分比浓度为50%.试分别写出过氧化钠和氧化钠跟水反应的化学方程式:
_________、_________,并计算原混和物中过氧化钠和氧化钠的质量分别为_______、
________。
22.我市有丰富的石灰石资源,为测定石灰石中碳酸钙的质量分数,取7.5g样品放入
烧杯,加入稀盐酸至恰好不再产生气体时消耗稀盐酸25g,放出的气体在常温下体积
为1.1L。
试卷第4页,共3页(1)常温下CO 气体的密度为2.0g/L,则上述反应放出气体的质量为___g。
2
(2)计算石灰石中CaCO 的质量分数和所用稀盐酸溶质质量分数___。
3
23.现有两种 与 的固体混合物X和Y。已知 受热难分解,而
受热解: 。
(1)现取 固体混合物X,充分加热至恒重,固体混合物质量减少了 ,则原
固体混合物中 的质量为_____________________。
(2)现取 固体混合物Y,充分加热至恒重,把产生的气体通入足量澄清石灰水中,
生成 沉淀,则原固体混合物中 的质量分数为______________________。参考答案:
1.D
【详解】A.含铬、镍的不锈钢耐腐蚀,能用于制作医疗器材、厨具,A项正确;
B.二氧化硫属于酸性氧化物,可以与碱反应生成盐和水,而氨水属于碱性溶液,因此,
工业上可用氨水吸收燃煤烟气中的二氧化硫从而消除污染,B项正确;
C.维生素C具有还原性,可用作水果罐头的抗氧化剂,C项正确;
D.氢氟酸能与二氧化硅反应,可用于刻蚀玻璃,但HF属于弱酸,不属于强酸,D项错误;
答案选D。
2.B
【详解】合金是金属与金属或金属与非金属熔合而成的,A项错误;合金的性能一般比单
一金属性能优良,但并不是任何情况都是,如纯铝的导电性比铝合金要好,C项错误;含
碳量高强度大,中碳钢比低碳钢强度高,D项错误。
3.B
【分析】硫的非金属性较弱,与变价金属化合时,只能生成低价态硫化物。
【详解】A.Fe和S高温下反应生成FeS,能直接用金属单质和硫单质反应制得,故A不
符合题意;
B.Cu和S高温下反应生成Cu S,不能直接用金属单质和硫单质反应制得,故B符合题意;
2
C.Zn和S高温下反应生成ZnS,能直接用金属单质和硫单质反应制得,故C不符合题意;
D.Mg和S高温下反应生成MgS,能直接用金属单质和硫单质反应制得,故D不符合题意;
答案选B。
4.B
【详解】A.纯金属中原子的排列比合金中规整,合金硬度大与原子排列无关,合金中含
有多种元素,例如钢是碳、镍、铬等元素溶解在铁中形成,这些元素与铁形成固溶体,对
基体有强化作用导致合金硬度变大,A错误;
B.储氢合金是一类能够大量吸收H,并与H 结合成金属氢化物的材料,这类金属材料属
2 2
于储氢合金,B正确;
C.合金的熔点一般比各成分金属的低,但是汞与其它金属形成合金,熔点大于汞的熔点,
C错误;
D.在我国使用最早的合金是铜合金,D错误;
故选B。5.B
【详解】A.纯铁的硬度比铁合金低,A争取;
B.生铁再与盐酸反应时,能构成原电池从而加快反应速率,而纯铁是不能的,所以选项B
不正确,
C.铁遇冷的浓硫酸、浓硝酸时形成致密的氧化膜阻止了进一步反应,即钝化,C正确;
D.纯铁不具备形成原电池的两个电极,在潮湿环境中不易被氧化,D正确。
答案选B。
6.C
【详解】A.合金比纯金属具有很多更优良的性能,所以在工业上的用途比纯金属更广,A
正确;
B.合金的硬度一般大于它的成分金属,B正确;
C.合金的熔点一般比它的成分金属低,C不正确;
D.合金比它的成分金属具有许多更优良的性能,D正确;
故选C。
7.C
【详解】A. 焦炭会把二氧化碳还原为一氧化碳,因此炼铁高炉中生成铁的反应方程式为
3C+Fe O 2Fe+3CO↑,故A错误;
2 3
B. 铝放入稀硫酸中,生成的硫酸铝的化学式为Al (SO ),反应的方程式为:2Al+3H SO =
2 4 3 2 4
Al (SO )+3H ↑,故B错误;
2 4 3 2
C. 向氢氧化钠溶液中加入硫酸铜溶液:2NaOH+CuSO =Cu(OH) ↓+Na SO ,故C正确;
4 2 2 4
D. 小苏打是碳酸氢钠,向小苏打中滴加稀硫酸的化学方程式为
2NaHCO +H SO =Na SO +2H O+2CO↑,故D错误;
3 2 4 2 4 2 2
故答案选C。
8.B
【详解】A.“沙里淘金”说明黄金在自然界中能够以单质形式存在,发生的是物理变化;
故A正确;B.刀耕火耨中包含着古人播种前先伐去树木烧掉野草,用余灰可以肥田,但
草木灰水溶液显碱性不能降低土壤碱性,故B错误;C.生铁和钢的主要区别在于含碳量
不同,钢的碳含量低,在空气中锤打,目的是让碳和氧气反应生成二氧化碳,从而降低含
碳量,达到钢的标准,故C正确;D.不同的金属灼烧产生不同的焰色,火树银花利用金
属的焰色反应,故D正确;故选B。
答案第2页,共2页9.C
【解析】根据金属的化合价和氢气的物质的量求出金属的物质的量,进而求出金属的摩尔
质量,再利用摩尔质量与相对原子质量的关系来解答。
【详解】ag氢气的物质的量为:n(H )= =0.5amol,
2
设金属为A,bg金属的物质的量为x,
根据反应方程式:2A+3HSO =A (SO )+3H ↑
2 4 2 4 3 2
2 3
x 0.5amol
则: ,解得:x= mol,
则金属的摩尔质量M(金属)= = = g/mol,
由金属的摩尔质量与其相对原子质量在数值上相等,即金属的相对原子质量为 。
答案选C。
10.B
【分析】54g铝粉的物质的量n(Al)= = =2mol,
n(HCl)=n(NaOH)=cV=1L×3mol∙L-1=3mol,反应的化学方程式为2Al+6HCl=2AlCl +3H ↑、
3 2
2Al+2H O+2NaOH=2NaAlO +3H ↑,据此判断反应物过量情况,并计算出生成氢气的物质
2 2 2
的量,结合相同条件下氢气的体积之比等于其物质的量之比进行计算。
【详解】54g铝粉的物质的量n(Al)= = =2mol,
n(HCl)=n(NaOH)=cV=1L×3mol∙L-1=3mol,铝和盐酸反应的化学方程式为
2Al+6HCl=2AlCl +3H ↑,由于2mol×6>3mol×2,则Al过量,3molHCl完全反应生成氢气
3 2
的物质的量为 ×3mol=1.5mol,铝和NaOH反应的化学方程式为
2Al+2H O+2NaOH=2NaAlO +3H ↑,由于2mol×2<3mol×2,则NaOH过量,2molAl完全反
2 2 2应生成氢气的物质的量为 ×2mol=3mol,相同条件下氢气的体积之比等于其物质的量之比,
所以铝粉分别与盐酸、氢氧化钠溶液反应产生的氢气的体积比为1.5mol∶3mol=1∶2,答案选
B。
11.D
【详解】设混合物中CO 和水的物质的量分别是xmol和ymol,则根据反应的方程式
2
2NaO+2CO=2NaCO+O △m
2 2 2 2 3 2
2mol 56g
2NaO+2HO=4NaOH+O △m
2 2 2 2
2mol 4g
可知28x+2y=3.6,又因为44x+18y=11.6,解得x=0.1、y=0.4,所以原混合气体的平均
摩尔质量为 ,D项正确,
答案选D。
12.D
【详解】A、CHCOOH为弱酸,不能拆成离子形式,错误;
3
B、Ba(OH) 与HSO 的反应还包含了H+与OH‾生成HO,错误;
2 2 4 2
C、CaCO 为难溶物质,不能拆成离子形式,错误;
3
D、HNO 和Cu(NO ) 为易溶于水的强电解质,拆成离子形式可得离子方程式,正确。
3 3 2
故答案为:D。
13.D
【详解】A.钠和水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2HO=2Na+
2
+2OH-+H ↑,故A错误;B.NaHCO 溶液中加过量Ca(OH) 溶液,离子方程式:Ca2+
2 3 2
+OH-+HCO-═CaCO+H O,故B错误;C.向氢氧化钡溶液中加入稀硫酸发生的离子反应
3 3 2
方程式为Ba2++2OH-+2H++SO 2-=BaSO ↓+2H 0,故C错误;D.NaAlO 溶液中通入过量
4 4 2 2
CO 制Al(OH),反应的离子方程式为:AlO-+CO +2H O=Al(OH)↓+HCO-,故D正
2 3 2 2 2 3 3
确;故选D。
点睛:离子方程式正误判断是高考高频知识点,解这类题主要是从以下几个方面考虑:①
反应原理,如:铁与盐酸或稀硫酸反应只生成二价铁;三氯化铝溶液与碳酸钠溶液混合发
生的是双水解反应,而不是复分解反应;Mg2+遇OH-和CO2-时更宜生成的是Mg(OH) 沉淀
3 2
等。②电解质的拆分,化学反应方程式改写为离子方程式时只有强酸、强碱及可溶性盐可
答案第4页,共2页以改写成完全电离形式,如NaHCO 只能改写成Na+和HCO -。③配平,离子方程式的配平
3 3
不能简单的满足原子守恒,而应该优先满足电子守恒、电荷守恒及原子守恒。④注意反应
物的用量对离子反应的影响。
14.C
【详解】A、单质铝的化学性质非常活泼,但在空气中会生成一层致密的氧化膜,防止Al
继续被腐蚀,所以铝在空气中不易腐蚀,选项A正确;
B.铝原子的最外层有3个电子,在化学反应中易失去3个电子而达8电子的稳定结构,失
去电子表现还原性,选项B正确;
C.铝和氧气反应生成了氧化铝,又因三氧化二铝的熔点高于铝的熔点,而三氧化二铝在
铝的表面,所以加热铝箔的时候铝失去了光泽,铝熔化了但是不会滴落,不会发生剧烈的
燃烧,选项C错误;
D、铝和氧气反应生成了氧化铝,又因三氧化二铝的熔点高于铝的熔点,而三氧化二铝在
铝的表面,兜住融化的铝,所以加热铝箔,铝熔化了但不会滴落,选项D正确;
答案选C。
【点睛】本题考查学生金属铝的有关知识,比较基础,旨在考查学生对基础知识的掌握。
15.B
【详解】A.合金的熔点比其组成金属的熔点要低,故纯铁的熔点高于铁合金,A错误;
B.纯铁和铁合金中都含有金属,故都能导电、传热,B正确;
C.合金的强度和硬度一般比组成金属的纯金属更高,故纯铁的硬度和强度都低于铁合金,
C错误;
D.不锈钢是铁合金,里面还有碳元素,D错误;
故选B。
16.B
【详解】①制程硬币的材料为合金,故①正确;② 根据胶体的性质当带不同电荷的胶粒相
遇时会发生聚沉,不同地方的泥土胶粒电荷不同,在入海口出聚沉形成沉淀,日积月累形
成三角洲,故②正确;③“钡餐”是硫酸钡,但硫酸钡是强电解质,因为尽管硫酸钡是难
溶物但溶于水的部分确实完全电离的,故③错误;④ 太阳能电池板中的硅在元素周期表是
第三周期第四主族,处于金属与非金属的交界位置,故④正确;⑤ 常用的自来水消毒剂有
氯气和HO,HO 含有极性键和非极性键,而氯气只含有非极性键,故⑤错误;⑥ 橡胶
2 2 2 2
是高分子化合物,故⑥ 正确;答案为B。
17.C【详解】A. 食盐水属于溶液,而蛋白质溶液属于胶体,胶体有丁达尔效应而溶液没有,故
可用激光笔照射区别食盐水和蛋白质溶液,A正确;
B. 铁氰化钾溶液可与Fe2+生成蓝色沉淀,这是Fe2+的特征反应,因此, 向溶液中滴入铁氰
化钾溶液,可检验溶液中是否存在Fe2+,B正确;
C. 实验室通常将湿润的红色石蕊试纸检验氨气,湿润的红色石蕊试纸遇氨气变蓝,C错误;
D. 向溶液中滴入足量稀盐酸后可以排除可能存在的干扰离子,然后再滴入氯化钡溶液,可
检验溶液中是否存在SO ,若有则生成白色沉淀,D正确。
本题选C。
18.D
【详解】A选项,NH 是碱性气体,溶于水显碱性,使酚酞溶液变红,故A不符合题意;
3
B选项,NaSiO 溶于水显碱性,使酚酞溶液变红,故B不符合题意;
2 3
C选项,NaHCO 溶于水显碱性,使酚酞溶液变红,故C不符合题意;
3
D选项,Al(OH) 是两性氢氧化物,不溶于水,不能使酚酞溶液变红,故D符合题意;
3
综上所述,答案为D。
19.D
【详解】A.镁可以空气中的氧气、二氧化碳发生反应,产物氮化镁可以与水发生反应,
故应先除去空气中的二氧化碳、氧气再干燥气体,装置①中盛放NaOH溶液,装置③中装
有浓硫酸,故A正确;
B.维生素C具有还原性,则先除去氧气,故B正确;
C.实验前先通空气,排尽装置中的氧气、二氧化碳等气体,再点燃酒精灯,使镁与氮气
反应,故C正确;
D.装置⑤的作用是防止外界的水蒸气进入装置④中与产物反应,影响产物的纯度,不能
用NaCl替换,故D错误;
故选:D。
20. ④⑧ ①③⑤⑧ ②⑥⑦ ①②③⑧
①⑤⑧ NaCO=2Na++CO 2- 渗析 1∶1 L
2 3 3
【分析】电解质:在水溶液中或熔融状态下能导电的化合物;
非电解质:在水溶液中和熔融状态下不能导电的化合物;
答案第6页,共2页物质导电条件:存在自由移动的离子,或者存在自由移动的电子;
金属离子或铵根离子(NH +)与酸根离子结合的化合物属于盐;
4
碳酸钠为强电解质,在水溶液中完全电离产生钠离子和碳酸根离子;
根据胶体与溶液中分散质微粒大小分离;
利用n= 及N=n·N 计算O原子数目;
A
利用微粒数目与质量成正比计算cg该气体的分子数目,再结合N=n·N 计算气体的物质的
A
量,最后根据V=n·V 计算气体在标准状况下的体积。
m
【详解】①NaCl固体,属于电解质;不含自由移动的离子,因此不导电;溶于水,能产生
自由移动的离子,水溶液能导电;
②液态CO,属于非电解质;不含自由移动的离子,因此不导电;溶于水,与水反应生成
2
电解质HCO,能产生自由移动的离子,水溶液能导电;
2 3
③液态氯化氢,属于电解质;由分子构成,不含自由移动的离子,因而不导电;溶于水,
在水分子作用下电离产生自由移动的离子,水溶液能导电;
④汞是金属单质,既不是电解质也不是非电解质;含有自由移动的电子,能导电;不溶于
水;
⑤固体BaSO,是由金属阳离子Ba2+和酸根离子SO 2-组成的化合物,属于电解质;不含自
4 4
由移动的离子,因而不导电;水中溶解度很小,水溶液几乎不导电;
⑥蔗糖,非电解质;不含自由移动的离子,不导电,水溶液也不导电;
⑦酒精,非电解质;不含自由移动的离子,不导电,水溶液也不导电;
⑧熔融的NaCO,是电解质;含有自由移动的离子,能导电;水溶液能电离产生自由移动
2 3
的离子Na+、CO2-,能导电;
3
因此在上述物质中
(1)能导电的是④⑧;
(2)属于电解质的是①③⑤⑧;
(3)属于非电解质的是②⑥⑦;
(4)物质溶于水后形成的溶液能导电的是①②③⑧;
(5)①NaCl固体;⑤固体BaSO;⑧熔融的NaCO,都是由金属阳离子与酸根离子形成化合
4 2 3
物,属于盐,故物质序号应该是①⑤⑧;
(6)碳酸钠为强电解质,在水溶液中完全电离产生Na+和CO2-,电离方程式:NaCO=2Na+
3 2 3
+CO 2-;
3(7)胶体分散质微粒直径在1nm~100nm之间,不能透过半透膜,而溶液中溶质微粒直径小
于1nm,可以透过半透膜,因此可用半透膜,通过渗析的方法分离胶体和溶液;
(8)假设物质的质量都是mg,则O 中含有的O原子的物质的量是n(O)= =
2
mol,O 中含有的O原子的物质的量是n(O)= = mol,可见等质量的O 和O
3 2 3
中含有的O原子的物质的量相同,根据N=n·N 可知:原子的物质的量相等,则原子数目
A
也相等,故二者含有的O原子个数比为1:1;
(9)若ag某气体中含有的分子数为b,则c g该气体含有的分子数目为N= ,由于N 为阿
A
伏加德罗常数的数值,则cg该气体的物质的量是n= = mol,则该气体在标准
状况下的体积V=n·V = mol×22.4L/mol= L。
m
【点睛】本题考查了物质的分类及物质的量的有关计算,熟悉电解质,非电解质,盐的概
念,掌握物质的量的有关计算公式,明确物质导电条件和微粒与物质质量、气体体积关系
式是解题关键。
21. 2NaO+2H O═4NaOH+O↑ NaO+HO═2NaOH 39g 31g
2 2 2 2 2 2
【分析】根据化学反应原理并结合物质的量在化学方程式计算中的应用分析。
【详解】过氧化钠和氧化钠分别跟水反应的化学方程式为2NaO+2H O═4NaOH+O↑,
2 2 2 2
NaO+HO═2NaOH;
2 2
设混和物中含NaO 的物质的量为xmol,NaO的物质的量为ymol,根据题意则有:
2 2 2
78x+62y=70、 ;解得:x=0.50、y=0.50;则
NaO 质量为0.50mol×78g/mol=39g,NaO的质量为0.50mol×62g/mol=31g。
2 2 2
【点睛】考查氧化钠和过氧化钠的性质和有关方程式的简单计算,明确反应原理是解题关
答案第8页,共2页键,可灵活应用原子守恒解题。
22. 2.2ɡ 66.7%、14.6%
【分析】在石灰石中加入稀盐酸,石灰石中的碳酸钙与盐酸反应生成氯化钙、水和二氧化
碳,根据生成的二氧化碳的量结合反应的化学方程式计算解答。
【详解】(1)反应生成二氧化碳的质量为:2.0g/L×1.1L=2.2g,故答案为:2.2ɡ;
(2)设石灰石中碳酸钙的质量为x,消耗氯化氢的质量为y。
= = ,解得:x=5g,y=3.55g,
石灰石中CaCO 的质量分数为 ×100%=66.7%;所用稀盐酸中溶质的质量分数为
3
×100%= 14.6%,故答案为:66.7%;14.6%。
23.
【分析】(1)根据方程式先求 ,再求原固体混合物中 的质量。
(2)根据方程式得到关系式, ,再求质量分数。
【详解】(1) , ,解
得 ,原固体混合物中 的质量为 ;故答
案为:4.16g。
(2) , ,
由此得关系式: ,则 ,解得;故答案为:67.2%。
【点睛】利用碳酸氢钠受热分解生成的二氧化碳,二氧化碳通入到澄清石灰水生成碳酸钙
沉淀,建立碳酸氢钠与碳酸钙的关系式进行计算。
答案第10页,共2页