文档内容
高一化学上学期第一次月考-(基础 A 卷)
班级___________ 姓名___________ 学号____________ 分数____________
(考试时间:90分钟 试卷满分:100分)
考试范围:第一章 物质及其变化 难度:★★★☆☆
注意事项:
1.本试卷分第I卷(选择题)和第II卷(非选择题)两部分。答卷前,考生务必将自己的班级、姓名、
学号填写在试卷上。
2.回答第I卷时,选出每小题答案后,将答案填在选择题上方的答题表中。
3.回答第II卷时,将答案直接写在试卷上。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
答案
第Ⅰ卷(选择题 54 分)
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.《神农本草经》说:“水银……熔化(加热)还复为丹”。《黄帝九鼎神丹经》中的“柔丹”“伏丹”都
是在土釡中加热Hg制得的。这里的“丹”是指( )
A.合金 B.氯化物
C.氧化物 D.硫化物
2.将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
3.下列不属于分散系的是( )
A.硫酸铜溶液 B.淀粉溶液 C.冰和水 D.氢氧化铁胶体
4.胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.产生丁达尔现象
C.分散质粒子直径在1~100 nmD.胶体在一定条件下能稳定存在
5.“纳米材料”(1 nm=10-9m )是指研究开发直径为几纳米至几十纳米的材料。如将“纳米材料”分散到
某液体中,对于所得分散系的叙述不正确的是( )
A.光束通过此分散系时会形成一条光亮的“通路”
B.此分散系中“纳米材料”的粒子在做不停的、无序的运动
C.在外加电场作用下,“纳米材料”的粒子可能向电极做定向运动
D.用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料”
6.如图表示的一些物质或概念间的从属关系中不正确的是( )
A.X为含氧酸、Y为酸、Z为化合物
B.X为氧化物、Y为化合物、Z为纯净物
C.X为强碱、Y为碱、Z为化合物
D.X为非金属氧化物、Y为酸性氧化物、Z为氧化物
7.下列物质属于电解质且能导电的是
A.酒精 B.金属铜 C.液态氯化氢 D.熔融氯化钾
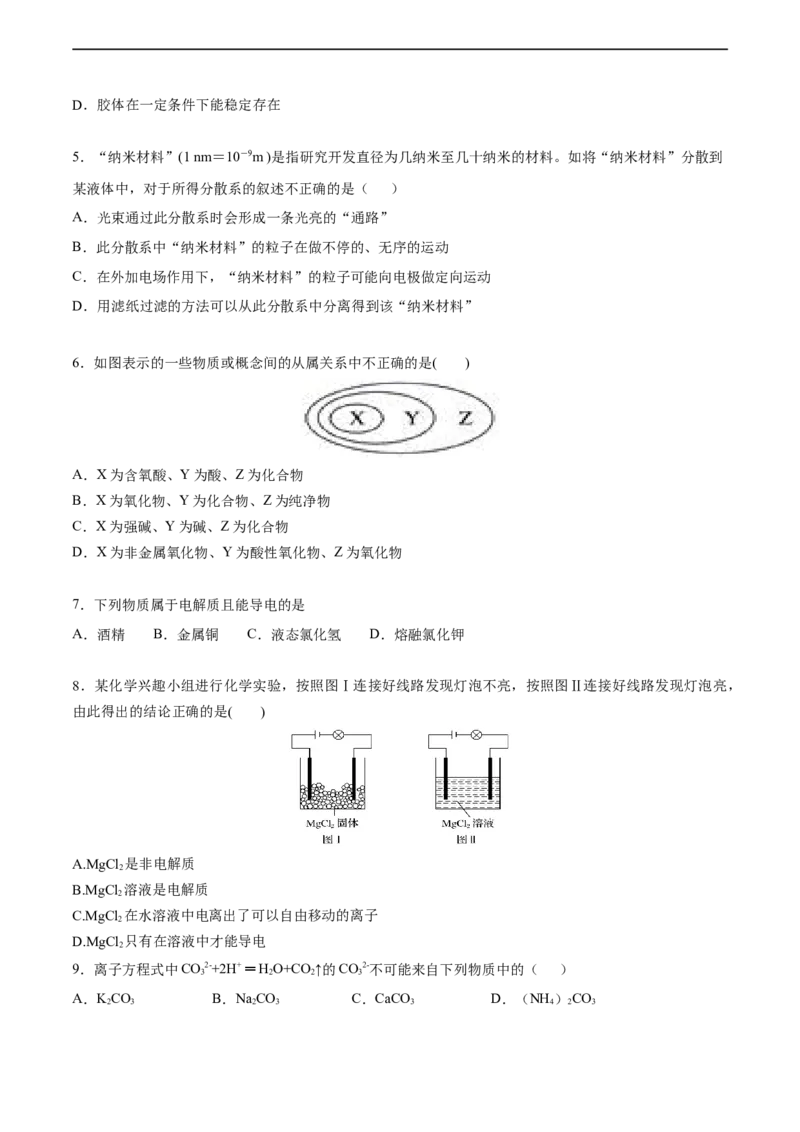
8.某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,
由此得出的结论正确的是( )
A.MgCl 是非电解质
2
B.MgCl 溶液是电解质
2
C.MgCl 在水溶液中电离出了可以自由移动的离子
2
D.MgCl 只有在溶液中才能导电
2
9.离子方程式中CO2-+2H+ ═ HO+CO↑的CO2-不可能来自下列物质中的( )
3 2 2 3
A.KCO B.NaCO C.CaCO D.(NH )CO
2 3 2 3 3 4 2 310.下列离子方程式中,正确的是
A.稀盐酸滴在铁片上:2Fe + 6 H+ = 2Fe3++3H ↑
2
B.碳酸氢钠溶液与稀盐酸混合:H++HCO- = H O+CO↑
3 2 2
C.硫酸铜溶液与氢氧化钡溶液混合:Cu2++2OH- = Cu(OH) ↓
2
D.硝酸银溶液与氯化钠溶液混合: AgNO+ Cl-=AgCl↓+ NO -
3 3
11.能用H+ + OH-= H O 来表示的化学反应是:( )
2
A. 溶液和 溶液反应 B.KOH溶液和 溶液反应
C.NaOH溶液和 溶液反应 D.CuO溶于稀 HCl
12.下列各组中的离子,能在溶液中大量共存的是( )。
A.H+、Cl-、Ca2+、
B.Na+、Mg2+、SO 2-、OH-
4
C.K+、Na+、OH-、Cl-
D.Cu2+、Ba2+、Cl-、SO 2-
4
13.下列物质转化过程中硫元素化合价降低的是( )
A.HSO →SO B.HS→SO
2 4 2 2 2
C.S→SO D.SO →SO
2 2 3
14.在下列变化中,需要加入合适的氧化剂才能实现的是( )
A.HCl→H B.CO→CO
2 2
C.Fe O→Fe D.Br-→Br
2 3 2
15.下列化学反应中,水既不是氧化剂又不是还原剂的是( )
A.2NaO+2HO===4NaOH+O↑
2 2 2 2
B.2F+2HO===4HF+O
2 2 2
C.2Na+2HO===2NaOH+H↑
2 2
D.NaH+HO===NaOH+H↑
2 216.一定条件下硝酸铵受热分解的化学方程式为:5NH NO =2HNO +4N ↑+9H O,在反应中被氧化与被还
4 3 3 2 2
原的氮原子数之比是( )
A.5:4 B.4:5 C.5:3 D.3:5
17.11.已知Co O 在酸性溶液中易被还原成Co2+,Co O 、Cl 、FeCl 、I 的氧化性依次减弱,下列反应
2 3 2 3 2 3 2
在水溶液中不可能发生的是( )
A.3Cl+6FeI===2FeCl +4FeI
2 2 3 3
B.Cl+2KI===2KCl+I
2 2
C.Co O+6HCl===2CoCl +Cl↑+3HO
2 3 2 2 2
D.2FeCl +Cl===2FeCl
2 2 3
18.黑火药在适当的外界能量作用下,能进行迅速的燃烧,瞬间产生大量的热并生成氮气、二氧化碳等气
体,由于体积急剧膨胀,压力猛烈增大,于是发生了爆炸。反应方程式为
S+2KNO +3C===K S+N↑+3CO ↑,下列说法不正确的是( )
3 2 2 2
A.S和KNO 都是氧化剂
3
B.生成1个N 转移10个电子
2
C.CO 是氧化产物
2
D.KS和N 都是还原产物
2 2
第 II 卷(非选择题 46 分)
二、非选择题(46分)
19.(8分)现有下列物质:①NaCO •10H O晶体 ②铜 ③硫酸溶液 ④CO ⑤NaHSO 固
3 2 2 4
体 ⑥Ba(OH) 固体 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩Al (SO ) 固体。
2 2 4 3
(1)上述物质属于电解质的有__________________(填编号)。
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H O,写出该离子反应对应的化学方程式
2
___________________________________。
(3)制取⑦的化学方程式___________________________;将⑥的溶液滴加到⑤的溶液中至恰好完全沉淀
时的离子方程式 。
20.(8分)某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH-、NO -六种
3
离子。(1)甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子_________、________、_________。
(2)乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。如果在乙厂废
水中加一定量_________(选填:活性炭或铁粉),离子方程式是 ,并
且能够回收其中的金属____________(填写金属元素符号)。
21(8分).用离子方程式表达下列应用或现象
(1)水垢的主要成分是碳酸钙和氢氧化镁,家庭中可用一定浓度的醋酸( CHCOOH)将其浸泡除去
3
(任写一个即可)
。
(2)向澄清石灰水中通二氧化碳气体变浑浊 。
(3)小苏打治疗胃酸过多 。
(4)向NaHSO 溶液中加入锌粉 。
4
22( 14分).取少量 Fe O 粉末( 红棕色) 加入适量盐酸, 得到黄色溶液, 用此溶液进行以下实验:
2 3
(1)在小烧杯中加入 20mL 蒸馏水, 加热至沸腾后, 向沸水中加入制取的黄色溶液 2mL, 继续煮沸
至液体呈______色, 停止加热, 用激光笔照射烧杯中的液体, 可以观察到液体中
, 用这个实验可以区别_______和_______。
(2)氢氧化铁胶体制备的原理
(3)向烧杯中逐滴加入过量的盐酸, 会出现一系列变化:现象
原因 ( 用离子方程式表示)
(4)氢氧化铁胶体稳定存在的主要原因是______________________________________。
23(8分).根据反应8NH +3Cl=6NHCl+N ,回答下列问题:
3 2 4 2
(1)氧化剂是_______________ , 还原剂是________________。
(2)氧化剂和还原剂的分子个数比___________________________。
(3)当有68克氨气参加反应时,被氧化的物质为_____________克, 生成还原产物为_________克。