文档内容
下学期期末测试卷 03 4.国际纯粹与应用化学联合会(IUPAC)将周期表第116号元素Lv命名为“鉝”(lì)。下列关于 Lv
高一化学 的说法中,不正确的是
A.中子数为293 B.与氧、硫位于同一主族
(考试时间:90分钟 试卷满分:100分)
注意事项: C.核外电子数为116 D.与 Lv互为同位素
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
5.下列有关有机物种类众多的原因的叙述中不正确的是
证号填写在答题卡上。
A.碳原子既可以跟碳原子形成共价键,又可以跟其它原子形成共价键
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
B.碳原子性质活泼,可以跟多数原子形成共价键和离子键
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。 的
C.碳原子之间既可以形成稳定 单键,又可以形成稳定的双键和三键
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
D.碳原子之间可以形成长度不同的碳链和碳环,且碳链、碳环之间又可以相互结合
4.测试范围:新人教版(2019)必修2全册。
5.考试结束后,将本试卷和答题卡一并交回。 6.氮气的用途很广泛,下列不属于氮气用途的是
6.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
A.合成氨制作氮肥 B.充入灯泡作保护气
Ca 40 Fe 56 Zn-65
C.液氮可作制冷剂 D.医疗上可作为危重病人的急救气
第Ⅰ卷
7.SO 可用作红酒的防腐剂。下列关于SO 的叙述不正确的是
2 2
A.无色无味气体
一、选择题:本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,只有一项符合题目要
B.能与氢氧化钠溶液反应
求。
C.能使品红溶液褪色
1.近年来,我国在探索太空、开发5G,以及在抗击新冠肺炎等方面都取得了举世瞩目的成就这些成就都
D.一定条件下,能与氧气反应
与化学有着密切的联系。下列有关说法正确的是
的
8.下列金属在冷、浓 硝酸或硫酸中,能形成致密氧化膜的是
A.用75%的医用酒精杀死新型冠状病毒,是利用了酒精的强氧化性
B.大飞机C919采用了大量复合材料与铝锂合金,铝锂合金属于金属材料
A.Mg B.Fe C.Cu D.Na
C.5G技术的应用离不开光缆,我国光缆线路总长度超过了三千万千米,光缆的主要成分是晶体硅
9.在2 L密闭容器中充入一定量的SO 和O,化学方程式是2 SO + O 2 SO 。经测定反应开
2 2 2 2 3
D.“神舟十二号”宇宙飞船返回舱外表面使用的高温结构陶瓷属于有机高分子材料
始后3 s末O 的物质的量减小了1.5 mol,则前3 s内SO 的平均反应速率为
2 2
2.化学与生活、生产、社会可持续发展密切相关。下列说法错误的是
A.0.25 mol·L-1·s-1 B.0.5 mol·L-1·s-1 C.0.75 mol·L-1·s-1 D.0.83 mol·L-1·s-1
A.牙膏中添加的NaPO F、NaF所提供的氟离子浓度相等时,它们防治龋齿的作用相同
2 3 10.下列性质的比较中,正确的是
B.“光化学烟雾” “硝酸型酸雨”的形成都与氮氧化合物有关
A.非金属性:Br > Cl B.稳定性:HS > HO
2 2
C.用聚氯乙烯代替木材,生产快餐盒,以减少木材的使用
C.酸性:HCO > HNO D.碱性:Ca(OH) > Mg(OH)
2 3 3 2 2
D.碳纳米管比表面积大,可用作新型储氢材料
11.中国科学院上海硅酸盐研究所设计出以金属锂作负极,以“催化剂一碳一催化剂”结构的材料作正极
3.国内大多数一二线城市都已经或即将在2021年底前基本建成生活垃圾分类处理系统。下列关于垃圾处理
的高稳定锂硫电池,具有较高的能量密度(单位质量的电池所放出的能量)。下列关于这种电池的说
的说法不正确的是
法错误的是
A.废旧塑料瓶可回收利用 B.废旧电池可直接掩埋
A.能量密度高的原因之一是锂的相对原子质量小
C.电子垃圾可用适当的方法回收利用 D.厨余垃圾可经生物技术处理堆肥
B.放电时电能转化为化学能C.放电时硫在正极上发生还原反应 下列说法不正确的是( )
D.放电时锂离子向正极移动
A.制取乙酸乙酯的反应为:CHCOOH + C H18OH CHCO18OC H+ HO
3 2 5 3 2 5 2
11.用化学方法区别NaCl、MgCl 、AlCl 、CuCl 、FeCl 和NH Cl六种溶液(必要时可加热),下列试剂
2 3 2 3 4
B.步骤②~④有机层处于下层,涉及的实验操作为分液、过滤
中可选用的是
C.步骤②目的是将碳酸钠从乙酸乙酯中萃取出来
A.KSCN溶液 B.AgNO 溶液 C.BaCl 溶液 D.NaOH溶液
3 2
D.步骤③目的是除去乙醇
13.下列说法中,正确的是
18.下列实验结论与实验操作及现象不相符的一组是
A.标准状况下,1.0 mol SO 体积约为22.4 L
2
选项 实验操作及现象 实验结论
B.63 g HNO 含有的原子总数约为6.02×1023
3
C.标准状况下,18 g HO的体积约为22.4 L 向某酸雨样品中加入Ba(OH) 溶液,有白色沉
2 A 2 酸雨试样中一定含SO 2-
淀生成 4
D.0.1 mol/L MgCl 溶液中含有0.2 mol Cl-
2
B 向KI-淀粉溶液中滴入氯水,溶液变成蓝色 I-的还原性强于Cl-
14.自热食品不用火电,将水倒在发热包上,发热包遇水自动升温,从而加热食物。发热包的主要成分是:
生石灰、铁粉、焦炭粉、活性炭、碳酸钠、焙烧硅藻土等,下列不正确的是 将Ba(OH) ·8H O和NH Cl晶体在小烧杯中混 Ba(OH) ·8H O与NH Cl
C 2 2 4 2 2 4
合搅拌,用手触摸烧杯外壁感觉变凉 的反应是吸热反应
A.生石灰和水反应生成熟石灰放出热量
向某盐溶液中加入NaOH溶液,加热,用湿润
B.熟石灰和碳酸钠反应:Ca(OH) + NaCO = CaCO ↓ + 2 NaOH D 该盐溶液中含有NH +
2 2 3 3 的红色石蕊试纸放在试管口,试纸变蓝 4
C.过程中形成许多微小的铁碳原电池,其中碳做正极
19.一定条件下,在密闭容器中进行反应:3 SiCl (g) + 2 N(g) + 6 H(g) Si N(s) +
4 2 2 3 4
D.铁碳原电池的正极反应为:O + 4e-+ 4 H+ = 2 HO
2 2
12HCl(g)。不能表示上述反应达到化学平衡状态的是
15.合成氨工业为人类解决粮食问题做出了巨大贡献。一定条件下,在密闭容器中进行合成氨反应:N(g)
2
A.单位时间消耗2 mol N,同时生成6 mol H
2 2
+ 3 H(g) NH (g),当正、逆反应速率相等且不等于零时,下列说法不正确的是
2 3
B.c(HCl)保持不变
A.N、H 完全转化为NH B.N、H、NH 在容器中共存
2 2 3 2 2 3
C.混合气体密度保持不变
C.反应已达到化学平衡状态 D.N、H、NH 的浓度不再改变
2 2 3
D.c(N )∶c(H )∶c(HCl) = 1∶3∶6
2 2
16.设N 表示阿伏加德罗常数,下列叙述正确的是
A
20.黑火药爆炸时的反应为:S+2KNO+3C=K S+N↑+3CO↑,下列说法错误的是
3 2 2 2
A. 15g甲基( )中含有的电子数为9N A A.每生成11.2 L的N 2 ,该反应转移电子物质的量为6 mol
B.被氧化的物质为:C
B. 标准状况下,2.24L辛烷中所含碳原子数为0.8N
A
C.氧化产物:CO
2
C. 1.8g 与DO的混合物中含有的质子数和电子数均为N
2 A
D.该反应中氧化剂是:S、KNO
3
D. —定条件下,密闭容器中2mol SO (g)与1mol O(g)充分反应,则容器中分子数为2N
2 2 A 第 II 卷(非选择题 60 分)
17.实验室制得的乙酸乙酯中常含有乙酸、乙醇和少量水,其精制过程如下:已知:乙醇能与CaCl 反应生
2
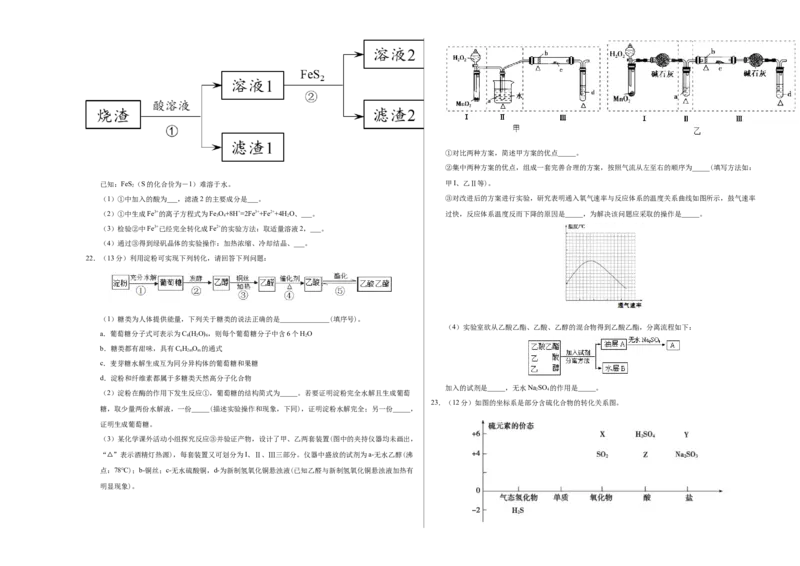
21.(11分)由硫铁矿“烧渣”(主要成分:Fe O、Fe O 和FeO)制备绿矾(FeSO ·7H O)的流程如图:
3 4 2 3 4 2
成CaCl •4C HOH,碳酸钠微溶于乙酸乙酯
2 2 5
①向粗制乙酸乙酯中加入饱和碳酸钠溶液,振荡
②静置分层后,取有机层,向其中加入饱和食盐水,振荡
③静置分层后,取有机层,向其中加入饱和氯化钙溶液,振荡
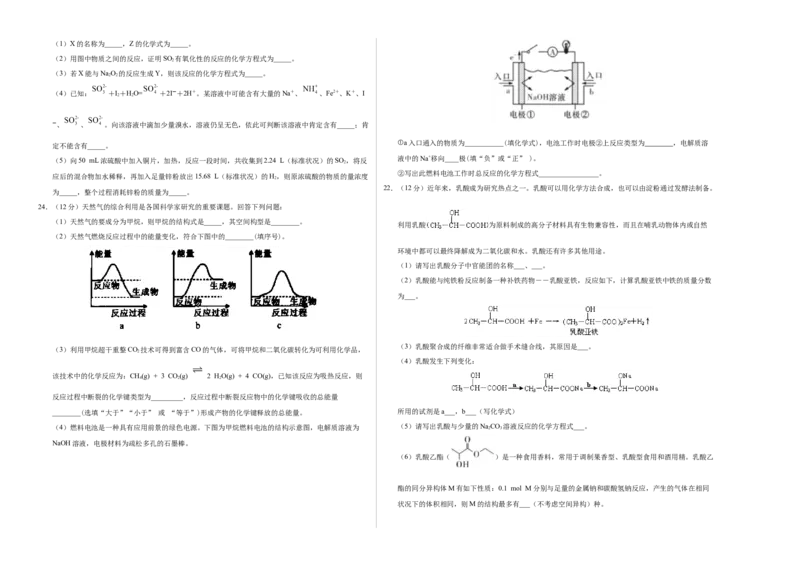
④静置分层后,取有机层,加入无水硫酸镁固体,进行干燥①对比两种方案,简述甲方案的优点_____。
②集中两种方案的优点,组成一套完善合理的方案,按照气流从左至右的顺序为_____(填写方法如:
已知:FeS(S的化合价为-1)难溶于水。 甲I、乙Ⅱ等)。
2
(1)①中加入的酸为___,滤渣2的主要成分是___。 ③对改进后的方案进行实验,研究表明通入氧气速率与反应体系的温度关系曲线如图所示,鼓气速率
(2)①中生成Fe3+的离子方程式为Fe O+8H+=2Fe3++Fe2++4H O、___。 过快,反应体系温度反而下降的原因是_____,为解决该问题应采取的操作是_____。
3 4 2
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,___。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、___。
22.(13分)利用淀粉可实现下列转化,请回答下列问题:
(1)糖类为人体提供能量,下列关于糖类的说法正确的是______________(填序号)。
(4)实验室欲从乙酸乙酯、乙酸、乙醇的混合物得到乙酸乙酯,分离流程如下:
a.葡萄糖分子式可表示为C (H O) ,则每个葡萄糖分子中含6个HO
6 2 6 2
b.糖类都有甜味,具有C H O 的通式
n 2m m
c.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
d.淀粉和纤维素都属于多糖类天然高分子化合物
加入的试剂是_____,无水NaSO 的作用是_____。
2 4
(2)淀粉在酶的作用下发生反应①,葡萄糖的结构简式为_____。若要证明淀粉完全水解且生成葡萄
23.(12分)如图的坐标系是部分含硫化合物的转化关系图。
糖,取少量两份水解液,一份_____(描述实验操作和现象,下同),证明淀粉水解完全;另一份_____,
证明生成葡萄糖。
(3)某化学课外活动小组探究反应③并验证产物,设计了甲、乙两套装置(图中的夹持仪器均未画出,
“ ”表示酒精灯热源),每套装置又可划分为I、Ⅱ、Ⅲ三部分。仪器中盛放的试剂为a-无水乙醇(沸
点△:78℃);b-铜丝;c-无水硫酸铜,d-为新制氢氧化铜悬浊液(已知乙醛与新制氢氧化铜悬浊液加热有
明显现象)。(1)X的名称为_____,Z的化学式为_____。
(2)用图中物质之间的反应,证明SO 有氧化性的反应的化学方程式为_____。
2
(3)若X能与NaO 的反应生成Y,则该反应的化学方程式为_____。
2 2
(4)已知: +I+HO= +2I-+2H+。某溶液中可能含有大量的Na+、 、Fe2+、K+、I
2 2
-、 、 。向该溶液中滴加少量溴水,溶液仍呈无色,依此可判断该溶液中肯定含有_____;肯
①a入口通入的物质为___________(填化学式),电池工作时电极②上反应类型为 ,电解质溶
定不能含有_____。
液中的Na+移向____极(填“负”或“正” )。
(5)向50 mL浓硫酸中加入铜片,加热,反应一段时间,共收集到2.24 L(标准状况)的SO ,将反
2
②写出此燃料电池工作时总反应的化学方程式_________________。
应后的混合物加水稀释,再加入足量锌粉放出15.68 L(标准状况)的H,则原浓硫酸的物质的量浓度
2
22.(12分)近年来,乳酸成为研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过发酵法制备。
为_____,整个过程消耗锌粉的质量为_____。
24.(12分)天然气的综合利用是各国科学家研究的重要课题。回答下列问题:
(1)天然气的要成分为甲烷,则甲烷的结构式是_____,其空间构型是________。
利用乳酸 为原料制成的高分子材料具有生物兼容性,而且在哺乳动物体内或自然
(2)天然气燃烧反应过程中的能量变化,符合下图中的________(填序号)。
环境中都可以最终降解成为二氧化碳和水。乳酸还有许多其他用途。
(1)请写出乳酸分子中官能团的名称___、___。
(2)乳酸能与纯铁粉反应制备一种补铁药物--乳酸亚铁,反应如下,计算乳酸亚铁中铁的质量分数
为___。
(3)乳酸聚合成的纤维非常适合做手术缝合线,其原因是___。
(3)利用甲烷超干重整CO 技术可得到富含CO的气体,可将甲烷和二氧化碳转化为可利用化学品,
2
(4)乳酸发生下列变化:
该技术中的化学反应为:CH(g) + 3 CO(g) 2 HO(g) + 4 CO(g),已知该反应为吸热反应,则
4 2 2
反应过程中断裂的化学键类型为_________,反应过程中断裂反应物中的化学键吸收的总能量
________(选填“大于”“小于” 或 “等于”)形成产物的化学键释放的总能量。 所用的试剂是a___,b___(写化学式)
(4)燃料电池是一种具有应用前景的绿色电源。下图为甲烷燃料电池的结构示意图,电解质溶液为 (5)请写出乳酸与少量的Na 2 CO 3 溶液反应的化学方程式___。
NaOH溶液,电极材料为疏松多孔的石墨棒。
(6)乳酸乙酯( )是一种食用香料,常用于调制果香型、乳酸型食用和酒用精。乳酸乙
酯的同分异构体M有如下性质:0.1 mol M分别与足量的金属钠和碳酸氢钠反应,产生的气体在相同
状况下的体积相同,则M的结构最多有___(不考虑空间异构)种。