文档内容
下学期期末测试卷 02
高一化学
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:人教版2019必修第二册全册
5.考试结束后,将本试卷和答题卡一并交回。
第Ⅰ卷
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,每题只有一项符合题目
要求。
1.下列化学物质在实际生产生活和科技等方面的叙述正确的是
A.SO 、漂白粉、NaO 都能使品红溶液褪色,其作用原理相同
2 2 2
B.在食品袋中放入装有硅胶、铁粉的透气小袋,可防止食物受潮、氧化变质
C.高温结构陶瓷、压电陶瓷等新型陶瓷均属于硅酸盐材料
D.某雨水样品放置一段时间酸性增强,是因为空气中的CO 溶解进入雨水
2
2.铁元素在细菌的作用下可发生下图所示的转化。下列说法正确的是A.反硝化过程均属于氮的固定
B.硝化过程中,含氮物质均发生还原反应
C.Fe3+将NH 转化为N 的离子方程式为:6Fe3++2NH = 6Fe2++N ↑+8H+
2 2
D.在氨氧化细菌作用下,水体中的铵态氮和硝态氮可转移到大气,该反应中每产生0.01mol氮气时,转移
的电子为0.06mol
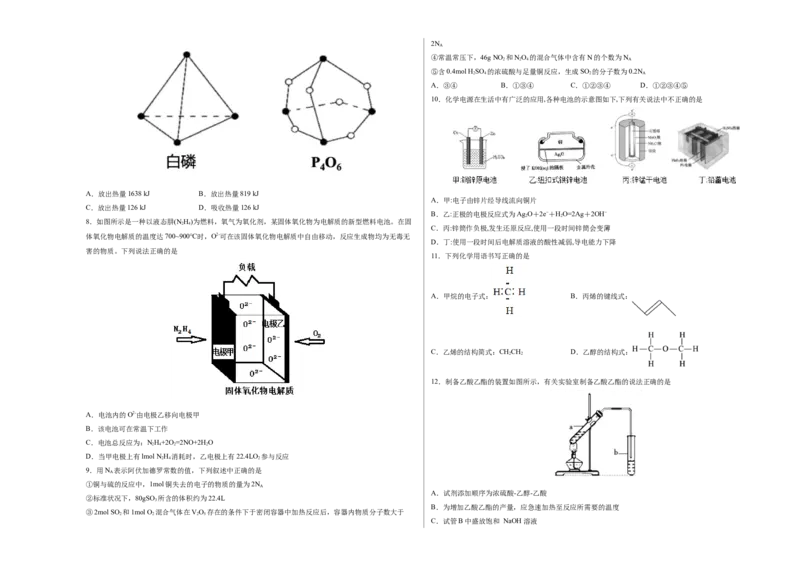
3.如图所示装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
气体 a b c
A CO 盐酸 碳酸钙 饱和NaHCO 溶液
2 3
B SO 浓硫酸 Fe 浓硫酸
2
C NH 浓氨水 生石灰 碱石灰
3 化石燃料的燃烧 植物的光合作用 氢气与氧气反应 氢气与氯气反应
D Cl 浓盐酸 MnO 粉末 浓硫酸
2 2
4.下列方程式书写不正确的是 6.反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为:
①v(A)=0.45mol/(L·min) ②v(B)=0.6mol/(L·s) ③v(C)=0.4mol/(L·s) ④v(D)=0.45mol/(L·s)
A.浓硫酸滴入蔗糖中,固体变黑,产生刺激性气味气体:C + 2H SO (浓) CO↑ + 2SO↑+ 2H O
2 4 2 2 2 下列有关反应速率的比较中正确的是
A.④>③=②>① B.①>④>③=② C.①>②>③>④ D.④>③>②>①
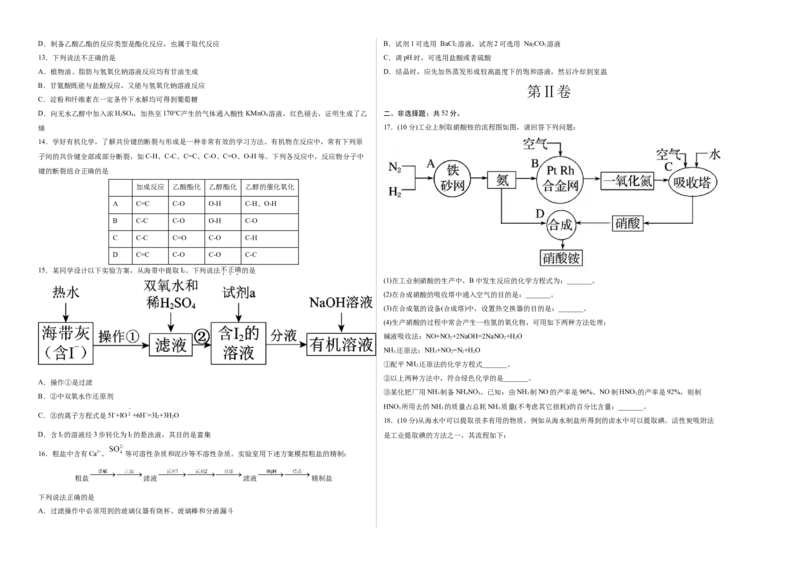
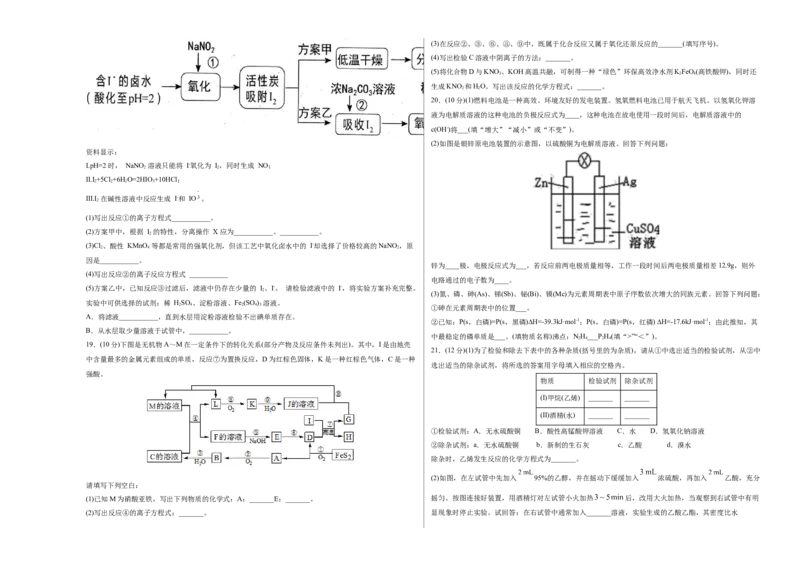
7.白磷(P )和PO 的分子结构如下图所示, 已知相关化学键的键能(断裂1 mol化学键所需的能量):P-P键
B.以空气和镁为原料制备MgN 的原理: 3Mg+N MgN 4 4 6
3 2 2 3 2
198 kJ/mol、P-O键360 kJ/mol、O=O键498 kJ/mol。则62g白磷(P )发生反应:P (白磷)+3O P O 时的
4 4 2 4 6
C.铁和硫加热条件下反应: 2Fe + 3S Fe S
2 3
能量变化为
D.“气肥”碳酸氢铵要低温保存,因其受热易分解:NH HCO NH ↑+CO ↑+ H O
4 3 3 2 2
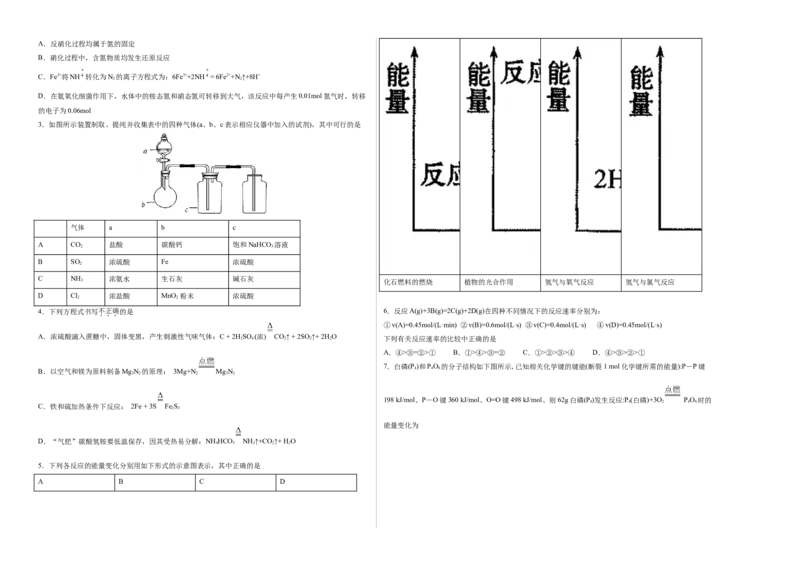
5.下列各反应的能量变化分别用如下形式的示意图表示,其中正确的是
A B C D2N
A
④常温常压下,46g NO 和NO 的混合气体中含有N的个数为N
2 2 4 A
⑤含0.4mol H SO 的浓硫酸与足量铜反应,生成SO 的分子数为0.2N
2 4 2 A
A.③④ B.①③④ C.①②③④ D.①②③④⑤
10.化学电源在生活中有广泛的应用,各种电池的示意图如下,下列有关说法中不正确的是
A.放出热量1638 kJ B.放出热量819 kJ
A.甲:电子由锌片经导线流向铜片
C.放出热量126 kJ D.吸收热量126 kJ
B.乙:正极的电极反应式为Ag O+2e−+HO=2Ag+2OH−
2 2
8.如图所示是一种以液态肼(N H)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。在固
2 4
C.丙:锌筒作负极,发生还原反应,使用一段时间锌筒会变薄
体氧化物电解质的温度达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无
D.丁:使用一段时间后电解质溶液的酸性减弱,导电能力下降
害的物质。下列说法正确的是
11.下列化学用语书写正确的是
A.甲烷的电子式: B.丙烯的键线式:
C.乙烯的结构简式:CHCH D.乙醇的结构式:
2 2
12.制备乙酸乙酯的装置如图所示,有关实验室制备乙酸乙酯的说法正确的是
A.电池内的O2-由电极乙移向电极甲
B.该电池可在常温下工作
C.电池总反应为:NH+2O =2NO+2HO
2 4 2 2
D.当甲电极上有lmol N H 消耗时,乙电极上有22.4LO 参与反应
2 4 2
9.用N 表示阿伏加德罗常数的值,下列叙述中正确的是
A
①铜与硫的反应中,1mol铜失去的电子的物质的量为2N
A
A.试剂添加顺序为浓硫酸-乙醇-乙酸
②标准状况下,80gSO 所含的体积约为22.4L
3
B.为增加乙酸乙酯的产量,应急速加热至反应所需要的温度
③2mol SO 和1mol O 混合气体在VO 存在的条件下于密闭容器中加热反应后,容器内物质分子数大于
2 2 2 5
C.试管B中盛放饱和 NaOH 溶液D.制备乙酸乙酯的反应类型是酯化反应,也属于取代反应 B.试剂1可选用 BaCl 溶液,试剂2可选用 NaCO 溶液
2 2 3
13.下列说法不正确的是 C.调pH时,可选用盐酸或者硫酸
A.植物油、脂肪与氢氧化钠溶液反应均有甘油生成 D.结晶时,应先加热蒸发形成较高温度下的饱和溶液,然后冷却到室温
B.甘氨酸既能与盐酸反应,又能与氢氧化钠溶液反应 第Ⅱ卷
C.淀粉和纤维素在一定条件下水解均可得到葡萄糖
D.向无水乙醇中加入浓HSO ,加热至170℃产生的气体通入酸性KMnO 溶液,红色褪去,证明生成了乙 二、非选择题:共52分。
2 4 4
烯 17.(10分)工业上制取硝酸铵的流程图如图,请回答下列问题:
14.学好有机化学,了解共价键的断裂与形成是一种非常有效的学习方法。有机物在反应中,常有下列原
子间的共价键全部或部分断裂,如C-H、C-C、C=C、C-O、C=O、O-H等。下列各反应中,反应物分子中
键的断裂组合正确的是
加成反应 乙酸酯化 乙醇酯化 乙醇的催化氧化
A C=C C-O O-H C-H、O-H
B C-C C-O O-H C-O
C C-C C=O C-O C-H
D C=C C-O C-O C-C
15.某同学设计以下实验方案,从海带中提取I。下列说法不正确的是
2
(1)在工业制硝酸的生产中,B中发生反应的化学方程式为:_______。
(2)在合成硝酸的吸收塔中通入空气的目的是:_______。
(3)在合成氨的设备(合成塔)中,设置热交换器的目的是:_______。
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO +2NaOH=2NaNO +H O
2 2 2
NH 还原法:NH +NO=N +H O
3 3 2 2 2
①配平NH 还原法的化学方程式_______。
3
②以上两种方法中,符合绿色化学的是_______。
A.操作①是过滤
③某化肥厂用NH 制备NH NO 。已知:由NH 制NO的产率是96%、NO制HNO 的产率是92%,则制
B.②中双氧水作还原剂 3 4 3 3 3
HNO 所用去的NH 的质量占总耗NH 质量(不考虑其它损耗)的百分比含量:_______。
3 3 3
C.③的离子方程式是5I–+IO +6H+=3I +3H O
2 2
18.(10分)从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法
D.含I 的溶液经3步转化为I 的悬浊液,其目的是富集 是工业提取碘的方法之一,其流程如下:
2 2
16.粗盐中含有Ca2+、 等可溶性杂质和泥沙等不溶性杂质。实验室用下述方案模拟粗盐的精制:
粗盐 滤液 滤液 精制盐
下列说法正确的是
A.过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和分液漏斗(3)在反应②、③、⑥、⑧、⑨中,既属于化合反应又属于氧化还原反应的_______(填写序号)。
(4)写出检验C溶液中阴离子的方法:_______。
(5)将化合物D与KNO、KOH高温共融,可制得一种“绿色”环保高效净水剂KFeO(高铁酸钾),同时还
3 2 4
生成KNO 和HO。写出该反应的化学方程式:_______。
2 2
20.(10分)(1)燃料电池是一种高效、环境友好的发电装置。氢氧燃料电池已用于航天飞机。以氢氧化钾溶
液为电解质溶液的这种电池的负极反应式为____,这种电池在放电使用一段时间后,电解质溶液中的
c(OH-)将___(填“增大”“减小”或“不变”)。
(2)如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
资料显示:
Ⅰ.pH=2 时, NaNO 溶液只能将 I-氧化为 I,同时生成 NO;
2 2
Ⅱ.I +5Cl+6H O=2HIO +10HCl;
2 2 2 3
Ⅲ.I 在碱性溶液中反应生成 I-和 IO 。
2
(1)写出反应①的离子方程式___________。
(2)方案甲中,根据 I 的特性,分离操作 X 应为___________、___________。
2
(3)Cl 、酸性 KMnO 等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO ,原
2 4 2
因是___________。
锌为____极,电极反应式为___,若反应前两电极质量相等,工作一段时间后两电极质量相差12.9g,则外
(4)写出反应②的离子反应方程式 ___________
电路通过的电子数为____。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I、I-。 请检验滤液中的 I-,将实验方案补充完整。
2
(3)氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
实验中可供选择的试剂:稀 HSO 、淀粉溶液、Fe (SO ) 溶液。
2 4 2 4 3
①砷在元素周期表中的位置___。
A.将滤液___________,直到水层用淀粉溶液检验不出碘单质存在。
②已知:P(s,白磷)=P(s,黑磷)∆H=-39.3kJ·mol-1;P(s,白磷)=P(s,红磷) ∆H=-17.6kJ·mol-1;由此推知,其
B.从水层取少量溶液于试管中,___________。
中最稳定的磷单质是___。(填物质名称)沸点:NH___PH(填“>”“<”)。
2 4 2 4
19.(10分)下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由地壳
21.(12分)(1)为了检验和除去下表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中
中含量最多的金属元素组成的单质,反应⑦为置换反应,D为红棕色固体,K是一种红棕色气体,C是一种
选出适当的除杂试剂,将所选的答案用字母填入相应的空格内。
强酸。
物质 检验试剂 除杂试剂
(Ⅰ)甲烷(乙烯) _______ _______
(Ⅱ)酒精(水) _______ _______
①检验试剂:A.无水硫酸铜 B.酸性高锰酸钾溶液 C.水 D.氢氧化钠溶液
②除杂试剂:a.无水硫酸铜 b.新制的生石灰 c.乙酸 d.溴水
除杂时,乙烯发生反应的化学方程式为_______。
(2)如图,在左试管中先加入 95%的乙醇,并在摇动下缓缓加入 浓硫酸,再加入 乙酸,充分
请填写下列空白:
(1)已知M为硝酸亚铁,写出下列物质的化学式:A:_______E:_______。 摇匀。按图连接好装置,用酒精灯对左试管小火加热 后,改用大火加热,当观察到右试管中有明
(2)写出反应④的离子方程式:_______。 显现象时停止实验。试回答:在右试管中通常加入_______溶液,实验生成的乙酸乙酯,其密度比水_______,是有特殊香味的液体,反应中加入浓硫酸的作用是_______。请写出左侧试管中的反应方程式
_______。