文档内容
绝密★考试结束前(寒假返校联考)
浙江省新阵地教育联盟 2024 届第三次联考
化学试题卷
考生须知:
1.本试题卷分选择题和非选择题两部分,满分100分,考试时间90分钟.
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字.
3.所有答案必须写在答题卷上,写在试卷上无效;考试结束后,只需上交答题卷.
4.可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Na-23 Si-28 S-32 Mg-24
Al-27 Fe-56 Cu-64
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分.每小题列出的四个选项中只有一个符合
题目要求,不选、多选、错选均不得分)
1.下列常见物质中,不属于碱性氧化物的是( )
A. B. C. D.
2.下列化学用语表示合理的是( )
A.氮的基态原子的价电子排布图:
B.异戊二烯的键线式为:
C.乙醛分子空间填充模型为:
D. 中 键的电子云轮廓图:
3.碳酸钠和碳酸氢钠在生产生活中有广泛的应用.下列有关说法不合理的是( )
A.通过化合反应可由碳酸钠制得碳酸氢钠
B.可用碳酸钠溶液处理锅炉水垢中的硫酸钙:
C.向 浓度均为 和 溶液中分别滴加浓的 溶液,只有碳酸钠溶液产生白
色沉淀
D.碳酸钠溶液和碳酸氢钠溶液都显碱性,均可用作食用碱
4.物质的性质决定用途.下列两者对应关系不正确的是( )
学科网(北京)股份有限公司A.二氧化硫具有漂白性,食品中添加适量的 有防腐和抗氧化作用
B.氯化铁溶液有氧化性,可用于蚀刻不锈钢广告牌上的图形
C.生铁硬度大,抗压性强,可用于铸造机器底座
D.新型陶瓷碳化硅( )硬度很大,可用作砂纸和砂轮的磨料
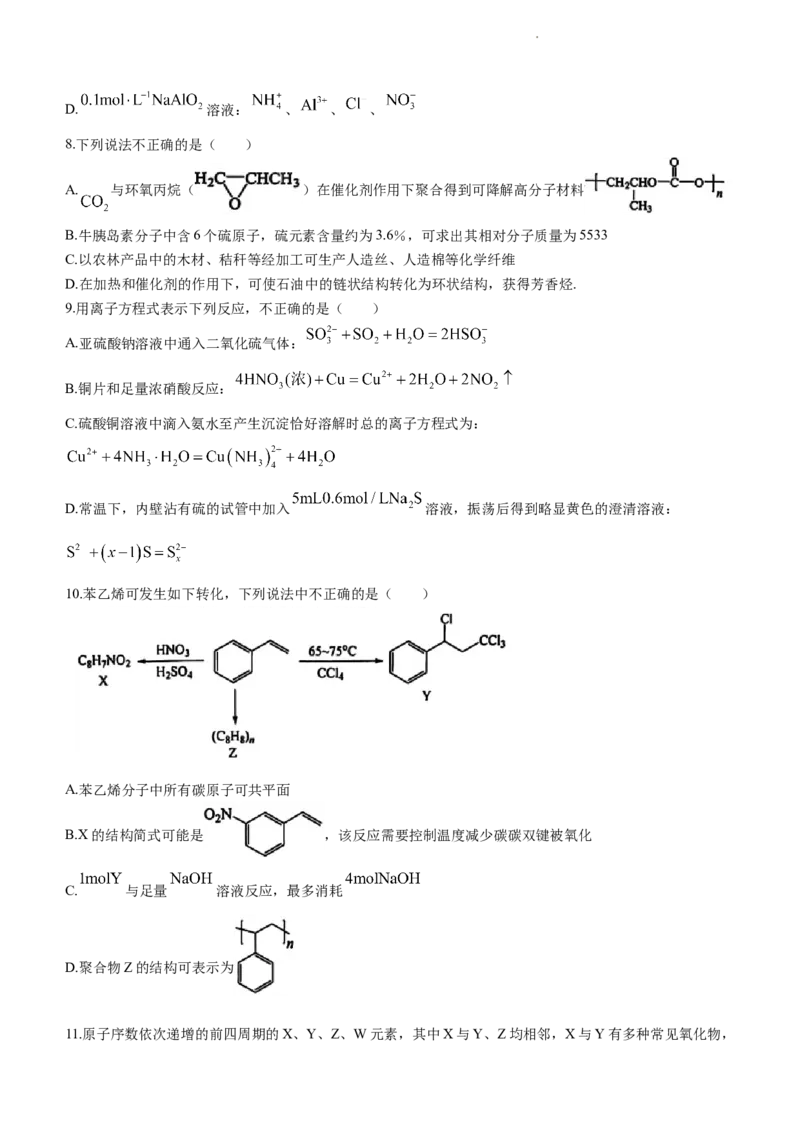
5.下列设计正确且能实现实验目的的是( )
图① 图② 图③ 图④
A.图①,验证 可溶于氨水
B.图②,验证氯气和甲烷反应生成了
C.图③,闭合 一段时间,再打开 闭合 可制得简易燃料电池,左侧石墨为电池负极
D.图④,分别加热不能证明 分解温度高于
6.二氧化氯泡腾片是常用的鱼缸消毒剂,也可用于除居室甲醛,其反应方程式可表示为:
,下列说法不正确的是( )
A.甲醛具有还原性
B.二氧化氯是氧化剂,还原产物为
C.反应生成 ,则转移4mol电子
D.若将二氧化氯改为次氯酸钠,消耗等量甲醛所需 与 的物质的量之比为
7.室温下,下列各组离子在指定溶液中可能大量共存的是( )
A.水电离出的 的溶液中: 、 、 、
B.加入铝粉能放出氢气的溶液中: 、 、
C.透明的溶液中: 、 、 、
学科网(北京)股份有限公司D. 溶液: 、 、 、
8.下列说法不正确的是( )
A. 与环氧丙烷( )在催化剂作用下聚合得到可降解高分子材料
B.牛胰岛素分子中含6个硫原子,硫元素含量约为3.6%,可求出其相对分子质量为5533
C.以农林产品中的木材、秸秆等经加工可生产人造丝、人造棉等化学纤维
D.在加热和催化剂的作用下,可使石油中的链状结构转化为环状结构,获得芳香烃.
9.用离子方程式表示下列反应,不正确的是( )
A.亚硫酸钠溶液中通入二氧化硫气体:
B.铜片和足量浓硝酸反应:
C.硫酸铜溶液中滴入氨水至产生沉淀恰好溶解时总的离子方程式为:
D.常温下,内壁沾有硫的试管中加入 溶液,振荡后得到略显黄色的澄清溶液:
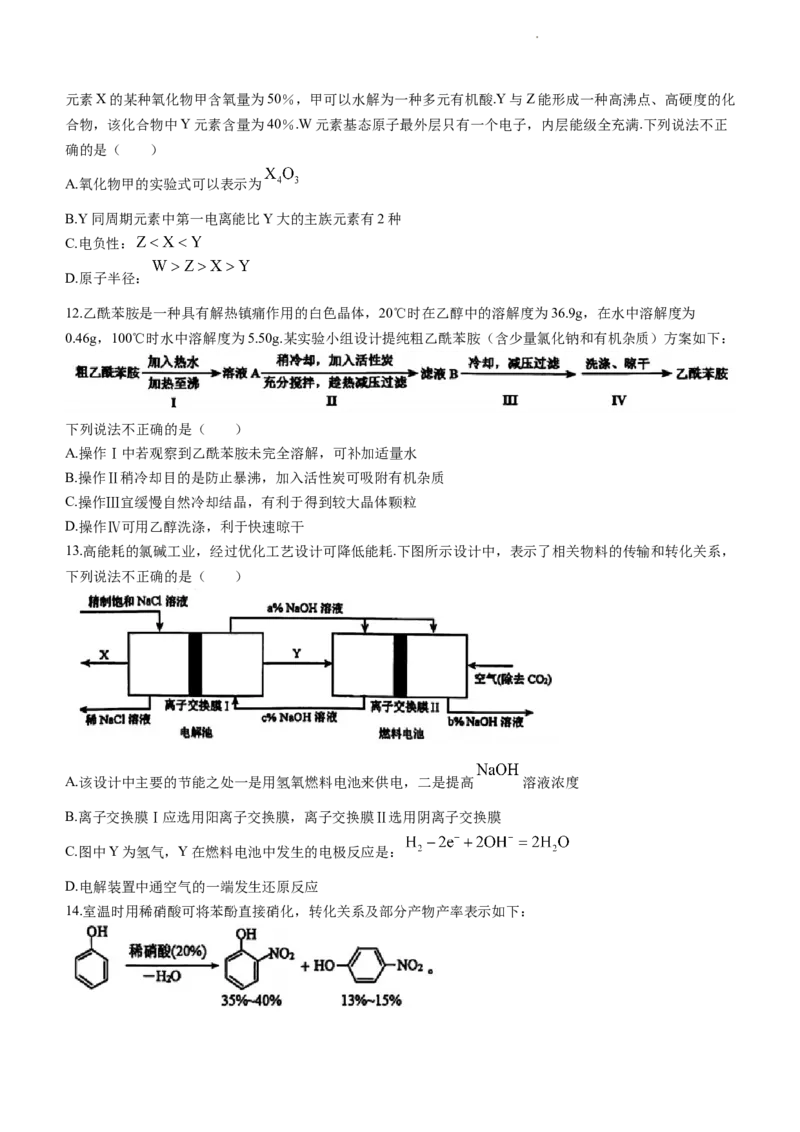
10.苯乙烯可发生如下转化,下列说法中不正确的是( )
A.苯乙烯分子中所有碳原子可共平面
B.X的结构简式可能是 ,该反应需要控制温度减少碳碳双键被氧化
C. 与足量 溶液反应,最多消耗
D.聚合物Z的结构可表示为
11.原子序数依次递增的前四周期的X、Y、Z、W元素,其中X与Y、Z均相邻,X与Y有多种常见氧化物,
学科网(北京)股份有限公司元素X的某种氧化物甲含氧量为50%,甲可以水解为一种多元有机酸.Y与Z能形成一种高沸点、高硬度的化
合物,该化合物中Y元素含量为40%.W元素基态原子最外层只有一个电子,内层能级全充满.下列说法不正
确的是( )
A.氧化物甲的实验式可以表示为
B.Y同周期元素中第一电离能比Y大的主族元素有2种
C.电负性:
D.原子半径:
12.乙酰苯胺是一种具有解热镇痛作用的白色晶体,20℃时在乙醇中的溶解度为36.9g,在水中溶解度为
0.46g,100℃时水中溶解度为5.50g.某实验小组设计提纯粗乙酰苯胺(含少量氯化钠和有机杂质)方案如下:
下列说法不正确的是( )
A.操作Ⅰ中若观察到乙酰苯胺未完全溶解,可补加适量水
B.操作Ⅱ稍冷却目的是防止暴沸,加入活性炭可吸附有机杂质
C.操作Ⅲ宜缓慢自然冷却结晶,有利于得到较大晶体颗粒
D.操作Ⅳ可用乙醇洗涤,利于快速晾干
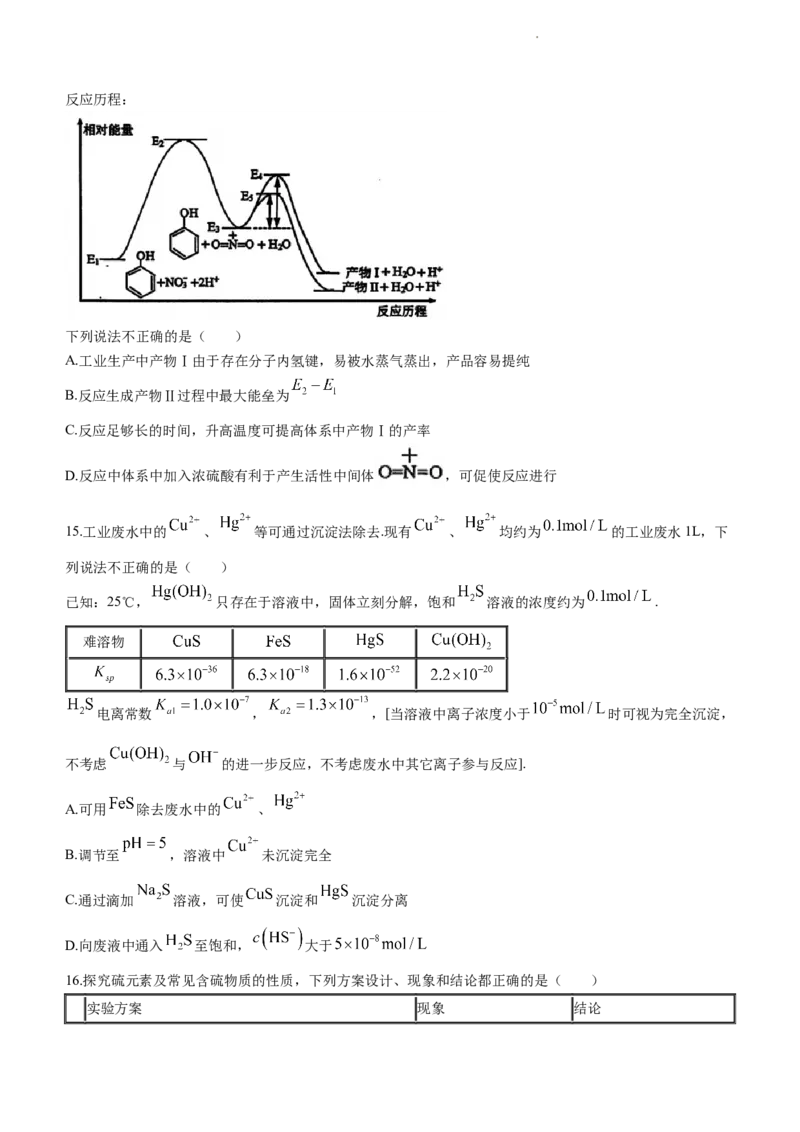
13.高能耗的氯碱工业,经过优化工艺设计可降低能耗.下图所示设计中,表示了相关物料的传输和转化关系,
下列说法不正确的是( )
A.该设计中主要的节能之处一是用氢氧燃料电池来供电,二是提高 溶液浓度
B.离子交换膜Ⅰ应选用阳离子交换膜,离子交换膜Ⅱ选用阴离子交换膜
C.图中Y为氢气,Y在燃料电池中发生的电极反应是:
D.电解装置中通空气的一端发生还原反应
14.室温时用稀硝酸可将苯酚直接硝化,转化关系及部分产物产率表示如下:
学科网(北京)股份有限公司反应历程:
下列说法不正确的是( )
A.工业生产中产物Ⅰ由于存在分子内氢键,易被水蒸气蒸出,产品容易提纯
B.反应生成产物Ⅱ过程中最大能垒为
C.反应足够长的时间,升高温度可提高体系中产物Ⅰ的产率
D.反应中体系中加入浓硫酸有利于产生活性中间体 ,可促使反应进行
15.工业废水中的 、 等可通过沉淀法除去.现有 、 均约为 的工业废水1L,下
列说法不正确的是( )
已知:25℃, 只存在于溶液中,固体立刻分解,饱和 溶液的浓度约为 .
难溶物
电离常数 , ,[当溶液中离子浓度小于 时可视为完全沉淀,
不考虑 与 的进一步反应,不考虑废水中其它离子参与反应].
A.可用 除去废水中的 、
B.调节至 ,溶液中 未沉淀完全
C.通过滴加 溶液,可使 沉淀和 沉淀分离
D.向废液中通入 至饱和, 大于
16.探究硫元素及常见含硫物质的性质,下列方案设计、现象和结论都正确的是( )
实验方案 现象 结论
学科网(北京)股份有限公司溶液加入 生成硫单质,不能证明
出现乳白色浑浊,产生
A
气体 有氧化性
溶液,振荡
开始时铜丝表面变黑,
由氧化还原规律可知黑色
B 将铜丝放入浓硫酸中,加热 产生无色气体,后黑色
固体一定是
固体溶解
C 久置于空气中的 水溶液 出现乳白色浑浊 不稳定,易分解
硫粉与铁粉接触面积大,
粉末呈红热状态,持续
0.5g硫粉和1.0g铁粉混合均匀,在石棉网上堆成条 反应放热,生成黑色
D 反应,冷却后得到黑色
状,用灼热的玻璃棒接触混合粉末的一段
固体
非选择题部分
二、非选择题(本大题共5小题,共52分)
17.(10分)碳、硅元素及其化合物在生产生活中应用广泛.请回答:
(1)基态硅原子核外电子排布式:____________.
(2)与碳的氢化物类似,硅元素的氢化物硅烷的通式为: .
下列有关说法不正确的是__________.
A. 没有同分异构体
B. 键能比 键能小,故热稳定性:
C. 中 原子杂化方式均为
D. 可与水反应生成氢气
(3)硅酸盐是地壳中的主要成分.硅酸盐的最简单阴离子为 ,为硅氧四面体,结构如图1. 在溶液
中形成的分子形态脱水易形成凝胶状的固体物质—硅胶.硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架
— (硅石).
联系相关信息,解释硅胶转变为硅石后,硬度变大的原因:___________.
图1
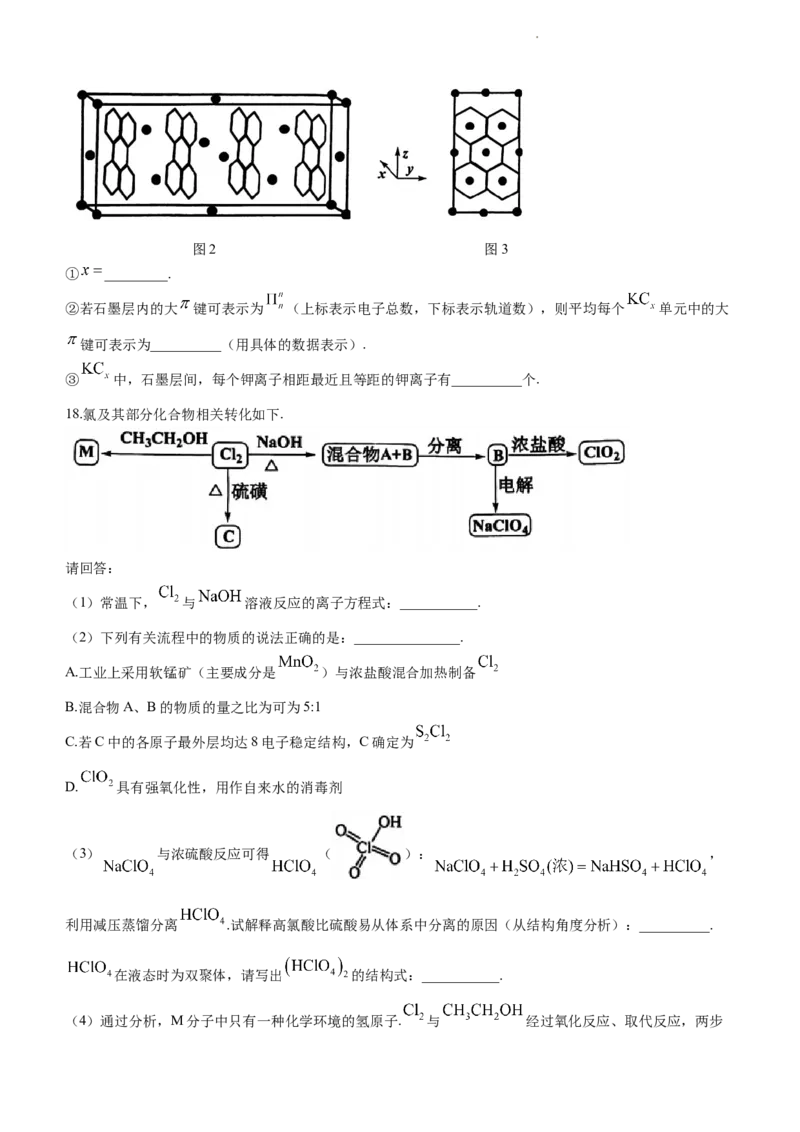
(4)石墨与金属钾反应生成钾的石墨插层化合物 : . 晶胞结构如图2(碳原子省
略),如图3是晶胞沿 轴方向的投影.
学科网(北京)股份有限公司图2 图3
① _________.
②若石墨层内的大 键可表示为 (上标表示电子总数,下标表示轨道数),则平均每个 单元中的大
键可表示为__________(用具体的数据表示).
③ 中,石墨层间,每个钾离子相距最近且等距的钾离子有__________个.
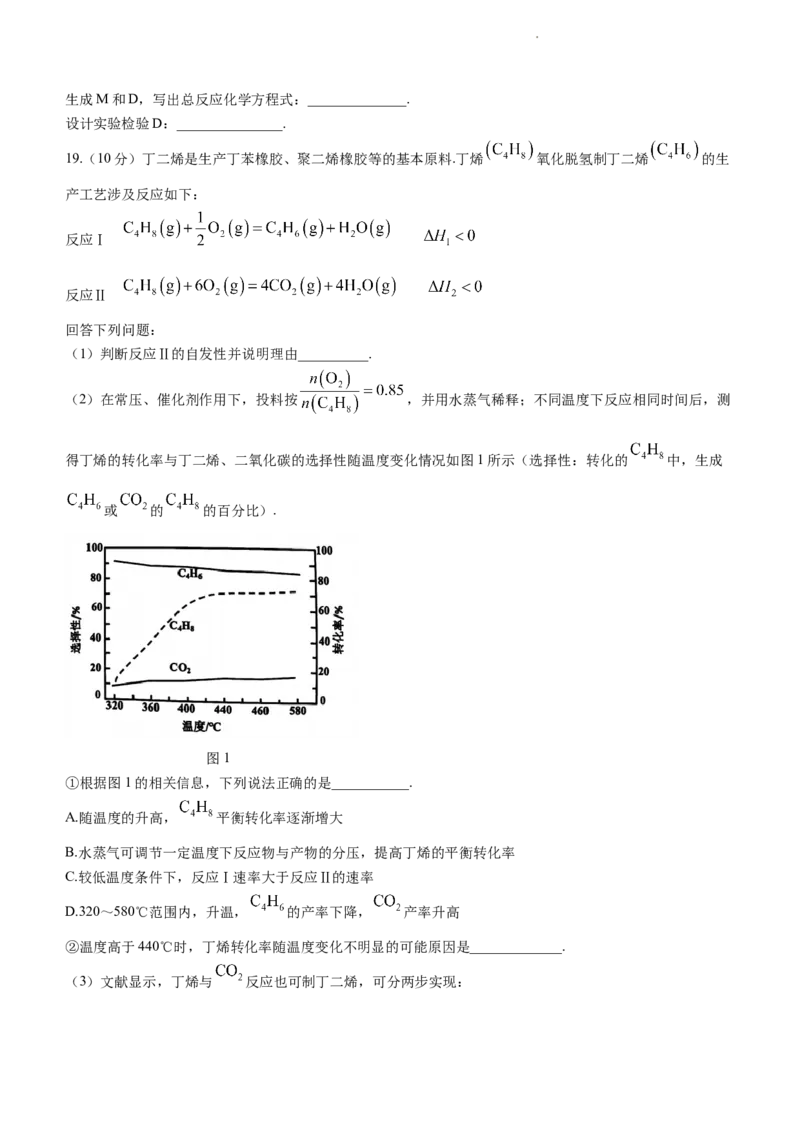
18.氯及其部分化合物相关转化如下.
请回答:
(1)常温下, 与 溶液反应的离子方程式:___________.
(2)下列有关流程中的物质的说法正确的是:_______________.
A.工业上采用软锰矿(主要成分是 )与浓盐酸混合加热制备
B.混合物A、B的物质的量之比为可为5:1
C.若C中的各原子最外层均达8电子稳定结构,C确定为
D. 具有强氧化性,用作自来水的消毒剂
(3) 与浓硫酸反应可得 ( ): ,
利用减压蒸馏分离 .试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):__________.
在液态时为双聚体,请写出 的结构式:___________.
(4)通过分析,M分子中只有一种化学环境的氢原子. 与 经过氧化反应、取代反应,两步
学科网(北京)股份有限公司生成M和D,写出总反应化学方程式:______________.
设计实验检验D:_______________.
19.(10分)丁二烯是生产丁苯橡胶、聚二烯橡胶等的基本原料.丁烯 氧化脱氢制丁二烯 的生
产工艺涉及反应如下:
反应Ⅰ
反应Ⅱ
回答下列问题:
(1)判断反应Ⅱ的自发性并说明理由__________.
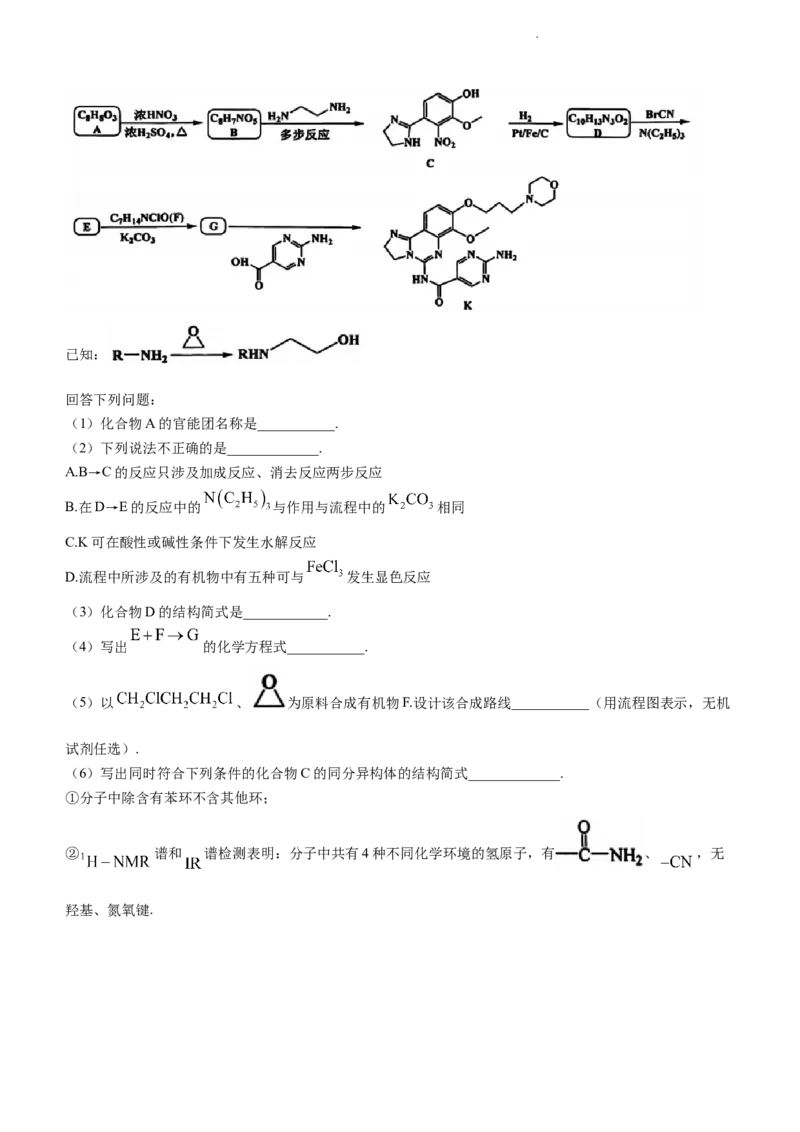
(2)在常压、催化剂作用下,投料按 ,并用水蒸气稀释;不同温度下反应相同时间后,测
得丁烯的转化率与丁二烯、二氧化碳的选择性随温度变化情况如图1所示(选择性:转化的 中,生成
或 的 的百分比).
图1
①根据图1的相关信息,下列说法正确的是___________.
A.随温度的升高, 平衡转化率逐渐增大
B.水蒸气可调节一定温度下反应物与产物的分压,提高丁烯的平衡转化率
C.较低温度条件下,反应Ⅰ速率大于反应Ⅱ的速率
D.320~580℃范围内,升温, 的产率下降, 产率升高
②温度高于440℃时,丁烯转化率随温度变化不明显的可能原因是_____________.
(3)文献显示,丁烯与 反应也可制丁二烯,可分两步实现:
学科网(北京)股份有限公司反应Ⅲ
反应Ⅳ
600℃时,恒定总压0.10MPa、以起始物质的量均为1mol的 、 投料,达平衡时,测得 和
的转化率分别为80%、10%.600℃时,反应Ⅳ的平衡常数 _________.
(4)有人设计一种电解装置,用乙炔合成二丁烯 的装置如图2.电解质溶液为 溶
液.
图2
①请写出生成 的电极的电极反应式:____________.
②用 溶液吸收阳极逸出的气体再生电解质溶液.
不考虑气体溶解残留.当电路中转移 时,计算再生液的 ____________.
(已知 的电离常数 , )
20.(10分)某学习小组利用相对密度法测定 分子量,实验装置如图:
简要步骤如下:
学科网(北京)股份有限公司步骤Ⅰ:利用上图装置获取纯净 ;
步骤Ⅱ:取一只洁净而干燥的锥形瓶(E),用合适的橡胶塞塞紧后在塞子上作上标记,用电子天平称量,
质量: .用E收集 .
集满后,在电子天平上称量,质量( +瓶+塞子): .
步骤Ⅲ: 分子量的测定
依据阿伏加德罗定律的推论: ,
可得:
请回答下列问题:
(1)写出装置A反应的离子方程式:____________.
(2) 的纯净程度是保证实验结果准确的关键.B、C、D装置是 的净化装置,请按顺序选择最适当
的试剂:___________.
a.水 b.浓硫酸 c.无水氯化钙及玻璃纤维
d.饱和碳酸氢钠溶液 e.碱石灰及玻璃纤维
(3)E没有设置防对流,能否收集到纯净 ,说明理由:__________.
(4)下列说法正确的是____________.
A.当装置B、C中有气泡时,即可以开始收集
B. 即是锥形瓶的质量
C.对E进行称量时,应缓缓取出导管,再塞上橡胶塞至标记处,称量
D.通过对E反复称量,对比质量的变化,即可判断 是否集满
(5)通过向锥形瓶装水至橡胶塞塞至的标记处,用托盘天平称量,质量(水+瓶+塞子): ,此时,水
的质量远大于空气.可测定锥形瓶的体积: _________mL.若体积折算成标准状况,则
________(用 、 、 的计算式表示,无需化简).
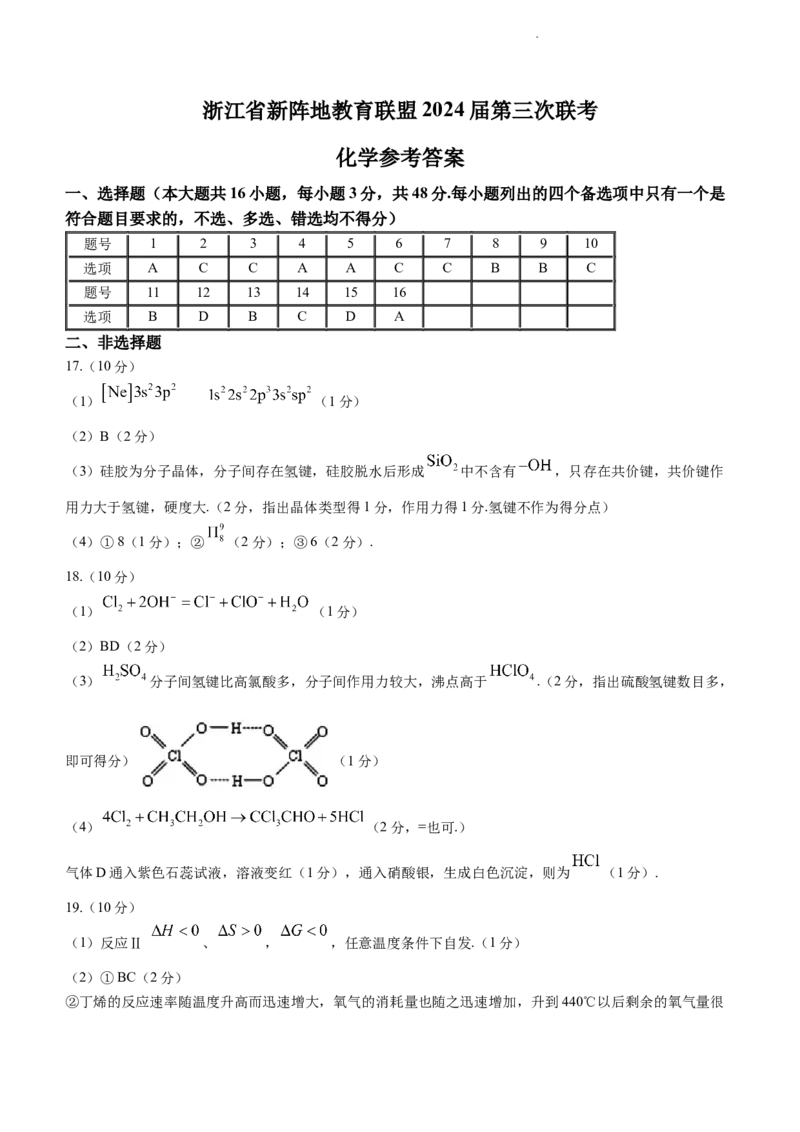
21.(12分)某研究小组按下列路线合成药物库潘尼西(K).
学科网(北京)股份有限公司已知:
回答下列问题:
(1)化合物A的官能团名称是___________.
(2)下列说法不正确的是_____________.
A.B→C的反应只涉及加成反应、消去反应两步反应
B.在D→E的反应中的 与作用与流程中的 相同
C.K可在酸性或碱性条件下发生水解反应
D.流程中所涉及的有机物中有五种可与 发生显色反应
(3)化合物D的结构简式是____________.
(4)写出 的化学方程式___________.
(5)以 、 为原料合成有机物F.设计该合成路线___________(用流程图表示,无机
试剂任选).
(6)写出同时符合下列条件的化合物C的同分异构体的结构简式_____________.
①分子中除含有苯环不含其他环;
② 谱和 谱检测表明:分子中共有4种不同化学环境的氢原子,有 、 ,无
羟基、氮氧键.
学科网(北京)股份有限公司浙江省新阵地教育联盟 2024 届第三次联考
化学参考答案
一、选择题(本大题共16小题,每小题3分,共48分.每小题列出的四个备选项中只有一个是
符合题目要求的,不选、多选、错选均不得分)
题号 1 2 3 4 5 6 7 8 9 10
选项 A C C A A C C B B C
题号 11 12 13 14 15 16
选项 B D B C D A
二、非选择题
17.(10分)
(1) (1分)
(2)B(2分)
(3)硅胶为分子晶体,分子间存在氢键,硅胶脱水后形成 中不含有 ,只存在共价键,共价键作
用力大于氢键,硬度大.(2分,指出晶体类型得1分,作用力得1分.氢键不作为得分点)
(4)①8(1分);② (2分);③6(2分).
18.(10分)
(1) (1分)
(2)BD(2分)
(3) 分子间氢键比高氯酸多,分子间作用力较大,沸点高于 .(2分,指出硫酸氢键数目多,
即可得分) (1分)
(4) (2分,=也可.)
气体D通入紫色石蕊试液,溶液变红(1分),通入硝酸银,生成白色沉淀,则为 (1分).
19.(10分)
(1)反应Ⅱ 、 , ,任意温度条件下自发.(1分)
(2)①BC(2分)
②丁烯的反应速率随温度升高而迅速增大,氧气的消耗量也随之迅速增加,升到440℃以后剩余的氧气量很
学科网(北京)股份有限公司少,丁烯和氧气的反应受氧气含量的限制,因此1-丁烯的转化率基本不变;反应Ⅰ速率快, 升温,
平衡逆移,生成1-丁烯与反应消耗1-丁烯基本持平,因此1-丁烯的转化率基本不变.(2分,答对1点即可)
(3) 或0.0159(2分)
(4)① (2分)② (2分)
20.(10分)
(1) (1分)
(2)dbc(2分,全对给分)
(3)可以,因为 的密度比空气大很多,不会与空气形成对流,向上排空即可收集到纯净的 (2
分)
(4)CD(2分)
(5) (1分) (2分,其他合理答案也可)
21.(12分)
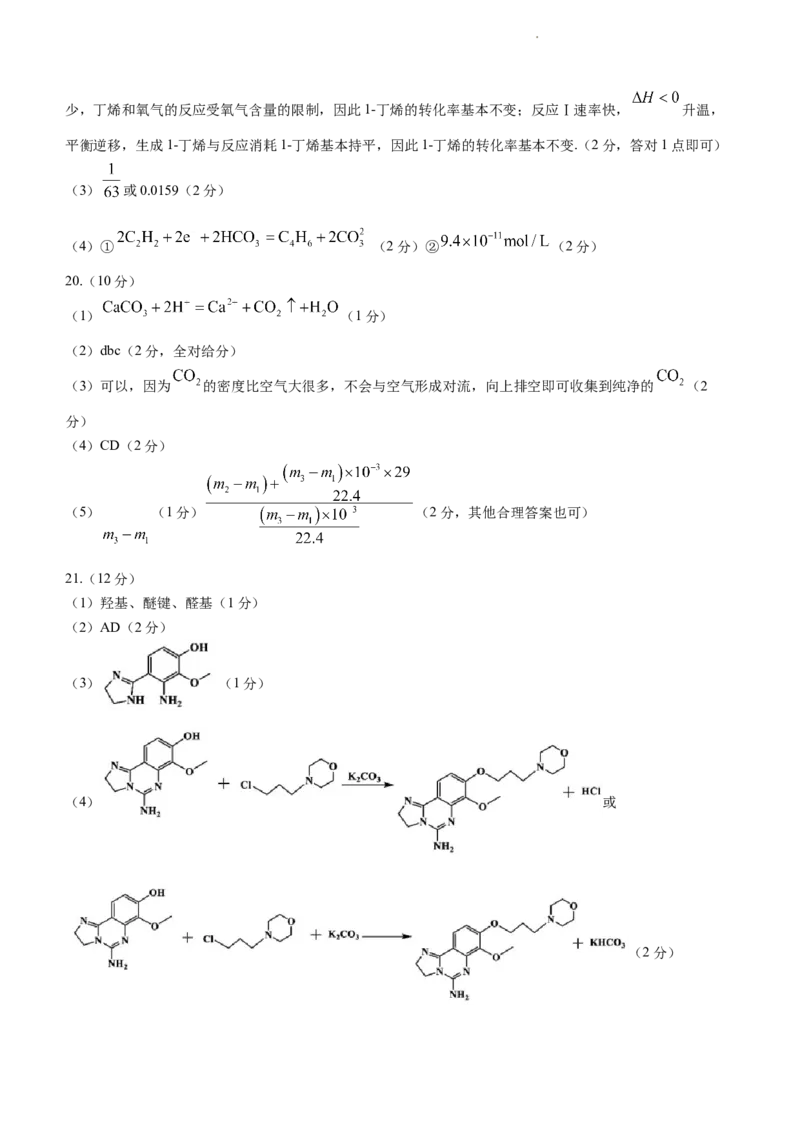
(1)羟基、醚键、醛基(1分)
(2)AD(2分)
(3) (1分)
(4) 或
(2分)
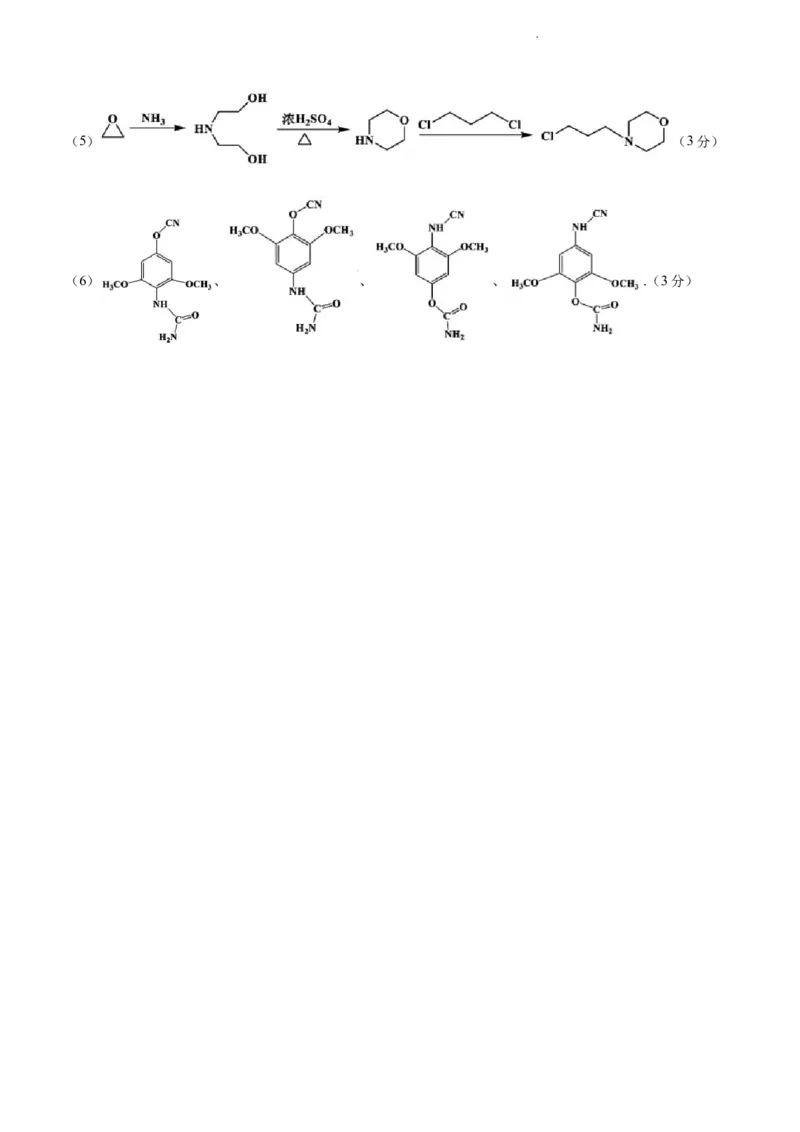
学科网(北京)股份有限公司(5) (3分)
(6) 、 、 、 .(3分)
学科网(北京)股份有限公司