文档内容
泉州市 2024 届高中毕业班适应性练习卷
高三化学
2024.5
满分100分,考试时间75分钟。
注意事项:
1.考试前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确黏贴在条形码区域内。
2.选择题必须使用 2B铅笔填涂;非选择题必须使用 0.5毫米黑色字迹的签字笔书写,字体
工整,笔迹清楚。
3.请按照题号顺序在各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、
试题卷上答题无效。
4.保持卡面清洁,不要折叠,不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
一、选择题(本题共10小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题
目要求的)
1.今年泉州蟳埔的“簪花围”和“蚵壳厝”火出圈,传统的簪花是把鲜花用金银簪固定。下列说法不正
确的是( )
A.金银簪属于金属材料 B.蚵壳的主要成分属于硅酸盐
C.某些鲜花释放的香气中含有酯类物质 D.海蛎中蛋白质属于有机高分子
2.用PVA包裹的 是纳米级抗癌药物载体,具有良好的水溶性和靶向性,PVA的结构为
,下列说法不正确的是( )
A.PVA在人体内不能发生水解反应 B.PVA与 互为同系物
C.该载体分散于水中可形成胶体 D.该载体在磁场作用下具有靶向性
3.某有机合成中间体X的结构简式如下图。下列关于X的说法正确的是( )
A.分子式为 B.分子中含有2个手性碳原子
学科网(北京)股份有限公司C.①和② 键的键长相等 D.与足量 溶液反应能生成甘油
4.下列实验对应的离子方程式正确的是( )
A.用 溶液刻蚀印刷电路板:
B.将重晶石转化为酸溶性钡盐:
C.用 溶液吸收含溴尾气:
D.验证 的漂白性:
5.以 为原料制备 ,理论上可用下列两个反应进行。
反应ⅰ:
反应ⅱ:
为阿伏伽德罗常数的值,下列说法不正确的是( )
A.反应ⅰ需在高温下才能自发进行
B.反应ⅰ中,每分解142g 产生44.8L (标准状况)
C.由反应ⅰ、ⅱ分别制备 ,转移电子数均为
D. 溶液中存在:
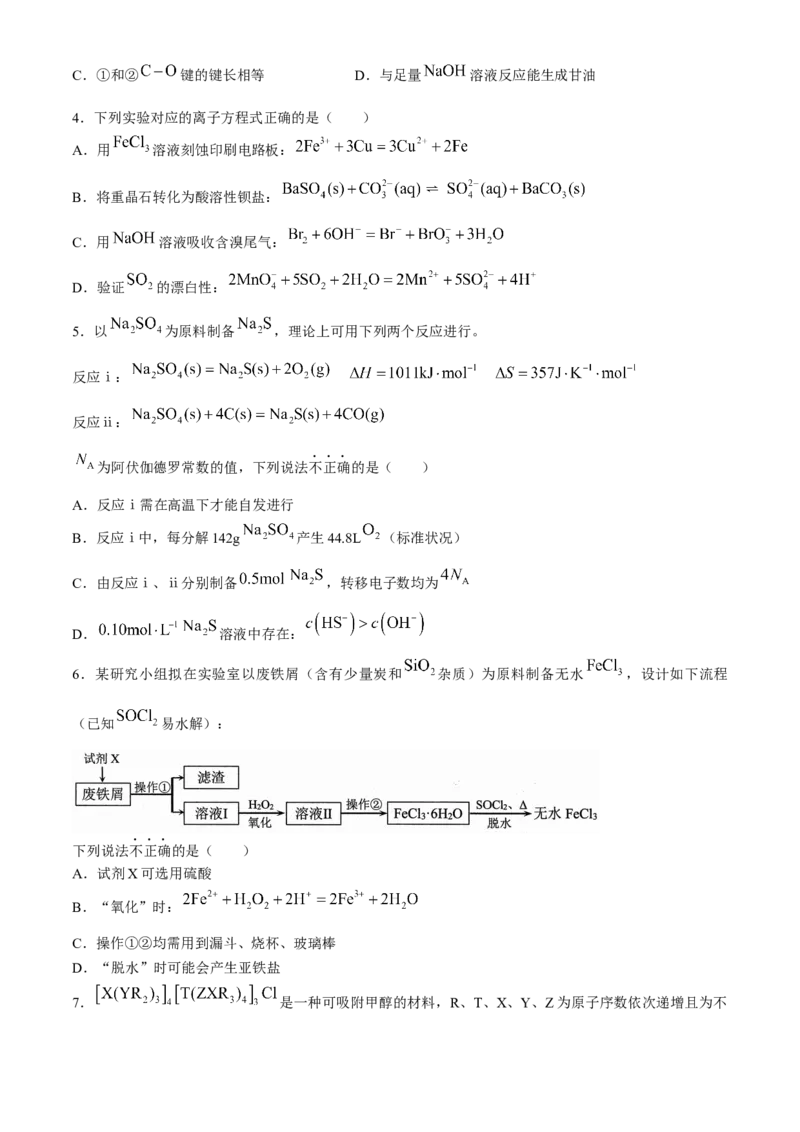
6.某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水 ,设计如下流程
(已知 易水解):
下列说法不正确的是( )
A.试剂X可选用硫酸
B.“氧化”时:
C.操作①②均需用到漏斗、烧杯、玻璃棒
D.“脱水”时可能会产生亚铁盐
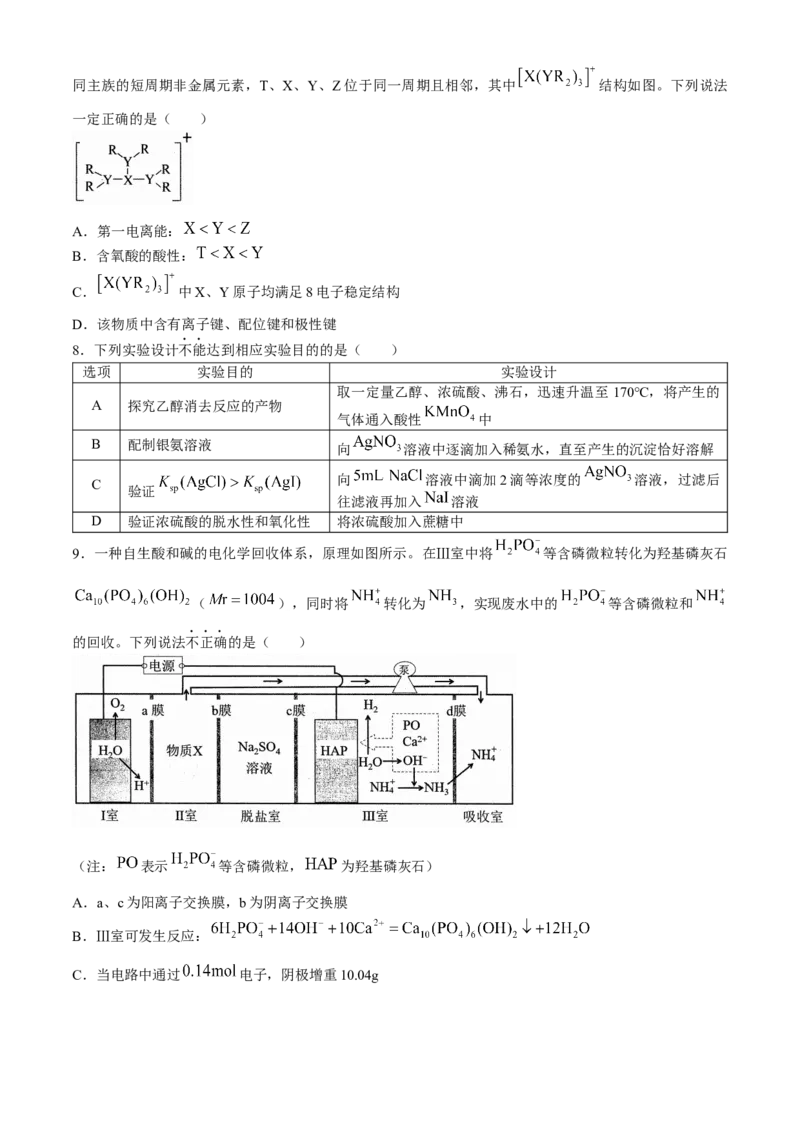
7. 是一种可吸附甲醇的材料,R、T、X、Y、Z为原子序数依次递增且为不
学科网(北京)股份有限公司同主族的短周期非金属元素,T、X、Y、Z位于同一周期且相邻,其中 结构如图。下列说法
一定正确的是( )
A.第一电离能:
B.含氧酸的酸性:
C. 中X、Y原子均满足8电子稳定结构
D.该物质中含有离子键、配位键和极性键
8.下列实验设计不能达到相应实验目的的是( )
选项 实验目的 实验设计
取一定量乙醇、浓硫酸、沸石,迅速升温至 170℃,将产生的
A 探究乙醇消去反应的产物
气体通入酸性 中
B 配制银氨溶液
向 溶液中逐滴加入稀氨水,直至产生的沉淀恰好溶解
向 溶液中滴加2滴等浓度的 溶液,过滤后
C
验证
往滤液再加入 溶液
D 验证浓硫酸的脱水性和氧化性 将浓硫酸加入蔗糖中
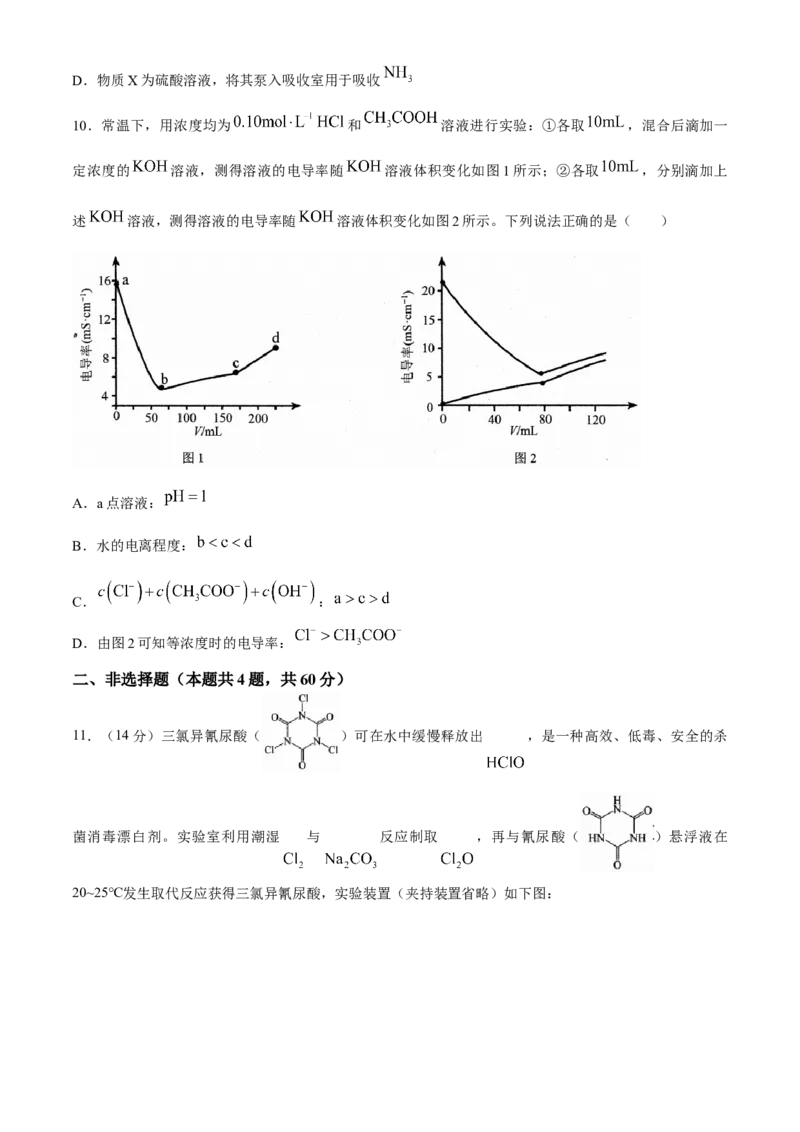
9.一种自生酸和碱的电化学回收体系,原理如图所示。在Ⅲ室中将 等含磷微粒转化为羟基磷灰石
( ),同时将 转化为 ,实现废水中的 等含磷微粒和
的回收。下列说法不正确的是( )
(注: 表示 等含磷微粒, 为羟基磷灰石)
A.a、c为阳离子交换膜,b为阴离子交换膜
B.Ⅲ室可发生反应:
C.当电路中通过 电子,阴极增重10.04g
学科网(北京)股份有限公司D.物质X为硫酸溶液,将其泵入吸收室用于吸收
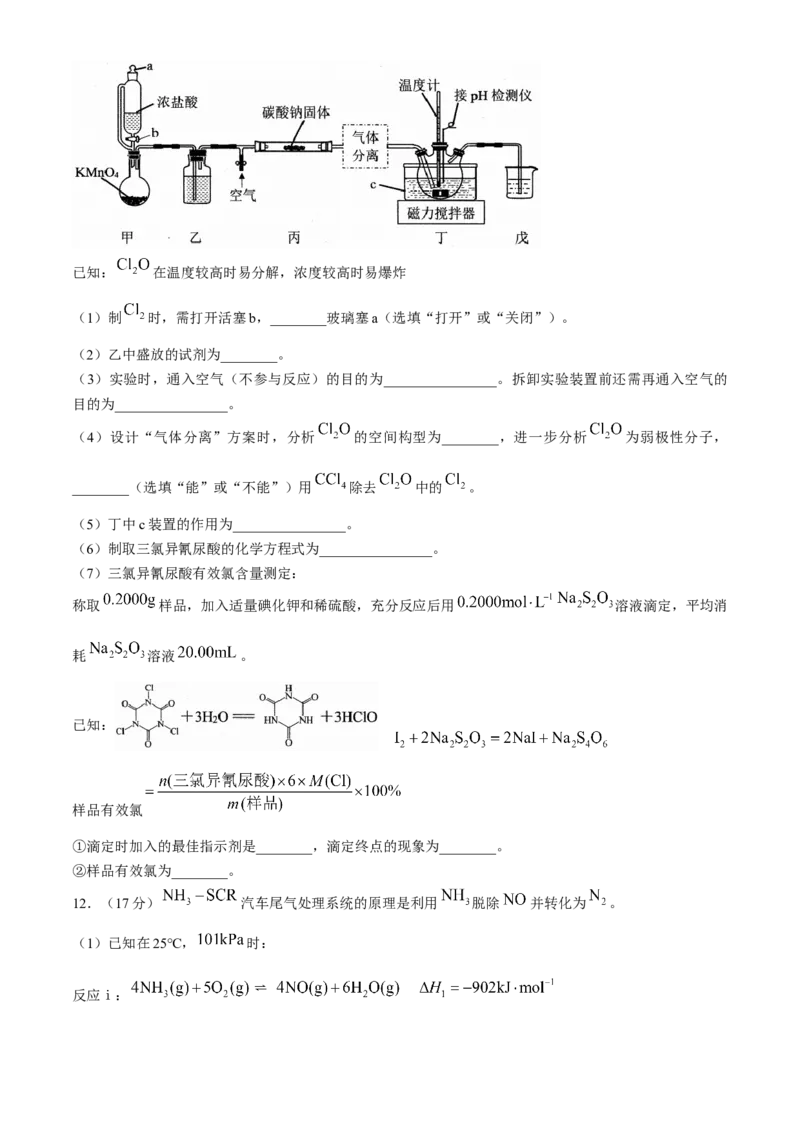
10.常温下,用浓度均为 和 溶液进行实验:①各取 ,混合后滴加一
定浓度的 溶液,测得溶液的电导率随 溶液体积变化如图1所示;②各取 ,分别滴加上
述 溶液,测得溶液的电导率随 溶液体积变化如图2所示。下列说法正确的是( )
A.a点溶液:
B.水的电离程度:
C. :
D.由图2可知等浓度时的电导率:
二、非选择题(本题共4题,共60分)
11.(14分)三氯异氰尿酸( )可在水中缓慢释放出 ,是一种高效、低毒、安全的杀
菌消毒漂白剂。实验室利用潮湿 与 反应制取 ,再与氰尿酸( )悬浮液在
20~25℃发生取代反应获得三氯异氰尿酸,实验装置(夹持装置省略)如下图:
学科网(北京)股份有限公司已知: 在温度较高时易分解,浓度较高时易爆炸
(1)制 时,需打开活塞b,________玻璃塞a(选填“打开”或“关闭”)。
(2)乙中盛放的试剂为________。
(3)实验时,通入空气(不参与反应)的目的为________________。拆卸实验装置前还需再通入空气的
目的为________________。
(4)设计“气体分离”方案时,分析 的空间构型为________,进一步分析 为弱极性分子,
________(选填“能”或“不能”)用 除去 中的 。
(5)丁中c装置的作用为________________。
(6)制取三氯异氰尿酸的化学方程式为________________。
(7)三氯异氰尿酸有效氯含量测定:
称取 样品,加入适量碘化钾和稀硫酸,充分反应后用 溶液滴定,平均消
耗 溶液 。
已知:
样品有效氯
①滴定时加入的最佳指示剂是________,滴定终点的现象为________。
②样品有效氯为________。
12.(17分) 汽车尾气处理系统的原理是利用 脱除 并转化为 。
(1)已知在25℃, 时:
反应ⅰ:
学科网(北京)股份有限公司反应ⅱ:
反应ⅲ: ________
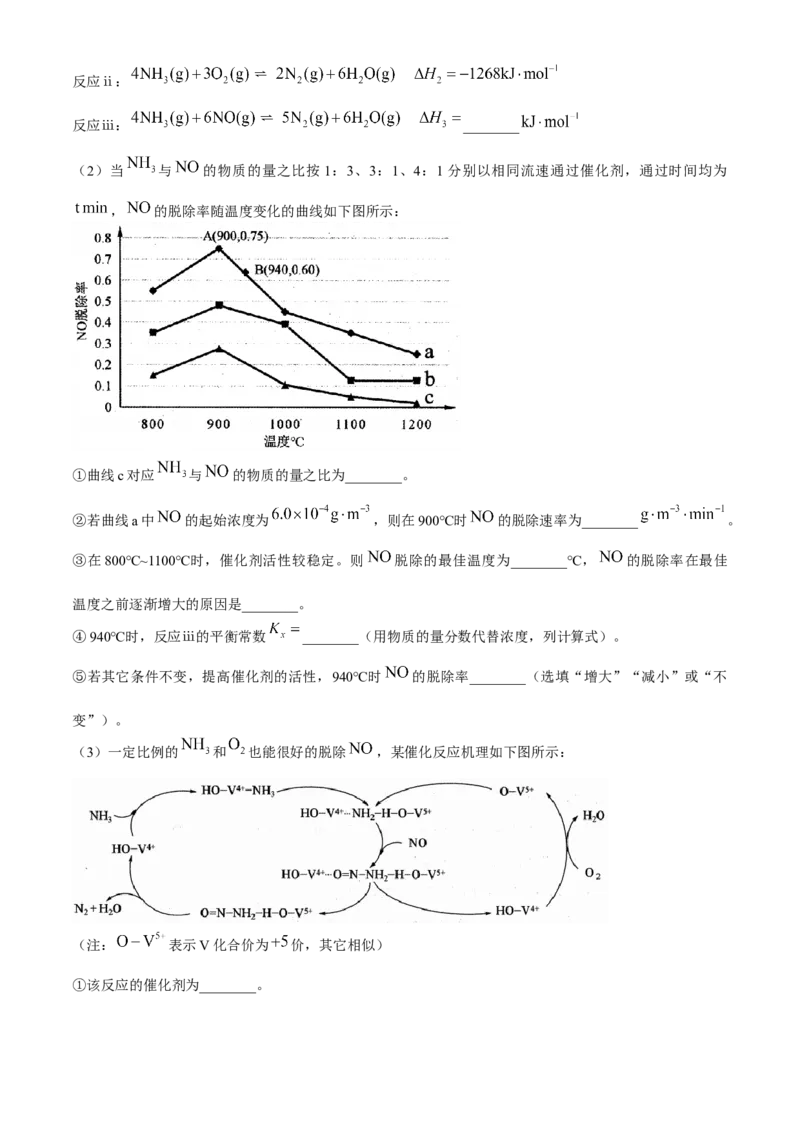
(2)当 与 的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为
, 的脱除率随温度变化的曲线如下图所示:
①曲线c对应 与 的物质的量之比为________。
②若曲线a中 的起始浓度为 ,则在900℃时 的脱除速率为________ 。
③在800℃~1100℃时,催化剂活性较稳定。则 脱除的最佳温度为________℃, 的脱除率在最佳
温度之前逐渐增大的原因是________。
④940℃时,反应ⅲ的平衡常数 ________(用物质的量分数代替浓度,列计算式)。
⑤若其它条件不变,提高催化剂的活性,940℃时 的脱除率________(选填“增大”“减小”或“不
变”)。
(3)一定比例的 和 也能很好的脱除 ,某催化反应机理如下图所示:
(注: 表示V化合价为 价,其它相似)
①该反应的催化剂为________。
学科网(北京)股份有限公司② 转化为 过程中 与 的物质的量比为________。
③ 转化为 , 键角增大的原因是________。
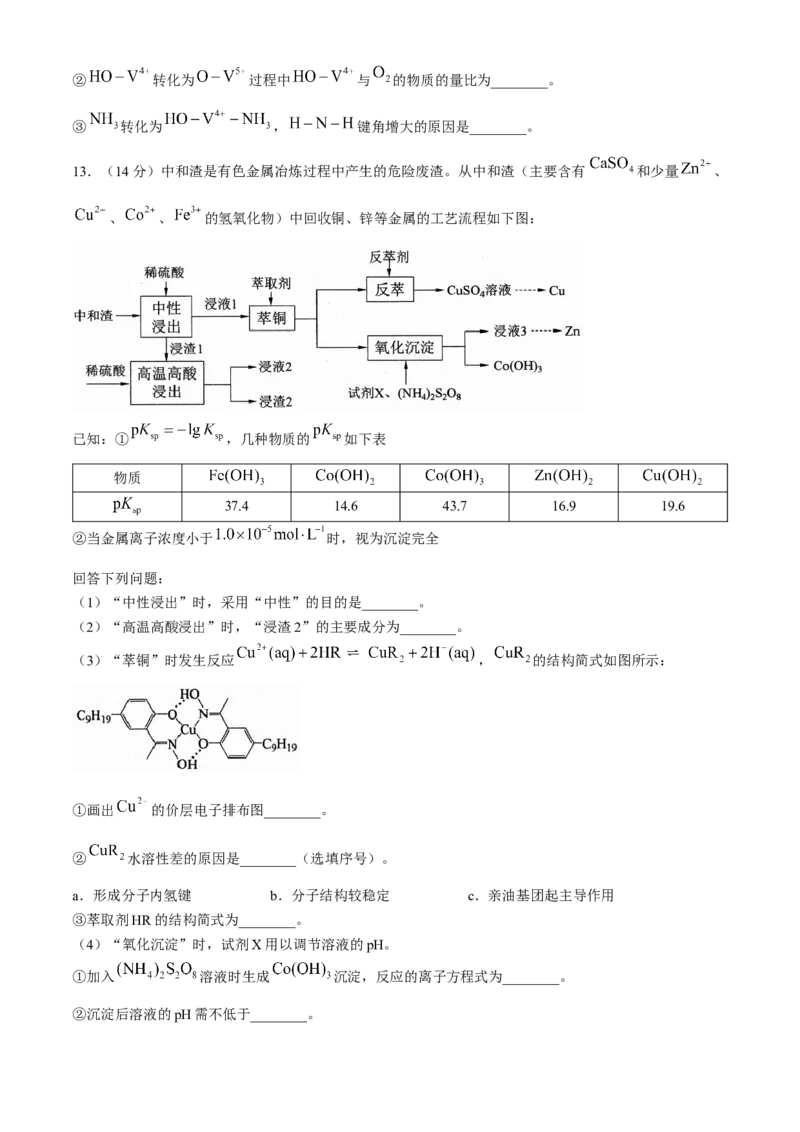
13.(14分)中和渣是有色金属冶炼过程中产生的危险废渣。从中和渣(主要含有 和少量 、
、 、 的氢氧化物)中回收铜、锌等金属的工艺流程如下图:
已知:① ,几种物质的 如下表
物质
37.4 14.6 43.7 16.9 19.6
②当金属离子浓度小于 时,视为沉淀完全
回答下列问题:
(1)“中性浸出”时,采用“中性”的目的是________。
(2)“高温高酸浸出”时,“浸渣2”的主要成分为________。
(3)“萃铜”时发生反应 , 的结构简式如图所示:
①画出 的价层电子排布图________。
② 水溶性差的原因是________(选填序号)。
a.形成分子内氢键 b.分子结构较稳定 c.亲油基团起主导作用
③萃取剂HR的结构简式为________。
(4)“氧化沉淀”时,试剂X用以调节溶液的pH。
①加入 溶液时生成 沉淀,反应的离子方程式为________。
②沉淀后溶液的pH需不低于________。
学科网(北京)股份有限公司(5)该流程中,可以循环使用的物质有________。
(6)某黄铜合金晶胞结构如图,其中A、B的原子坐标均可为 。与Zn原子距离最近且相等的Cu
原子有________个,C的原子坐标为________。
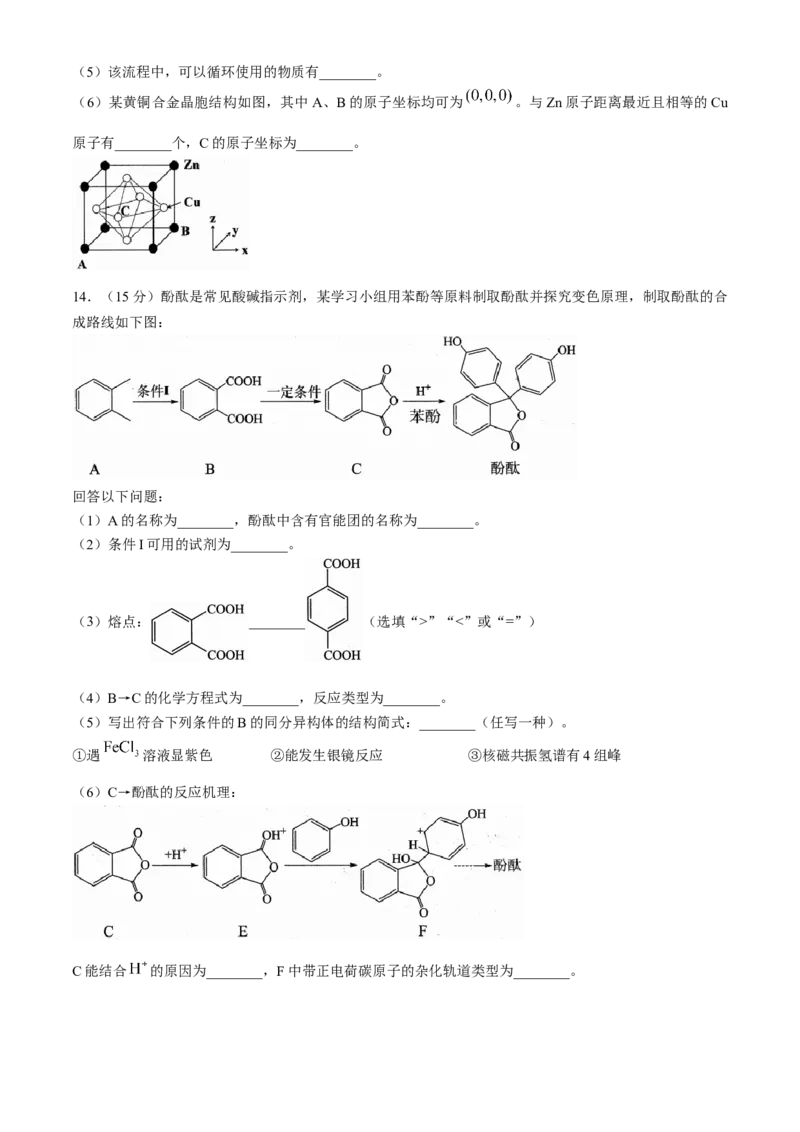
14.(15分)酚酞是常见酸碱指示剂,某学习小组用苯酚等原料制取酚酞并探究变色原理,制取酚酞的合
成路线如下图:
回答以下问题:
(1)A的名称为________,酚酞中含有官能团的名称为________。
(2)条件I可用的试剂为________。
(3)熔点: ________ (选填“>”“<”或“=”)
(4)B→C的化学方程式为________,反应类型为________。
(5)写出符合下列条件的B的同分异构体的结构简式:________(任写一种)。
①遇 溶液显紫色 ②能发生银镜反应 ③核磁共振氢谱有4组峰
(6)C→酚酞的反应机理:
C能结合 的原因为________,F中带正电荷碳原子的杂化轨道类型为________。
学科网(北京)股份有限公司(7)酚酞在一定pH溶液中生成阴离子 ,该离子的结构简式为________。
学科网(北京)股份有限公司