文档内容
2024 年秋“宜昌一中、荆州中学”高二十月联考
化学试题
命题人: 审题人:
一、选择题:本题共15小题,45分。每小题有且仅有一个选项符合题目要求。
1.日常生活中的下列做法,与调控化学反应速率无关的是( )
A.向炉膛内鼓风,可以使炉火更旺 B.在月饼包装内放置脱氧剂
C.医疗上使用75%的酒精杀菌消毒 D.在汽车尾气系统中安装催化转换器
2.下列离子方程式正确的是( )
A. 溶液中加入稀硫酸:
B.用酸性 标准溶液滴定草酸:
C.用 溶解 :
D.将过量 通入漂白粉溶液中:
3.常温下,下列事实不能说明某一元酸HX是弱酸的是( )
A. 溶液
B.NaX与 反应生成HX
C. 溶液比 溶液导电能力弱
D. 溶液与 溶液恰好中和
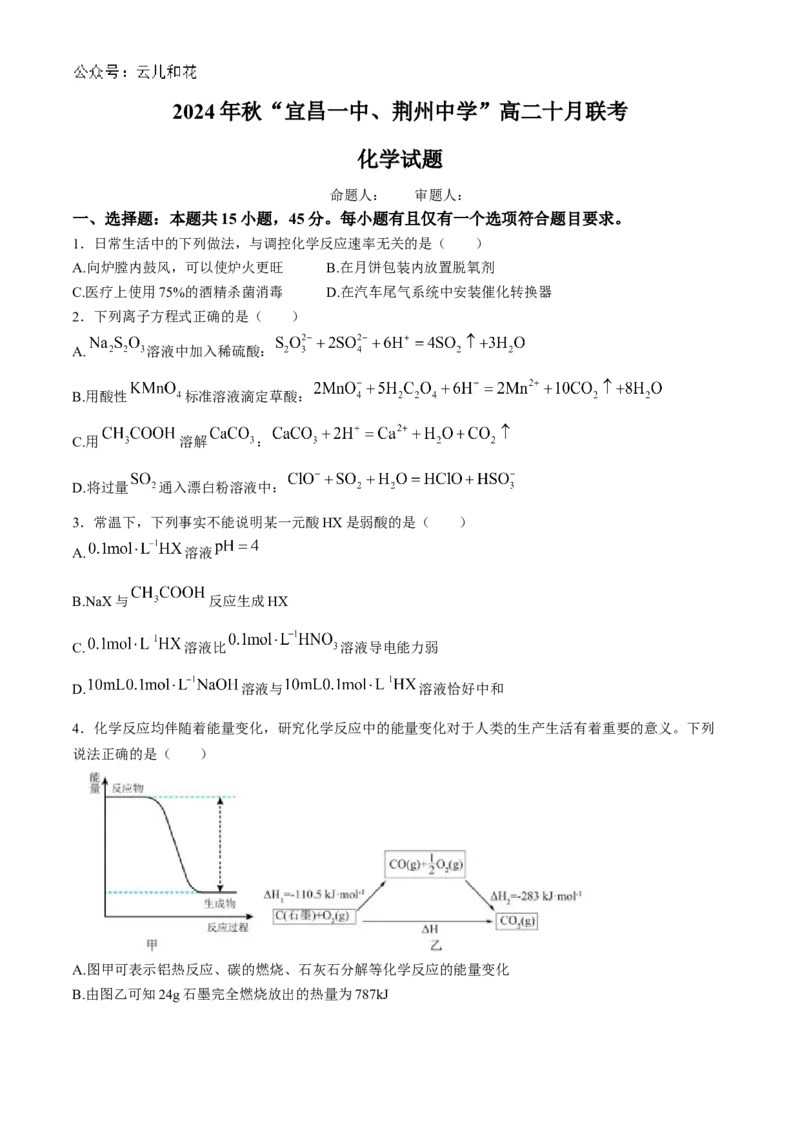
4.化学反应均伴随着能量变化,研究化学反应中的能量变化对于人类的生产生活有着重要的意义。下列
说法正确的是( )
A.图甲可表示铝热反应、碳的燃烧、石灰石分解等化学反应的能量变化
B.由图乙可知24g石墨完全燃烧放出的热量为787kJC.由图乙可知CO的燃烧热
D.由图乙可判断CO能量比 能量高
5.与纯水的电离相似,液氨中也存在着微弱的电离: ,一定温度下,液氨的电离
达到平衡时,下列有关说法错误的是( )
A.同时含有 、 、 三种微粒 B. 是常数
C.存在关系: D.升高温度,液氨的电离程度会变化
6.在恒温密闭容器中发生反应 ,反应达到平衡后,将容器容积压缩到原来的一半,
当再次达到平衡时,C的浓度为原平衡的1.9倍,下列叙述中错误的是( )
A.化学平衡常数K不变 B.a>b+c
C.压缩瞬间, 、 都增大 D.A的转化率减小
7. 时在1L恒容密闭容器充入 和 ,发生反应
,达平衡后,升温至 。已知实验测得: 、 , 、
为速率常数,且只与温度有关。下列说法正确的是( )
A.当 时,该反应达到平衡状态
B.平衡常数可表示为 ,且
C.向 下的平衡体系中再充入一定量 ,再次达平衡时 的体积分数一定变大
D.向 下的平衡体系中再充入一定量 的转化率减小
8.下列说法正确的是( )
A.已知稀溶液中, ,则稀氨水与稀盐酸反应生成1mol
水时放出的热量小于57.3kJ
B.已知葡萄糖燃烧热 ,则C.已知 ,则该反应的正反应活化能比逆反应活化能高
D.一定条件下,将 和 置于密闭容器中充分反应生成 时放出热量79.2kJ,
则该反应的热化学方程式为
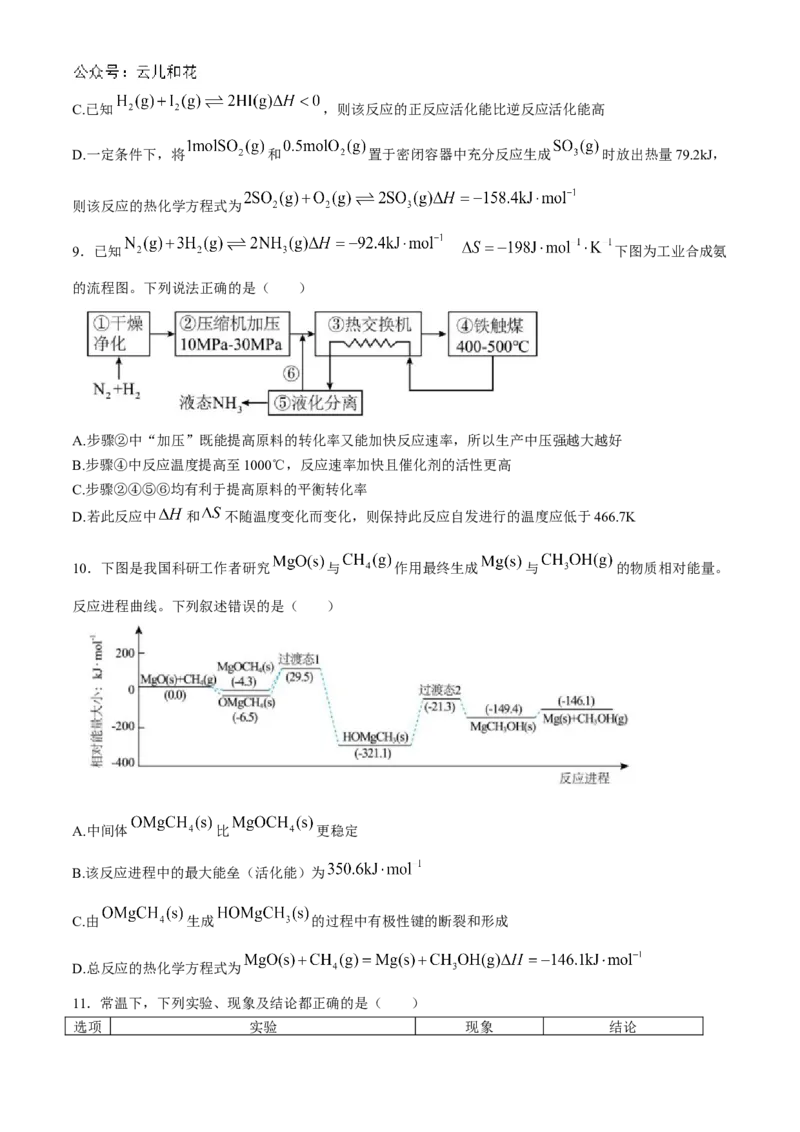
9.已知 下图为工业合成氨
的流程图。下列说法正确的是( )
A.步骤②中“加压”既能提高原料的转化率又能加快反应速率,所以生产中压强越大越好
B.步骤④中反应温度提高至1000℃,反应速率加快且催化剂的活性更高
C.步骤②④⑤⑥均有利于提高原料的平衡转化率
D.若此反应中 和 不随温度变化而变化,则保持此反应自发进行的温度应低于466.7K
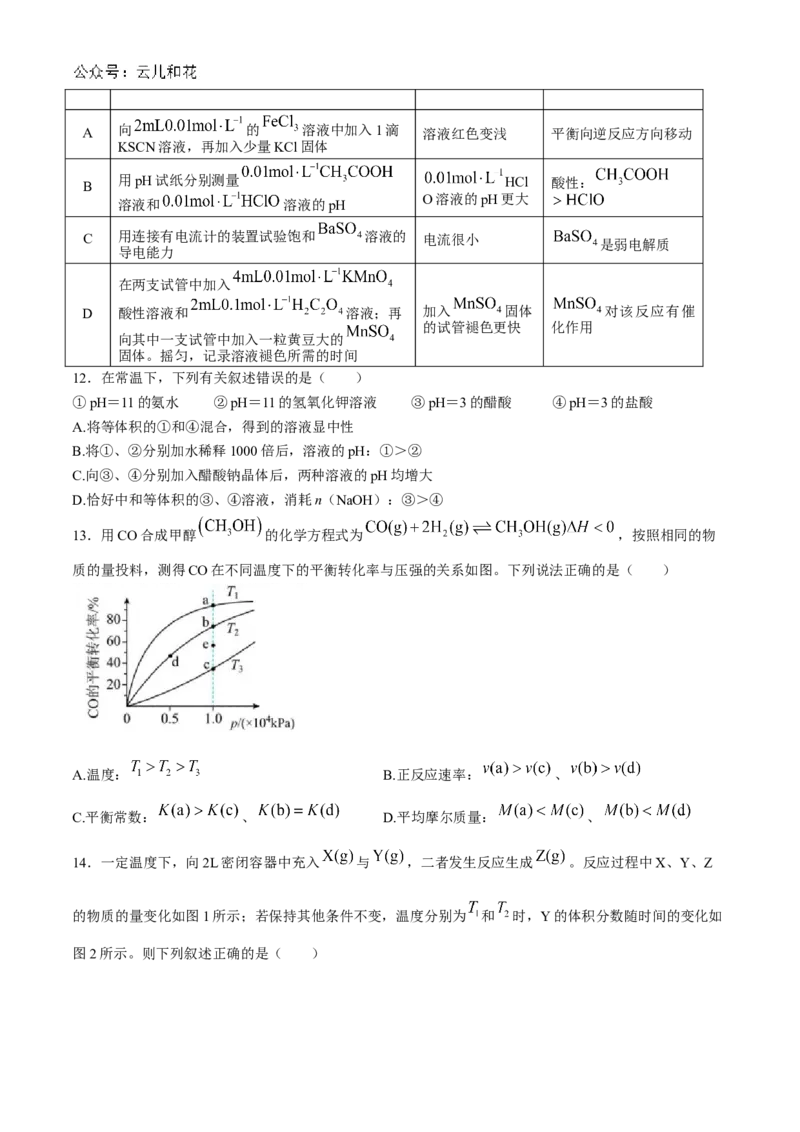
10.下图是我国科研工作者研究 与 作用最终生成 与 的物质相对能量。
反应进程曲线。下列叙述错误的是( )
A.中间体 比 更稳定
B.该反应进程中的最大能垒(活化能)为
C.由 生成 的过程中有极性键的断裂和形成
D.总反应的热化学方程式为
11.常温下,下列实验、现象及结论都正确的是( )
选项 实验 现象 结论A 向 的 溶液中加入1滴 溶液红色变浅 平衡向逆反应方向移动
KSCN溶液,再加入少量KCl固体
B 用pH试纸分别测量 HCl 酸性:
O溶液的pH更大
溶液和 溶液的pH
C 用连接有电流计的装置试验饱和 溶液的 电流很小
是弱电解质
导电能力
在两支试管中加入
D 酸性溶液和 溶液;再 加入 固体 对该反应有催
的试管褪色更快 化作用
向其中一支试管中加入一粒黄豆大的
固体。摇匀,记录溶液褪色所需的时间
12.在常温下,下列有关叙述错误的是( )
①pH=11的氨水 ②pH=11的氢氧化钾溶液 ③pH=3的醋酸 ④pH=3的盐酸
A.将等体积的①和④混合,得到的溶液显中性
B.将①、②分别加水稀释1000倍后,溶液的pH:①>②
C.向③、④分别加入醋酸钠晶体后,两种溶液的pH均增大
D.恰好中和等体积的③、④溶液,消耗n(NaOH):③>④
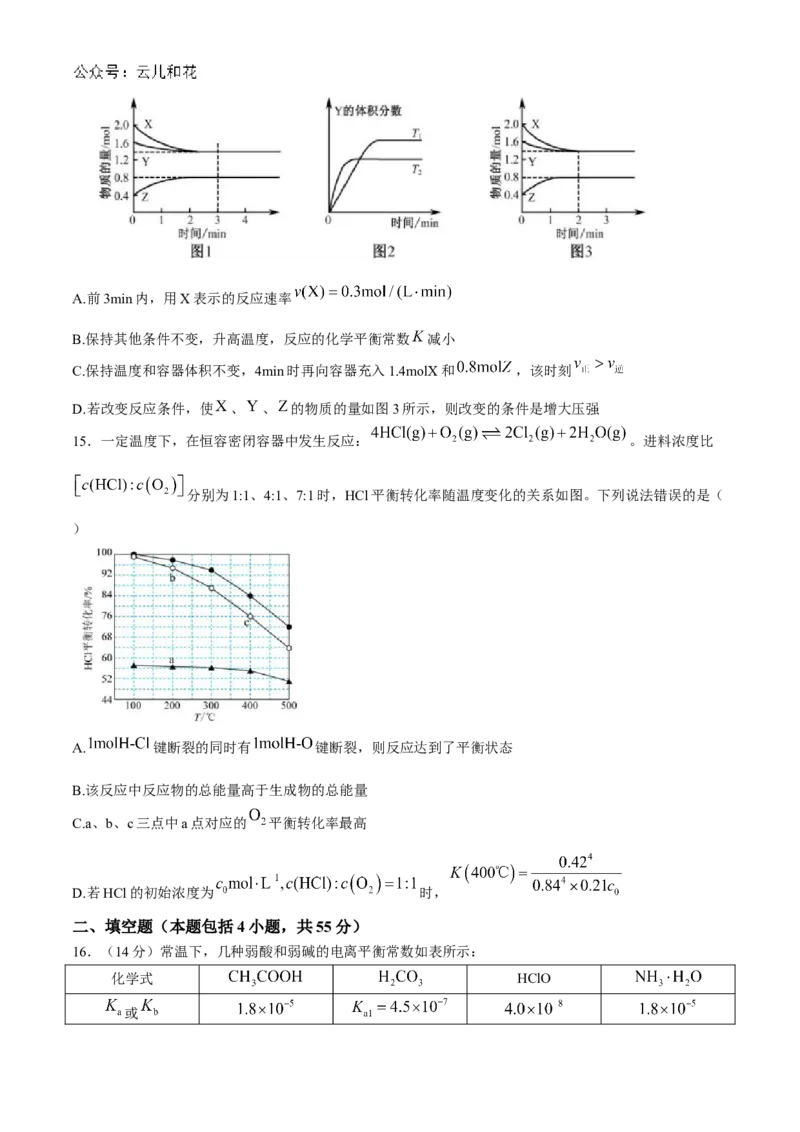
13.用CO合成甲醇 的化学方程式为 ,按照相同的物
质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图。下列说法正确的是( )
A.温度: B.正反应速率: 、
C.平衡常数: 、 D.平均摩尔质量: 、
14.一定温度下,向2L密闭容器中充入 与 ,二者发生反应生成 。反应过程中X、Y、Z
的物质的量变化如图1所示;若保持其他条件不变,温度分别为 和 时,Y的体积分数随时间的变化如
图2所示。则下列叙述正确的是( )A.前3min内,用X表示的反应速率
B.保持其他条件不变,升高温度,反应的化学平衡常数 减小
C.保持温度和容器体积不变,4min时再向容器充入1.4molX和 ,该时刻
D.若改变反应条件,使 、 、 的物质的量如图3所示,则改变的条件是增大压强
15.一定温度下,在恒容密闭容器中发生反应: 。进料浓度比
分别为1:1、4:1、7:1时,HCl平衡转化率随温度变化的关系如图。下列说法错误的是(
)
A. 键断裂的同时有 键断裂,则反应达到了平衡状态
B.该反应中反应物的总能量高于生成物的总能量
C.a、b、c三点中a点对应的 平衡转化率最高
D.若HCl的初始浓度为 时,
二、填空题(本题包括4小题,共55分)
16.(14分)常温下,几种弱酸和弱碱的电离平衡常数如表所示:
化学式 HClO
或(1) 、 、 、 结合 的能力由强到弱的顺序是______。
(2)取 醋酸溶液,若加入少量NaOH溶液,则 ______(填“增大”
“减小”或“不变”,下同);若通入少量HCl,则 ______。
(3) 的氨水中水电离出的 ______ ,该溶液水的电离程度与 ______的
溶液中水的电离程度相同。
(4)写出向NaClO溶液中通入少量 的离子反应方程式:______
(5)向氨水中加入 至溶液显中性,测得此时 ,则
______ 。
17.(13分)将浓度均为 的 、 、 、 溶液及淀粉溶液混合,一定时
间后溶液变为蓝色。该实验是一种“碘钟实验”,某小组同学在室温下对其的原理进行探究。
资料:该“碘钟实验”的总反应为 ,反应分两步进行。
反应A:______;反应B: 。
(1)反应A的离子方程式是______。
(2)对于总反应, 的作用相当于______, 可以改变单位体积内的______(填标号),从而改变反应
速率。
a.活化分子数 b.活化分子百分数 c.分子总数
(3)为证明反应A、B的存在,进行实验Ⅰ。
实验Ⅰ:a.向酸化的 溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入 溶液,溶液的蓝色褪去。
试剂X是______溶液。
(4)为探究硫酸浓度对溶液变蓝快慢的影响进行实验Ⅱ和实验Ⅲ(各溶液浓度均为 )。
用量 溶液 溶液 溶液 试剂X溶液
实验Ⅱ 5 4 8 3 0实验Ⅲ 5 2 x y z
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是15min,实验Ⅲ是20min。
①实验Ⅲ中x、y、z所对应的数值分别是______、______、______。
②对比实验Ⅱ和实验Ⅲ,可得出的实验结论是______。
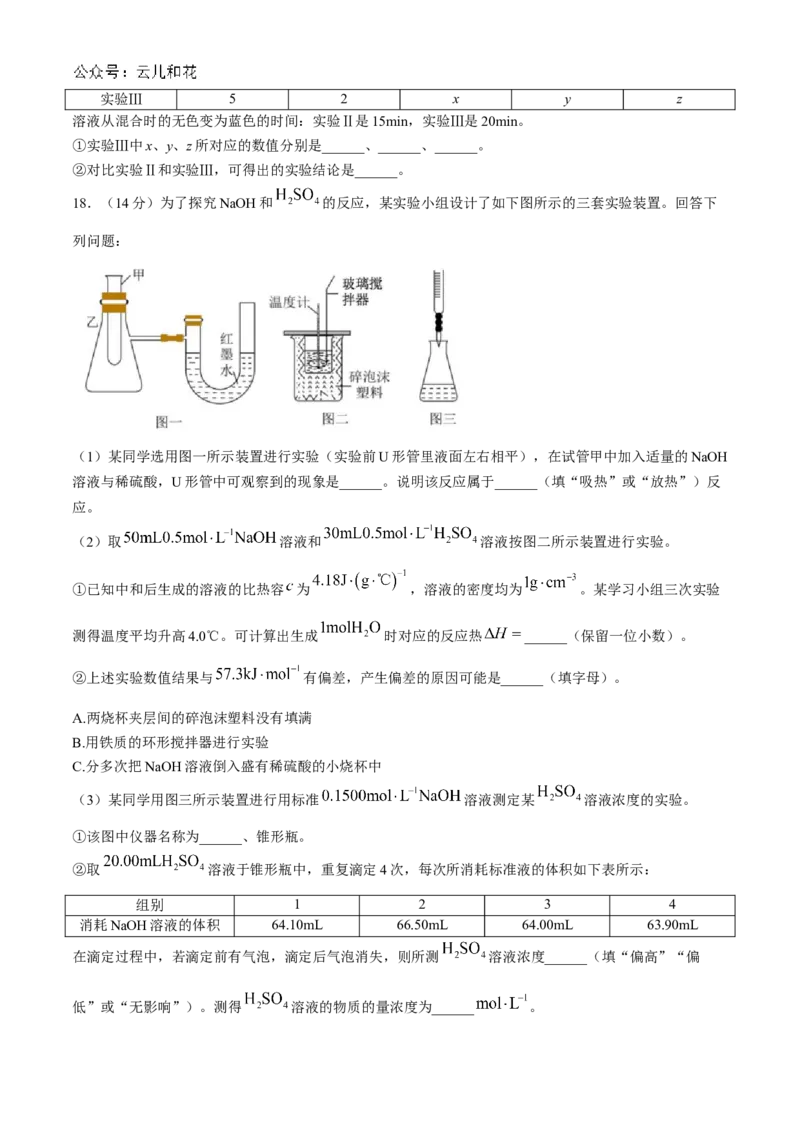
18.(14分)为了探究NaOH和 的反应,某实验小组设计了如下图所示的三套实验装置。回答下
列问题:
(1)某同学选用图一所示装置进行实验(实验前U形管里液面左右相平),在试管甲中加入适量的NaOH
溶液与稀硫酸,U形管中可观察到的现象是______。说明该反应属于______(填“吸热”或“放热”)反
应。
(2)取 溶液和 溶液按图二所示装置进行实验。
①已知中和后生成的溶液的比热容 为 ,溶液的密度均为 。某学习小组三次实验
测得温度平均升高4.0℃。可计算出生成 时对应的反应热 ______(保留一位小数)。
②上述实验数值结果与 有偏差,产生偏差的原因可能是______(填字母)。
A.两烧杯夹层间的碎泡沫塑料没有填满
B.用铁质的环形搅拌器进行实验
C.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
(3)某同学用图三所示装置进行用标准 溶液测定某 溶液浓度的实验。
①该图中仪器名称为______、锥形瓶。
②取 溶液于锥形瓶中,重复滴定4次,每次所消耗标准液的体积如下表所示:
组别 1 2 3 4
消耗NaOH溶液的体积 64.10mL 66.50mL 64.00mL 63.90mL
在滴定过程中,若滴定前有气泡,滴定后气泡消失,则所测 溶液浓度______(填“偏高”“偏
低”或“无影响”)。测得 溶液的物质的量浓度为______ 。(4)某温度时,测得 溶液 。在该温度下, 溶液与bL0.05
溶液混合后溶液 ,若混合溶液体积为 ,则 ______。
19.(14分)丙烯是重要的石油化工中间体,工业上常用丙烷催化脱氢和甲醇催化分解等方法制备。回答
下列问题:
Ⅰ.丙烷催化脱氢法制丙烯:
(1)已知 、 、 的燃烧热分别 、
、 ,则 催化脱氢生成 和 的热化
学方程式为______。
(2)570℃、 ,用 的混合气进行直接脱氢反应,3h后达到平衡,
的平衡转化率为 ,脱氢反应的 ______ (结果保留3位有效数字, 为以平衡分压代替平
衡浓度表示的平衡常数,分压=总压×物质的量分数)。在上述温度和压强下,请从平衡移动的角度解释
通入水蒸气的作用:______。
(3)下列能说明该体系在恒温恒压密闭容器中反应达到平衡状态的是______(填字母)。
A. 的物质的量分数保持不变 B. 保持不变
C.气体密度保持不变 D.速率关系:
Ⅱ.甲醇催化分解:
(4)该反应的实验数据遵循Arhenius经验公式: ( 为活化能,假设其受温度影响忽
略不计, 为速率常数,R和C为常数),此经验公式说明对于某个基元反应,当升高相同温度时,其活
化能越大,反应速率增大地______(填“越多”或“越少”)。根据如图曲线a计算该反应的活化能 为
______ 。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是
______。高二化学十月联考答案
一、选择题:本题共15小题,45分。每小题有且仅有一个选项符合题目要求。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C B D B C B B A D B D A C C D
二、填空题(本题包括4小题,共55分)
16.(14分,每空两分)
(1)
(2)增大 减小
(3) 4
(4)
(5)0.18
17.(13分,除标注外,其余每空两分)
(1)
(2)催化剂 ab
(3)淀粉KI
(4)8(1分) 3(1分) 2(1分) 其他条件不变,增大硫酸浓度可以加快反应速率
18.(14分,除标注外,其余每空两分)
(1)U形管中液面左低右高(1分) 放热(1分)
(2)① ②ABC
(3)碱式滴定管 偏高 0.2400
(4)11:9
19.(14分,每空两分)
(1)
(2)29.6 在恒温恒压条件下,通入水蒸气会使 的分压减小,平衡正向移动,增大 转
化率
(3)AC
(4)越多 31 改用更高效的催化剂