文档内容
2025—2026 学年度上学期 2024 级
期中考试化学试卷
命题人:付四喜 审题人:蔡璇
考试时间:2025年11月14日
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H:1 C:12 O:16
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1.速率控制在生产生活中较为常见。下列操作或措施与速率控制无关的是
A.用食醋浸泡水垢 B.固相反应时高速研磨
C.食品袋中加入铁粉作抗氧化剂 D.煅烧硫铁矿时将其粉碎
2.下表中物质的分类组合完全正确的是
选项 A B C D
强电解质 盐酸 NaCl
弱电解质 HClO 醋酸
非电解质 乙醇
A.A B.B C.C D.D
3.下列关于能量变化的说法正确的是
A.在高温、高压条件下发生的反应一定是吸热反应
B.古文说“冰,水为之,而寒于水”,说明水和冰相比,水的能量更高
C.化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
D.P(s,白磷)= 4P(s,红磷) ΔH<0,则红磷比白磷稳定
4
4.下列事实不能用勒夏特列原理解释的是
A.工业合成氨时,选定温度为400℃-500℃,而不是常温
B.浓氨水中加入氢氧化钠固体产生刺激性气味的气体
C.工业上生产硫酸时,充入适当过量的空气以提高SO 的转化率
2
D.实验室中常用排饱和食盐水的方法收集氯气
5.下列平衡移动方向和现象判断正确的是
A. ,加水稀释,平衡逆向移动,溶液黄色变浅
B. ,升温,溶液由蓝色变
为黄绿色
C. ,压缩容器体积,平衡不移动,气体颜色无变化
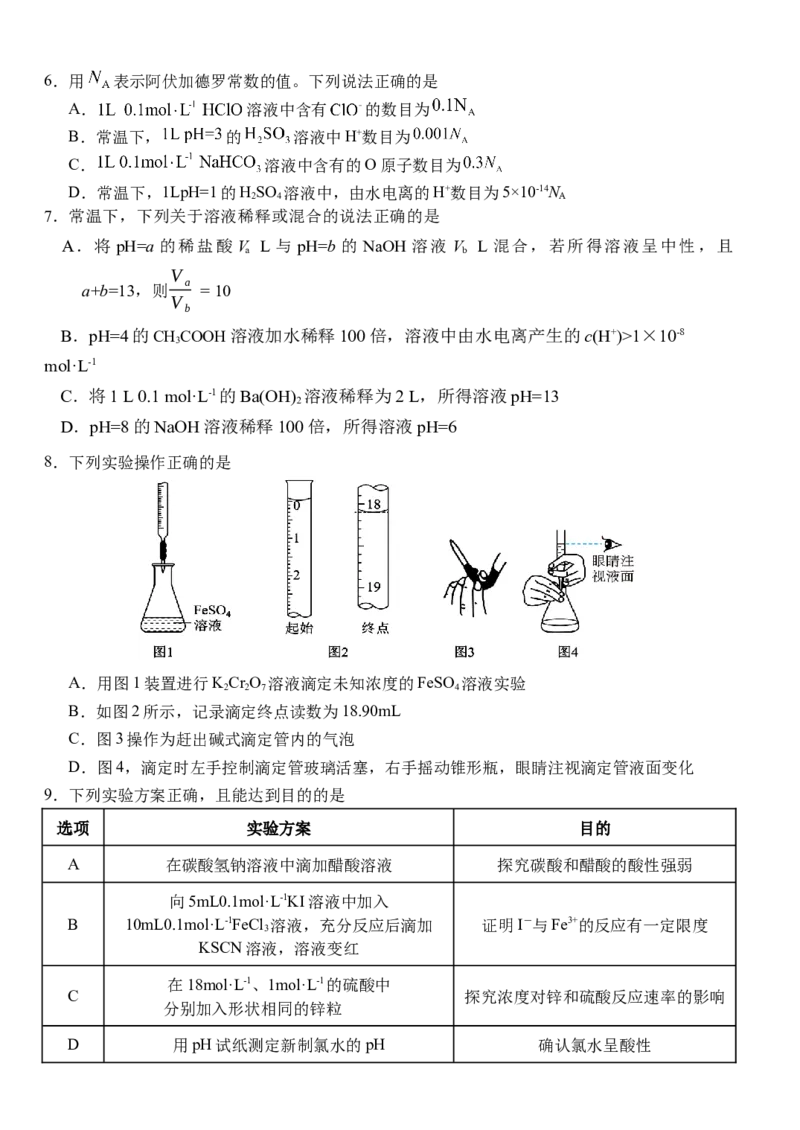
D. ,加入Fe粉,平衡正向移动,溶液颜色加深6.用 表示阿伏加德罗常数的值。下列说法正确的是
A. 溶液中含有 的数目为
B.常温下, 的 溶液中H+数目为
C. 溶液中含有的O原子数目为
D.常温下,1LpH=1的HSO 溶液中,由水电离的H+数目为5×10-14N
2 4 A
7.常温下,下列关于溶液稀释或混合的说法正确的是
A.将 pH=a 的稀盐酸 V L 与 pH=b 的 NaOH 溶液 V L 混合,若所得溶液呈中性,且
a b
V
a
a+b=13,则 = 10
V
b
B.pH=4的CHCOOH溶液加水稀释100倍,溶液中由水电离产生的c(H+)>1×10-8
3
mol·L-1
C.将1 L 0.1 mol·L-1的Ba(OH) 溶液稀释为2 L,所得溶液pH=13
2
D.pH=8的NaOH溶液稀释100倍,所得溶液pH=6
8.下列实验操作正确的是
A.用图1装置进行KCr O 溶液滴定未知浓度的FeSO 溶液实验
2 2 7 4
B.如图2所示,记录滴定终点读数为18.90mL
C.图3操作为赶出碱式滴定管内的气泡
D.图4,滴定时左手控制滴定管玻璃活塞,右手摇动锥形瓶,眼睛注视滴定管液面变化
9.下列实验方案正确,且能达到目的的是
选项 实验方案 目的
A 在碳酸氢钠溶液中滴加醋酸溶液 探究碳酸和醋酸的酸性强弱
向5mL0.1mol·L-1KI溶液中加入
B 10mL0.1mol·L-1FeCl 溶液,充分反应后滴加 证明I-与Fe3+的反应有一定限度
3
KSCN溶液,溶液变红
在18mol·L-1、1mol·L-1的硫酸中
C 探究浓度对锌和硫酸反应速率的影响
分别加入形状相同的锌粒
D 用pH试纸测定新制氯水的pH 确认氯水呈酸性A.A B.B C.C D.D
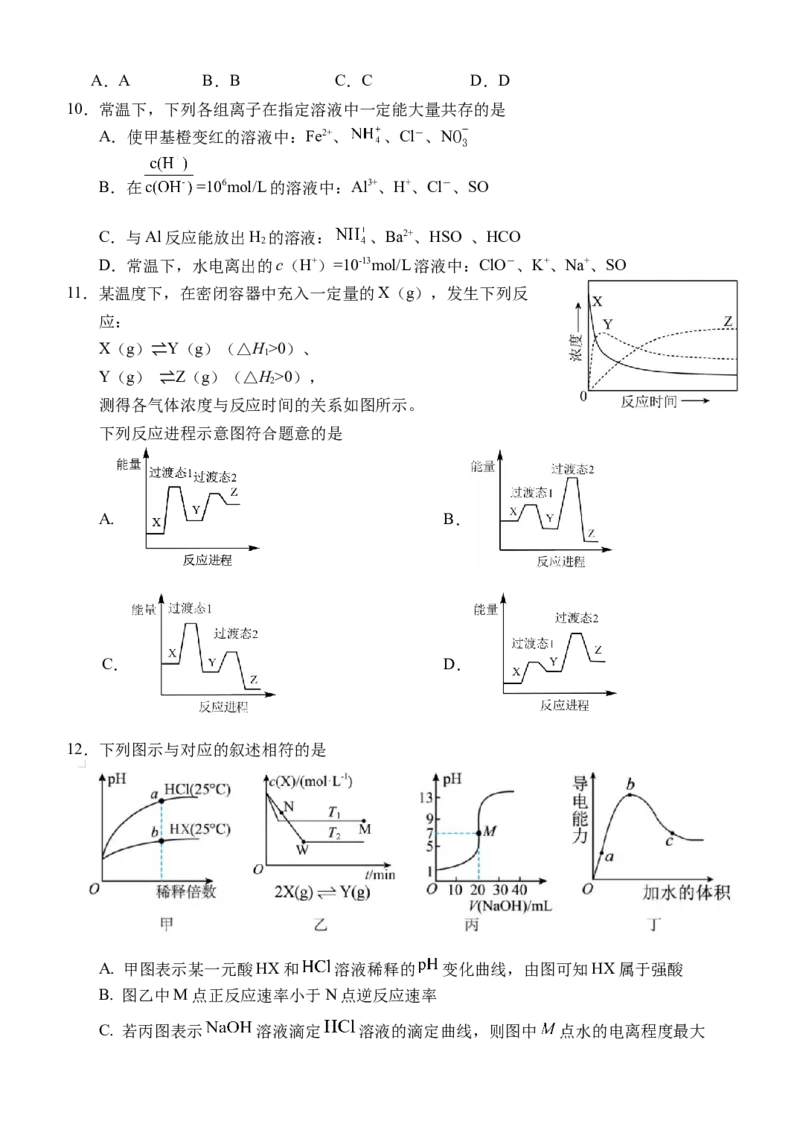
10.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使甲基橙变红的溶液中:Fe2+、 、Cl-、NO−
3
B.在 =106mol/L的溶液中:Al3+、H+、Cl-、SO
C.与Al反应能放出H 的溶液: 、Ba2+、HSO 、HCO
2
D.常温下,水电离出的c(H+)=10-13mol/L溶液中:ClO-、K+、Na+、SO
11.某温度下,在密闭容器中充入一定量的X(g),发生下列反
应:
X(g)⇌Y(g)(△H
1
>0)、
Y(g) ⇌Z(g)(△H
2
>0),
测得各气体浓度与反应时间的关系如图所示。
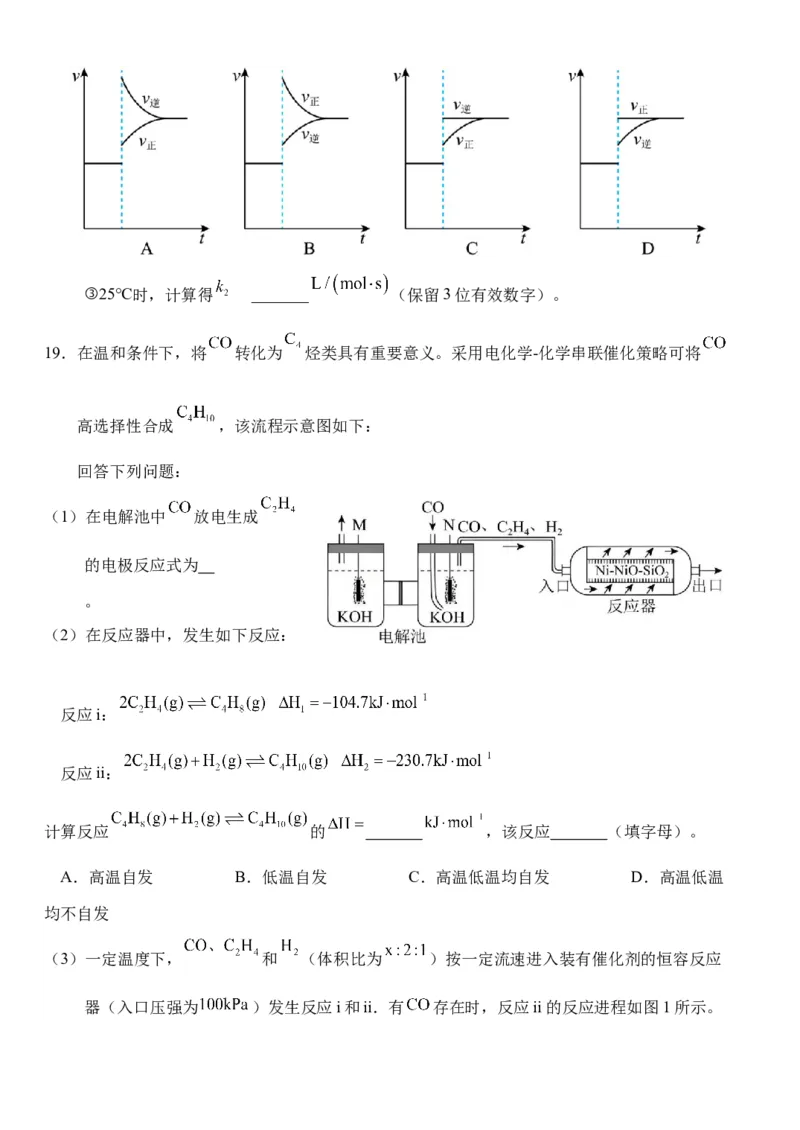
下列反应进程示意图符合题意的是
A. B.
C. D.
12.下列图示与对应的叙述相符的是
A. 甲图表示某一元酸HX和 溶液稀释的 变化曲线,由图可知HX属于强酸
B. 图乙中M点正反应速率小于N点逆反应速率
C. 若丙图表示 溶液滴定 溶液的滴定曲线,则图中 点水的电离程度最大D. 若丁图表示一定温度下向冰醋酸中加水后溶液导电能力的变化曲线,则图中 三点
的电离程度:
13.根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸性越强;结合质
子的物质是碱,结合质子能力越强,碱性越强。下表是常温下几种弱酸的电离常数:
依据上表数据,下列说法正确的是
A.酸性强弱顺序:
B.向 溶液中滴加少量 溶液,发生反应生成 和
C.根据酸碱质子理论,碱性强弱顺序:
D.向 溶液中通入足量的 可生成大量的 气体
14.图像是表征化学反应速率和化学平衡的重要方式。下列说法错误的是
A.图1升高温度时,反应 的平衡常数会减小
B.图2为 在绝热恒容密闭容器中进行,该反应为放热反应
C.图3为温度T时合成氨反应,在a、b、c三点所处的平衡状态中, 的转化率最高的是b点
D.图4为反应 ,L线上所有的点都是平衡点,则E点
15.两种酸式碳酸盐的分解反应如下。某温度平衡时总压强分别为p 和p
1 2。
反应1:NH HCO (s) NH (g)+H O(g)+CO (g) p=3.6×104Pa
4 3 3 2 2 1
反应2:2NaHCO (s) NaCO(s)+H O(g)+CO (g) p=4×103Pa
3 2 3 2 2 2
该温度下,刚性密闭容器中放入NH HCO 和NaCO 固体,平衡后以上3种固体均大量存
4 3 2 3
在。
(已知在化学平衡体系中,由各气体物质的分压替代浓度,计算的平衡常数叫压强平衡常
数,用符号K 表示,其单位与表达式有关。分压=总压×物质的量分数。)
p
下列说法错误的是A.平衡后总压强为4.36×105Pa
B.反应2的平衡常数Kp为4×106
C.缩小体积,平衡后总压强不变
D.通入NH ,再次平衡后总压强不变
3
二、非选择题(共55分)
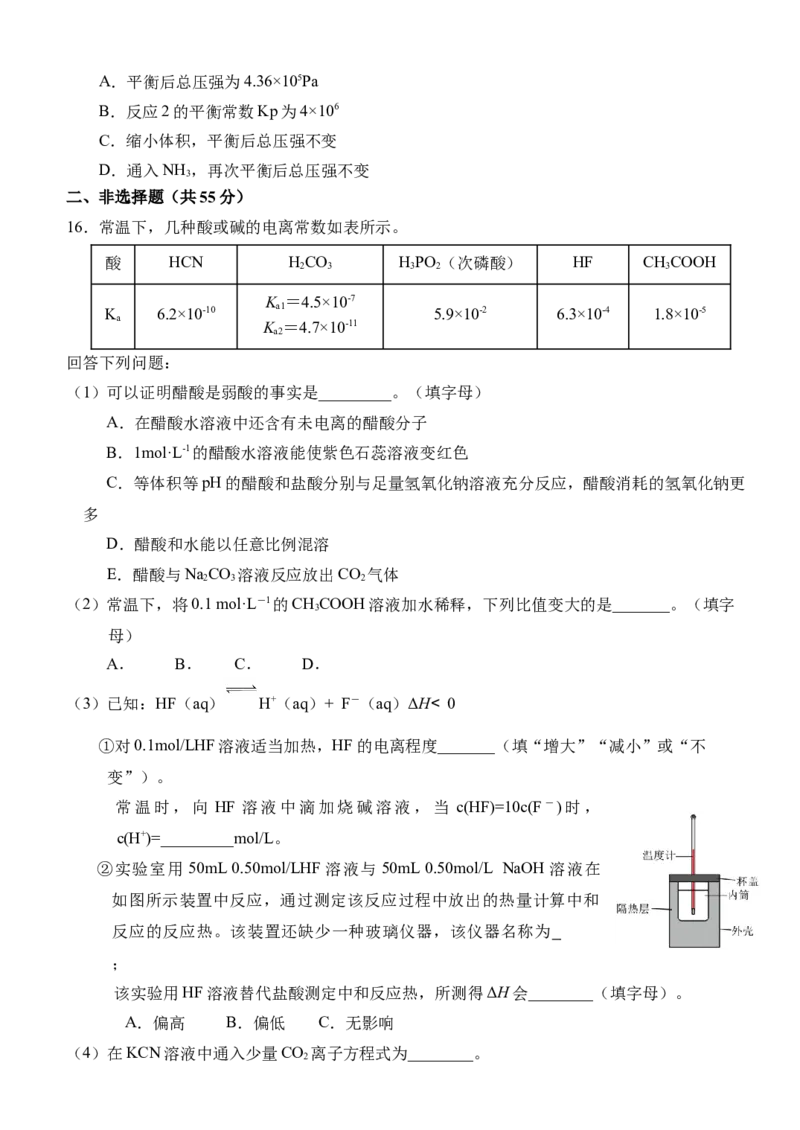
16.常温下,几种酸或碱的电离常数如表所示。
酸 HCN HCO HPO (次磷酸) HF CHCOOH
2 3 3 2 3
K =4.5×10-7
K 6.2×10-10 a1 5.9×10-2 6.3×10-4 1.8×10-5
a
K =4.7×10-11
a2
回答下列问题:
(1)可以证明醋酸是弱酸的事实是_________。(填字母)
A.在醋酸水溶液中还含有未电离的醋酸分子
B.1mol·L-1的醋酸水溶液能使紫色石蕊溶液变红色
C.等体积等pH的醋酸和盐酸分别与足量氢氧化钠溶液充分反应,醋酸消耗的氢氧化钠更
多
D.醋酸和水能以任意比例混溶
E.醋酸与NaCO 溶液反应放出CO 气体
2 3 2
(2)常温下,将0.1 mol·L-1的CHCOOH溶液加水稀释,下列比值变大的是_______。(填字
3
母)
A. B. C. D.
(3)已知:HF(aq) H+(aq)+ F-(aq)ΔH< 0
①对0.1mol/LHF溶液适当加热,HF的电离程度_______(填“增大”“减小”或“不
变”)。
常温时,向 HF 溶液中滴加烧碱溶液,当 c(HF)=10c(F-)时,
c(H+)=_________mol/L。
②实验室用 50mL 0.50mol/LHF溶液与50mL 0.50mol/L NaOH溶液在
如图所示装置中反应,通过测定该反应过程中放出的热量计算中和
反应的反应热。该装置还缺少一种玻璃仪器,该仪器名称为
;
该实验用HF溶液替代盐酸测定中和反应热,所测得ΔH会________(填字母)。
A.偏高 B.偏低 C.无影响
(4)在KCN溶液中通入少量CO 离子方程式为________。
2(5)次磷酸是一元酸,30mL0.1mol/LNaOH溶液和__________mL0.1mol/L 溶液恰好完全
反应,写出HPO 的电离方程式___________。
3 2
(6)常温时,反应CHCOOH+CN- CHCOO-+HCN的化学平衡常数为 (保留两位有
3 3
效数字)。
17.GB2719-2018《食品安全国家标准食醋》中规定食醋总酸指标≥3.5g/100mL(以乙酸计),
某同学在实验室用中和滴定法检测某品牌食醋是否合格。回答下列问题:
I.实验步骤:
(1)用___________(填仪器名称)量取 食用白醋,在烧杯中用水稀释后转移到
容量瓶中定容,摇匀即得待测白醋溶液。
(2)量取 待测白醋溶液于锥形瓶中,向其中滴加2滴__________作指示剂。
(3)读取盛装 溶液的碱式滴定管的初始读数。
(4)滴定。滴定终点的现象是___________。
Ⅱ.数据记录:
滴定次数
1 2 3 4
实验数据/
V(样品) 20.00 20.00 20.00 20.00
(消耗) 15.95 15.00 15.05 14.95
Ⅲ.数据处理:
(5)该白醋的总酸度为_________ ,该品牌白醋_________(填“合格”或“不合
格”)。
IV.误差分析:
(6)实验过程中该同学出现了以下操作,其中可能导致结果偏大的是___________(填字母)。A.酸式滴定管没有进行润洗
B.锥形瓶用待测白醋润洗
C.滴定开始时滴定管中有气泡,结束时无气泡
D.指示剂变色立即停止滴定
E.滴定开始时俯视读数,结束时仰视读数
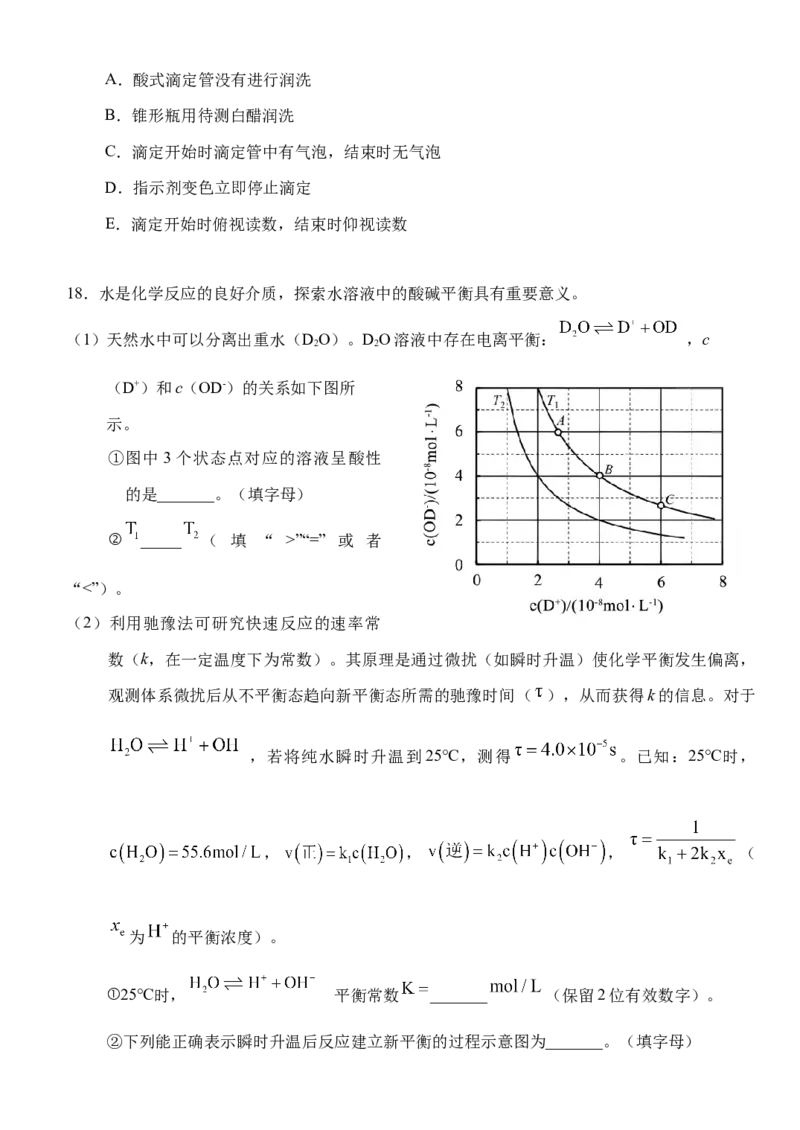
18.水是化学反应的良好介质,探索水溶液中的酸碱平衡具有重要意义。
(1)天然水中可以分离出重水(DO)。DO溶液中存在电离平衡: ,c
2 2
(D+)和c(OD-)的关系如下图所
示。
①图中3个状态点对应的溶液呈酸性
的是_______。(填字母)
② _____ ( 填 “ >”“=” 或 者
“<”)。
(2)利用驰豫法可研究快速反应的速率常
数(k,在一定温度下为常数)。其原理是通过微扰(如瞬时升温)使化学平衡发生偏离,
观测体系微扰后从不平衡态趋向新平衡态所需的驰豫时间( ),从而获得k的信息。对于
,若将纯水瞬时升温到25℃,测得 。已知:25℃时,
, , , (
为 的平衡浓度)。
的
①25℃时, 平衡常数 _______ (保留2位有效数字)。
②下列能正确表示瞬时升温后反应建立新平衡的过程示意图为_______。(填字母)为
③25℃时,计算得 _______ (保留3位有效数字)。
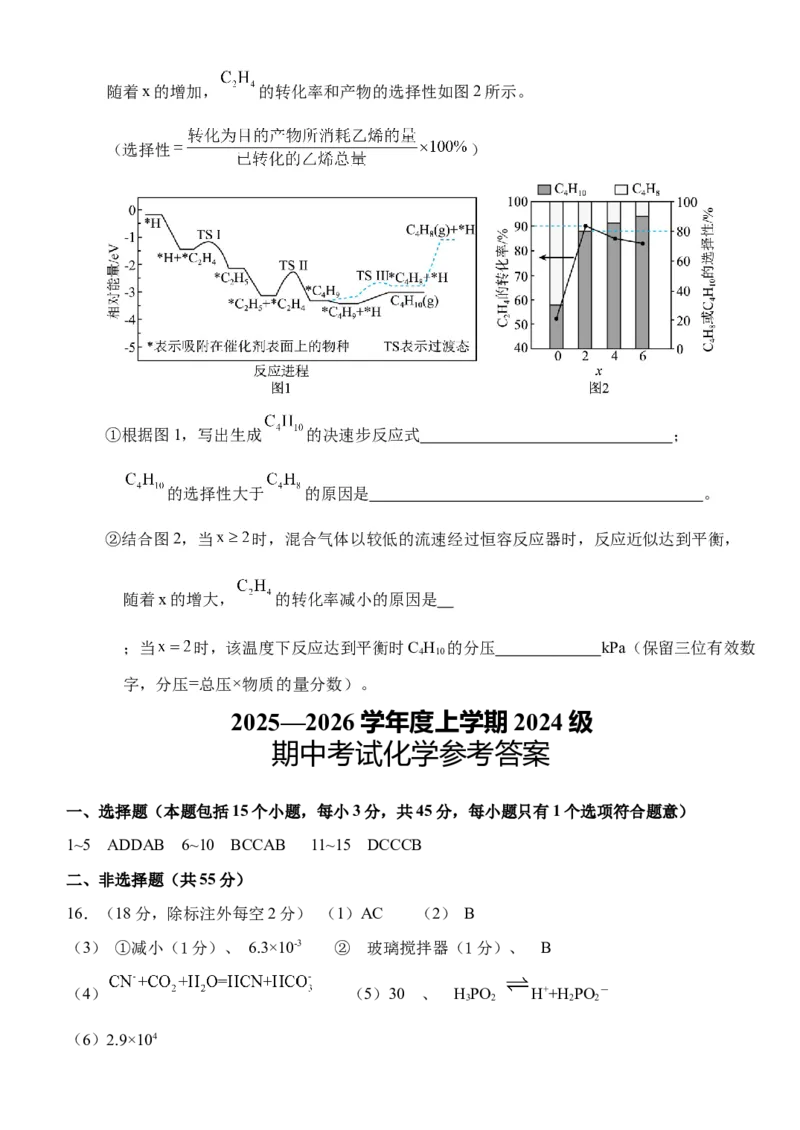
19.在温和条件下,将 转化为 烃类具有重要意义。采用电化学-化学串联催化策略可将
高选择性合成 ,该流程示意图如下:
回答下列问题:
(1)在电解池中 放电生成
的电极反应式为
。
(2)在反应器中,发生如下反应:
反应i:
反应ii:
计算反应 的 ,该反应 (填字母)。
A.高温自发 B.低温自发 C.高温低温均自发 D.高温低温
均不自发
(3)一定温度下, 和 (体积比为 )按一定流速进入装有催化剂的恒容反应
器(入口压强为 )发生反应i和ii.有 存在时,反应ii的反应进程如图1所示。随着x的增加, 的转化率和产物的选择性如图2所示。
(选择性 )
①根据图1,写出生成 的决速步反应式 ;
的选择性大于 的原因是 。
②结合图2,当 时,混合气体以较低的流速经过恒容反应器时,反应近似达到平衡,
随着x的增大, 的转化率减小的原因是
;当 时,该温度下反应达到平衡时C H 的分压 kPa(保留三位有效数
4 10
字,分压=总压×物质的量分数)。
2025—2026 学年度上学期 2024 级
期中考试化学参考答案
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1~5 ADDAB 6~10 BCCAB 11~15 DCCCB
二、非选择题(共55分)
16.(18分,除标注外每空2分) (1)AC (2) B
(3) ①减小(1分)、 6.3×10-3 ② 玻璃搅拌器(1分)、 B
(4) (5)30 、 HPO H++H PO -
3 2 2 2
(6)2.9×10417.(12分)(1)酸式滴定管 (1分); (2)酚酞 (2分)
(4)加入半滴氢氧化钠溶液后,溶液由无色恰好变为浅红色,且在半分钟内不变色 (2分);
(5) ①4.5 (3分) ②合格 (1分)
(6) BCE(3分)
18.(10分, 每空2分)(1) ① C ② >
(2) ① ②D ③
19(15分,除标注外每空2分)(1)
(2)﹣126 B
(3) ① ; 由 (或 )生成 时,活化能较大,反应速率
慢 。
②入口压强为 ,随着x的增大,CO的分压增大,对于反应i和反应ii相当于减压,反
应i和反应ii平衡均逆向移动,所以 的转化率减小 ;
14.4(3分)