文档内容
2024~2025 学年第一学期期末学业质量监测卷
高二化学
(75分钟 100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案字母涂黑,如需改
动,用橡皮擦干净后,再选涂其他答案字母。回答非选择题时,将答案写在答题卡上,写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 S—32 Pb—207
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意。
1. 化学与人类生产、生活密切相关。下列有关说法正确的是
A. 自来水厂用明矾净水,漂白粉也能代替明矾净水
B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C. 草木灰和铵态氮肥混合使用则肥效更好
D. 电解 饱和溶液,可制得金属镁
2. 下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是
选项 A B C D
强电解质 Fe NaCl
弱电解质
非电解质 蔗糖 酒精
A. A B. B C. C D. D
3. 已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别如下:
据此判断,下列说法正确的是A. 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B. 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C. 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D. 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
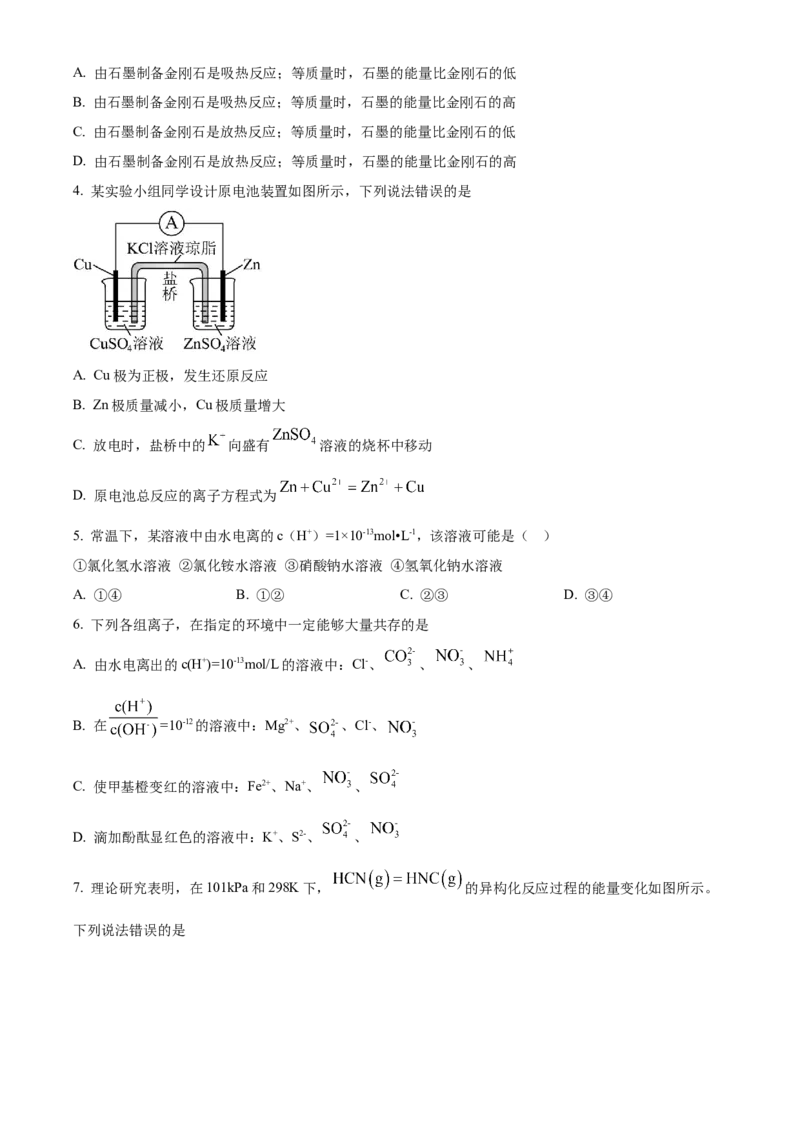
4. 某实验小组同学设计原电池装置如图所示,下列说法错误的是
A. Cu极为正极,发生还原反应
B. Zn极质量减小,Cu极质量增大
C. 放电时,盐桥中的 向盛有 溶液的烧杯中移动
D. 原电池总反应的离子方程式为
5. 常温下,某溶液中由水电离的c(H+)=1×10-13mol•L-1,该溶液可能是( )
①氯化氢水溶液 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A. ①④ B. ①② C. ②③ D. ③④
6. 下列各组离子,在指定的环境中一定能够大量共存的是
A. 由水电离出的c(H+)=10-13mol/L的溶液中:Cl-、 、 、
B. 在 =10-12的溶液中:Mg2+、 、Cl-、
C. 使甲基橙变红的溶液中:Fe2+、Na+、 、
D. 滴加酚酞显红色的溶液中:K+、S2-、 、
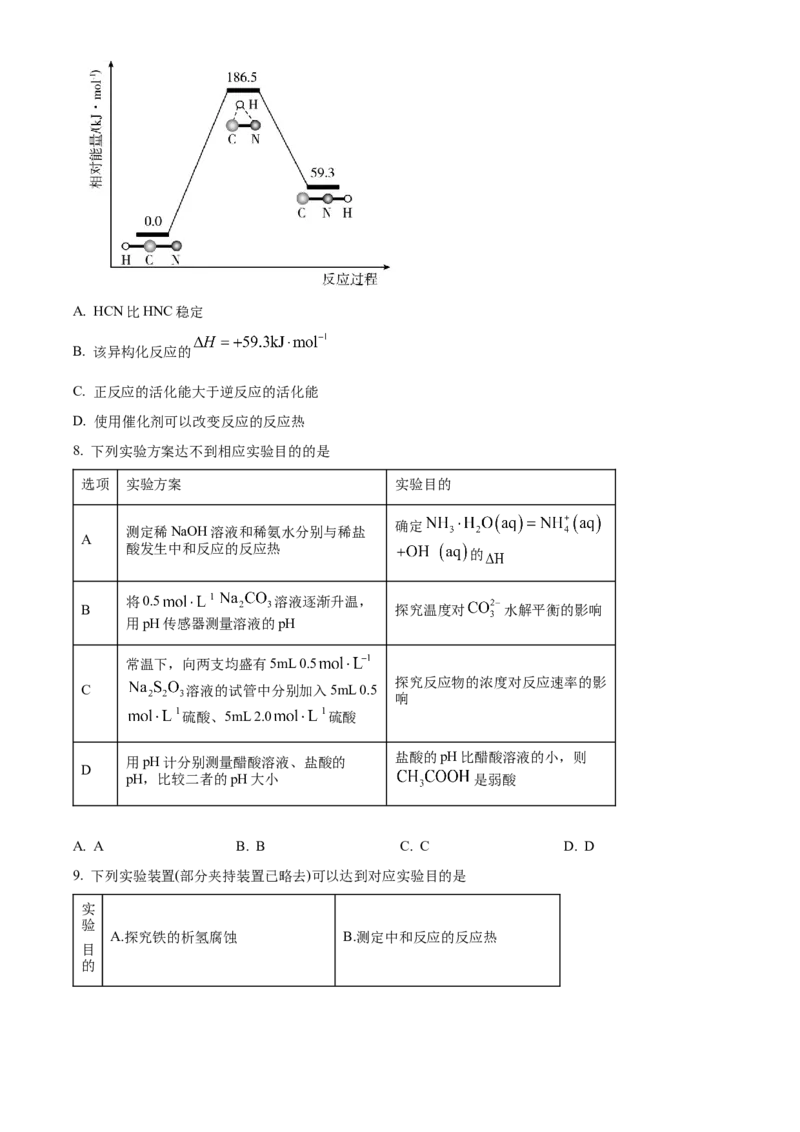
7. 理论研究表明,在101kPa和298K下, 的异构化反应过程的能量变化如图所示。
下列说法错误的是A. HCN比HNC稳定
B. 该异构化反应的
C. 正反应的活化能大于逆反应的活化能
D. 使用催化剂可以改变反应的反应热
8. 下列实验方案达不到相应实验目的的是
选项 实验方案 实验目的
确定
测定稀NaOH溶液和稀氨水分别与稀盐
A
酸发生中和反应的反应热
的
将0.5 溶液逐渐升温,
B 探究温度对 水解平衡的影响
用pH传感器测量溶液的pH
常温下,向两支均盛有5mL 0.5
探究反应物的浓度对反应速率的影
C 溶液的试管中分别加入5mL 0.5
响
硫酸、5mL 2.0 硫酸
盐酸的pH比醋酸溶液的小,则
用pH计分别测量醋酸溶液、盐酸的
D
pH,比较二者的pH大小 是弱酸
A. A B. B C. C D. D
9. 下列实验装置(部分夹持装置已略去)可以达到对应实验目的是
实
验
A.探究铁的析氢腐蚀 B.测定中和反应的反应热
目
的实
验
装
置
实
验 D.探究温度对化学平衡移动的影
C.比较AgCl和 的溶解度大小
目 响
的
实
验
装
置
A. A B. B C. C D. D
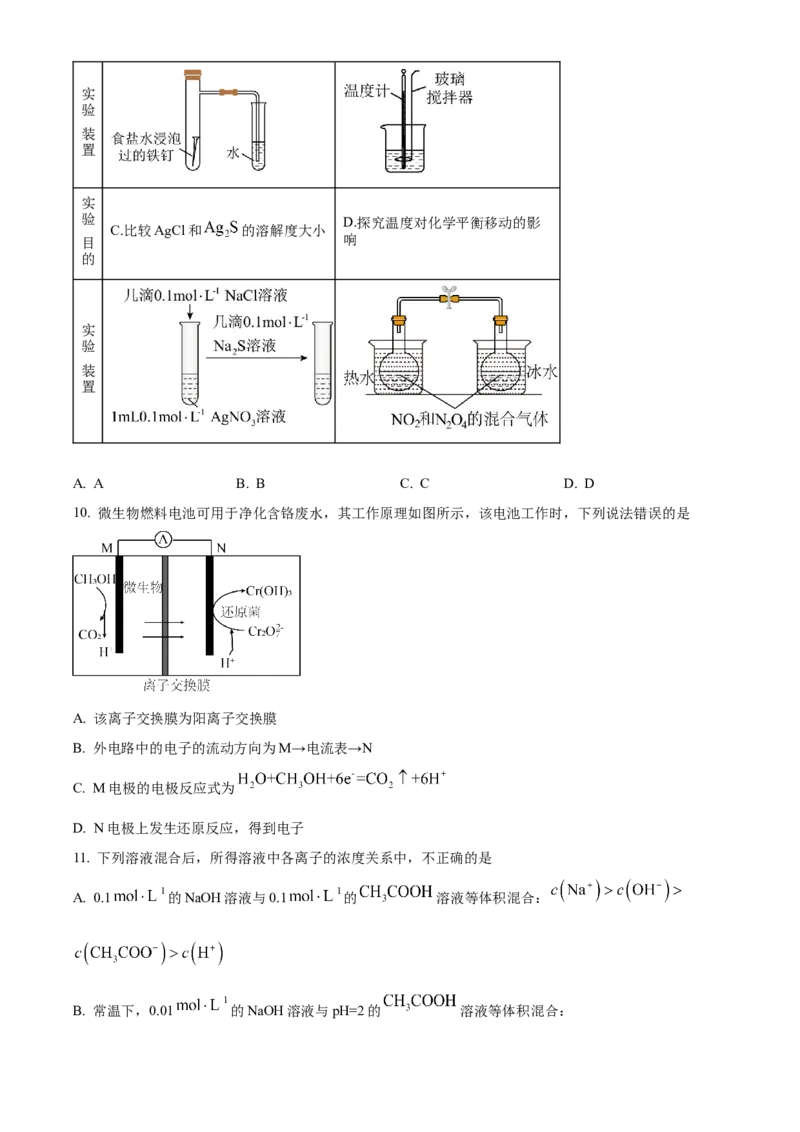
10. 微生物燃料电池可用于净化含铬废水,其工作原理如图所示,该电池工作时,下列说法错误的是
A. 该离子交换膜为阳离子交换膜
B. 外电路中的电子的流动方向为M→电流表→N
C. M电极的电极反应式为
D. N电极上发生还原反应,得到电子
11. 下列溶液混合后,所得溶液中各离子的浓度关系中,不正确的是
A. 0.1 的NaOH溶液与0.1 的 溶液等体积混合:
B. 常温下,0.01 的NaOH溶液与pH=2的 溶液等体积混合:C. 常温下,0.1 的 溶液与0.1 的NaOH溶液混合后使pH=7,则
D. 0.1 的 溶液与0.1 的 溶液等体积混合:
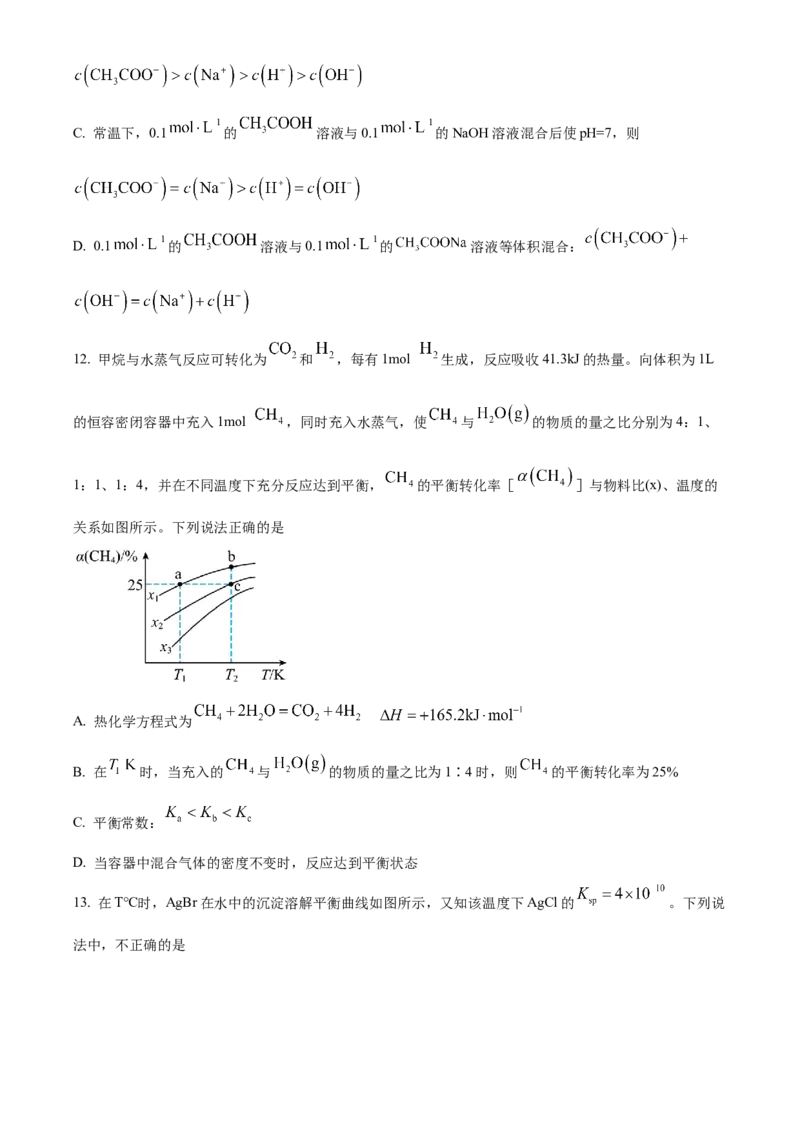
12. 甲烷与水蒸气反应可转化为 和 ,每有1mol 生成,反应吸收41.3kJ的热量。向体积为1L
的恒容密闭容器中充入1mol ,同时充入水蒸气,使 与 的物质的量之比分别为4:1、
1:1、1:4,并在不同温度下充分反应达到平衡, 的平衡转化率[ ]与物料比(x)、温度的
关系如图所示。下列说法正确的是
A. 热化学方程式为
B. 在 时,当充入的 与 的物质的量之比为1∶4时,则 的平衡转化率为25%
C. 平衡常数:
D. 当容器中混合气体的密度不变时,反应达到平衡状态
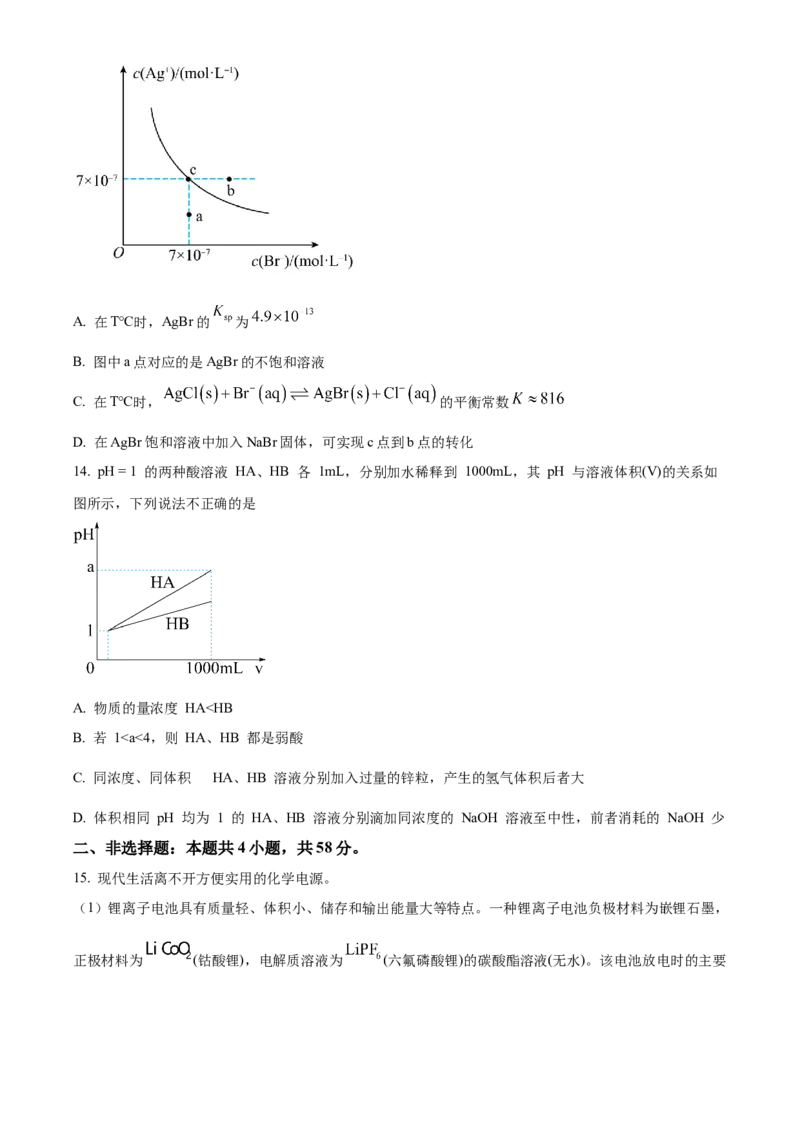
13. 在T℃时,AgBr在水中的沉淀溶解平衡曲线如图所示,又知该温度下AgCl的 。下列说
法中,不正确的是A. 在T℃时,AgBr的 为
B. 图中a点对应的是AgBr的不饱和溶液
C. 在T℃时, 的平衡常数
D. 在AgBr饱和溶液中加入NaBr固体,可实现c点到b点的转化
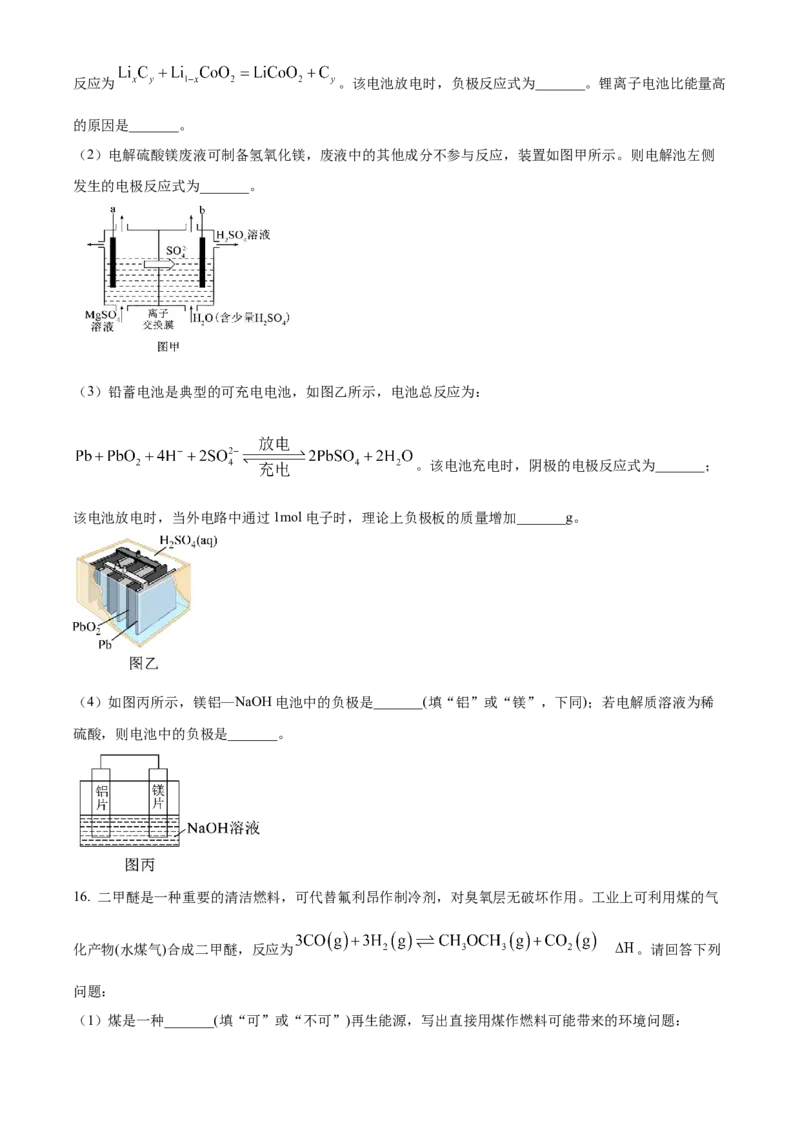
14. pH = 1 的两种酸溶液 HA、HB 各 1mL,分别加水稀释到 1000mL,其 pH 与溶液体积(V)的关系如
图所示,下列说法不正确的是
A. 物质的量浓度 HA”“<”或“=”)。
(5)b点溶液中: _______ (填“>”“<”或“=”)。
(6)c点溶液中含氮粒子浓度由大到小的顺序是_______(填粒子符号)。2024~2025 学年第一学期期末学业质量监测卷
高二化学答案
1-7.BCACA.DD 8. BD 9.D 10.C 11-14.ABDC
15. (1) ①. ②. 锂是最轻的金属,使得每单位质量能够储存更多的能
量
(2)
(3) ①. ②. 48
(4) ①. 铝 ②. 镁
16. (1) ①. 不可 ②. 酸雨、粉尘等
(2)-268kJ/mol
(3) ①. 0.45 ②. ③. AD
(4) ①. ②. 2.5
17. (1) ①. 增大接触面积,加快溶浸速率 ②. 还原 、
(2) ①. ②. 4.7≤pH<6.6
(3) ①. ②. 0.7
(4)
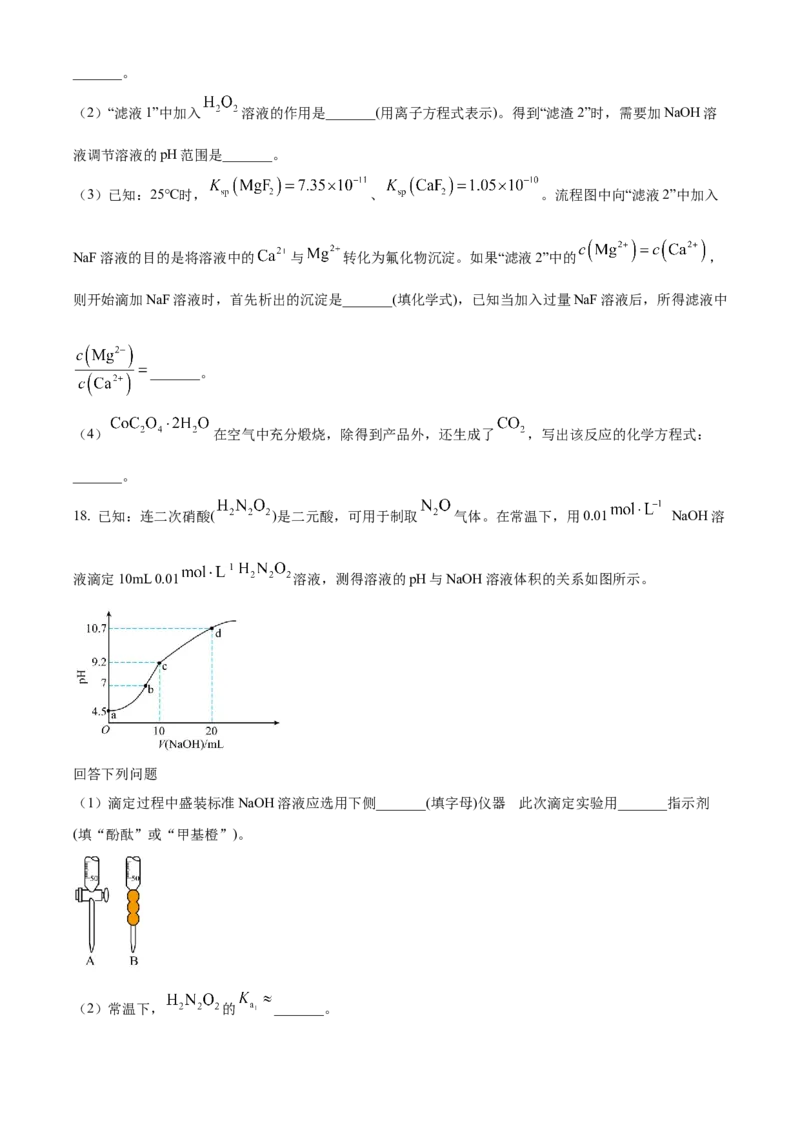
18. (1) ①. B ②. 酚酞
(2)
(3)不能 (4)<
(5)= (6)