文档内容
武汉外国语学校 2023-2024 学年度下学期期末考试
高二化学试卷
命题教师:高二化学组 审题教师:高二化学组
考试时间:2024年6月27日 考试时长:75分钟 试卷满分:100分
相对原子质量:H-1 Li-7 C-12 O-16 Cl-35.5
一、选择题:本题共 15个小题,每小题 3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.中华文化源远流长,化学与文化传承密不可分。下列说法错误的是( )
A.制墨时使松木在窑内焖烧,发生不完全燃烧
B.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
C.中国古代书写用的简牍竹简,主要成分是纤维素
D.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
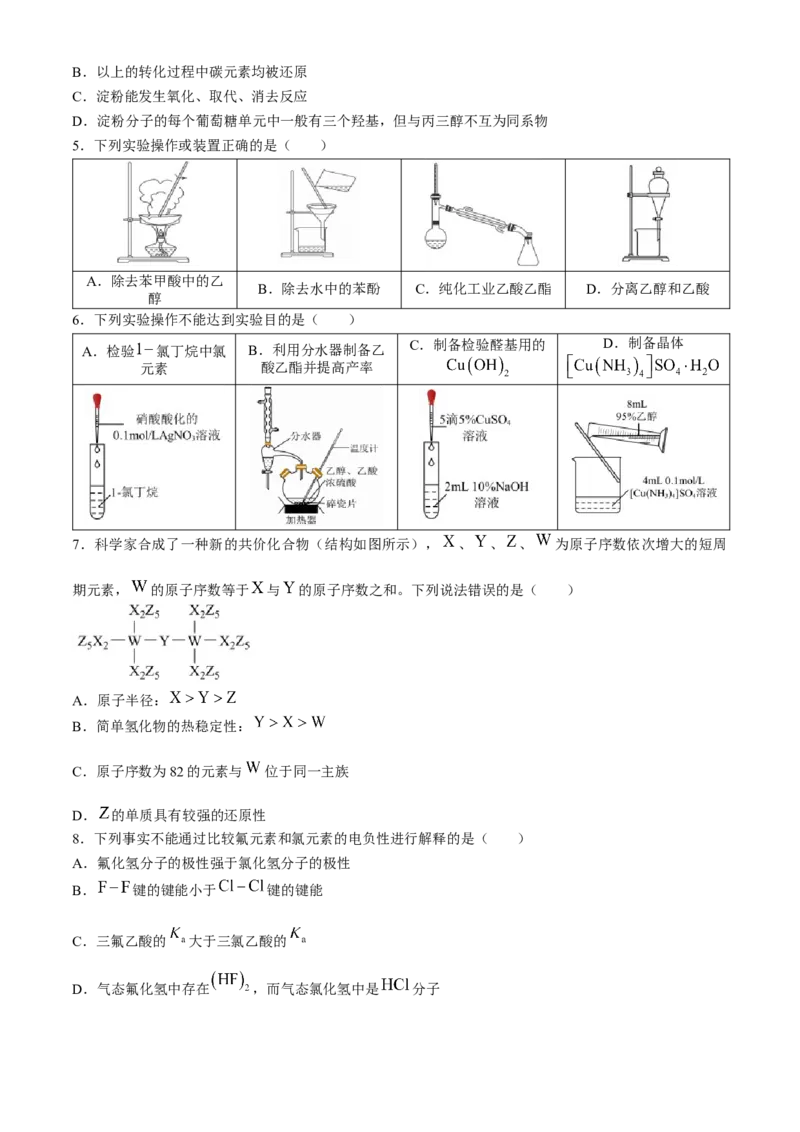
2.下列图示错误的是( )
B. 的 C.基态 的价层电子的轨 D. 键的电子云轮廓
A. 中 键
模型 道表示式 图
3.中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。下列关于金刚石、石墨、石
墨炔的说法正确的是( )
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
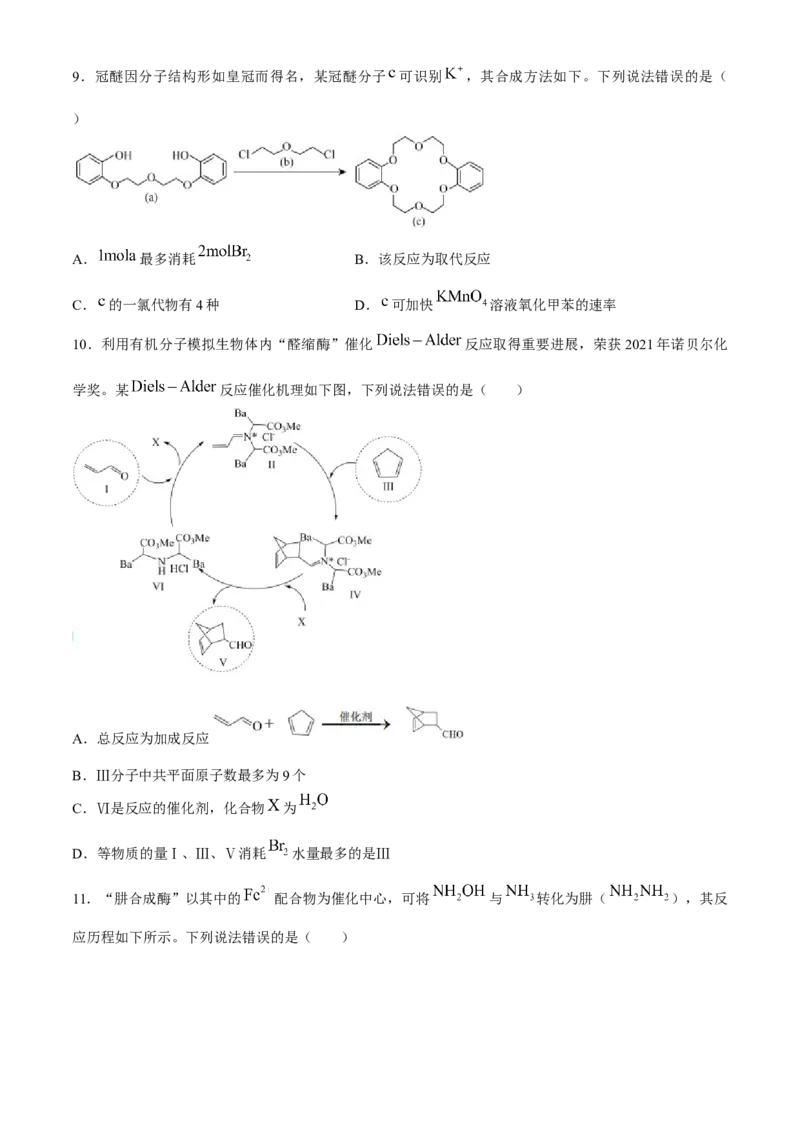
4.中科院天津工业生物所首度在实验室实现了二氧化碳人工合成淀粉的重大科技突破,这是世界级的生
物技术科研成就,其路径如图所示,下列有关说法错误的是( )
A.步骤③中存在非极性键的断裂和生成B.以上的转化过程中碳元素均被还原
C.淀粉能发生氧化、取代、消去反应
D.淀粉分子的每个葡萄糖单元中一般有三个羟基,但与丙三醇不互为同系物
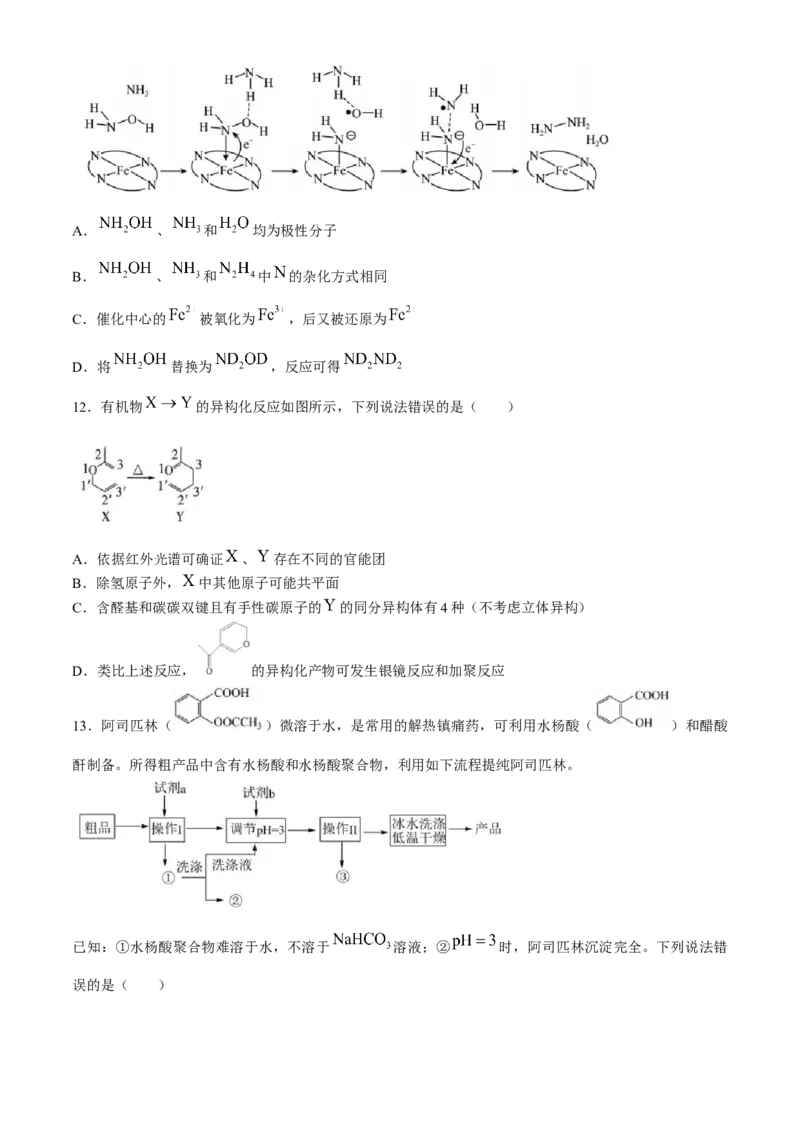
5.下列实验操作或装置正确的是( )
A.除去苯甲酸中的乙
B.除去水中的苯酚 C.纯化工业乙酸乙酯 D.分离乙醇和乙酸
醇
6.下列实验操作不能达到实验目的是( )
C.制备检验醛基用的 D.制备晶体
A.检验 氯丁烷中氯 B.利用分水器制备乙
元素 酸乙酯并提高产率
7.科学家合成了一种新的共价化合物(结构如图所示), 、 、 、 为原子序数依次增大的短周
期元素, 的原子序数等于 与 的原子序数之和。下列说法错误的是( )
A.原子半径:
B.简单氢化物的热稳定性:
C.原子序数为82的元素与 位于同一主族
D. 的单质具有较强的还原性
8.下列事实不能通过比较氟元素和氯元素的电负性进行解释的是( )
A.氟化氢分子的极性强于氯化氢分子的极性
B. 键的键能小于 键的键能
C.三氟乙酸的 大于三氯乙酸的
D.气态氟化氢中存在 ,而气态氯化氢中是 分子9.冠醚因分子结构形如皇冠而得名,某冠醚分子 可识别 ,其合成方法如下。下列说法错误的是(
)
A. 最多消耗 B.该反应为取代反应
C. 的一氯代物有4种 D. 可加快 溶液氧化甲苯的速率
10.利用有机分子模拟生物体内“醛缩酶”催化 反应取得重要进展,荣获2021年诺贝尔化
学奖。某 反应催化机理如下图,下列说法错误的是( )
A.总反应为加成反应
B.Ⅲ分子中共平面原子数最多为9个
C.Ⅵ是反应的催化剂,化合物 为
D.等物质的量Ⅰ、Ⅲ、Ⅴ消耗 水量最多的是Ⅲ
11.“肼合成酶”以其中的 配合物为催化中心,可将 与 转化为肼( ),其反
应历程如下所示。下列说法错误的是( )A. 、 和 均为极性分子
B. 、 和 中 的杂化方式相同
C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得
12.有机物 的异构化反应如图所示,下列说法错误的是( )
A.依据红外光谱可确证 、 存在不同的官能团
B.除氢原子外, 中其他原子可能共平面
C.含醛基和碳碳双键且有手性碳原子的 的同分异构体有4种(不考虑立体异构)
D.类比上述反应, 的异构化产物可发生银镜反应和加聚反应
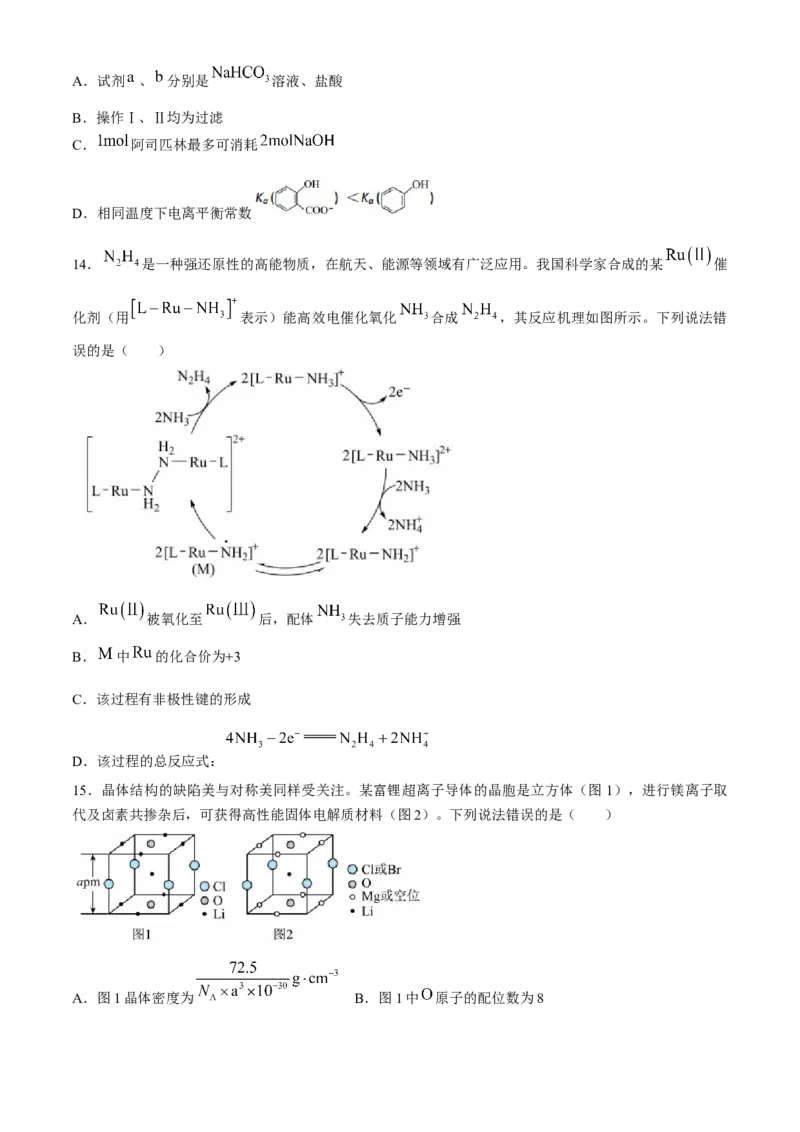
13.阿司匹林( )微溶于水,是常用的解热镇痛药,可利用水杨酸( )和醋酸
酐制备。所得粗产品中含有水杨酸和水杨酸聚合物,利用如下流程提纯阿司匹林。
已知:①水杨酸聚合物难溶于水,不溶于 溶液;② 时,阿司匹林沉淀完全。下列说法错
误的是( )A.试剂 、 分别是 溶液、盐酸
B.操作Ⅰ、Ⅱ均为过滤
C. 阿司匹林最多可消耗
D.相同温度下电离平衡常数
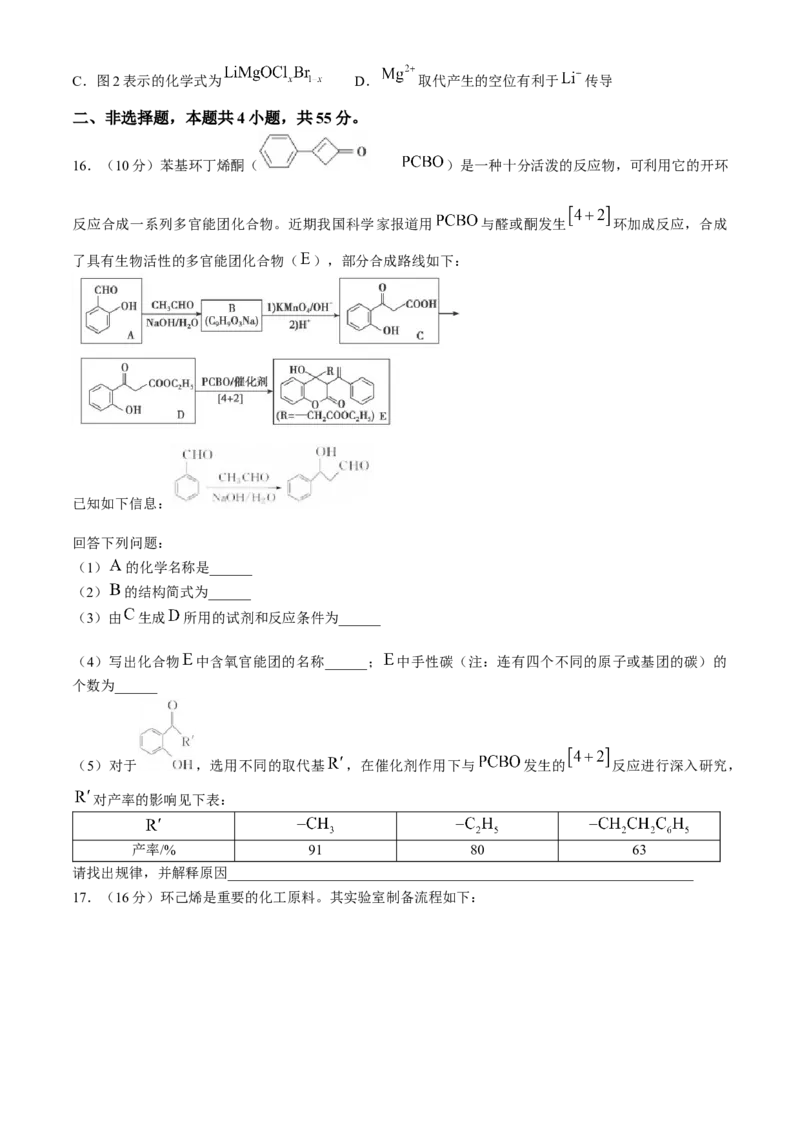
14. 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某 催
化剂(用 表示)能高效电催化氧化 合成 ,其反应机理如图所示。下列说法错
误的是( )
A. 被氧化至 后,配体 失去质子能力增强
B. 中 的化合价为+3
C.该过程有非极性键的形成
D.该过程的总反应式:
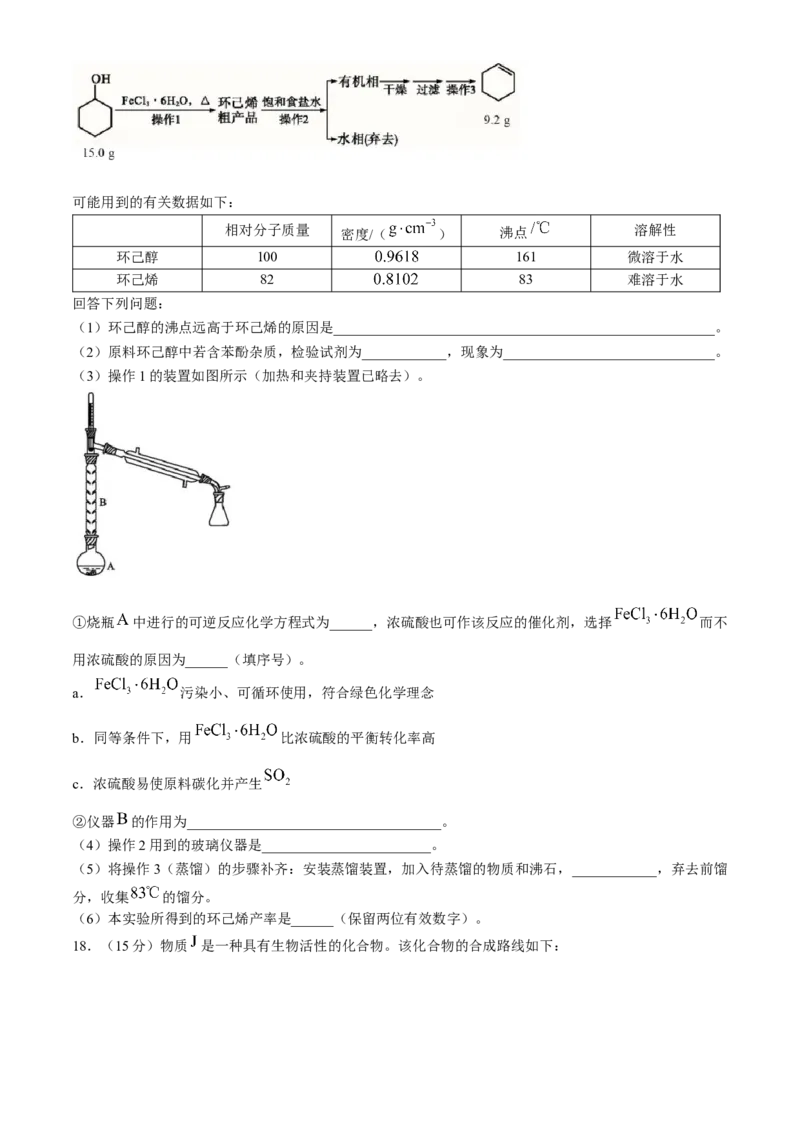
15.晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图 1),进行镁离子取
代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是( )
A.图1晶体密度为 B.图1中 原子的配位数为8C.图2表示的化学式为 D. 取代产生的空位有利于 传导
二、非选择题,本题共4小题,共55分。
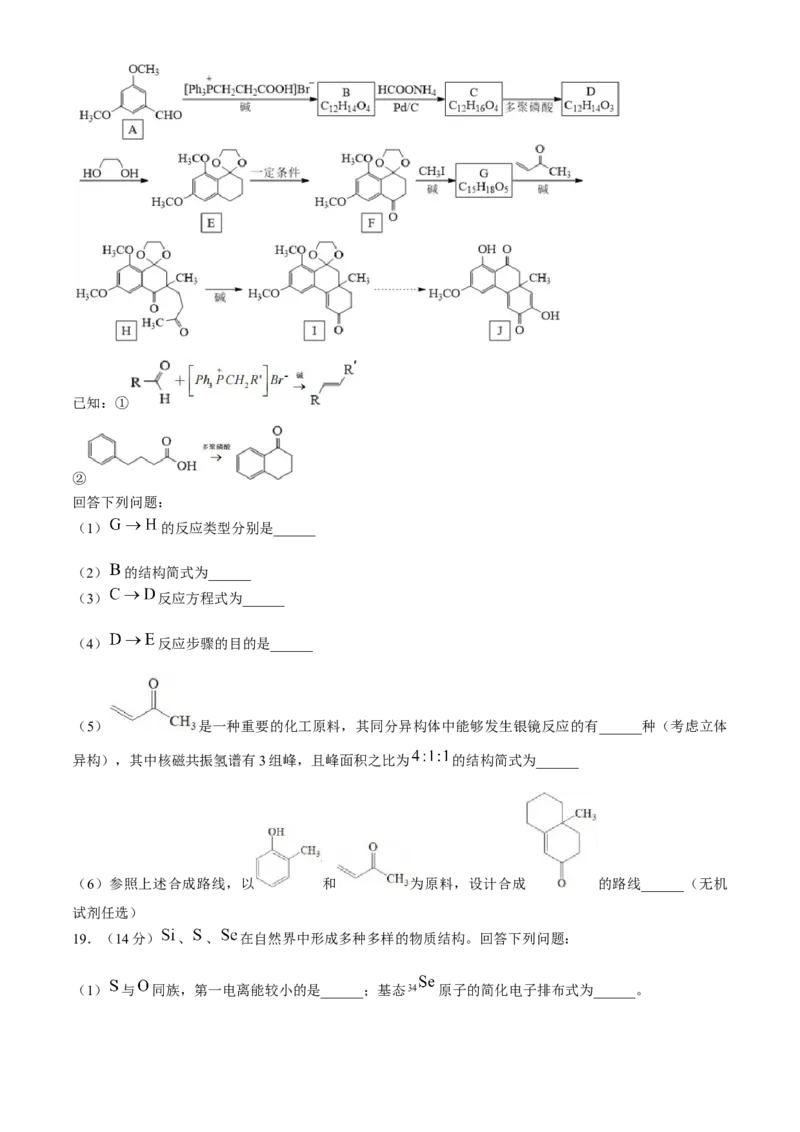
16.(10分)苯基环丁烯酮( )是一种十分活泼的反应物,可利用它的开环
反应合成一系列多官能团化合物。近期我国科学家报道用 与醛或酮发生 环加成反应,合成
了具有生物活性的多官能团化合物( ),部分合成路线如下:
已知如下信息:
回答下列问题:
(1) 的化学名称是______
(2) 的结构简式为______
(3)由 生成 所用的试剂和反应条件为______
(4)写出化合物 中含氧官能团的名称______; 中手性碳(注:连有四个不同的原子或基团的碳)的
个数为______
(5)对于 ,选用不同的取代基 ,在催化剂作用下与 发生的 反应进行深入研究,
对产率的影响见下表:
产率/% 91 80 63
请找出规律,并解释原因__________________________________________________________________
17.(16分)环己烯是重要的化工原料。其实验室制备流程如下:可能用到的有关数据如下:
相对分子质量 密度/( ) 沸点 溶解性
环己醇 100 161 微溶于水
环己烯 82 83 难溶于水
回答下列问题:
(1)环己醇的沸点远高于环己烯的原因是______________________________________________________。
(2)原料环己醇中若含苯酚杂质,检验试剂为____________,现象为______________________________。
(3)操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶 中进行的可逆反应化学方程式为______,浓硫酸也可作该反应的催化剂,选择 而不
用浓硫酸的原因为______(填序号)。
a. 污染小、可循环使用,符合绿色化学理念
b.同等条件下,用 比浓硫酸的平衡转化率高
c.浓硫酸易使原料碳化并产生
②仪器 的作用为____________________________________。
(4)操作2用到的玻璃仪器是________________________。
(5)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,____________,弃去前馏
分,收集 的馏分。
(6)本实验所得到的环己烯产率是______(保留两位有效数字)。
18.(15分)物质 是一种具有生物活性的化合物。该化合物的合成路线如下:已知:①
②
回答下列问题:
(1) 的反应类型分别是______
(2) 的结构简式为______
(3) 反应方程式为______
(4) 反应步骤的目的是______
(5) 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有______种(考虑立体
异构),其中核磁共振氢谱有3组峰,且峰面积之比为 的结构简式为______
(6)参照上述合成路线,以 和 为原料,设计合成 的路线______(无机
试剂任选)
19.(14分) 、 、 在自然界中形成多种多样的物质结构。回答下列问题:
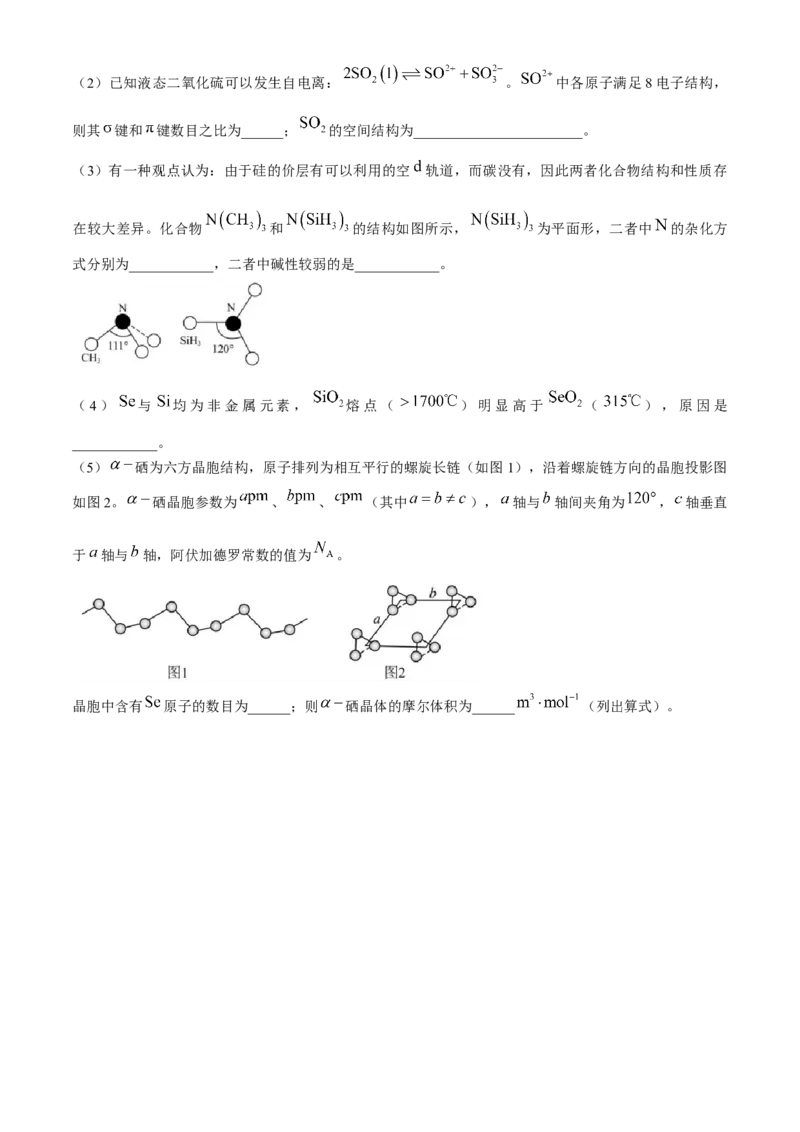
(1) 与 同族,第一电离能较小的是______;基态 原子的简化电子排布式为______。(2)已知液态二氧化硫可以发生自电离: 。 中各原子满足8电子结构,
则其 键和 键数目之比为______; 的空间结构为________________________。
(3)有一种观点认为:由于硅的价层有可以利用的空 轨道,而碳没有,因此两者化合物结构和性质存
在较大差异。化合物 和 的结构如图所示, 为平面形,二者中 的杂化方
式分别为____________,二者中碱性较弱的是____________。
(4) 与 均为非金属元素, 熔点( )明显高于 ( ),原因是
____________。
(5) 硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图
如图2。 硒晶胞参数为 、 、 (其中 ), 轴与 轴间夹角为 , 轴垂直
于 轴与 轴,阿伏加德罗常数的值为 。
晶胞中含有 原子的数目为______;则 硒晶体的摩尔体积为______ (列出算式)。武汉外国语学校 2023-2024 学年度下学期期末考试
高二化学参考答案
1 2 3 4 5 6 7 8 9 10
B C A B C A D B A D
11 12 13 14 15
D C C B B
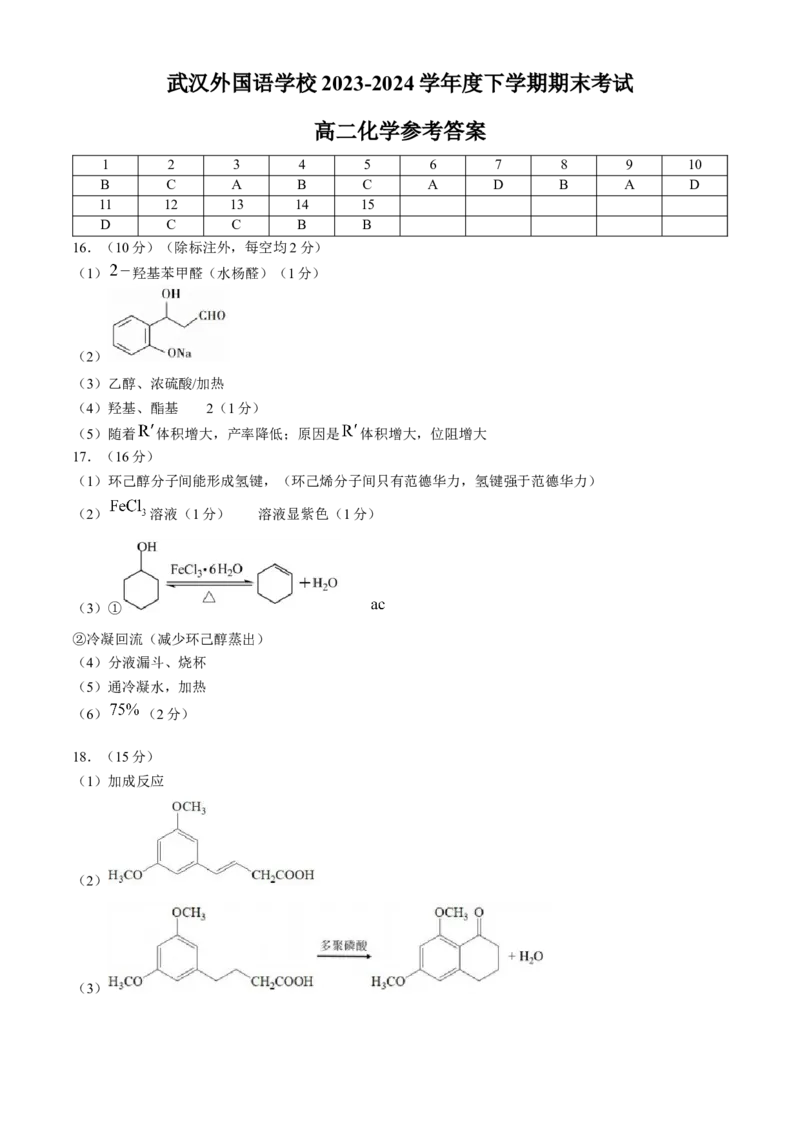
16.(10分)(除标注外,每空均2分)
(1) 羟基苯甲醛(水杨醛)(1分)
(2)
(3)乙醇、浓硫酸/加热
(4)羟基、酯基 2(1分)
(5)随着 体积增大,产率降低;原因是 体积增大,位阻增大
17.(16分)
(1)环己醇分子间能形成氢键,(环己烯分子间只有范德华力,氢键强于范德华力)
(2) 溶液(1分) 溶液显紫色(1分)
(3)①
②冷凝回流(减少环己醇蒸出)
(4)分液漏斗、烧杯
(5)通冷凝水,加热
(6) (2分)
18.(15分)
(1)加成反应
(2)
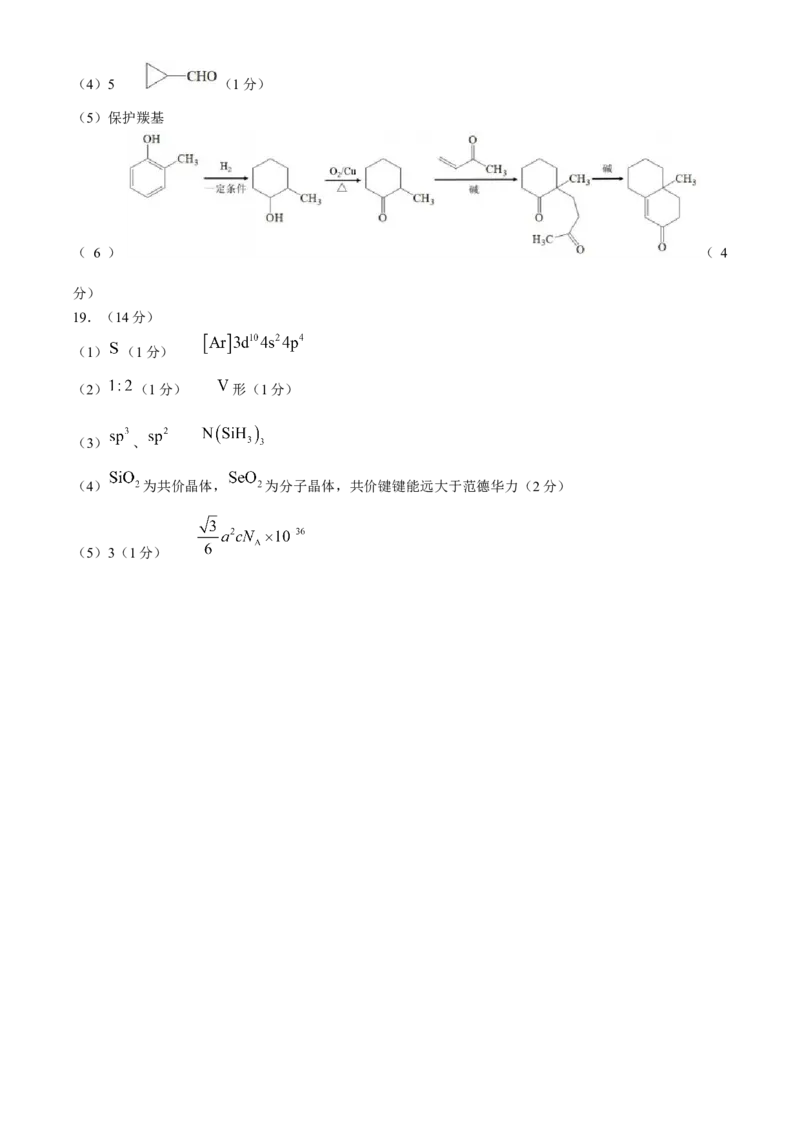
(3)(4)5 (1分)
(5)保护羰基
( 6 ) ( 4
分)
19.(14分)
(1) (1分)
(2) (1分) 形(1分)
(3) 、
(4) 为共价晶体, 为分子晶体,共价键键能远大于范德华力(2分)
(5)3(1分)