绝密★启用前
望城二中高二期中考试化学试卷
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,用橡皮擦干
净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
3.考试结束后,本试卷和答题卡一并交回。
第I卷(选择题)
一、单选题:本大题共14小题,共42分。
1.已知反应:①101kPa时, 2C(s)+O (g)=2CO(g) ΔH=−221kJ/mol ②稀溶液中,
2
H+ (aq)+OH− (aq)=H O(l)ΔH=−57.3kJ/mol 。下列结论正确的是( )
2
A. 碳的燃烧热大于110.5kJ/mol
B. ①的反应热为221kJ/mol
C. 稀硫酸与稀NaOH溶液反应的中和热为114.6kJ/mol
D. 稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
2.对下列实验的描述不正确的是 ( )
第 页,共 页
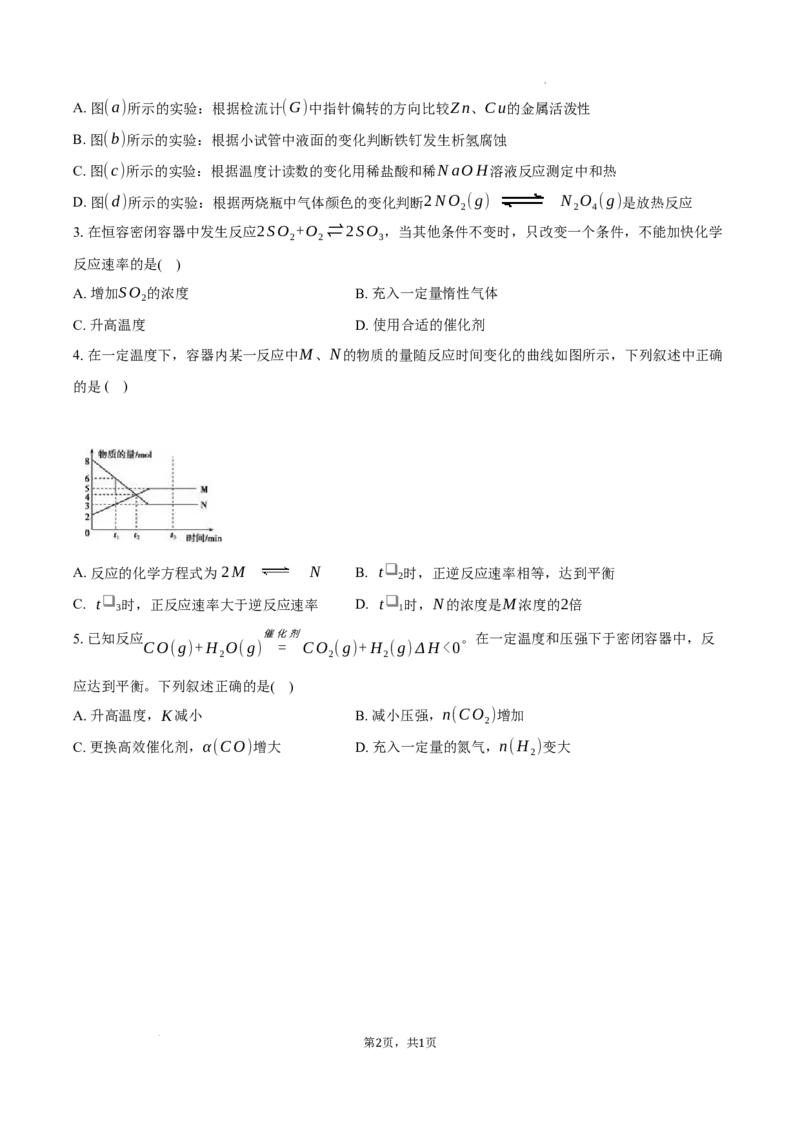
学科网(北京)股份有限公司 1 1A. 图(a)所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性
B. 图(b)所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀
C. 图(c)所示的实验:根据温度计读数的变化用稀盐酸和稀NaOH溶液反应测定中和热
D. 图(d)所示的实验:根据两烧瓶中气体颜色的变化判断2NO (g) N O (g)是放热反应
2 2 4
3.在恒容密闭容器中发生反应2SO +O ⇌2SO ,当其他条件不变时,只改变一个条件,不能加快化学
2 2 3
反应速率的是( )
A. 增加SO 的浓度 B. 充入一定量惰性气体
2
C. 升高温度 D. 使用合适的催化剂
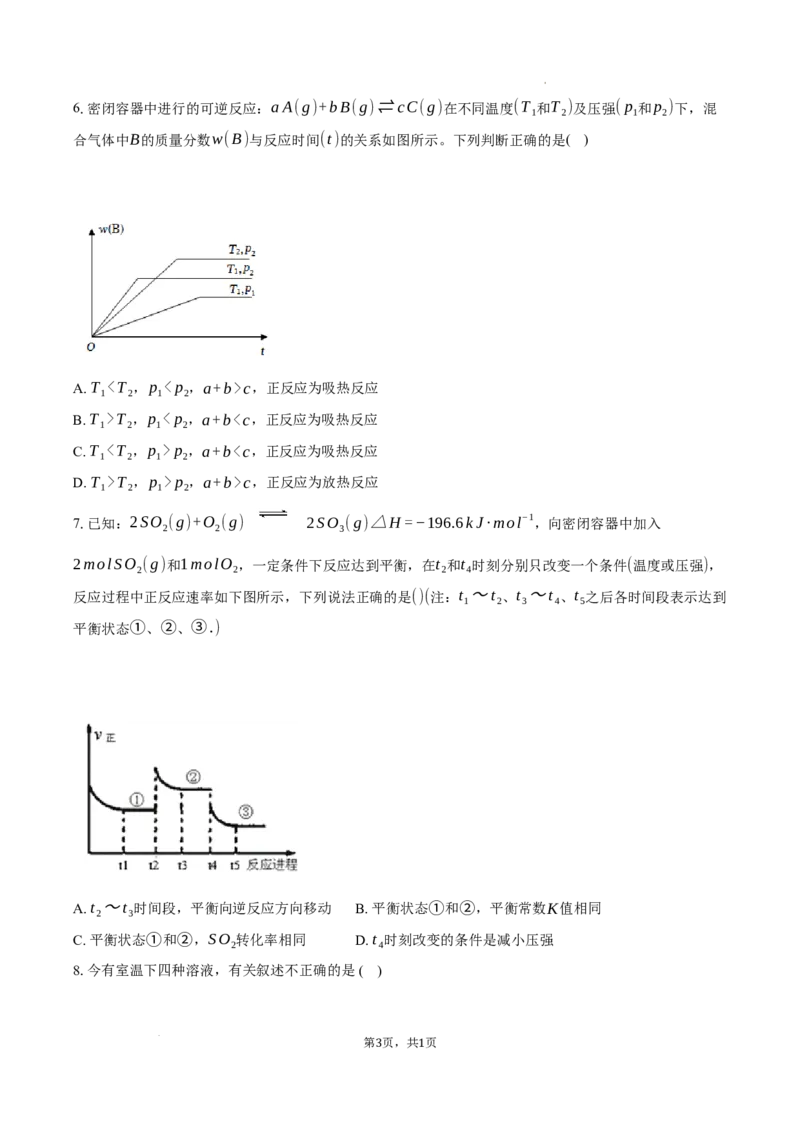
4.在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列叙述中正确
的是 ( )
A. 反应的化学方程式为 2M N B. t❑ 时,正逆反应速率相等,达到平衡
2
C. t❑ 时,正反应速率大于逆反应速率 D. t❑ 时,N的浓度是M浓度的2倍
3 1
5.已知反应 催化剂 。在一定温度和压强下于密闭容器中,反
CO(g)+H O(g) = CO (g)+H (g)ΔH<0
2 2 2
应达到平衡。下列叙述正确的是( )
A. 升高温度,K减小 B. 减小压强,n(CO )增加
2
C. 更换高效催化剂,α(CO)增大 D. 充入一定量的氮气,n(H )变大
2
第 页,共 页
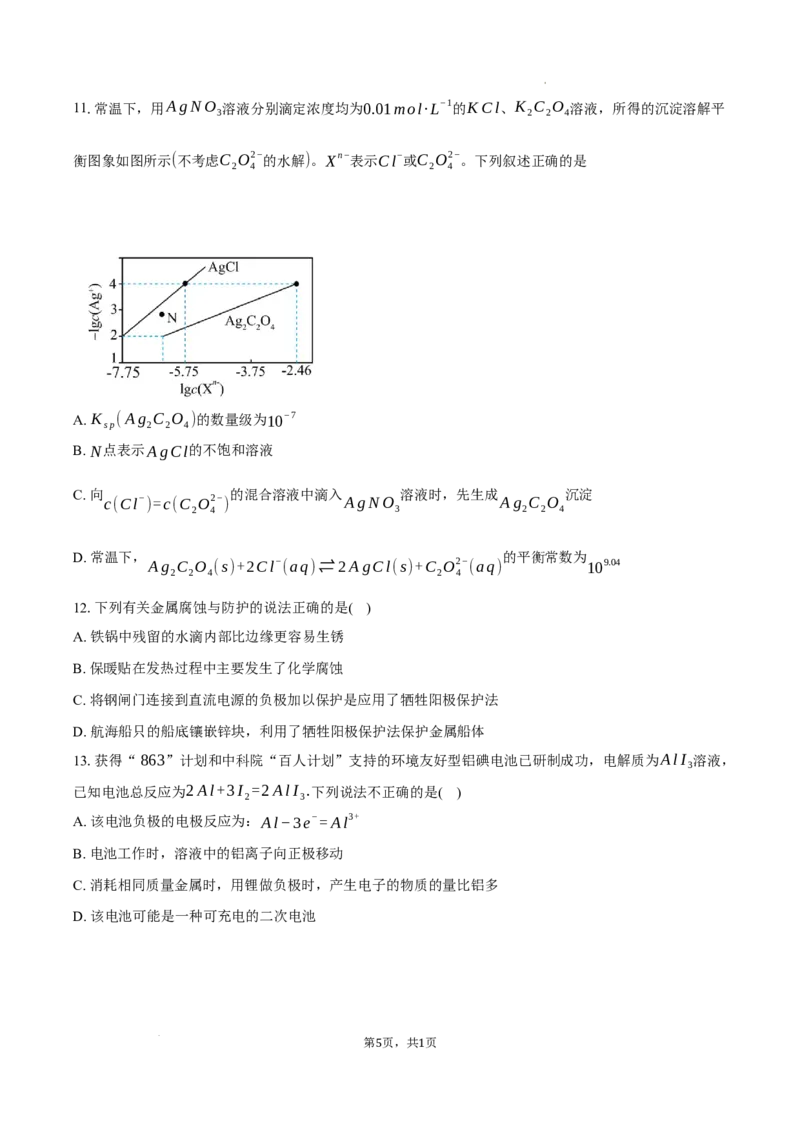
学科网(北京)股份有限公司 2 16.密闭容器中进行的可逆反应:aA(g)+bB(g)⇌cC(g)在不同温度(T 和T )及压强(p 和p )下,混
1 2 1 2
合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是( )
A. T
c,正反应为吸热反应
1 2 1 2
B. T >T ,p p ,a+bT ,p >p ,a+b>c,正反应为放热反应
1 2 1 2
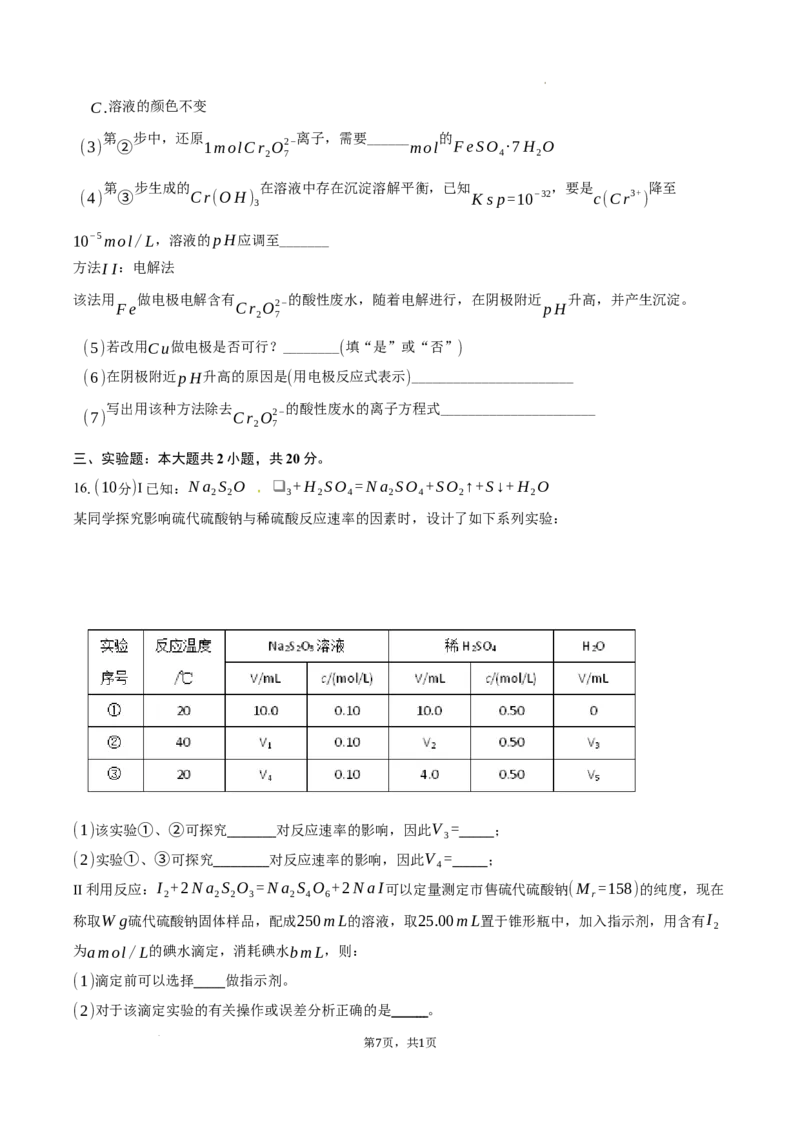
7.已知:2SO (g)+O (g) 2SO (g)△H=−196.6kJ·mol−1 ,向密闭容器中加入
2 2 3
2molSO (g)和1molO ,一定条件下反应达到平衡,在t 和t 时刻分别只改变一个条件(温度或压强),
2 2 2 4
反应过程中正反应速率如下图所示,下列说法正确的是()(注:t ~t 、t ~t 、t 之后各时间段表示达到
1 2 3 4 5
平衡状态①、②、③.)
A. t ~t 时间段,平衡向逆反应方向移动 B. 平衡状态①和②,平衡常数K值相同
2 3
C. 平衡状态①和②,SO 转化率相同 D. t 时刻改变的条件是减小压强
2 4
8.今有室温下四种溶液,有关叙述不正确的是 ( )
第 页,共 页
学科网(北京)股份有限公司 3 1① ② ③ ④
pH 11 11 3 3
溶液 氨水 氢氧化钠溶液 醋酸 盐酸
A. ①.②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B. 分别加入水稀释10倍,四种溶液的pH:①>②>④>③
C. ①.④两溶液等体积混合,所得溶液中 c(Cl−)=c(N H4+)>c(OH−)=c(H+)
D. V L④与 V L②溶液混合后,若混合后溶 液pH=7,则 V = V
a b a b
9.某化工厂制备净水剂硫酸铁铵晶体[N H Fe(SO ) ·6H O]的一种方案如图:
4 4 2 2
下列说法不正确的是 ( )
A. 滤渣A的主要成分是CaSO
4
B. 相同条件下,N H Fe(SO ) ·6H O净水能力比FeCl 强
4 4 2 2 3
C. “合成”反应要控制温度,温度过高,产率会降低
D. “系列操作”包括蒸发浓缩、降温结晶、过滤、洗涤、干燥等
10.常温下将稀NaOH溶液与稀CH COOH溶液混合,不可能出现的结果是( )
3
A. ,且
pH>7 c(OH− )>c(Na+ )>c(H+ )>c(CH COO− )
3
B. ,且
pH>7 c(Na+ )+c(H+ )=c(OH− )+c(CH COO− )
3
C. ,且
pH<7 c(CH COO− )>c(H+ )>c(Na+ )>c(OH− )
3
D. ,且
pH=7 c(CH COO− )=c(Na+ )>c(H+ )=c(OH− )
3
第 页,共 页
学科网(北京)股份有限公司 4 111.常温下,用AgNO 溶液分别滴定浓度均为0.01mol·L−1的KCl、K C O 溶液,所得的沉淀溶解平
3 2 2 4
衡图象如图所示(不考虑C O2− 的水解)。Xn−表示Cl−或C O2− 。下列叙述正确的是
2 4 2 4
A. K (Ag C O )的数量级为10−7
sp 2 2 4
B. N点表示AgCl的不饱和溶液
C. 向 的混合溶液中滴入 溶液时,先生成 沉淀
c(Cl− )=c(C O2− ) AgNO Ag C O
2 4 3 2 2 4
D. 常温下, 的平衡常数为
Ag C O (s)+2Cl− (aq)⇌2AgCl(s)+C O2− (aq) 109.04
2 2 4 2 4
12.下列有关金属腐蚀与防护的说法正确的是( )
A. 铁锅中残留的水滴内部比边缘更容易生锈
B. 保暖贴在发热过程中主要发生了化学腐蚀
C. 将钢闸门连接到直流电源的负极加以保护是应用了牺牲阳极保护法
D. 航海船只的船底镶嵌锌块,利用了牺牲阳极保护法保护金属船体
13.获得“ 863”计划和中科院“百人计划”支持的环境友好型铝碘电池已研制成功,电解质为AlI 溶液,
3
已知电池总反应为2Al+3I =2AlI .下列说法不正确的是( )
2 3
A. 该电池负极的电极反应为:Al−3e−=Al3+
B. 电池工作时,溶液中的铝离子向正极移动
C. 消耗相同质量金属时,用锂做负极时,产生电子的物质的量比铝多
D. 该电池可能是一种可充电的二次电池
第 页,共 页
学科网(北京)股份有限公司 5 114.以惰性电极电解Cu SO 和NaCl的混合溶液,两电极上产生的气体(标准状况下测定)体积如下图
4
所示,下列有关说法正确的是 ( )
A. a表示阴极上产生的气体,t 前产生的为Cl
1 2
B. 原溶液中CuSO 和NaCl物质的量之比为1:1
4
C. 若t 时溶液的体积为 1L,此时溶液的pH为13
2
D. 若原溶液体积为 ,则原溶液中 的物质的量浓度为
1L SO2− 0.2mol/L
4
第II卷(非选择题)
二、流程题:本大题共1小题,共8分。
15.工业废水中常含有一定量的 和 ,它们会对人类及生态系统产生很大的伤害,必须进行
Cr O2− CrO2−
2 7 4
处理。常用的处理方法有两种。
方法I:还原沉淀法
该法的工艺流程为: ,其中第 步加入 ,第 步加入 ,
CrO2−→Cr O2−→Cr3+→Cr(OH) ① H+ ② Fe2+
4 2 7 3
第 步加入 。第 步存在的平衡: 黄色 橙色
③ OH− ① 2CrO2− ( )+2H+ ⇋Cr O2− ( )+H O
4 2 7 2
(1)若上述平衡体系的pH=2,则溶液呈______色
(2)能说明第①步反应到达平衡状态的是______
和 浓度相同
A.Cr O2− CrO2−
2 7 4
B.2v(Cr O2− )=v(CrO2− )
2 7 4
第 页,共 页
学科网(北京)股份有限公司 6 1C.溶液的颜色不变
第 步中,还原 离子,需要______ 的
(3) ② 1molCr O2− mol FeSO ·7H O
2 7 4 2
第 步生成的 在溶液中存在沉淀溶解平衡,已知 ,要是 降至
(4) ③ Cr(OH) Ksp=10−32 c(Cr3+ )
3
10−5mol/L,溶液的pH应调至_______
方法I I:电解法
该法用 做电极电解含有 的酸性废水,随着电解进行,在阴极附近 升高,并产生沉淀。
Fe Cr O2− pH
2 7
(5)若改用Cu做电极是否可行?________(填“是”或“否”)
(6)在阴极附近pH升高的原因是(用电极反应式表示)_______________________
写出用该种方法除去 的酸性废水的离子方程式______________________
(7) Cr O2−
2 7
三、实验题:本大题共2小题,共20分。
16.(10分)Ⅰ 已知:Na S O ❑ +H SO =Na SO +SO ↑+S↓+H O
2 2 3 2 4 2 4 2 2
某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)该实验①、②可探究 对反应速率的影响,因此V = ;
3
(2)实验①、③可探究 对反应速率的影响,因此V = ;
4
Ⅱ 利用反应:I +2Na S O =Na S O +2NaI可以定量测定市售硫代硫酸钠(M =158)的纯度,现在
2 2 2 3 2 4 6 r
称取W g硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用含有I
2
为amol/L的碘水滴定,消耗碘水bmL,则:
(1)滴定前可以选择 做指示剂。
(2)对于该滴定实验的有关操作或误差分析正确的是 。
第 页,共 页
学科网(北京)股份有限公司 7 1A. 滴定前,应对滴定管、锥形瓶进行润洗操作
B. 滴定过程中,标准液滴到锥形瓶外,会使所测结果偏大
C. 滴定管在滴定开始时尖嘴有气泡,滴定完成后气泡消失,则所测得的纯度将会偏小
D. 滴定前仰视读数而滴定结束时俯视读数,则所测得的纯度将会偏小
(3)样品中硫代硫酸钠纯度的表达式为 。
17.(10分)工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过电解生成
Fe(OH) 沉淀。Fe(OH) 有吸附性,可吸附污物而沉积下来,具有净化水的作用。某科研小组用 此法
3 3
处理污水,设计如下所示装置示意图。
(1)实验时若污水中离子浓度较小,导电能力较差;此时,最好应向污水中加入适量的____________。
A.NaOH B.CaCO C.K SO D.CH CH OH
3 2 4 3 2
(2)电解池阳极发生了两个电极反应:其中一个反应式为 ,另一个反应生成了一种无色气体,其反
应式为:4OH−−4e−=O ↑+2H O。
2 2
(3)该燃料电池是以熔融碳酸盐为电解质,CH 为燃料,空气为氧化剂,稀土金属材料做电极。已知负极
4
的电极反应是CH +4CO2−−8e−=5CO +2H O,则正极的电极反应是 。为了使该燃料电
4 3 2 2
池长时间稳定运行,电池的电解质组成应保持稳定,此电池工作时必须有部分A物质参加循环,则A物质
的化学式是 。
(4)实验中,若在阴极产生了11.2L(标准状况,下同)气体,则熔融盐燃料电池消耗CH L。
4
四、简答题:本大题共1小题,共8分。
第 页,共 页
学科网(北京)股份有限公司 8 118.(10分)已知体积为 2L的恒容密闭容器中发生反应:2SO (g)+O (g) 2SO (g),请根据化
2 2 3
学反应的有关原理回答下列问题:
(1)一定条件下,充入2molSO (g)和2molO (g),20s后,测得SO 的体积百分含量为12.5%,则用
2 2 2
SO 表示该反应在这20s内的反应速率为 mol/(L·s)。
2
(2)该反应的平衡常数(K)表达式为 。
(3)如图表示该反应的速率(v)随时间(t)的变化的关系:据图分析:你认为t❑ 时改变的外界条件可能是
3
________。
(4)如图,P是可自由平行滑动的活塞,在相同温度时,向A容器中充入4molSO (g),关闭K,向B容
3
器中充入2molSO (g),两容器内分别充分发生反应。已知起始时容器A和B的体积均为aL。试回答:
3
①反应达到平衡时容器B的体积为 1.2 aL,容器B中SO 转化率为________。
3
②若打开K,一段时间后重新达到平衡,容器B的体积为________L(连通管中气体体积忽略不计,且不考
虑温度的影响)。
第 页,共 页
学科网(北京)股份有限公司 9 1