文档内容
常州市二○○八年初中毕业、升学统一考试
化 学 试 题
说明:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷1至2页,第Ⅱ卷3
至8页。考试结束,将本试卷和答题卡一并交回。
2.试卷满分为100分。考试时间为100分钟。考试时不得使用计算器。
3.可能用到的相对原子质量:Ar(H)=1 Ar(C)=12 Ar(O)=16 Ar(N)=14 Ar(Na)=23
第Ⅰ卷(选择题 共40分)
注意事项:
1.答第Ⅰ卷前,考生务必在答题卡上将自己的姓名、考试证号用钢笔或圆珠笔填写清楚,并
用2B铅笔将考试证号、考试科目相对应的方框涂黑。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其他答案,答在试题卷上无效。
一、选择题(本题包括20小题,共40分。每小题只有一个选项符合题意)
1.下列物质中属于钾肥的是
A.NH NO B.KSO C.CO(NH) D.Ca (PO )
4 3 2 4 2 2 3 4 2
2.关于仪器的用途,下列叙述中不正确的是
A.试管可以用作反应容器 B.托盘天平可以称量物质质量
C.量筒可以用作稀释浓硫酸的容器 D.玻璃棒可以用来搅拌液体
3.下列各组物质中,前者属于单质、后者属于混合物的是
A.氮气 蒸馏水 B.生铁 稀盐酸 C.氢气 大理石 D.二氧化碳 空
气
4.下列物质的名称、俗名与化学式完全对应的是
A.氯化钠 食盐 NaCl B.碳酸氢钠 纯碱 NaHCO
2 3
C.氢氧化钙 熟石灰 CaO D.氢氧化钠 火碱 NaOH
5.钇铁石榴石(YFe O )可用作雷达微波过滤器里使用的铁氧磁性体,其中钇(Y)显+3价,
3 5 12
则Fe的化合价为
A.0 B.+2 C.+3 D.+6
6.等质量的下列物质中,蛋白质含量最高的是
A.鱼 B.大米 C.青菜 D.苹果
7.下列仪器一般需经过磨砂处理的是
A.试管 B.烧杯 C.集气瓶 D.量筒
8.常用的消毒剂有氯气(Cl)、二氧化氯(ClO )、漂白粉[Ca(ClO) ]等,这三种物质都含
2 2 2
A.原子团 B.氯分子 C.氯离子 D.氯元素
9.下列反应中属于中和反应的是
A.NaCO+2HCl== 2NaCl+HO+CO↑ B.2NaOH+HSO == Na SO +2HO
2 3 2 2 2 4 2 4 2
C.SO+2NaOH== Na SO+HO D.Zn+CuSO===ZnSO+Cu
2 2 3 2 4 4
10.铁生锈的条件
A.仅需要氧气 B.仅需要水 C.氧气或水 D.氧气和水
11.青蒿素(C H O)是我国首创的新型抗疟疾药,下列关于青蒿素的叙述错误的是
15 22 5
A.属于无机物 B.含有三种元素
C.相对分子质量为282 D.碳元素的质量分数约为63.8%
12.下列关于溶液的叙述,正确的是
A.无色透明的液体一定是溶液 B.溶液中各部分的性质均相同
C.植物油分散到水中可以形成溶液 D.溶液中只能有一种溶质
13.下列叙述中,正确的是
A.原子的质量主要集中在原子核上
B.构成物质的微粒只有分子和原子
C.气体易被压缩,说明构成气体的分子在不断运动
第1页,共9页D.物质在不同条件下的三态变化主要是由于分子的大小发生了变化
14.“节能减排,保护环境,建设生态文明”成为确保我国可持续性发展的新的关键词。下列
活动或举措与该主题无关的是
A.我市开展的“捐献一张废纸,献出一片爱心”活动
B.我市对雨水、污水管道实施规范化整治,做到清污分流
C.2007年6月我市举办的“珍爱生命 拒绝毒品”大型签名活动
D.2008年6月1日起,我国全面实施“限塑令”
15.对比实验是运用比较的方法来揭示事物的性质或变化规律的一种实验方法。课本中设计
的下列实验不属于对比实验的是
A.铁钉锈蚀实验 B.几种纤维的性质实验
C.粉尘爆炸实验 D.探究影响物质溶解性因素的实验
16.下列各种物质间的转换通过一步反应不能实现的是
A.P→P O B.CaCO →CO C.Fe→FeCl D.CuO→CuSO
2 5 3 2 4
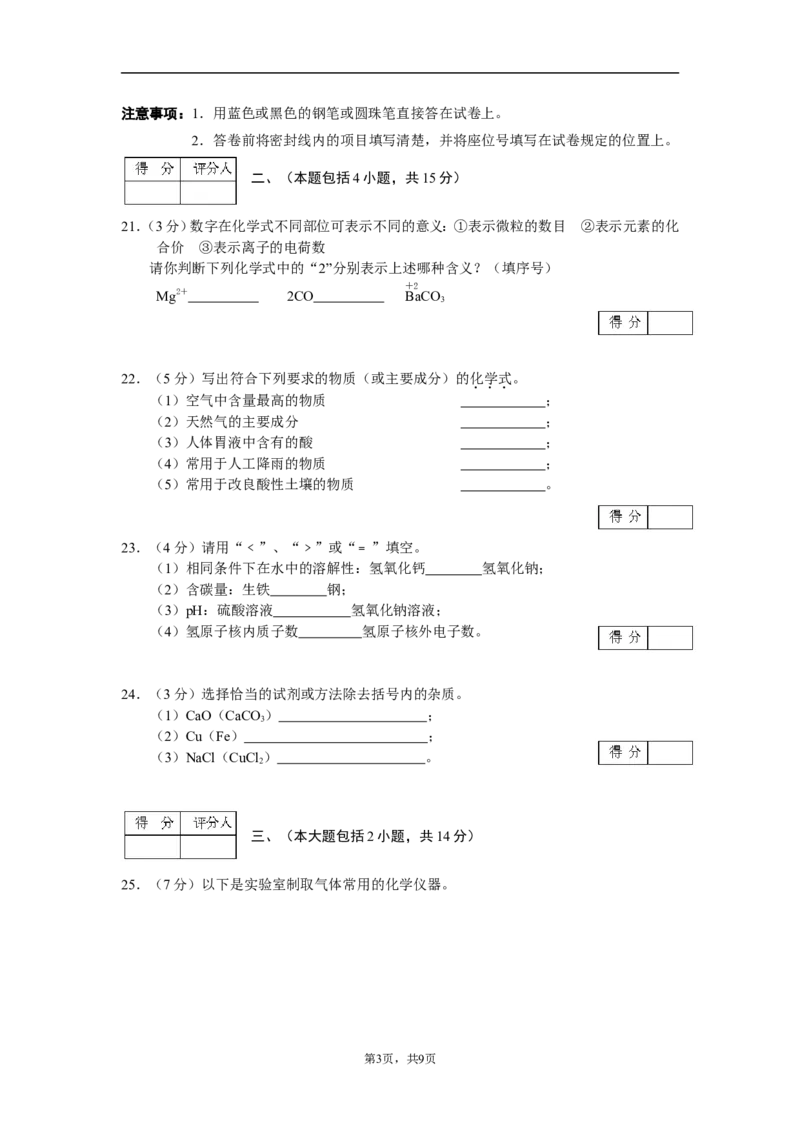
17.将一大烧杯倒扣在培养皿上,培养皿上所放物质如右
图所示。下列对有关实验现象的描述肯定不正确的是
A.Ⅰ处试液变蓝
B.Ⅱ处溶液变浑浊
C.Ⅲ处溶液颜色逐渐变浅
D.Ⅳ处试纸变红
18.“绿色化学”能实现零排放(即反应物中的原子利用率达到100%)。CO和H 在一定条
2
件下按照不同的比例可以合成不同的有机化工原料。根据零排放的要求,以CO和H 合
2
成的有机物不可能是
A.甲醇(CHO) B.乙醇(C HO) C.甲醛(CHO) D.乙酸(C HO)
4 2 6 2 2 4 2
19.图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间
的关系符合图3所示关系的是
X Y Z
A. 溶质 溶剂 溶液
B. 悬浊液 乳浊液 溶液
C. 氧化物 酸碱盐 化合物
D. 饱和溶液 不饱和溶液 浓溶液
20.右图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现
M、N间的相互转化的是(A从溶液中析出时不带结晶水)
A.从N→M:先向N中加入适量固体A再降温
B.从N→M:先将N降温再加入适量固体A
C.从M→N:先将M降温再将其升温
D.从M→N:先将M升温再将其蒸发掉部分水
常州市二○○八年初中毕业、升学统一考试
第Ⅱ卷总分 核总分
化 学 试 题
结分人 核分人
第Ⅱ卷(非选择题 共60分)
题 号 二 三 四 五 六
得 分
第2页,共9页注意事项:1.用蓝色或黑色的钢笔或圆珠笔直接答在试卷上。
2.答卷前将密封线内的项目填写清楚,并将座位号填写在试卷规定的位置上。
二、(本题包括4小题,共15分)
21.(3分)数字在化学式不同部位可表示不同的意义:①表示微粒的数目 ②表示元素的化
合价 ③表示离子的电荷数
请你判断下列化学式中的“2”分别表示上述哪种含义?(填序号)
+2
Mg2+ 2CO BaCO
3
22.(5分)写出符合下列要求的物质(或主要成分)的化学式。
(1)空气中含量最高的物质 ;
(2)天然气的主要成分 ;
(3)人体胃液中含有的酸 ;
(4)常用于人工降雨的物质 ;
(5)常用于改良酸性土壤的物质 。
23.(4分)请用“﹤”、“﹥”或“﹦”填空。
(1)相同条件下在水中的溶解性:氢氧化钙 氢氧化钠;
(2)含碳量:生铁 钢;
(3)pH:硫酸溶液 氢氧化钠溶液;
(4)氢原子核内质子数 氢原子核外电子数。
24.(3分)选择恰当的试剂或方法除去括号内的杂质。
(1)CaO(CaCO ) ;
3
(2)Cu(Fe) ;
(3)NaCl(CuCl ) 。
2
三、(本大题包括2小题,共14分)
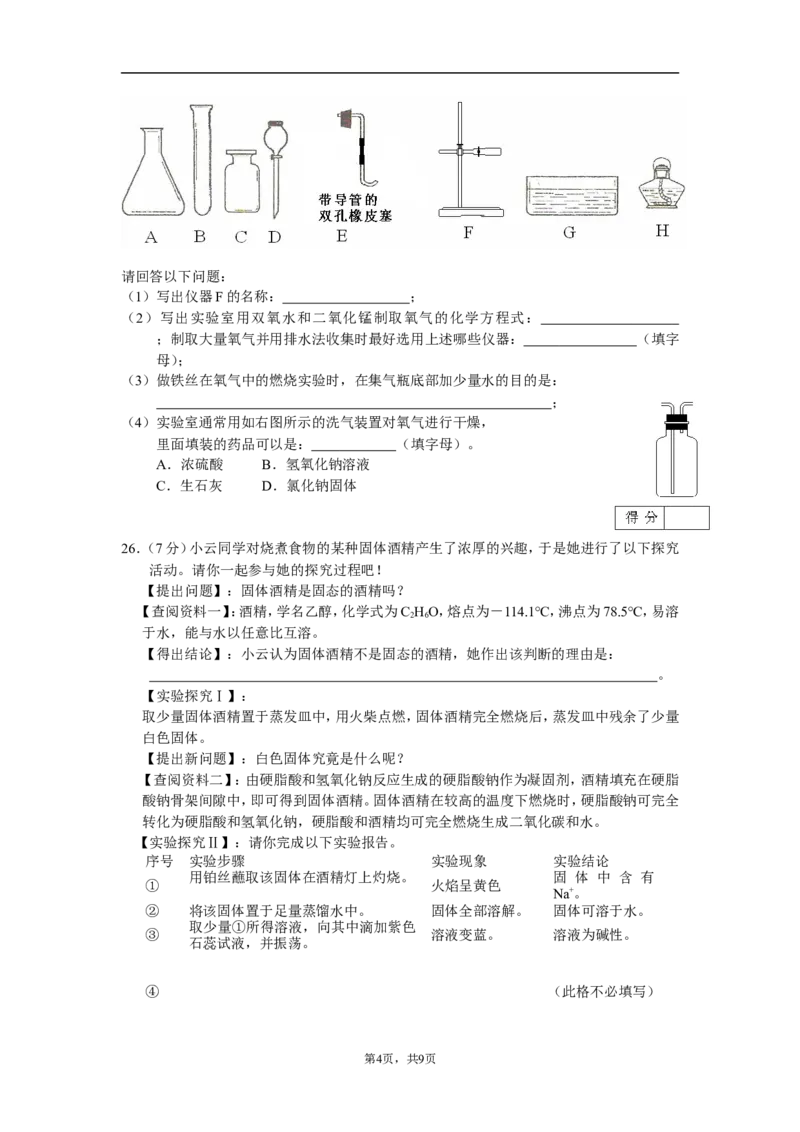
25.(7分)以下是实验室制取气体常用的化学仪器。
第3页,共9页请回答以下问题:
(1)写出仪器F的名称: ;
(2)写出实验室用双氧水和二氧化锰制取氧气的化学方程式:
;制取大量氧气并用排水法收集时最好选用上述哪些仪器: (填字
母);
(3)做铁丝在氧气中的燃烧实验时,在集气瓶底部加少量水的目的是:
;
(4)实验室通常用如右图所示的洗气装置对氧气进行干燥,
里面填装的药品可以是: (填字母)。
A.浓硫酸 B.氢氧化钠溶液
C.生石灰 D.氯化钠固体
26.(7分)小云同学对烧煮食物的某种固体酒精产生了浓厚的兴趣,于是她进行了以下探究
活动。请你一起参与她的探究过程吧!
【提出问题】:固体酒精是固态的酒精吗?
【查阅资料一】:酒精,学名乙醇,化学式为C HO,熔点为-114.1℃,沸点为78.5℃,易溶
2 6
于水,能与水以任意比互溶。
【得出结论】:小云认为固体酒精不是固态的酒精,她作出该判断的理由是:
。
【实验探究Ⅰ】:
取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残余了少量
白色固体。
【提出新问题】:白色固体究竟是什么呢?
【查阅资料二】:由硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,酒精填充在硬脂
酸钠骨架间隙中,即可得到固体酒精。固体酒精在较高的温度下燃烧时,硬脂酸钠可完全
转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水。
【实验探究Ⅱ】:请你完成以下实验报告。
序号 实验步骤 实验现象 实验结论
用铂丝蘸取该固体在酒精灯上灼烧。 固 体 中 含 有
① 火焰呈黄色
Na+。
② 将该固体置于足量蒸馏水中。 固体全部溶解。 固体可溶于水。
取少量①所得溶液,向其中滴加紫色
③ 溶液变蓝。 溶液为碱性。
石蕊试液,并振荡。
④ (此格不必填写)
第4页,共9页实验结论:小云认为该白色固体为 。
【联想与解释】小云联想到老师用玻璃导管将纯净的氢气导出并点燃时,燃烧火焰为黄色,其
原因可能是: 。
四、(本题包括2小题,共14分)
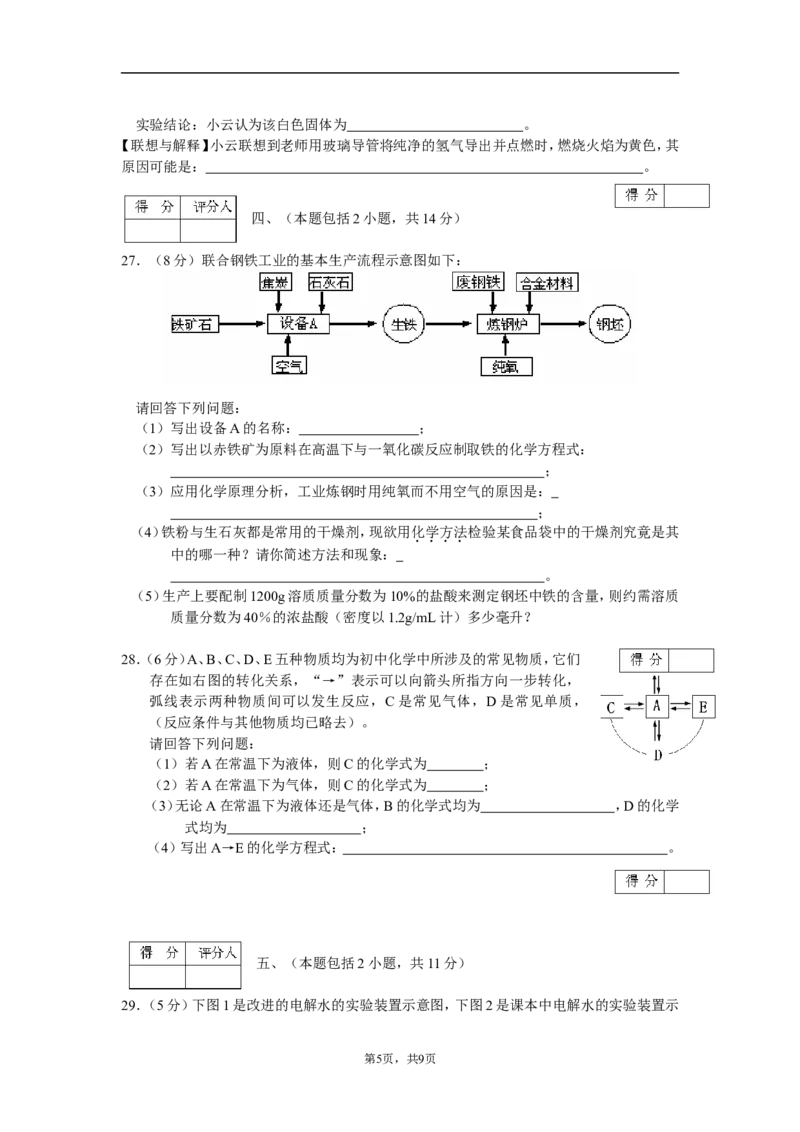
27.(8分)联合钢铁工业的基本生产流程示意图如下:
请回答下列问题:
(1)写出设备A 的名称: ;
(2)写出以赤铁矿为原料在高温下与一氧化碳反应制取铁的化学方程式:
;
(3)应用化学原理分析,工业炼钢时用纯氧而不用空气的原因是:
;
(4)铁粉与生石灰都是常用的干燥剂,现欲用化学方法检验某食品袋中的干燥剂究竟是其
中的哪一种?请你简述方法和现象:
。
(5)生产上要配制1200g溶质质量分数为10%的盐酸来测定钢坯中铁的含量,则约需溶质
质量分数为40%的浓盐酸(密度以1.2g/mL计)多少毫升?
28.(6分)A、B、C、D、E五种物质均为初中化学中所涉及的常见物质,它们
存在如右图的转化关系,“→”表示可以向箭头所指方向一步转化,
弧线表示两种物质间可以发生反应,C是常见气体,D是常见单质,
(反应条件与其他物质均已略去)。
请回答下列问题:
(1)若A在常温下为液体,则C的化学式为 ;
(2)若A在常温下为气体,则C的化学式为 ;
(3)无论A在常温下为液体还是气体,B的化学式均为 ,D的化学
式均为 ;
(4)写出A→E的化学方程式: 。
五、(本题包括2小题,共11分)
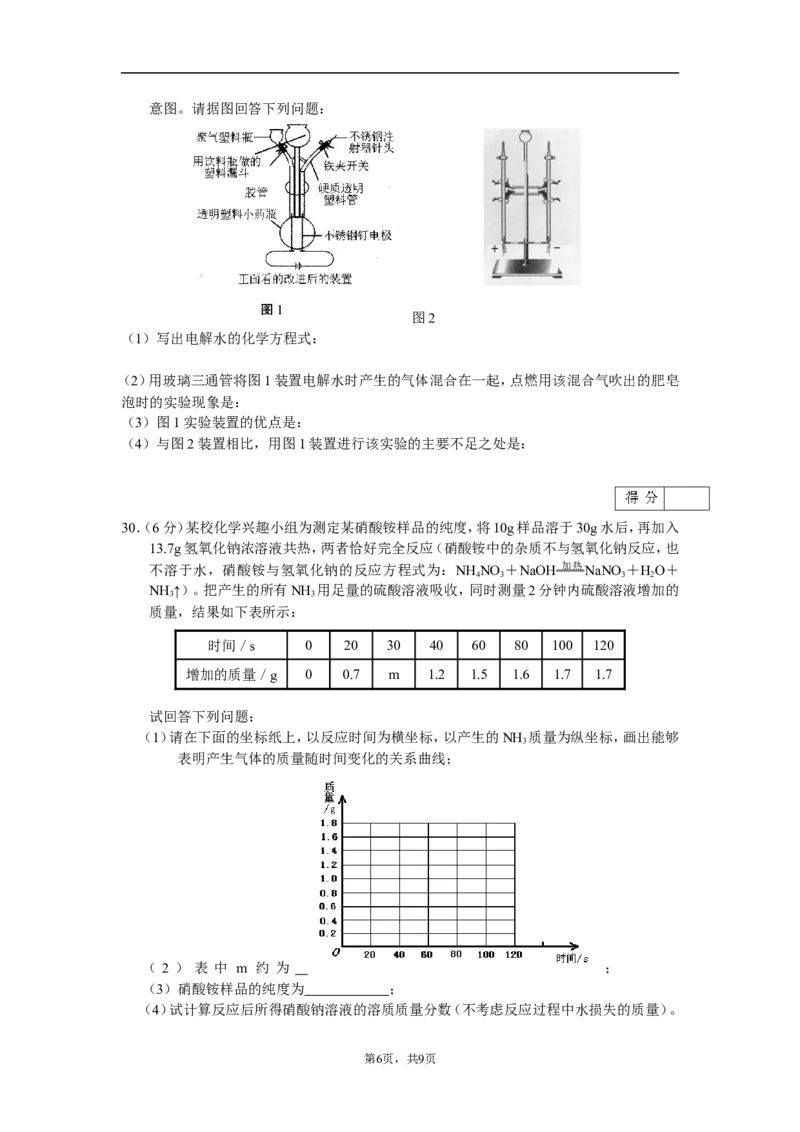
29.(5分)下图1是改进的电解水的实验装置示意图,下图2是课本中电解水的实验装置示
第5页,共9页意图。请据图回答下列问题:
图2
(1)写出电解水的化学方程式:
(2)用玻璃三通管将图1装置电解水时产生的气体混合在一起,点燃用该混合气吹出的肥皂
泡时的实验现象是:
(3)图1实验装置的优点是:
(4)与图2装置相比,用图1装置进行该实验的主要不足之处是:
30.(6分)某校化学兴趣小组为测定某硝酸铵样品的纯度,将10g样品溶于30g水后,再加入
13.7g氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不与氢氧化钠反应,也
不溶于水,硝酸铵与氢氧化钠的反应方程式为:NH NO +NaOH 加热 NaNO +HO+
4 3 3 2
NH ↑)。把产生的所有NH 用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的
3 3
质量,结果如下表所示:
时间/s 0 20 30 40 60 80 100 120
增加的质量/g 0 0.7 m 1.2 1.5 1.6 1.7 1.7
试回答下列问题:
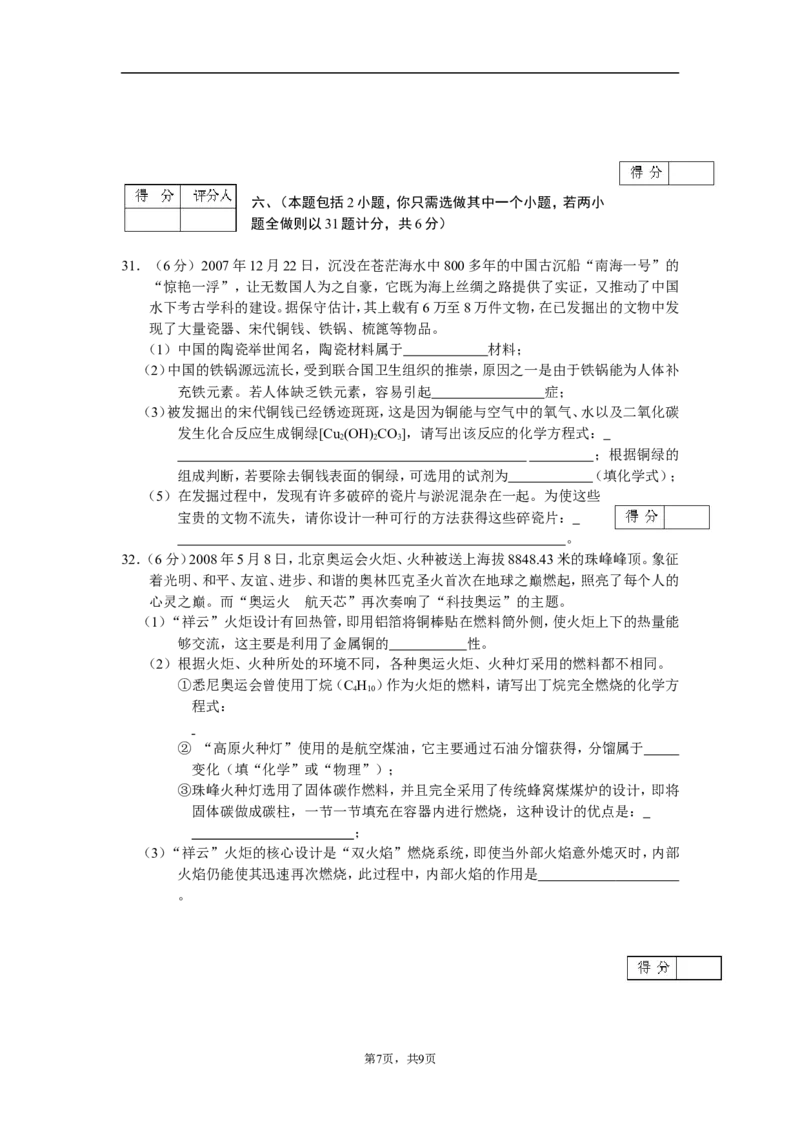
(1)请在下面的坐标纸上,以反应时间为横坐标,以产生的NH 质量为纵坐标,画出能够
3
表明产生气体的质量随时间变化的关系曲线;
( 2 ) 表 中 m 约 为 ;
(3)硝酸铵样品的纯度为 ;
(4)试计算反应后所得硝酸钠溶液的溶质质量分数(不考虑反应过程中水损失的质量)。
第6页,共9页六、(本题包括2小题,你只需选做其中一个小题,若两小
题全做则以31题计分,共6分)
31.(6分)2007年12月22日,沉没在苍茫海水中800多年的中国古沉船“南海一号”的
“惊艳一浮”,让无数国人为之自豪,它既为海上丝绸之路提供了实证,又推动了中国
水下考古学科的建设。据保守估计,其上载有6万至8万件文物,在已发掘出的文物中发
现了大量瓷器、宋代铜钱、铁锅、梳篦等物品。
(1)中国的陶瓷举世闻名,陶瓷材料属于 材料;
(2)中国的铁锅源远流长,受到联合国卫生组织的推崇,原因之一是由于铁锅能为人体补
充铁元素。若人体缺乏铁元素,容易引起 症;
(3)被发掘出的宋代铜钱已经锈迹斑斑,这是因为铜能与空气中的氧气、水以及二氧化碳
发生化合反应生成铜绿[Cu (OH) CO],请写出该反应的化学方程式:
2 2 3
;根据铜绿的
组成判断,若要除去铜钱表面的铜绿,可选用的试剂为 (填化学式);
(5)在发掘过程中,发现有许多破碎的瓷片与淤泥混杂在一起。为使这些
宝贵的文物不流失,请你设计一种可行的方法获得这些碎瓷片:
。
32.(6分)2008年5月8日,北京奥运会火炬、火种被送上海拔8848.43米的珠峰峰顶。象征
着光明、和平、友谊、进步、和谐的奥林匹克圣火首次在地球之巅燃起,照亮了每个人的
心灵之巅。而“奥运火 航天芯”再次奏响了“科技奥运”的主题。
(1)“祥云”火炬设计有回热管,即用铝箔将铜棒贴在燃料筒外侧,使火炬上下的热量能
够交流,这主要是利用了金属铜的 性。
(2)根据火炬、火种所处的环境不同,各种奥运火炬、火种灯采用的燃料都不相同。
①悉尼奥运会曾使用丁烷(C H )作为火炬的燃料,请写出丁烷完全燃烧的化学方
4 10
程式:
② “高原火种灯”使用的是航空煤油,它主要通过石油分馏获得,分馏属于
变化(填“化学”或“物理”);
③珠峰火种灯选用了固体碳作燃料,并且完全采用了传统蜂窝煤煤炉的设计,即将
固体碳做成碳柱,一节一节填充在容器内进行燃烧,这种设计的优点是:
;
(3)“祥云”火炬的核心设计是“双火焰”燃烧系统,即使当外部火焰意外熄灭时,内部
火焰仍能使其迅速再次燃烧,此过程中,内部火焰的作用是
。
第7页,共9页常州市二○○八年初中毕业、升学统一考试
化学参考答案及评分标准
一、选择题(本大题包括20小题,每小题2分,共40分)
1.B 2.C 3.C 4.D 5.C
6.A 7.C 8.D 9.B 10.D
11.A 12.B 13.A 14.C 15.C
16.B 17.A 18.B 19.C 20.D
二、(本题包括4小题,共15分)
21.(3分)③①② (各1分)
22.(5分)(1)N (2)CH (3)HCl (4)CO (5)Ca(OH) (各1分)
2 4 2 2
23.(4分)(1)﹤ (2)﹥ (3)﹤ (4)=(各1分)
24.(3分)(1)加热 (2)稀盐酸 (3)氢氧化钠溶液(各1分)
三、(本大题包括2小题,共14分)
25.(7分)
(1)铁架台 (1分)
(2)2H
2
O
2
MnO2 2H
2
O+O
2
↑(2分) ACDEG或BCDEFG(1分)
(3)防止生成的高温熔融物炸裂集气瓶(1分)
(4)AC(填对一个给1分,有错不给分,共2分)
26.(7分)
酒精的熔点为-114.1℃,即在常温下,酒精不可能为固态(1分)
【实验探究Ⅱ】:请你完成以下实验报告。
序号 实验步骤 实验现象 实验结论
④ 取少量①所得溶液放入试管 有白色沉淀生成,
中,滴加过量氯化钙溶液,待充 溶液变红
(此格不须填写)
分反应后,滴加数滴无色酚酞
试液。
实验结论:该白色固体为氢氧化钠、碳酸钠。
本处仅检验氢氧化钠为1分,仅检验碳酸钠为3分(实验步骤、实验现象、实验结论
各1分,两者都检验为5分(实验步骤、实验现象各2分,实验结论1分)。
玻璃导管的成分中可能含有钠离子(1分)
四、(本大题包括2小题,共14分)
27.(8分)
(1)高炉 (1分)
(2)3CO+Fe O 高温 2Fe+3CO (2分)
2 3 2
(3)促使反应更加剧烈,并获得更多的热量(1分)
(4)加入稀盐酸,有气泡产生的为铁粉,否则为生石灰(合理即可,1分)
(5)250mL(列式正确给2分,结果正确给1分,共3分)
28.(6分)
(1)H(1分) (2)CO(1分)
2
(3)HCO(1分) O(1分)
2 3 2
(4)6CO+6H O C H O+6O (2分)
2 2 6 12 6 2
五、(本题包括2小题,共11分)
29.(5分)
(1)2HO 通电 2H↑+O ↑(2分)
2 2 2
(2)产生剧烈的爆鸣声(1分)
第8页,共9页(3)仪器和装置都用生活中废旧物品制成,体现了环保与节约资源的理念(1分)
(4)硬质塑料管没有刻度,无法测量两种气体的体积比(1分)
30.(6分)
(1)曲线图要求:曲线平滑、趋势正确、给出平台(1分)
(2)1.0g(1分)
(3)80%(1分)
(4)解:设纯净硝酸铵的质量为x
NH NO +NaOH== NaNO +HO+NH ↑
4 3 3 2 3
85 17
x 1.7g
85/17=== y/1.7g y=8.5g --------------------(1分)
--------------------(2分)
答:反应后所得溶液的溶质质量分数为17%。
六、(本题包括2小题,你只需选做其中一个小题,若两小题全做则以31题计分,共6分)
31.(6分)
(1)无机非金属 (1分) (2)贫血 (1分)
(3)2Cu+O+CO+HO==Cu (OH) CO(2分) HCl(或HSO )(1分)
2 2 2 2 2 3 2 4
(5)用网眼小于碎瓷片的铁丝筐将混有淤泥的瓷片浸入水中旋转,然后取出(用类似
过滤的方法即可)(1分)
32.(6分)
(1)导热性(1分)
(2)①2C H +13O 点燃 8CO+10HO (2分) ②物理(1分)
4 10 2 2 2
③方便添加燃料,便于灰渣的排出,有利于空气的流通(任答1点,1分)
(3)使熄灭的外部火焰的气体的温度达到着火点(1分)
说明:1.凡合理答案均相应给分。
2.对化学用语的评分仍要严格。具体要求为:
(1)书写化学方程式时,化学式有错不得分;配平、条件、生成物状态有错、计量数不
是最简比、没画“=”(有机反应除外)等扣1分。
(2)化学专用名词写错别字,整体扣1分。
(3)元素符号书写不规范,整体扣1分。
3.解计算题格式必须规范。解题过程中,无设和答步骤、设未知量带单位、运算过程中
物理量的数值不带单位、解得未知量的单位带括号等共扣1分。
4.最小得分值为1分。
第9页,共9页