文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第 1 课时 化学反应与热能
1.化学反应A+B ===2AB的能量变化如图所示,则下列说法正确的是( )
2 2
A.该反应是吸热反应
B.断裂1 mol A—A键和1 mol B—B键放出x kJ的能量
C.断裂2 mol A—B键需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A 和1 mol B 的总能量
2 2
【答案】C
【解析】从题图可以看出,反应物的总能量高于生成物的总能量,该反应是放热反应,A、D项错
误;断键时需要吸收能量,B项错误,C项正确。
2.根据下面的信息,判断下列叙述正确的是( )
A.氢气跟氧气反应生成水的同时释放能量
B.氢气跟氧气反应生成水的同时吸收能量
C.1 mol H 跟 mol O 反应生成1 mol H O一定释放能量245 kJ
2 2 2
D.2 mol H (g)跟1 mol O (g)反应生成2 mol H O(g)吸收能量490 kJ
2 2 2
【答案】A
【解析】由题中信息可知,1 mol H (g)的共价键断裂吸收能量436 kJ, mol O(g)的共价键断裂吸收
2 2
能量249 kJ,两项共吸收能量685 kJ;1 mol H (g)与mol O(g)形成1 mol H O(g)共释放能量930 kJ。
2 2 2
在1 mol H (g)跟 mol O(g)反应生成1 mol H O(g)的过程中,放出的能量比吸收的能量多 245 kJ,C
2 2 2
项中缺少物质的状态,所以释放的能量不一定是245 kJ。
3.下列各图中,表示该化学反应是吸热反应的是 ( )【答案】A
【解析】吸热反应中反应物的总能量小于生成物的总能量,A项正确。
4.已知断裂1 mol共价键所需要吸收的能量分别为H—H:436 kJ,I—I:151 kJ,H—I:299 kJ,
下列对H(g)+I(g)=2HI(g)的反应类型判断错误的是( )
2 2
A.放出能量的反应 B.吸收能量的反应
C.氧化还原反应 D.可逆反应
【答案】B
【解析】依题意,断裂1 mol H—H键和1 mol I—I键吸收的能量为436 kJ+151 kJ=587 kJ,生成2
mol H—I键放出的能量为299 kJ×2=598 kJ,因为598 kJ>587 kJ,所以,该反应的正反应是放出能
量的反应,即该反应是放出能量的反应;根据反应式可知该反应是可逆反应,也是氧化还原反应。
5.下列说法正确的是 ( )
A.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量
B.任何放热反应在常温条件下一定能发生反应
C.形成生成物化学键释放的能量大于破坏反应物化学键所吸收的能量时,反应为吸热反应
D.等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
【答案】A
【解析】放热反应在常温下不一定能发生,如煤的燃烧,B错误。形成生成物化学键释放的能量大
于破坏反应物化学键所吸收的能量时,反应为放热反应,C错误;等量的硫蒸气和硫固体分别完全
燃烧,后者放出的热量少,D错误。
6.下列对化学反应的认识错误的是( )
A.会引起化学键的变化
B.会产生新的物质
C.必然引起物质状态的变化
D.必然伴随着能量的变化
【答案】C【解析】化学反应的本质是化学键的断裂和形成,表现为有新物质生成,并伴随着能量的变化,而
化学变化中的反应物和生成物的状态在反应前后可能相同,也可能不相同,故正确【答案】为C。
7.从宏观来看化学变化的本质是有新物质生成。从微观角度来看,下列变化不能说明发生了化学
变化的是( )
A.变化时有电子的得失或共用电子对的形成
B.变化过程中有化学键的断裂和形成
C.变化时释放出能量
D.变化前后原子的种类和数目没有改变,分子种类增加了
【答案】C
【解析】某些物理变化也能释放能量,如浓HSO 、NaOH等溶于水放出热量,白炽灯工作时发光
2 4
发热等。
8.下列变化过程吸收能量的是( )
A.Na+―→Na B.Cl―→Cl-
C.H+Cl―→HCl D.H―→H+H
2
【答案】D
9.下列说法正确的是( )
A.任何化学反应都伴随着能量的变化
B.HO(g)―→HO(l)该过程放出大量的热,所以该过程是化学变化
2 2
C.化学反应中能量的变化都表现为热量的变化
D.对于如图所示的过程,是吸收能量的过程
【答案】A
【解析】任何化学反应都有能量的变化,但有能量变化的过程不一定是化学变化,如物质的三态变
化,虽然存在能量变化,但不存在旧化学键的断裂与新化学键的形成,故不是化学变化,所以A项
正确,B项错误;化学反应中能量变化的形式有多种,除热能外,还有光能、电能等,C项错误;
由图像知,该过程中反应物的总能量大于生成物的总能量,故该过程中放出了能量,D项错误。
10.下列反应一定属于放热反应的是( )
A.氢氧化钡晶体和氯化铵晶体的反应
B.能量变化如图所示的反应C.化学键断裂吸收的能量比化学键形成放出的能量少的反应
D.不需要加热就能发生的反应
【答案】C
【解析】氢氧化钡晶体和氯化铵晶体的反应属于吸热反应;生成物的总能量比反应物的总能量大的
反应为吸热反应;化学键断裂吸收的能量比化学键形成放出的能量少的反应为放热反应;不需要加
热就能发生的反应可能为吸热反应,也可能为放热反应。
11.已知2 mol氢气完全燃烧生成水蒸气时放出能量 484 kJ,且氧气中1 mol O===O键完全断裂时
吸收能量496 kJ,水蒸气中1 mol H—O键形成时放出能量463 kJ,则氢气中1 mol H—H键断裂
时吸收能量为 ( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
【答案】C
【解析】设1 mol H—H键断裂时吸收能量为x kJ。首先写出化学反应方程式2H+O=====2HO,
2 2 2
然后分析过程,2H-H+O===O=====2H—O—H,由过程可知2 mol氢气完全燃烧生成水蒸气时应
该拆开2 mol H—H键、1 mol O===O键,吸收的能量为(2x+496)kJ;生成2 mol H O形成4 mol H
2
—O键,放出的能量为4×463 kJ=1 852 kJ,依据能量守恒定律放出能量 484 kJ=1 852 kJ-(2x+
496)kJ,即可求出x=436。
12.已知化学反应2C(s)+O(g)=====2CO(g)、2CO(g)+O(g)=====2CO(g)都是放热反应。据此判
2 2 2
断,下列说法不正确的是(其他条件相同) ( )
A.12 g C所具有的能量一定高于28 g CO所具有的能量
B.56 g CO和32 g O 所具有的总能量大于88 g CO 所具有的总能量
2 2
C.12 g C和32 g O 所具有的总能量大于44 g CO 所具有的总能量
2 2
D.将一定质量的C燃烧,生成CO 比生成CO时放出的热量多
2
【答案】A
【解析】放出热量的化学反应,反应物的总能量一定高于生成物的总能量。C和CO的燃烧反应都
是放热反应,所以C+O=====CO 必然是放热反应,因此,B、C两项的说法正确。12 g C并不代
2 2
表反应物的全部,O 也是反应物,所以A项不正确。由于C――→CO放热、CO――→CO 放热,
2 2所以C――→CO 比C――→CO放出的热量要多,即D项说法正确。
2
13.(1)在1 mol氢分子中,含有________mol氢原子,含有________mol H—H键。
(2)已知在25 ℃和101 kPa条件下,由2 mol H原子形成1 mol H—H键时,放出436 kJ的能量。
若要使1 mol氢分子变为2 mol氢原子时,需要断开1 mol H—H键,其能量变化是__________。
(3)在CH 中,断开1 mol C—H键要吸收415 kJ的能量。若要形成1 mol CH 中的C—H键其能
4 4
量变化是________________。
【答案】(1)2 1 (2)吸收436 kJ的能量 (3)放出4 mol×415 kJ·mol-1=1 660 kJ的能量
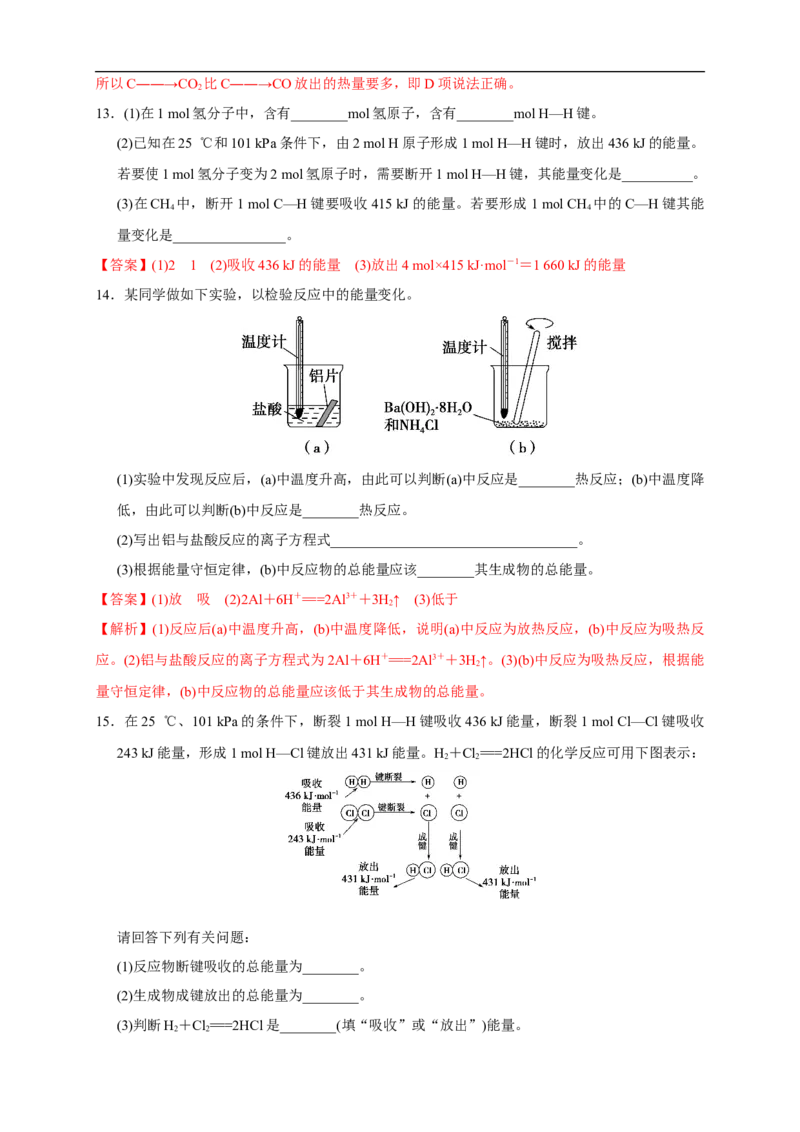
14.某同学做如下实验,以检验反应中的能量变化。
(1)实验中发现反应后,(a)中温度升高,由此可以判断(a)中反应是________热反应;(b)中温度降
低,由此可以判断(b)中反应是________热反应。
(2)写出铝与盐酸反应的离子方程式___________________________________。
(3)根据能量守恒定律,(b)中反应物的总能量应该________其生成物的总能量。
【答案】(1)放 吸 (2)2Al+6H+===2Al3++3H↑ (3)低于
2
【解析】(1)反应后(a)中温度升高,(b)中温度降低,说明(a)中反应为放热反应,(b)中反应为吸热反
应。(2)铝与盐酸反应的离子方程式为2Al+6H+===2Al3++3H↑。(3)(b)中反应为吸热反应,根据能
2
量守恒定律,(b)中反应物的总能量应该低于其生成物的总能量。
15.在25 ℃、101 kPa的条件下,断裂1 mol H—H键吸收436 kJ能量,断裂1 mol Cl—Cl键吸收
243 kJ能量,形成1 mol H—Cl键放出431 kJ能量。H+Cl===2HCl的化学反应可用下图表示:
2 2
请回答下列有关问题:
(1)反应物断键吸收的总能量为________。
(2)生成物成键放出的总能量为________。
(3)判断H+Cl===2HCl是________(填“吸收”或“放出”)能量。
2 2(4)反应物的总能量________(填“>”,“=”或“<”)生成物的总能量。
【答案】(1)679 kJ (2)862 kJ (3)放出 (4)>
【解析】 (1)反应物断键吸收的总能量应该是断裂1 mol H—H键与1 mol Cl—Cl键吸收的能量之
和,即436 kJ+243 kJ=679 kJ。(2)生成物成键放出的总能量为2×431 kJ=862 kJ。(3)、(4)由于吸收
的总能量小于放出的总能量,所以反应放热即反应物的总能量大于生成物的总能量。
16.在人类生产、生活对能量的需求日益增长的今天,研究化学反应及其能量变化,对合理利用常
规能源和开发新能源具有十分重要的意义。能源是人类赖以生存和发展不可缺少的因素。请完
成下列问题:
(1)人类利用能源分为三个阶段,即________、________、________。
(2)矿物能源是现代人类社会赖以生存的重要物质基础。目前,全球仍主要处于化石能源时期。
下列不属于化石能源的是________。(填序号,下同)
A.石油 B.煤
C.天然气 D.生物质能
(3)下列对能源的看法合理的是 ( )
A.化石能源属于不可再生能源,只会越用越少
B.生物能是一种可再生能源,有广泛的前景
C.太阳能、氢能、核能、地热能都属于新能源
D.我国人口众多、资源相对匮乏、环境承载能力较弱,因此要建设节约型社会
【答案】(1)柴草时期 化石能源时期 多能源结构时期(2)D (3)ABCD
【解析】人类利用能源的三个阶段在教材中有介绍;生物质能不属于化石能源。
17.2012年发射的“神舟九号”宇宙飞船有两个重大使命,一是航天员在太空首次进行手动交会
对接,二是实现航天员在“天宫一号”内进行实验操作。“神舟”系列火箭用偏二甲肼(C HN)
2 8 2
作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体。
(1)写出反应的化学方程式:___________________________________________
_________________________________________________________________。
(2)该反应是__________(填“放热”或“吸热”)反应,反应物的总能量__________(填“大于”、
“小于”或“等于”)生成物的总能量,断开化学键________的总能量________(填“大于”、
“小于”或“等于”)形成化学键________的总能量。
【答案】(1)C HN+2NO=====2CO↑+3N↑+4HO (2)放热 大于 吸收 小于 放出
2 8 2 2 4 2 2 2
18.在一个小烧杯里加入约20 g已研磨成粉末的氢氧化钡晶体[Ba(OH) ·8H O],将小烧杯放在事先
2 2
已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10 g氯化铵晶体,并立即用玻璃棒迅速搅拌。
试回答下列问题:(1)写出反应的化学方程式:__________________________________________。
(2)实验中要立即用玻璃棒迅速搅拌的原因是__________________________。
(3)如果实验中没有看到“结冰”现象,可能的原因是(答出三个或三个以上原
因)____________________________________。
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?
____________________________________________________(答出两种方案)。
(5)“结冰”现象说明该反应是一个________(填“放出”或“吸收”)能量的反应。即断开旧化学
键________(填“吸收”或“放出”)的能量________(填“>”或“<”)形成新化学键________(填
“吸收”或“放出”)的能量。
(6)该反应在常温下就可进行,说明___________________________________。
【答案】(1)Ba(OH) ·8H O+2NH Cl===BaCl +8HO+2NH ·H O(2)使反应物充分混合,迅速发生反
2 2 4 2 2 3 2
应,使体系的温度降低(3)①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已
部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末(其他答案合理均正确)
(4)第一种方案:在烧杯中的反应物中插入温度计,通过测量,发现反应后温度计的示数下降,说明
反应是吸热反应;第二种方案:用皮肤感受,感觉烧杯外壁很凉,说明此反应为吸热反应(5)吸收
吸收 > 放出(6)有的吸热反应不需要加热也可发生
【解析】本题考查了化学反应中的能量变化以及吸热反应、放热反应与反应条件的关系。以
Ba(OH) ·8H O与NH Cl固体的反应为背景考查了分析问题、解决问题的能力和实验设计能力。反
2 2 4
应放出或吸收的热量可以通过触觉感知,也可以通过温度计测量。