文档内容
2008年全国统一高考化学试卷(全国卷Ⅱ)
一、选择题(共8小题,每小题5分,满分40分)
1.(5分)2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中
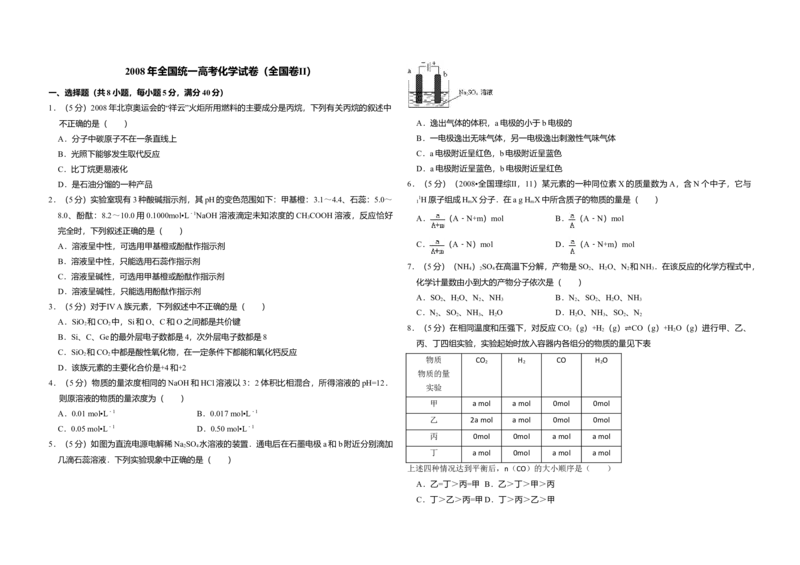
不正确的是( ) A.逸出气体的体积,a电极的小于b电极的
A.分子中碳原子不在一条直线上 B.一电极逸出无味气体,另一电极逸出刺激性气味气体
B.光照下能够发生取代反应 C.a电极附近呈红色,b电极附近呈蓝色
C.比丁烷更易液化 D.a电极附近呈蓝色,b电极附近呈红色
D.是石油分馏的一种产品 6.(5分)(2008•全国理综Ⅱ,11)某元素的一种同位素 X的质量数为A,含N个中子,它与
2.(5分)实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4、石蕊:5.0~ 1H原子组成H X分子.在a g H X中所含质子的物质的量是( )
1 m m
8.0、酚酞:8.2~10.0用0.1000mol•L﹣1NaOH溶液滴定未知浓度的CH
3
COOH溶液,反应恰好
A. (A﹣N+m)mol B. (A﹣N)mol
完全时,下列叙述正确的是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂 C. (A﹣N)mol D. (A﹣N+m)mol
B.溶液呈中性,只能选用石蕊作指示剂
7.(5分)(NH ) SO 在高温下分解,产物是SO 、H O、N 和NH .在该反应的化学方程式中,
4 2 4 2 2 2 3
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
化学计量数由小到大的产物分子依次是( )
D.溶液呈碱性,只能选用酚酞作指示剂
A.SO 、H O、N 、NH B.N 、SO 、H O、NH
2 2 2 3 2 2 2 3
3.(5分)对于ⅣA族元素,下列叙述中不正确的是( )
C.N 、SO 、NH 、H O D.H O、NH 、SO 、N
2 2 3 2 2 3 2 2
A.SiO 和CO 中,Si和O、C和O之间都是共价键
2 2
8.(5分)在相同温度和压强下,对反应CO (g)+H (g) CO(g)+H O(g)进行甲、乙、
2 2 2
B.Si、C、Ge的最外层电子数都是4,次外层电子数都是8
丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
⇌
C.SiO 和CO 中都是酸性氧化物,在一定条件下都能和氧化钙反应
2 2
物质 CO H CO H O
2 2 2
D.该族元素的主要化合价是+4和+2
物质的量
4.(5分)物质的量浓度相同的NaOH和HCl溶液以3:2体积比相混合,所得溶液的pH=12.
实验
则原溶液的物质的量浓度为( )
甲 a mol a mol 0mol 0mol
A.0.01 mol•L﹣1 B.0.017 mol•L﹣1
乙 2a mol a mol 0mol 0mol
C.0.05 mol•L﹣1 D.0.50 mol•L﹣1
丙 0mol 0mol a mol a mol
5.(5分)如图为直流电源电解稀Na SO 水溶液的装置.通电后在石墨电极a和b附近分别滴加
2 4
丁 a mol 0mol a mol a mol
几滴石蕊溶液.下列实验现象中正确的是( )
上述四种情况达到平衡后,n(CO)的大小顺序是( )
A.乙=丁>丙=甲 B.乙>丁>甲>丙
C.丁>乙>丙=甲D.丁>丙>乙>甲成的化合物可作为一种重要的陶瓷材料,其化学式是 ;
(3)X的常见氢化物的空间构型是 ;它的另一氢化物X H 是一种火箭燃料的成分,其电子
2 4
二、非选择题 式是 ;
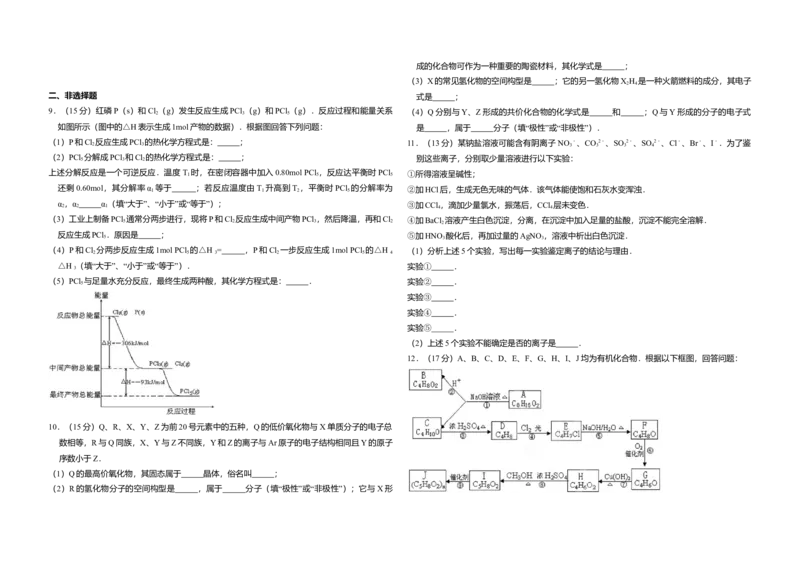
9.(15分)红磷P(s)和Cl 2 (g)发生反应生成PCl 3 (g)和PCl 5 (g).反应过程和能量关系 (4)Q分别与Y、Z形成的共价化合物的化学式是 和 ;Q与Y形成的分子的电子式
如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题: 是 ,属于 分子(填“极性”或“非极性”).
(1)P和Cl 反应生成PCl 的热化学方程式是: ; 11.(13分)某钠盐溶液可能含有阴离子 NO ﹣、CO 2﹣、SO 2﹣、SO 2﹣、Cl﹣、Br﹣、I﹣.为了鉴
2 3 3 3 3 4
(2)PCl 5 分解成PCl 3 和Cl 2 的热化学方程式是: ; 别这些离子,分别取少量溶液进行以下实验:
上述分解反应是一个可逆反应.温度 T
1
时,在密闭容器中加入 0.80mol PCl
5
,反应达平衡时PCl
5
①所得溶液呈碱性;
还剩0.60mol,其分解率α
1
等于 ;若反应温度由 T
1
升高到T
2
,平衡时PCl
5
的分解率为 ②加HCl后,生成无色无味的气体.该气体能使饱和石灰水变浑浊.
α 2 ,α 2 α 1 (填“大于”、“小于”或“等于”); ③加CCl 4 ,滴加少量氯水,振荡后,CCl 4 层未变色.
(3)工业上制备PCl 5 通常分两步进行,现将P和Cl 2 反应生成中间产物PCl 3 ,然后降温,再和Cl 2 ④加BaCl 2 溶液产生白色沉淀,分离,在沉淀中加入足量的盐酸,沉淀不能完全溶解.
反应生成PCl 5 .原因是 ; ⑤加HNO 3 酸化后,再加过量的AgNO 3 ,溶液中析出白色沉淀.
(4)P和Cl 分两步反应生成1mol PCl 的△H = ,P和Cl 一步反应生成1mol PCl 的△H (1)分析上述5个实验,写出每一实验鉴定离子的结论与理由.
2 5 3 2 5 4
△H (填“大于”、“小于”或“等于”). 实验① .
3
(5)PCl 与足量水充分反应,最终生成两种酸,其化学方程式是: . 实验② .
5
实验③ .
实验④ .
实验⑤ .
(2)上述5个实验不能确定是否的离子是 .
12.(17分)A、B、C、D、E、F、G、H、I、J均为有机化合物.根据以下框图,回答问题:
10.(15分)Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总
数相等,R与Q同族,X、Y与Z不同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子
序数小于Z.
(1)Q的最高价氧化物,其固态属于 晶体,俗名叫 ;
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”);它与X形(1)B和C均为有支链的有机化合物,B的结构简式为 ;C在浓硫酸作用下加热反应只能
生成一种烯烃D,D的结构简式为 .
(2)G 能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式 .
(3)写出:
⑤的化学方程式是 .⑨的化学方程式是 .
(4)①的反应类型是 ,④的反应类型是 ,⑦的反应类型是 .
(5)与H具有相同官能团的H的同分异构体的结构简式为 .