文档内容
2012 年普通高等学校招生全国统一考试
C.化合物 是苯的同系物
理科综合能力测试
D.三硝酸甘油酯的分子式为C H N O
选择题部分(共 120 分) 3 5 3 9
12.下列说法正确的是
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
一、选择题(本小题17小题。在每小题给出的四个选项中,只有一项是符合题目要求的。)
B.为确定某酸H A是强酸还是弱酸,可测NaHA溶液的pH。
2
7.下列说法不正确的是 若pH>7,则H A是弱酸;若pH<7,则H A是强酸
2 2
A.利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 C.用0.2000 mol/L NaOH标准溶液滴定HCl与CH COOH的混合溶液(混合液中两种酸的浓度均约为0.1
3
B.蔗糖、淀粉、油脂及其水解产物均为非电解质 mol/L),至中性时,溶液中的酸未被完全中和
C.通过红外光谱分析可以区分乙醇和乙酸乙酯 D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1 mol/L氯化镁
D.石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、 溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③
丙烯等气态短链烃
13.水溶液X中只可能溶有K+、Mg2+、Al3+、AlO、SiO2、SO2、CO2、SO2中的若干种离子。某同学
2 3 3 3 4
8.下列说法正确的是
对该溶液进行了如下实验:
A.在“镀锌铁皮的镀层厚度的测定”实验中,将镀锌铁皮放入稀硫酸,待产生氢气的速率突然减小,可以判
ÆøÌå¼×
断锌镀层已反应完全
ÈÜÒºÒÒ
B.在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管 ¹ýÁ¿Ï¡ÑÎËá ¹ýÁ¿°±Ë®
ÈÜÒºX ÎÞÉ«ÈÜÒº¼×
中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在
C.在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时 °×É«³Áµí ÒÒ
³Áµí ¼×
停止加热
下列判断正确的是
D.受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,
A.气体甲一定是纯净物 B.沉淀甲是硅酸和硅酸镁的混合物
并视情况作进一步处理
C.K+、AlO和SiO2一定存在于溶液X中 D.CO2和SO2一定不存在于溶液X中
9.X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等, 2 3 3 4
X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
非选择题部分(共 180 分)
A.原子半径:Z>Y>X
B.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点
非选择题部分共 12 题,共 180 分。
C.CaY 与水发生氧化还原反应时,CaY 只作氧化剂
2 2
D.CaX 、CaY 和 CaZ 等 3种化合物中,阳离子 与阴 26.[14分]已知:I +2S O2 =S O2+2I-。相关物质的溶度积常数见下表:
2 2 2 2 2 3 4 6
离子个数比均为1︰2 物质 Cu(OH) Fe(OH) CuCl CuI
2 3
10.以铬酸钾为原料,电化学法制备重铬酸钾的实验装 不锈钢 惰性电极 置示 Ksp 2.2×10-20 2.6×10-39 1.7×10-7 1.3×10-12
意图如下:
(1)某酸性CuCl 溶液中含有少量的FeCl ,为得到纯净的CuCl •2H O晶体,加入________,调至pH=
下列说法不正确的是 2 3 2 2
A.在阴极式,发生的电极反应为:2H 2 O+2e-= 稀KOH溶液 | K 2 CrO 4 溶液 4,使 过 溶 滤 液 后 中 , 的 将 F 所 e3 得 +转 滤 化 液 为 低 F 温 e( 蒸 O 发 H) 、 3 沉 浓 淀 缩 , 结 此 晶 时 , 溶 可 液 得 中 到 的 C c u ( C F l e3 • + 2H )= O __ 晶 __ 体 __ 。 __ _____。
2OH-+H ↑ 2 2
2 阳离子交换膜
B.在阳极室,通电后溶液逐渐由黄色变为橙色, 是因 (2)在空气中直接加热CuCl 2 •2H 2 O晶体得不到纯的无水CuCl 2 ,原因是___________________(用化学方
为阳极区H+浓度增大,使平衡2CrO2+2H+ Cr O2+H O向右移动 程式表示)。由CuCl 2 •2H 2 O晶体得到纯的无水CuCl 2 的合理方法是___________。
4 2 7 2
(3)某学习小组用“间接碘量法”测定含有 CuCl •2H O晶体的试样(不含能与 I―发生反应的氧化性质杂
ͨµç 2 2
C.该制备过程总反应的化学方程式为:4K CrO +4H O 2K Cr O +4KOH+2H ↑+O ↑
2 4 2 2 2 7 2 2 质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L
d
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为1- Na S O 标准溶液滴定,到达滴定终点时,消耗Na S O 标准溶液20.00 mL。
2 2 3 2 2 3
2
①可选用___________作滴定指示剂,滴定终点的现象是_________________。
11.下列说法正确的是
CH(CH ) ②CuCl 溶液与KI反应的离子方程式为______________________________。
3 2 2
A.按系统命名法,化合物CH
3
CH
2
CHCH
2
CH
2
CH(CH
3
)
2
的名称为2,6-二甲基-5-乙基庚烷 ③该试样中CuCl
2
•2H
2
O的质量百分数为___________________________。
B.丙氨酸和苯丙氨酸脱水,最多可生成3种二肽
27.[15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水
蒸气,发生的主要化学反应有:反应过程 化学方程式 焓变△H(kJ/mol) 活化能Ea(kJ/mol)
CH (g)+2O (g)=CO (g)+2H O(g) -802.6 125.6
甲烷氧化 4 2 2 2
CH (g)+O (g)=CO (g)+2H (g) -322.0 172.5
4 2 2 2
CH (g)+H O(g)=CO(g)+3H (g) 206.2 240.1
蒸汽重整 4 2 2
CH (g)+2H O(g)=CO (g)+4H (g) 165.0 243.9
4 2 2 2
回答下列问题:
(1)反应CO(g)+H O(g)=CO (g)+H (g)的△H= kJ/mol。 2 2 2
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(P )代替物质的量浓度(c )也可表示平衡常数(记作K ),则
B B P
反应CH (g)+H O(g) CO(g)+3H (g)的K = ;
4 2 2 P
随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量角度分析,甲烷自热重整方法的先进之处在于 。
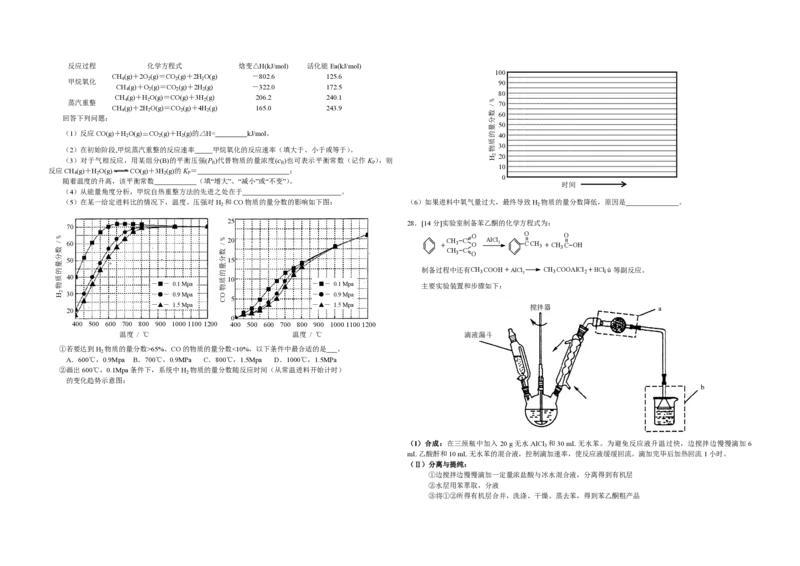
(5)在某一给定进料比的情况下,温度、压强对H 和CO物质的量分数的影响如下图:
2
70
60
50
40
30
20
400 500 600 700 800 900 1000 1100 1200
温度 / ℃
%
/ 数分量的质物
H 2
%
/ 数分量的质物OC
时间
25
20
15
10
-■- 0.1 Mpa -■- 0.1 Mpa
-●- 0.9 Mpa -●- 0.9 Mpa
5
-▲- 1.5 Mpa -▲- 1.5 Mpa
0
400 500 600 700 800 900 1000 1100 1200
温度 / ℃
①若要达到H 物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
2
A.600℃,0.9Mpa B.700℃,0.9MPa C.800℃,1.5Mpa D.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H 物质的量分数随反应时间(从常温进料开始计时)
2
的变化趋势示意图:
%
/
数分量的质物
H
2
100
90
80
70
60
50
40
30
20
10
0
(6)如果进料中氧气量过大,最终导致H 物质的量分数降低,原因是 。
2
28.[14分]实验室制备苯乙酮的化学方程式为:
O O O
CH C AlCl
+ 3 O 3 CCH 3 + CH 3 C OH CH C 3 O
制备过程中还有CH
3
COOH +AlCl
3
CH
3
COOAlCl
2
+HCl¡ü 等副反应。
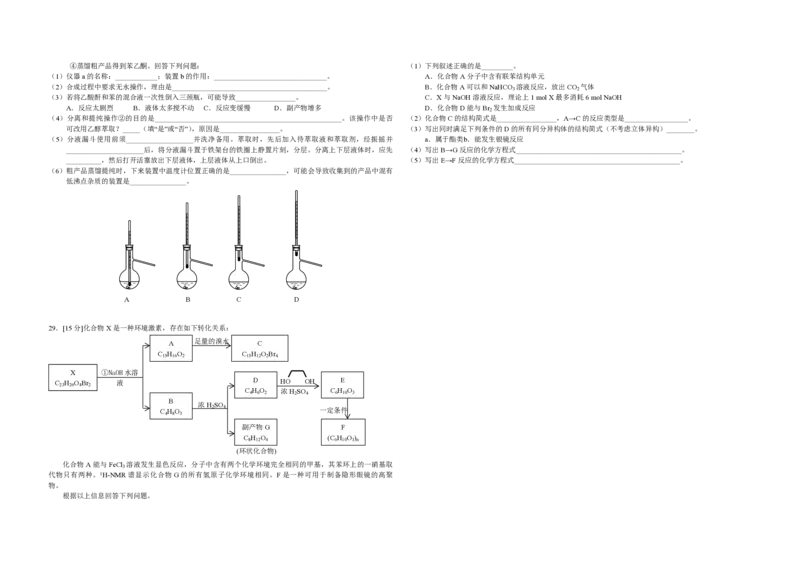
主要实验装置和步骤如下:
搅拌器 a
滴液漏斗
b
(I)合成:在三颈瓶中加入 20 g无水 AlCl 和 30 mL无水苯。为避免反应液升温过快,边搅拌边慢慢滴加 6
3
mL乙酸酐和10 mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。滴加完毕后加热回流1小时。
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品④蒸馏粗产品得到苯乙酮。回答下列问题: (1)下列叙述正确的是_________。
(1)仪器a的名称:____________;装置b的作用:________________________________。 A.化合物A分子中含有联苯结构单元
(2)合成过程中要求无水操作,理由是____________________________________________。 B.化合物A可以和NaHCO 溶液反应,放出CO 气体
3 2
(3)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致_________________。 C.X与NaOH溶液反应,理论上1 mol X最多消耗6 mol NaOH
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多 D.化合物D能与Br 发生加成反应
2
(4)分离和提纯操作②的目的是_____________________________________________________。该操作中是否 (2)化合物C的结构简式是_________________,A→C的反应类型是__________________。
可改用乙醇萃取?_____(填“是”或“否”),原因是_________________。 (3)写出同时满足下列条件的D的所有同分异构体的结构简式(不考虑立体异构)________。
(5)分液漏斗使用前须___________________并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振摇并 a.属于酯类 b.能发生银镜反应
______________________后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先 (4)写出B→G反应的化学方程式_______________________________________________。
__________,然后打开活塞放出下层液体,上层液体从上口倒出。 (5)写出E→F反应的化学方程式_______________________________________________。
(6)粗产品蒸馏提纯时,下来装置中温度计位置正确的是________________,可能会导致收集到的产品中混有
低沸点杂质的装置是________________。
A B C D
29.[15分]化合物X是一种环境激素,存在如下转化关系:
足量的溴水
A C
C H O C H O Br
15 16 2 15 12 2 4
X ①NaOH水溶
C H O Br 液 D HO OH E
23 26 4 2
②H+ C 4 H 6 O 2 浓H 2 SO 4 C 6 H 10 O 3
B
浓H SO
C H O 2 4 一定条件
4 8 3
副产物G F
C H O (C H O )
8 12 4 6 10 3 n
(环状化合物)
化合物A能与FeCl 溶液发生显色反应,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取
3
代物只有两种。1H-NMR谱显示化合物 G的所有氢原子化学环境相同。F是一种可用于制备隐形眼镜的高聚
物。
根据以上信息回答下列问题。