文档内容
2017 年 11 月浙江省普通高校招生选考科目考试试题
一、选择题(本大题共25小题,每小题2分,共50分。每小题列出的四个备选项中只有
一个是符合题目要求的,不选、多选、错选均不得分。)
1.下列属于氧化物的是( )
A.NaO B.Ca(OH)
2 2
C.HClO D.KCO
2 3
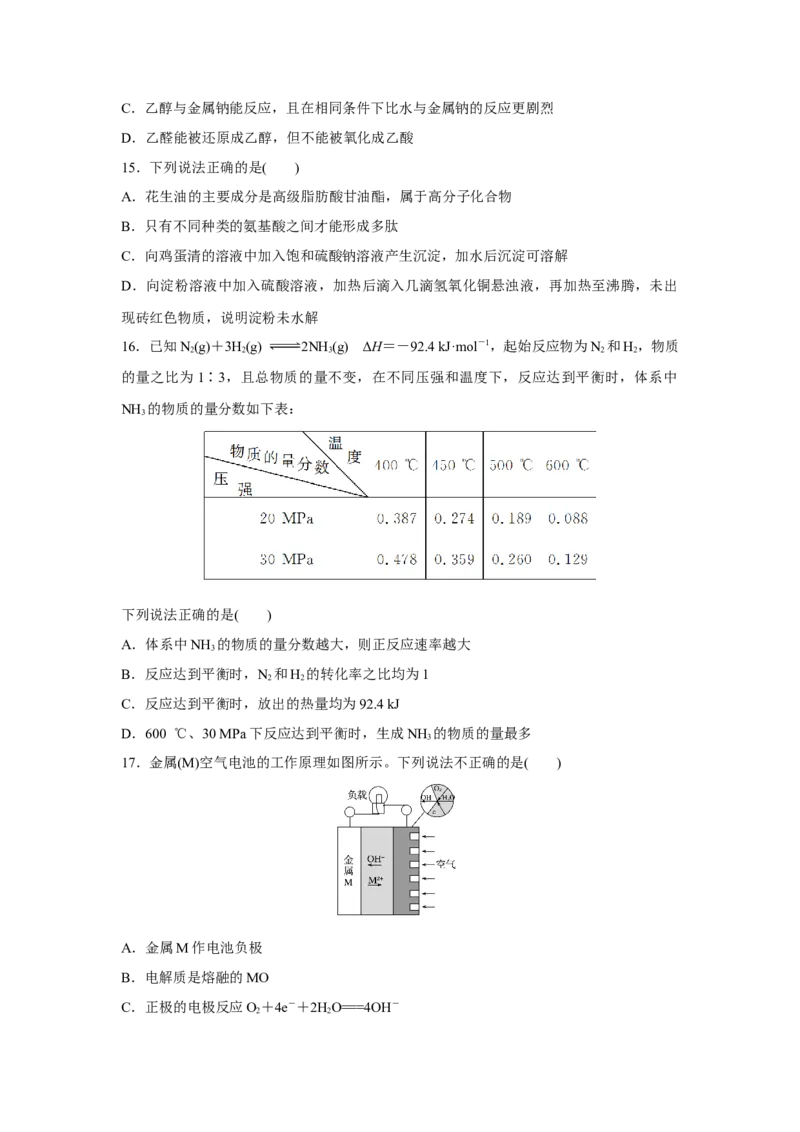
2.下列仪器名称为“蒸馏烧瓶”的是( )
3.下列属于电解质的是( )
A.镁 B.酒精
C.硫酸铜 D.食盐水
4.下列分散系属于悬浊液的是( )
A.牛奶 B.蔗糖溶液
C.泥浆水 D.氢氧化铁胶体
5.下列不属于化石燃料的是( )
A.煤 B.石油
C.天然气 D.甲醇
6.下列说法不正确的是( )
A.干冰可用于人工降雨 B.碘酸钾可用作加碘食盐的添加剂
C.碳酸钠是发酵粉的主要成分 D.次氯酸钙是漂白粉的主要成分
7.下列属于置换反应的是( )
A.2FeCl +Cu===CuCl +2FeCl B.2HClO=====2HCl+O↑
3 2 2 2
C.CO+CuO=====CO+Cu D.2Mg+CO=====2MgO+C
2 2
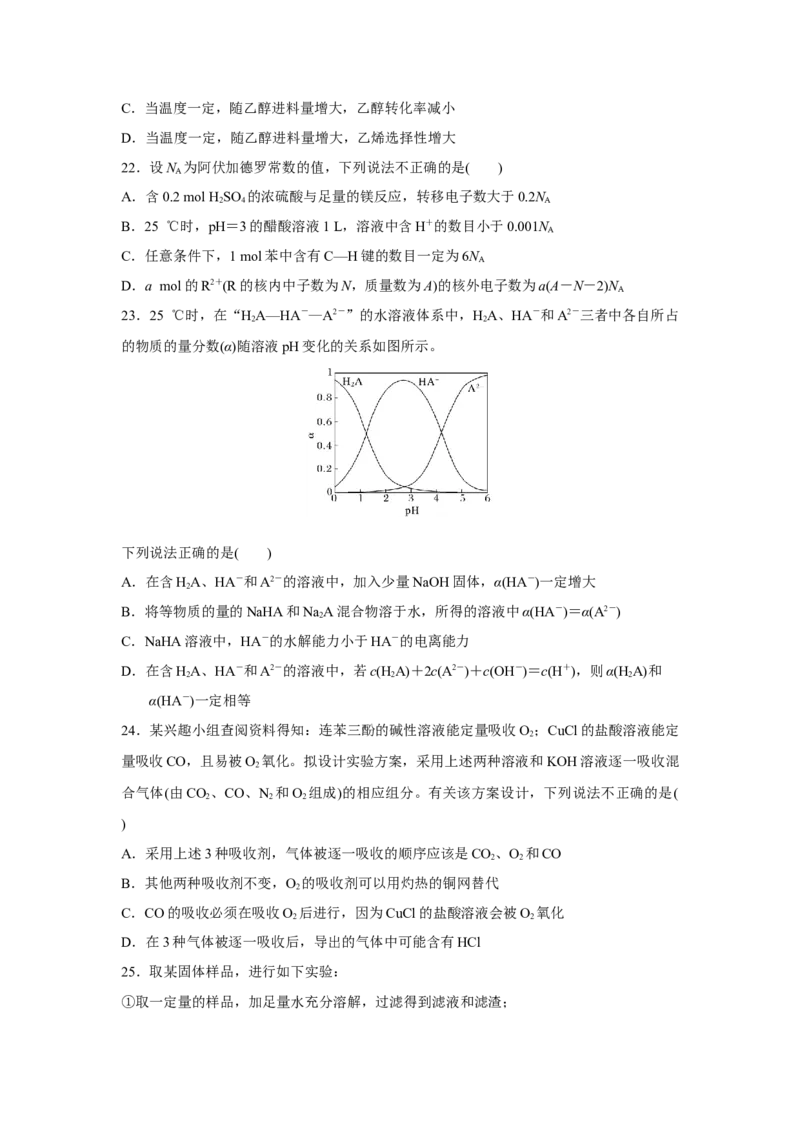
8.下列表示不正确的是( )
A.氯原子的结构示意图:
B.二氧化碳的结构式:O===C===OC.甲烷的球棍模型:
D.乙醛的官能团:—CHO
9.下列物质的水溶液不能使酚酞变红的是( )
A.NaOH B.NaCO
2 3
C.NaCl D.NH
3
10.下列方法(必要时可加热)不合理的是( )
A.用澄清石灰水鉴别CO和CO
2
B.用水鉴别苯和四氯化碳
C.用氢氧化钡溶液鉴别NH Cl、(NH )SO 和KSO
4 4 2 4 2 4
D.用淀粉碘化钾试纸鉴别碘水和溴水
11.下列说法正确的是( )
A.O表示中子数为10的氧元素的一种核素
B.金刚石和石墨互为同素异形体,两者之间不能相互转化
C.CHCOOH和CHCOOCH 互为同系物
3 3 3
D.C H 的同分异构体有4种,其熔点各不相同
6 14
12.下列离子方程式不正确的是( )
A.氢氧化钠溶液与二氧化硅反应:SiO+2OH-===SiO+HO
2 2
B.碳酸钠溶液与氢氧化钡溶液反应:CO+Ba(OH) ===BaCO ↓+2OH-
2 3
C.酸性硫酸亚铁溶液在空气中被氧化:4Fe2++O+4H+===4Fe3++2HO
2 2
D.氯气与氢氧化钠溶液反应:Cl+2OH-===ClO-+Cl-+HO
2 2
13.Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最
外层电子数之和为22,下列说法正确的是( )
X Y
Q Z
A.Y的原子半径比X的大
B.Q的最高价氧化物的水化物的酸性比Z的强
C.X、Y和氢3种元素形成的化合物中都只有共价键
D.Q的单质具有半导体的性质,Q与Z可形成化合物QZ
4
14.下列说法正确的是( )
A.正丁烷和异丁烷均有两种一氯取代物
B.乙烯和苯都能与H 发生加成反应,说明二者的分子中均含有碳碳双键
2C.乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
D.乙醛能被还原成乙醇,但不能被氧化成乙酸
15.下列说法正确的是( )
A.花生油的主要成分是高级脂肪酸甘油酯,属于高分子化合物
B.只有不同种类的氨基酸之间才能形成多肽
C.向鸡蛋清的溶液中加入饱和硫酸钠溶液产生沉淀,加水后沉淀可溶解
D.向淀粉溶液中加入硫酸溶液,加热后滴入几滴氢氧化铜悬浊液,再加热至沸腾,未出
现砖红色物质,说明淀粉未水解
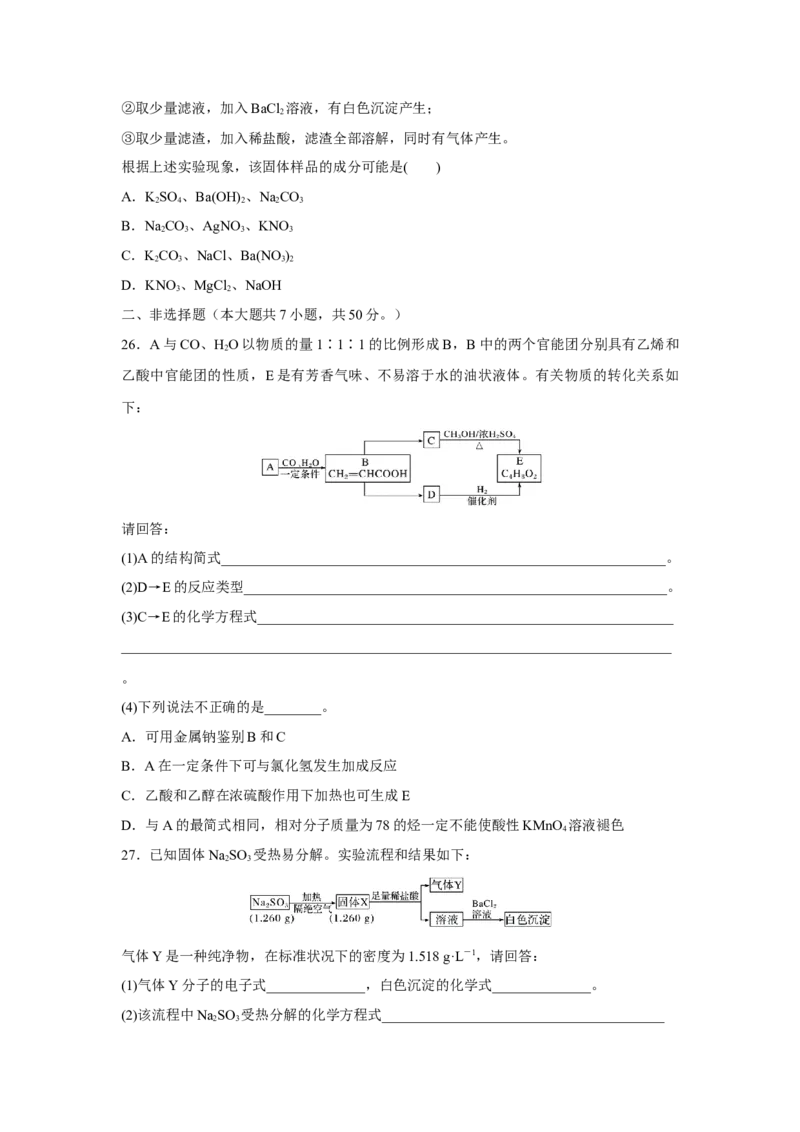
16.已知N(g)+3H(g) 2NH (g) ΔH=-92.4 kJ·mol-1,起始反应物为N 和H,物质
2 2 3 2 2
的量之比为1∶3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中
NH 的物质的量分数如下表:
3
下列说法正确的是( )
A.体系中NH 的物质的量分数越大,则正反应速率越大
3
B.反应达到平衡时,N 和H 的转化率之比均为1
2 2
C.反应达到平衡时,放出的热量均为92.4 kJ
D.600 ℃、30 MPa下反应达到平衡时,生成NH 的物质的量最多
3
17.金属(M)空气电池的工作原理如图所示。下列说法不正确的是( )
A.金属M作电池负极
B.电解质是熔融的MO
C.正极的电极反应O+4e-+2HO===4OH-
2 2D.电池反应2M+O+2HO===2M(OH)
2 2 2
18.下列说法不正确的是( )
A.pH<7的溶液不一定呈酸性
B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
C.在相同温度下,pH相等的盐酸、CHCOOH溶液,c(Cl-)=c(CHCOO-)
3 3
D.氨水和盐酸反应后的溶液,若c(Cl-)=c(NH),则溶液呈中性
19.根据Ca(OH) /CaO体系的能量循环图:
2
下列说法正确的是( )
A.ΔH>0
5
B.ΔH+ΔH=0
1 2
C.ΔH=ΔH+ΔH
3 4 5
D.ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5
20.下列说法不正确的是( )
A.Mg2+和S2-的最外电子层都形成8个电子的稳定结构
B.石英和金刚石都是原子间通过共价键结合形成的原子晶体
C.浓HSO 与HO混合时放出热量与微粒之间的作用力有关
2 4 2
D.HO 易分解是因为HO 分子间作用力弱
2 2 2 2
21.在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙
醇转化的物质的量的比值)随温度、乙醇进料量(单位:mL·min-1)的关系如图所示(保持其他
条件相同)。
在410~440 ℃温度范围内,下列说法不正确的是( )
A.当乙醇进料量一定,随乙醇转化率增大,乙烯选择性升高
B.当乙醇进料量一定,随温度的升高,乙烯选择性不一定增大C.当温度一定,随乙醇进料量增大,乙醇转化率减小
D.当温度一定,随乙醇进料量增大,乙烯选择性增大
22.设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.含0.2 mol HSO 的浓硫酸与足量的镁反应,转移电子数大于0.2N
2 4 A
B.25 ℃时,pH=3的醋酸溶液1 L,溶液中含H+的数目小于0.001N
A
C.任意条件下,1 mol苯中含有C—H键的数目一定为6N
A
D.a mol的R2+(R的核内中子数为N,质量数为A)的核外电子数为a(A-N-2)N
A
23.25 ℃时,在“HA—HA-—A2-”的水溶液体系中,HA、HA-和A2-三者中各自所占
2 2
的物质的量分数(α)随溶液pH变化的关系如图所示。
下列说法正确的是( )
A.在含HA、HA-和A2-的溶液中,加入少量NaOH固体,α(HA-)一定增大
2
B.将等物质的量的NaHA和NaA混合物溶于水,所得的溶液中α(HA-)=α(A2-)
2
C.NaHA溶液中,HA-的水解能力小于HA-的电离能力
D.在含HA、HA-和A2-的溶液中,若c(H A)+2c(A2-)+c(OH-)=c(H+),则α(H A)和
2 2 2
α(HA-)一定相等
24.某兴趣小组查阅资料得知:连苯三酚的碱性溶液能定量吸收O;CuCl的盐酸溶液能定
2
量吸收CO,且易被O 氧化。拟设计实验方案,采用上述两种溶液和KOH溶液逐一吸收混
2
合气体(由CO 、CO、N 和O 组成)的相应组分。有关该方案设计,下列说法不正确的是(
2 2 2
)
A.采用上述3种吸收剂,气体被逐一吸收的顺序应该是CO、O 和CO
2 2
B.其他两种吸收剂不变,O 的吸收剂可以用灼热的铜网替代
2
C.CO的吸收必须在吸收O 后进行,因为CuCl的盐酸溶液会被O 氧化
2 2
D.在3种气体被逐一吸收后,导出的气体中可能含有HCl
25.取某固体样品,进行如下实验:
①取一定量的样品,加足量水充分溶解,过滤得到滤液和滤渣;②取少量滤液,加入BaCl 溶液,有白色沉淀产生;
2
③取少量滤渣,加入稀盐酸,滤渣全部溶解,同时有气体产生。
根据上述实验现象,该固体样品的成分可能是( )
A.KSO 、Ba(OH) 、NaCO
2 4 2 2 3
B.NaCO、AgNO、KNO
2 3 3 3
C.KCO、NaCl、Ba(NO )
2 3 3 2
D.KNO、MgCl 、NaOH
3 2
二、非选择题(本大题共7小题,共50分。)
26.A与CO、HO以物质的量1∶1∶1的比例形成B,B中的两个官能团分别具有乙烯和
2
乙酸中官能团的性质,E是有芳香气味、不易溶于水的油状液体。有关物质的转化关系如
下:
请回答:
(1)A的结构简式_______________________________________________________________。
(2)D→E的反应类型____________________________________________________________。
(3)C→E的化学方程式___________________________________________________________
______________________________________________________________________________
。
(4)下列说法不正确的是________。
A.可用金属钠鉴别B和C
B.A在一定条件下可与氯化氢发生加成反应
C.乙酸和乙醇在浓硫酸作用下加热也可生成E
D.与A的最简式相同,相对分子质量为78的烃一定不能使酸性KMnO 溶液褪色
4
27.已知固体NaSO 受热易分解。实验流程和结果如下:
2 3
气体Y是一种纯净物,在标准状况下的密度为1.518 g·L-1,请回答:
(1)气体Y分子的电子式______________,白色沉淀的化学式______________。
(2)该流程中NaSO 受热分解的化学方程式________________________________________
2 3______________________________________________________________________________
。
(3)另取固体X试样和NaSO 混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生,写出
2 3
产 生 淡 黄 色 沉 淀 的 离 子 方 程 式
________________________________________________________
_______________________________________________________________________________
_
(不考虑空气的影响)。
28.为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。
已知:3Fe(s)+4HO(g)=====Fe O(s)+4H(g)
2 3 4 2
请回答:
(1)虚线框处宜选择的装置是______(填“甲”或“乙”);实验时应先将螺旋状铜丝加热,
变 黑 后 再 趁 热 迅 速 伸 入 所 制 得 的 纯 净 氢 气 中 , 观 察 到 的 实 验 现 象 是
_________________________
_______________________________________________________________________________
。
(2)实验后,取硬质玻璃管中适量的固体,用一定浓度的盐酸溶解,滴加 KSCN溶液,没有
出现血红色,说明该固体中没有+3 价的铁,判断结论是否正确并说明理由
__________________
_______________________________________________________________________________
。
29.取7.90 g KMnO,加热分解后剩余固体7.42 g。该剩余固体与足量的浓盐酸在加热条件
4
下充分反应,生成单质气体A,产物中锰元素以Mn2+存在。
请计算:
(1)KMnO 的分解率________。
4
(2)气体A的物质的量________。
30.[加试题](10分)(一)十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C H )→四氢
10 18萘(C H )→萘(C H)”的脱氢过程释放氢气。已知:
10 12 10 8
C H (l) C H (l)+3H(g) ΔH
10 18 10 12 2 1
C H (l) C H(l)+2H(g) ΔH
10 12 10 8 2 2
ΔH >ΔH >0,C H →C H 的活化能为E ,C H →C H 的活化能为E ,十氢萘的常
1 2 10 18 10 12 a1 10 12 10 8 a2
压沸点为192 ℃;在192 ℃,液态十氢萘脱氢反应的平衡转化率约为9%。
请回答:
(1)有利于提高上述反应平衡转化率的条件是______________________________。
A.高温高压 B.低温低压
C.高温低压 D.低温高压
(2)研究表明,将适量十氢萘置于恒容密闭反应器中,升高温度带来高压,该条件下也可显
著 释 氢 , 理 由 是
____________________________________________________________________
_______________________________________________________________________________
_
_______________________________________________________________________________
。
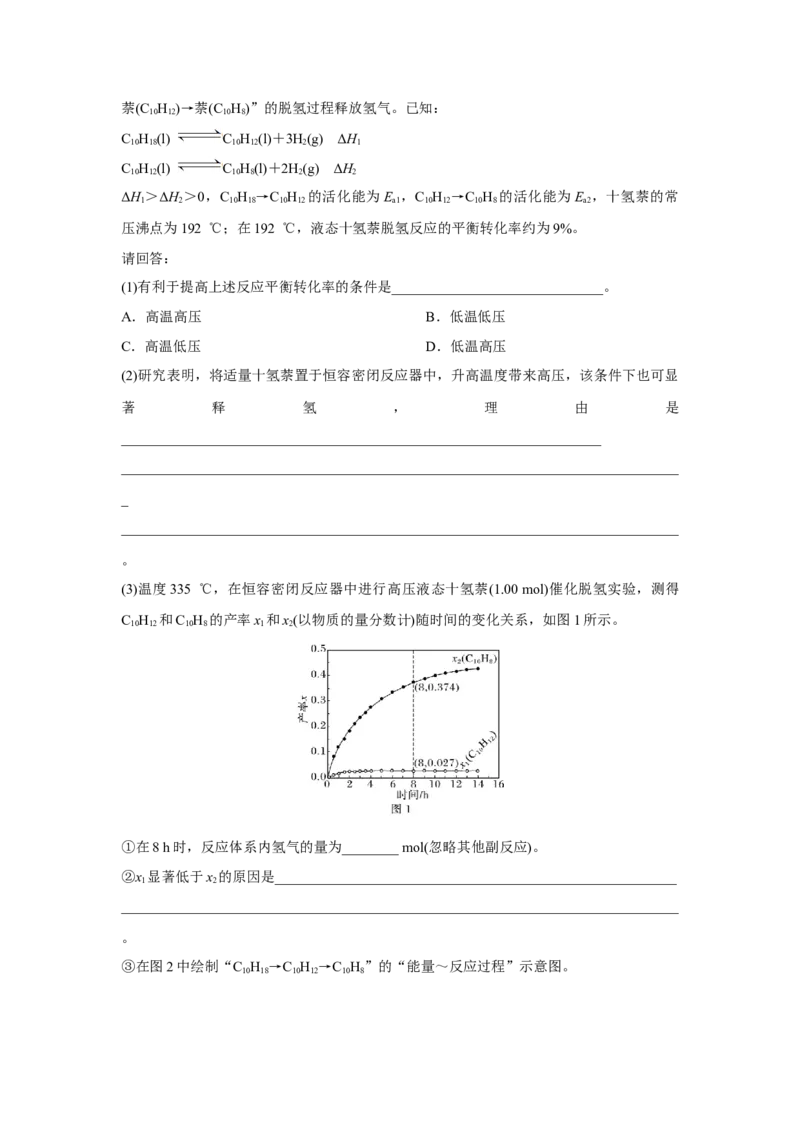
(3)温度335 ℃,在恒容密闭反应器中进行高压液态十氢萘(1.00 mol)催化脱氢实验,测得
C H 和C H 的产率x 和x(以物质的量分数计)随时间的变化关系,如图1所示。
10 12 10 8 1 2
①在8 h时,反应体系内氢气的量为________ mol(忽略其他副反应)。
②x 显著低于x 的原因是_________________________________________________________
1 2
_______________________________________________________________________________
。
③在图2中绘制“C H →C H →C H”的“能量~反应过程”示意图。
10 18 10 12 10 8(二)科学家发现,以HO和N 为原料,熔融NaOH—KOH为电解质,纳米Fe O 作催化剂,
2 2 2 3
在250 ℃和常压下可实现电化学合成氨。阴极区发生的变化可视为按两步进行。
请补充完整。
电极反应式:__________________________________________________________________
和
2Fe+3HO+N===2NH +Fe O。
2 2 3 2 3
31.[加试题](10分)某兴趣小组用铝箔制备Al O 、AlCl ·6H O及明矾大晶体,具体流程如
2 3 3 2
下:
已知:AlCl ·6H O易溶于水、乙醇及乙醚;明矾在水中的溶解度如下表
3 2
温度/℃ 0 10 20 30 40 60 80 90
溶解度/g 3.00 3.99 5.90 8.39 11.7 24.8 71.0 109
请回答:
(1)步骤Ⅰ中的化学方程式___________________________________________________
________________________________________________________________________;
步骤Ⅱ中生成Al(OH) 的离子方程式____________________________________________
3
___________________________________________________________________________。
(2)步骤Ⅲ,下列操作合理的是________。
A.坩埚洗净后,无需擦干,即可加入Al(OH) 灼烧
3
B.为了得到纯Al O,需灼烧至恒重
2 3
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,燃烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序________。
①迅速降至室温 ②用玻璃棒摩擦器壁 ③配制90 ℃的明矾饱和溶液 ④自然冷却至室温
⑤选规则明矾小晶体并悬挂在溶液中央 ⑥配制高于室温10~20 ℃的明矾饱和溶液
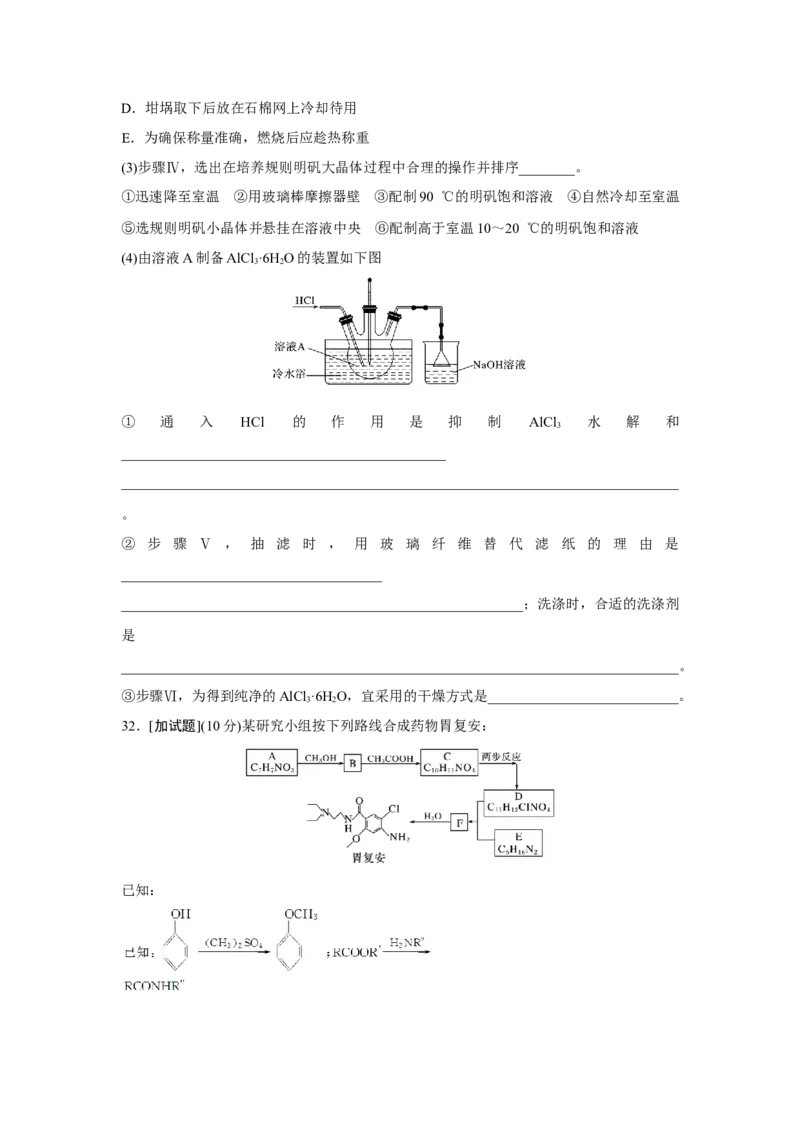
(4)由溶液A制备AlCl ·6H O的装置如下图
3 2
① 通 入 HCl 的 作 用 是 抑 制 AlCl 水 解 和
3
______________________________________________
_______________________________________________________________________________
。
② 步 骤 Ⅴ , 抽 滤 时 , 用 玻 璃 纤 维 替 代 滤 纸 的 理 由 是
_____________________________________
_________________________________________________________;洗涤时,合适的洗涤剂
是
_______________________________________________________________________________。
③步骤Ⅵ,为得到纯净的AlCl ·6H O,宜采用的干燥方式是___________________________。
3 2
32.[加试题](10分)某研究小组按下列路线合成药物胃复安:
已知:请回答:
(1)化合物A的结构简式________。
(2)下列说法不正确的是________。
A.化合物B能发生加成反应
B.化合物D能与FeCl 溶液发生显色反应
3
C.化合物E具有碱性
D.胃复安的分子式是C H ClN O
13 22 3 2
(3)设计化合物C经两步反应转变为D的合成路线(用流程图表示,试剂任选)________。
(4) 写 出 D + E→F 的 化 学 方 程 式
_____________________________________________________
_______________________________________________________________________________
。
(5) 写 出 化 合 物 E 可 能 的 同 分 异 构 体 的 结 构 简 式
_______________________________________
_______________________________________________________________________________
,
须同时符合:①1HNMR谱表明分子中有3种氢原子,IR谱显示有N—H键存在;②分子
中没有同一个碳上连两个氮 的结构。