文档内容
2020 海南化学高考真题 D. 选用适宜催化剂可达到尾气排放标准
一、选择题:本题共 8小题,每小题 2分,共 16 分。在每小题给出的四个选项中,只有一项是符合 7. 向CuSO 4 溶液中滴加氨水至过量,下列叙述正确的是
题目要求的。 A. 先出现沉淀,后沉淀溶解变为无色溶液
B. 离子方程式为Cu2+ + 4NH ·H O = [Cu(NH ) ]2+ + 4H O
1. 化学科学与社会活动密切相关。下述措施应积极推广的是 3 2 3 4 2
C. Cu2+与 NH 中的氮原子以π键结合
3
A. 在抗击新冠肺炎疫情斗争中,提高环境友好无残留消毒剂的使用比例
D. NH 分子中∠HNH为109º28ˊ
3
B. 原料药生产厂通过蒸发与焚烧过程,处理其生产废液
8. N 代表阿伏加德罗常数的值。下列说法正确的是
A
C. 海边建筑工程施工,就近取海水海沙生产混凝土 A. 1molHC≡CH分子中所含σ键数为5 N
A
D. 为保证食物的口感与风味,增加食品添加剂使用品种与数量 B. 1L0.1 mol·L-1的Na CO 溶液含CO2的数目为0.1 N
2 3 3 A
C. 78 g Na O 与足量水完全反应,电子转移数为N
2. 古籍《天工开物》收录了井盐的生产过程。其中“汲水而上,入于釜中煎炼,顷刻结盐,色成至白”的描述, 2 2 A
D. 标准状况下,2.24 L C H OH所含氢原子数为0.6 N
涉及的物质分离操作为 2 5 A
二、选择题:本题共 6小题,每小题 4分,共 24 分。每小题有一个或两个选项符合题意。
A 趁热过滤 B. 萃取分液 C. 常压蒸馏 D. 浓缩结晶
.
若正确答案只包括一个选项, 多选得 0分;若正确答案包括两个选项,只选一个且正确得 2分,选
3. 下列叙述正确的是 两个且都正确得 4分,但只要选错一个就得 0分。
A. HClO 的结构式为H-Cl-O B. 核内有33个中子的Fe表示为33Fe 9. 含有下列有害组分的尾气,常用NaOH溶液吸收以保护环境。吸收过程中发生歧化反应的是
26
A. SO B. Cl C. NO D. HBr
3 2 2
C. NH OH的电子式为 D. CH CHO 的球棍模型为
2 3 10. 姜黄素是我国古代劳动人民从姜黄根茎中提取得到的一种黄色食用色素。下列关于姜黄素说法正确的是
4. 实验室制备下列气体,能实现的是
A. Cl :MnO 与稀HCl溶液混合 B. C H :CaC 与H O混合
2 2 2 4 2 2
C. CO :加热饱和NaHCO 溶液 D. SO :Cu丝与稀H SO 混合
2 3 2 2 4
A. 分子式为C H O
21 22 6
5. 下列说法错误的是
B. 分子中存在手性碳原子
A. 新榨油脂不及时干燥脱水易变质 B. 聚氯乙烯可制作食品内包装材料
C. 分子中存在3种含氧官能团
C. 维生素C可作预包装食品抗氧剂 D. 卤水点豆腐本质属于蛋白质聚沉
D. 既能发生取代反应,又能发生加成反应
6. NO与CO是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
11. 某燃料电池主要构成要素如图所示,下列说法正确的是
1
CO(g)+ NO(g)=CO (g)+ N (g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确的是
2 2
2
A. K很大,NO与CO在排入大气之前就已反应完全
B. 增大压强,平衡将向右移动,K> 2.5×1060
C. 升高温度,既增大反应速率又增大K操作或方法 实验目的
A 向未知弱酸性试液中滴加含有SCN- 的溶液 确证试液中Fe2+存在
B
等体积0.1 mol·L-1Ag+和[Ag(NH ) ]+溶液分别与大 判断多步过程中, 分步反
3 2
量1 mol·L-1葡萄糖碱性溶液形成银镜 应速率与浓度的关系
A. 电池可用于乙醛的制备
B. b电极为正极
C
稀H SO 酸化n(KBrO ): n(KBr)= 1 :5的混合液
2 4 3
C. 电池工作时,a电极附近pH降低 降低液溴的贮存与使用风险
替代溴水
D. a电极的反应式为O +4e- -4H+ =2H O
2 2
D
12. 某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法错误的是 向0.1 mol·L-1 Na 2 S 2 O 3 溶液中缓慢滴加0.2 mol·L-1 由浑浊情况测定单质硫的溶
盐酸 解度
A. A B. B C. C D. D
三、非选择题:共 5题,60分。
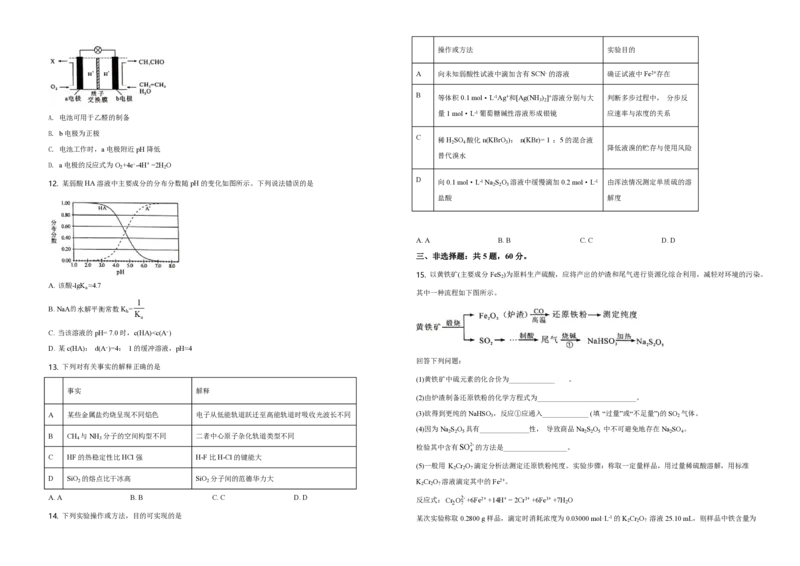
15. 以黄铁矿(主要成分FeS )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。
2
A. 该酸-lgK ≈4.7
a
其中一种流程如下图所示。
1
B. NaA的水解平衡常数K =
h K
a
C. 当该溶液的pH= 7.0时,c(HA)