文档内容
重庆乌江新高考协作体 2025 届高考质量调研(一)
化学试题
(分数:100分,时间:75分钟)
一、选择题
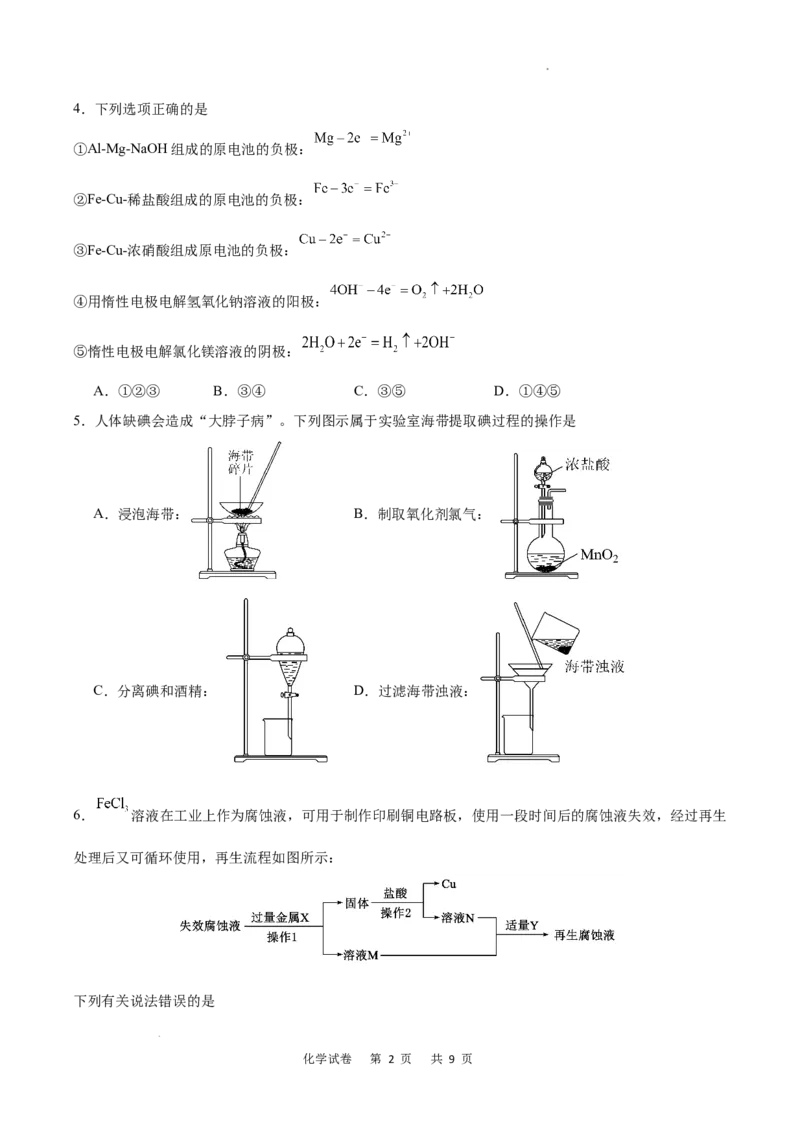
1.下列文物是重庆中国三峡博物馆的馆藏,其材质的主要成分为有机物的是
A B C D
A.战国巴蜀鸟纹铜戈 B.明代夔柄玉匜
C.明代何朝宗制观音像 D.明代嘉靖竹雕人物船
2.下列离子方程式错误的是
A.在含 的废水中加入 :
B.在亚硝化细菌作用下将 转化为 :
C.一定条件下用 处理 :
D.化学法中,可能发生反应:
3.直径为几十纳米的纳米金颗粒具有高电子密度和介电特性,它的一种制备方法是氯金酸 与硼
氢化钠(化学式为 ,B显+3价)反应: = 。
下列有关说法错误的是
A.纳米金分散在空气中形成的分散系属于胶体 B.硼氢化钠为还原剂
C.氧化产物为 和 D.每生成 ,转移 电子
化学试卷 第 1 页 共 9 页
学科网(北京)股份有限公司4.下列选项正确的是
①Al-Mg-NaOH组成的原电池的负极:
②Fe-Cu-稀盐酸组成的原电池的负极:
③Fe-Cu-浓硝酸组成原电池的负极:
④用惰性电极电解氢氧化钠溶液的阳极:
⑤惰性电极电解氯化镁溶液的阴极:
A.①②③ B.③④ C.③⑤ D.①④⑤
5.人体缺碘会造成“大脖子病”。下列图示属于实验室海带提取碘过程的操作是
A.浸泡海带: B.制取氧化剂氯气:
C.分离碘和酒精: D.过滤海带浊液:
6. 溶液在工业上作为腐蚀液,可用于制作印刷铜电路板,使用一段时间后的腐蚀液失效,经过再生
处理后又可循环使用,再生流程如图所示:
下列有关说法错误的是
化学试卷 第 2 页 共 9 页
学科网(北京)股份有限公司A.金属X最合适的是
B.在实验室中,操作1和操作2使用的主要玻璃仪器有漏斗、烧杯、玻璃棒
C.向溶液M中加入 溶液,溶液变红色
D.Y通常为 ,加入适量Y发生反应的离子方程式为
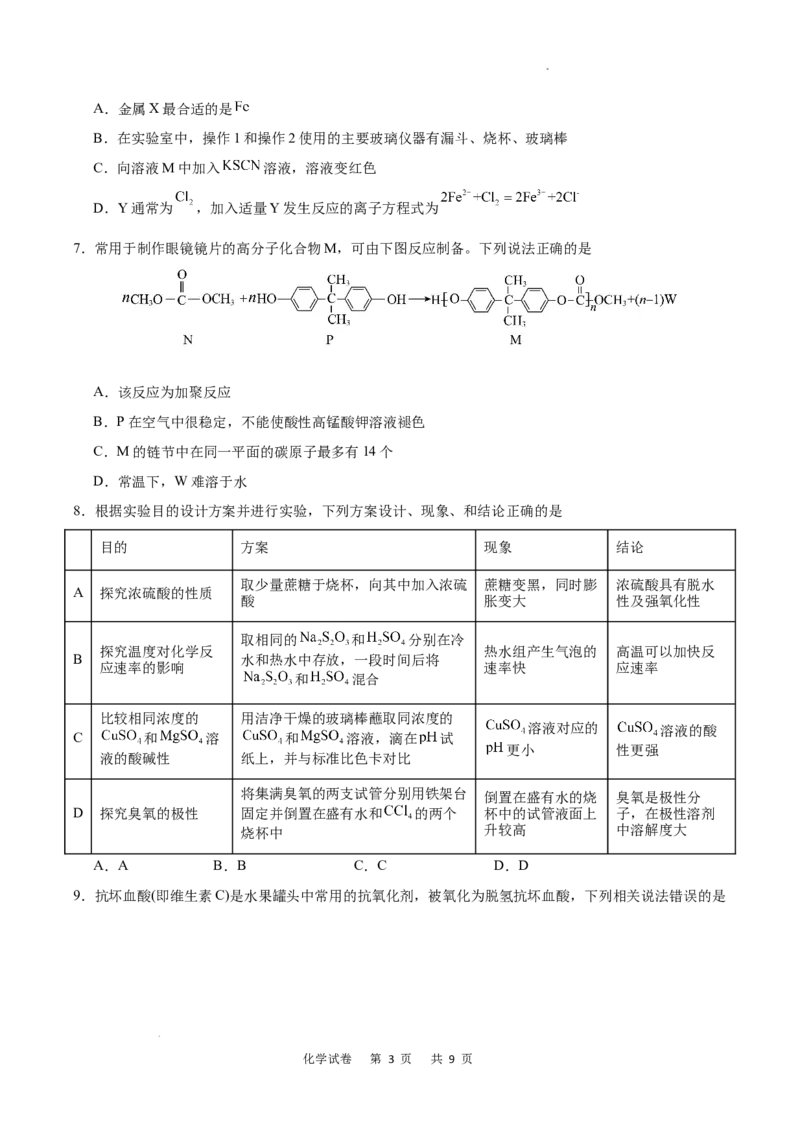
7.常用于制作眼镜镜片的高分子化合物M,可由下图反应制备。下列说法正确的是
A.该反应为加聚反应
B.P在空气中很稳定,不能使酸性高锰酸钾溶液褪色
C.M的链节中在同一平面的碳原子最多有14个
D.常温下,W难溶于水
8.根据实验目的设计方案并进行实验,下列方案设计、现象、和结论正确的是
目的 方案 现象 结论
取少量蔗糖于烧杯,向其中加入浓硫 蔗糖变黑,同时膨 浓硫酸具有脱水
A 探究浓硫酸的性质
酸 胀变大 性及强氧化性
取相同的 和 分别在冷
探究温度对化学反 热水组产生气泡的 高温可以加快反
B 水和热水中存放,一段时间后将
应速率的影响 速率快 应速率
和 混合
比较相同浓度的 用洁净干燥的玻璃棒蘸取同浓度的
溶液对应的 溶液的酸
C 和 溶 和 溶液,滴在 试
更小 性更强
液的酸碱性 纸上,并与标准比色卡对比
将集满臭氧的两支试管分别用铁架台 倒置在盛有水的烧 臭氧是极性分
D 探究臭氧的极性 固定并倒置在盛有水和 的两个 杯中的试管液面上 子,在极性溶剂
烧杯中 升较高 中溶解度大
A.A B.B C.C D.D
9.抗坏血酸(即维生素C)是水果罐头中常用的抗氧化剂,被氧化为脱氢抗坏血酸,下列相关说法错误的是
化学试卷 第 3 页 共 9 页
学科网(北京)股份有限公司A.抗坏血酸分子中,碳原子中仅4、5、6号连有氢原子
B.氧化前后官能团种类减少
C.抗坏血酸可发生加成、取代、氧化等反应
D.脱氢抗坏血酸在碱性溶液中不能稳定存在
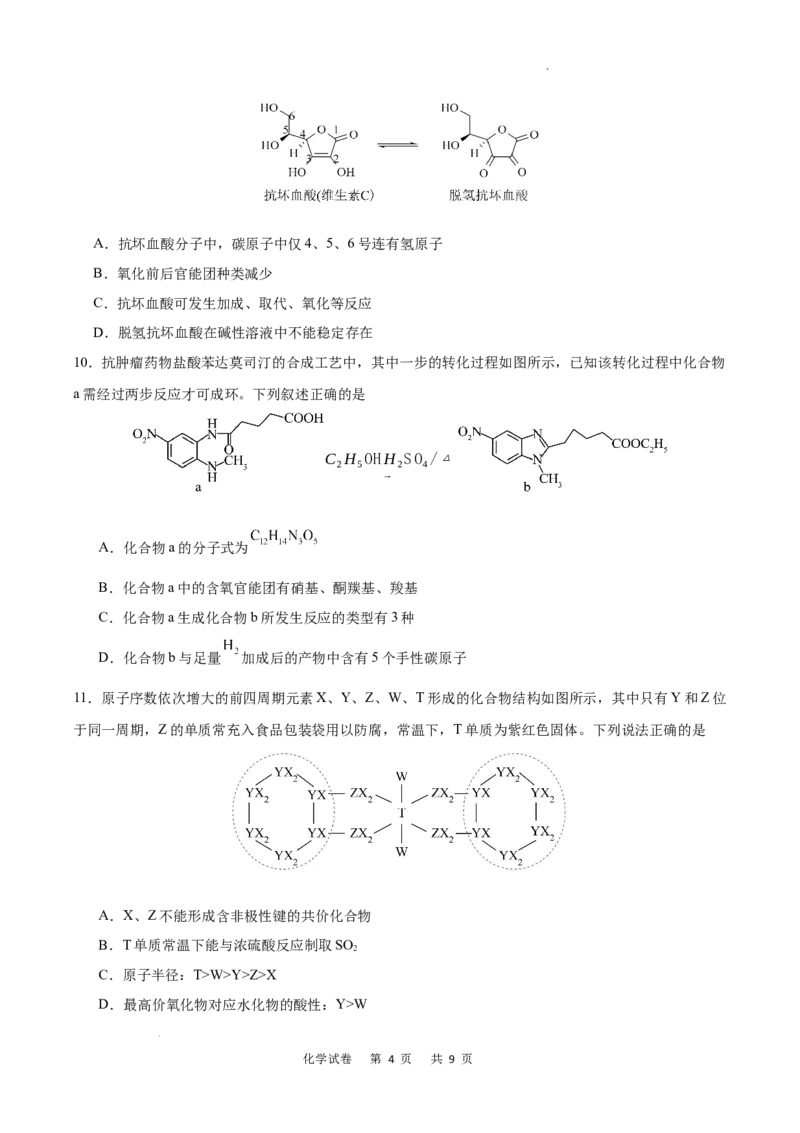
10.抗肿瘤药物盐酸苯达莫司汀的合成工艺中,其中一步的转化过程如图所示,已知该转化过程中化合物
a需经过两步反应才可成环。下列叙述正确的是
C H OHH SO /△
2 5 2 4
→
A.化合物a的分子式为
B.化合物a中的含氧官能团有硝基、酮羰基、羧基
C.化合物a生成化合物b所发生反应的类型有3种
D.化合物b与足量 加成后的产物中含有5个手性碳原子
11.原子序数依次增大的前四周期元素X、Y、Z、W、T形成的化合物结构如图所示,其中只有Y和Z位
于同一周期,Z的单质常充入食品包装袋用以防腐,常温下,T单质为紫红色固体。下列说法正确的是
A.X、Z不能形成含非极性键的共价化合物
B.T单质常温下能与浓硫酸反应制取SO
2
C.原子半径:T>W>Y>Z>X
D.最高价氧化物对应水化物的酸性:Y>W
化学试卷 第 4 页 共 9 页
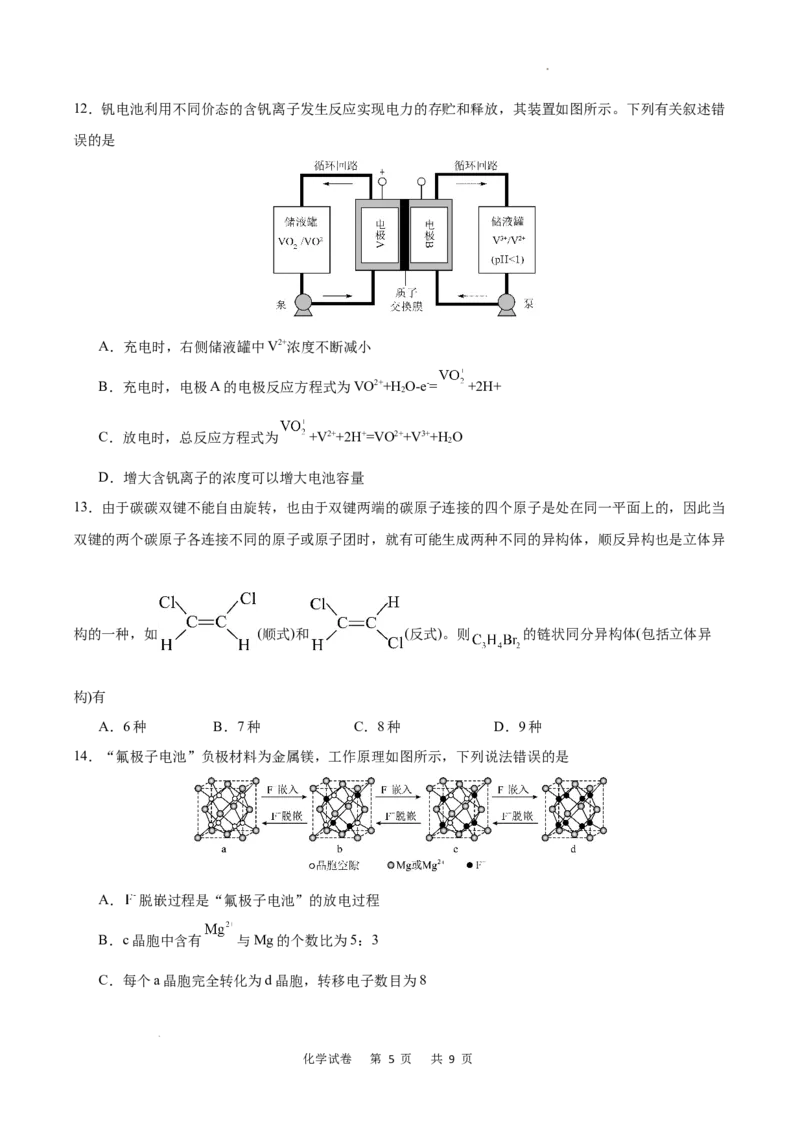
学科网(北京)股份有限公司12.钒电池利用不同价态的含钒离子发生反应实现电力的存贮和释放,其装置如图所示。下列有关叙述错
误的是
A.充电时,右侧储液罐中V2+浓度不断减小
B.充电时,电极A的电极反应方程式为VO2++H O-e-= +2H+
2
C.放电时,总反应方程式为 +V2++2H+=VO2++V3++H O
2
D.增大含钒离子的浓度可以增大电池容量
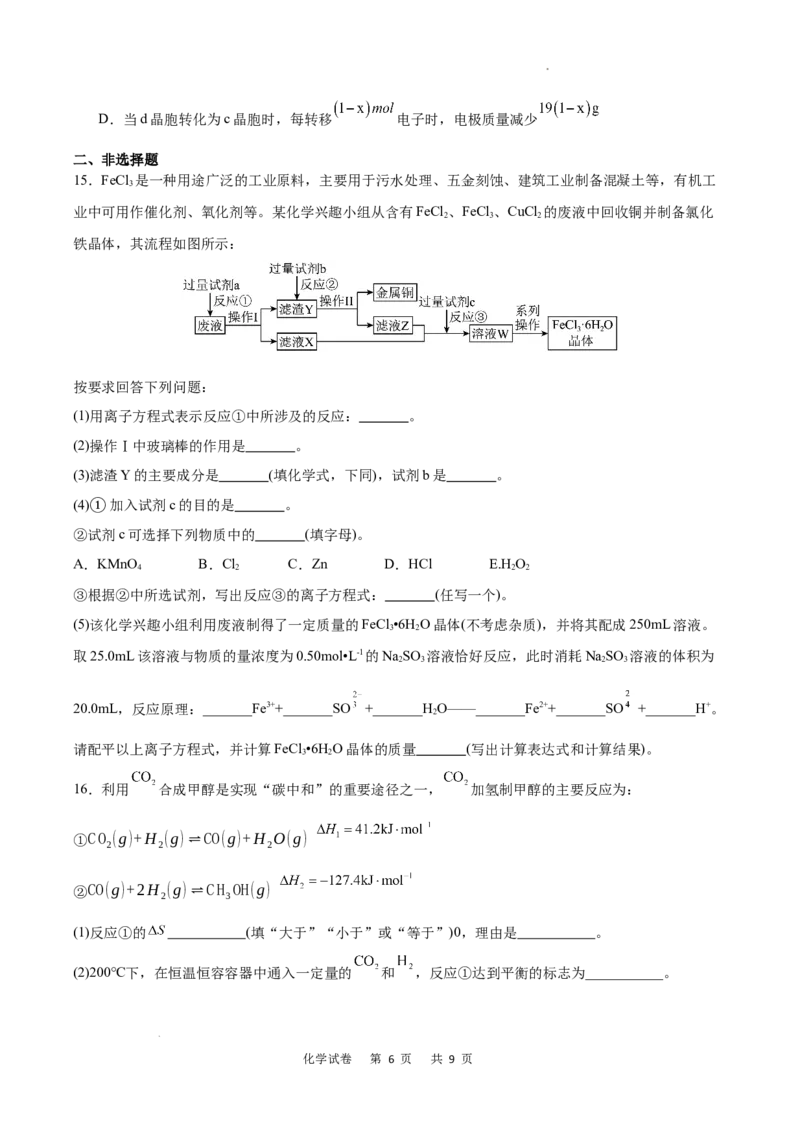
13.由于碳碳双键不能自由旋转,也由于双键两端的碳原子连接的四个原子是处在同一平面上的,因此当
双键的两个碳原子各连接不同的原子或原子团时,就有可能生成两种不同的异构体,顺反异构也是立体异
构的一种,如 (顺式)和 (反式)。则 的链状同分异构体(包括立体异
构)有
A.6种 B.7种 C.8种 D.9种
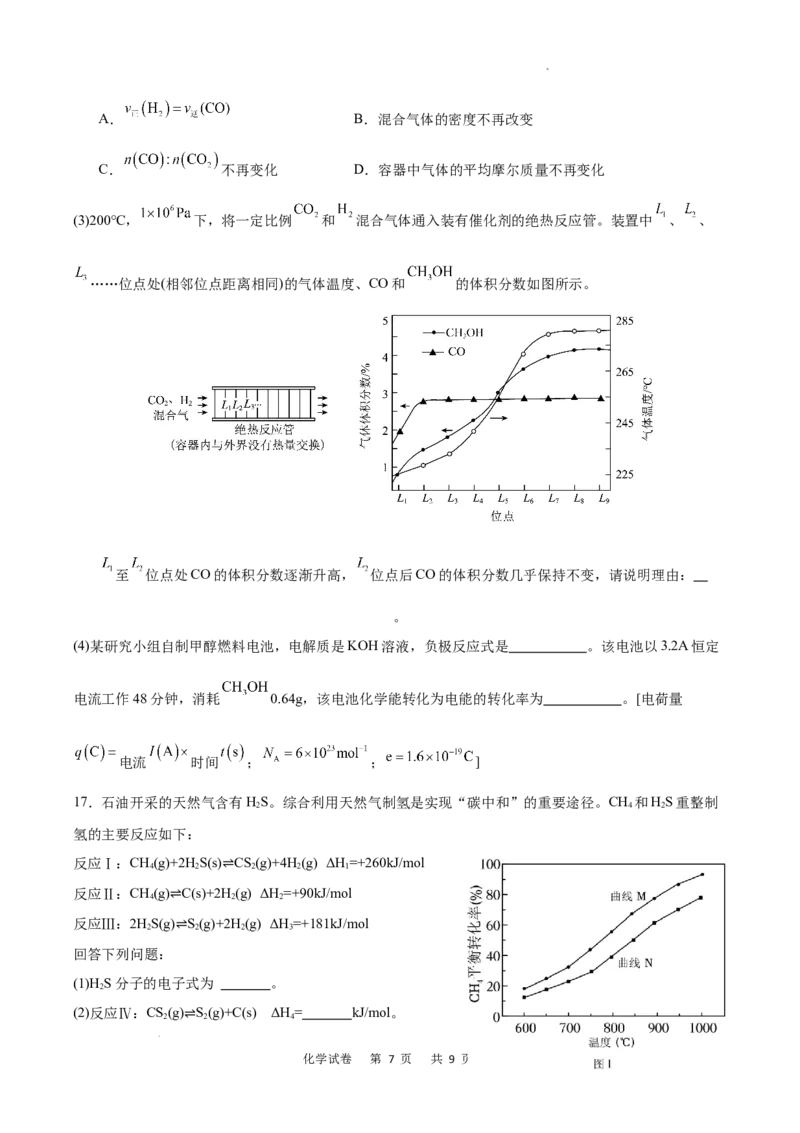
14.“氟极子电池”负极材料为金属镁,工作原理如图所示,下列说法错误的是
A. 脱嵌过程是“氟极子电池”的放电过程
B.c晶胞中含有 与Mg的个数比为5:3
C.每个a晶胞完全转化为d晶胞,转移电子数目为8
化学试卷 第 5 页 共 9 页
学科网(北京)股份有限公司D.当d晶胞转化为c晶胞时,每转移 电子时,电极质量减少
二、非选择题
15.FeCl 是一种用途广泛的工业原料,主要用于污水处理、五金刻蚀、建筑工业制备混凝土等,有机工
3
业中可用作催化剂、氧化剂等。某化学兴趣小组从含有FeCl 、FeCl 、CuCl 的废液中回收铜并制备氯化
2 3 2
铁晶体,其流程如图所示:
按要求回答下列问题:
(1)用离子方程式表示反应①中所涉及的反应: 。
(2)操作Ⅰ中玻璃棒的作用是 。
(3)滤渣Y的主要成分是 (填化学式,下同),试剂b是 。
(4) 加入试剂c的目的是 。
②试①剂c可选择下列物质中的 (填字母)。
A.KMnO B.Cl C.Zn D.HCl E.H O
4 2 2 2
③根据②中所选试剂,写出反应③的离子方程式: (任写一个)。
(5)该化学兴趣小组利用废液制得了一定质量的FeCl •6H O晶体(不考虑杂质),并将其配成250mL溶液。
3 2
取25.0mL该溶液与物质的量浓度为0.50mol•L-1的NaSO 溶液恰好反应,此时消耗NaSO 溶液的体积为
2 3 2 3
20.0mL,反应原理:_______Fe3++_______SO +_______H O——_______Fe2++_______SO +_______H+。
2
请配平以上离子方程式,并计算FeCl •6H O晶体的质量 (写出计算表达式和计算结果)。
3 2
16.利用 合成甲醇是实现“碳中和”的重要途径之一, 加氢制甲醇的主要反应为:
①CO (g)+H (g)⇌ CO(g)+H O(g)
2 2 2
②CO(g)+2H (g)⇌ CH OH(g)
2 3
(1)反应①的 (填“大于”“小于”或“等于”)0,理由是 。
(2)200℃下,在恒温恒容容器中通入一定量的 和 ,反应①达到平衡的标志为___________。
化学试卷 第 6 页 共 9 页
学科网(北京)股份有限公司A. B.混合气体的密度不再改变
C. 不再变化 D.容器中气体的平均摩尔质量不再变化
(3)200℃, 下,将一定比例 和 混合气体通入装有催化剂的绝热反应管。装置中 、 、
……位点处(相邻位点距离相同)的气体温度、CO和 的体积分数如图所示。
至 位点处CO的体积分数逐渐升高, 位点后CO的体积分数几乎保持不变,请说明理由:
。
(4)某研究小组自制甲醇燃料电池,电解质是KOH溶液,负极反应式是 。该电池以3.2A恒定
电流工作48分钟,消耗 0.64g,该电池化学能转化为电能的转化率为 。[电荷量
电流 时间 ; ; ]
17.石油开采的天然气含有HS。综合利用天然气制氢是实现“碳中和”的重要途径。CH 和HS重整制
2 4 2
氢的主要反应如下:
反应Ⅰ:CH(g)+2HS(s) CS(g)+4H(g) ΔH=+260kJ/mol
4 2 2 2 1
反应Ⅱ:CH(g) C(s)+2H⇌(g) ΔH=+90kJ/mol
4 2 2
反应Ⅲ:2HS(g⇌) S(g)+2H(g) ΔH=+181kJ/mol
2 2 2 3
回答下列问题:⇌
(1)H S分子的电子式为 。
2
(2)反应Ⅳ:CS(g) S(g)+C(s)ㅤΔH= kJ/mol。
2 2 4
⇌
化学试卷 第 7 页 共 9 页
学科网(北京)股份有限公司(3)保持反应器进料口总压为100kPa.分别以8kPaCH、24kPaHS(He作辅气)与25kPaCH、75kPaHS进料。
4 2 4 2
CH 平衡转化率与温度的关系如图1,含有He的曲线为
4
,理由是 。
(4)假设在10L的恒温刚性容器中,通入0.3mol CH 和
4
0.15mol H S发生反应Ⅰ、Ⅱ和Ⅲ,起始总压为P CH 和
2 0. 4
HS的转化率与时间的关系如图2,0~5min内H 的化学
2 2
反应速率为 mol/(L•min);5min时,容器内总压
为 。
(5)假设HS和CH 的混合气体在某固体催化剂上的吸附服从Langmuir等温吸附(吸附分子彼此不发生相互
2 4
作用,且气体分子为单分子层吸附)。吸附等温式为: 。其中a是气
体的吸附系数,V 是气体在固体表面的饱和吸附量(标态),P是气体的分压,V是气体分压为P时的平衡
m
吸附量(标态)。在一定温度下,HS的吸附系数是CH 的4倍,当HS的分压为2MPa及4MPa,CH 和
2 4 2 4
HS的分压相同时,HS平衡吸附量分别为0.6m3/kg和0.8m3/kg(已换算成标态),则HS的吸附系数为
2 2 2
MPa﹣1。
(6)与传统天然气制氢中需要脱硫将HS转化为硫黄和水相比,上述方法优点是 。
2
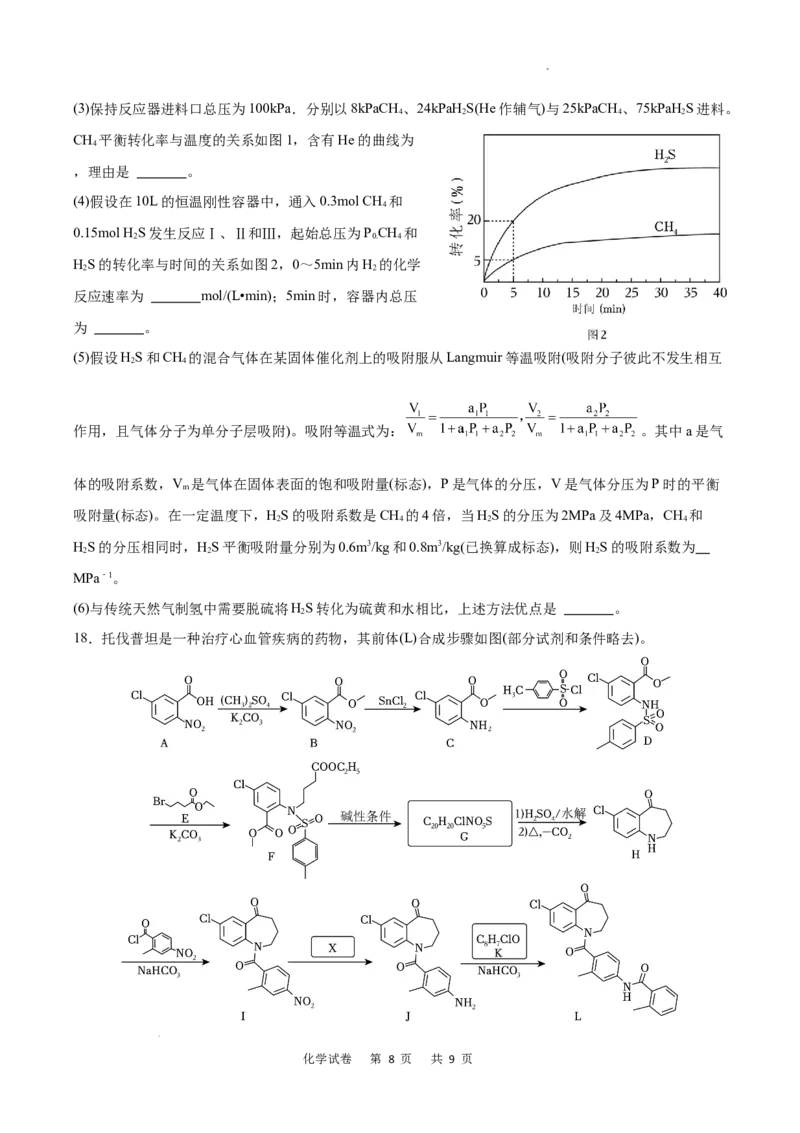
18.托伐普坦是一种治疗心血管疾病的药物,其前体(L)合成步骤如图(部分试剂和条件略去)。
化学试卷 第 8 页 共 9 页
学科网(北京)股份有限公司已知:
回答下列问题:(1)化合物A (填“能”或“不能”)形成分子内氢键。
(2)写出由C生成D的化学反应方程式 。(3)写出G的结构简式 。
(4)H到I的反应类型是 。(5)参照上述合成路线,试剂X的化学式是 。
(6)K完全水解后,有机产物的名称是 。
(7)E的消去产物(C H O)的同分异构体中,同时满足下列条件a、b和c的可能结构有 种(立体异
6 10 2
构中只考虑顺反异构);写出只满足下列条件a和c,不满足条件b的结构简式 (不考虑立体异构)。
a)能与饱和碳酸氢钠溶液反应产生CO;b)红外光谱中有碳碳双键特征吸收峰;c)核磁共振氢谱峰面积比
2
例为3 3 2 1 1。
∶ ∶ ∶ ∶
化学试卷 第 9 页 共 9 页
学科网(北京)股份有限公司