文档内容
机密★启用前
山西省 2025 年初中学业水平考试
化学
可能用到的相对原子质量:H-1 O-16 S-32 Zn-65
一、选择题(本大题共10个小题。每小题2分,共20分。在每小题给出的4个选项中,只有
1个选项符合题目要求,请选出并在答题卡上将该选项涂黑)
1. 城市生活垃圾主要分为厨余垃圾、可回收垃圾、有害垃圾和其他垃圾。出现在我们身边的有害垃圾是
A. 果皮菜叶 B. 过期药物 C. 废旧报纸 D. 陶瓷碎片
【答案】B
【解析】
A. 果皮菜叶:属于厨余垃圾,因其易腐烂分解,可用于堆肥;错误。
B. 过期药物:含有化学成分,随意丢弃可能污染环境或危害健康,属于有害垃圾;正确。
C. 废旧报纸:属于可回收垃圾,因废纸可回收再利用;错误。
D. 陶瓷碎片:属于其他垃圾,因不可回收且无害,通常填埋处理;错误。
故选B。
2. 以下是四种常见元素的元素符号,其中表示金属元素的是
A. B. S C. O D. C
【答案】A
【解析】
A. Ag为银元素的元素符号,带“钅”字旁,属于金属元素,故选项正确。
B. S为硫元素的元素符号,带“石”字旁,属于固态非金属元素,故选项错误。
C. O为氧元素的元素符号,带“气”字旁,属于非金属元素,故选项错误。
D. C为碳元素的元素符号,带“石”字旁,属于固态非金属元素,故选项错误。
故选A。
3. 某同学总结了食盐、纯碱、小苏打和碳酸钙的用途,其中错误的一项是
A. 食盐可用作调味品 B. 纯碱可治理盐碱地
C. 碳酸钙可作补钙剂 D. 小苏打可治疗胃酸过多
【答案】B
【解析】
A. 食盐的主要成分是氯化钠,在生活中常用作调味品,这是食盐的常见用途,正确。B. 盐碱地是土壤里含有过量盐分,而纯碱是碳酸钠,碳酸钠溶液呈碱性,若用纯碱治理盐碱地,会使土
壤碱性更强,不能治理盐碱地,错误。
C. 碳酸钙含有钙元素,能与胃酸(主要成分是盐酸 )反应生成可被人体吸收的氯化钙,所以可作补钙剂,
正确。
D. 小苏打是碳酸氢钠,碳酸氢钠能与胃酸中的盐酸反应,消耗盐酸,从而可治疗胃酸过多,正确。
故选B。
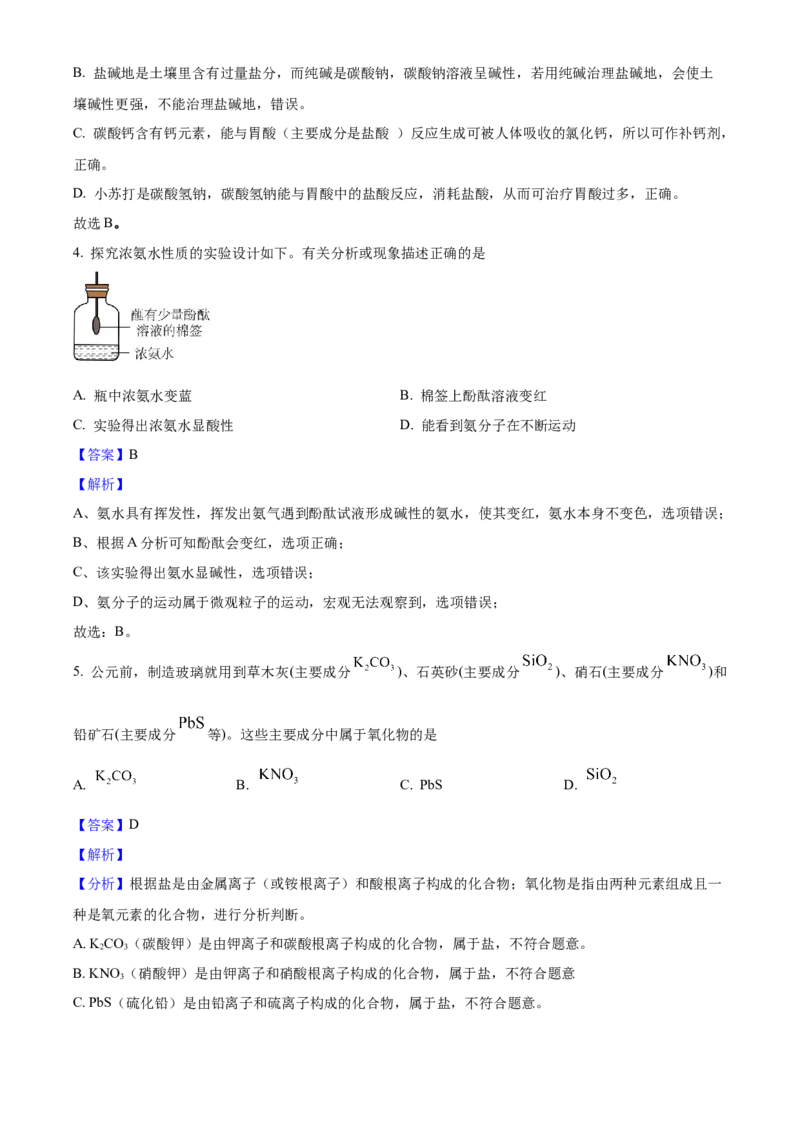
4. 探究浓氨水性质的实验设计如下。有关分析或现象描述正确的是
A. 瓶中浓氨水变蓝 B. 棉签上酚酞溶液变红
C. 实验得出浓氨水显酸性 D. 能看到氨分子在不断运动
【答案】B
【解析】
A、氨水具有挥发性,挥发出氨气遇到酚酞试液形成碱性的氨水,使其变红,氨水本身不变色,选项错误;
B、根据A分析可知酚酞会变红,选项正确;
C、该实验得出氨水显碱性,选项错误;
D、氨分子的运动属于微观粒子的运动,宏观无法观察到,选项错误;
故选:B。
5. 公元前,制造玻璃就用到草木灰(主要成分 )、石英砂(主要成分 )、硝石(主要成分 )和
铅矿石(主要成分 等)。这些主要成分中属于氧化物的是
A. B. C. PbS D.
【答案】D
【解析】
【分析】根据盐是由金属离子(或铵根离子)和酸根离子构成的化合物;氧化物是指由两种元素组成且一
种是氧元素的化合物,进行分析判断。
A. K CO(碳酸钾)是由钾离子和碳酸根离子构成的化合物,属于盐,不符合题意。
2 3
B. KNO (硝酸钾)是由钾离子和硝酸根离子构成的化合物,属于盐,不符合题意 。
3
C. PbS(硫化铅)是由铅离子和硫离子构成的化合物,属于盐,不符合题意。D. SiO (二氧化硅)是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,符合题意。
2
故选D。
的
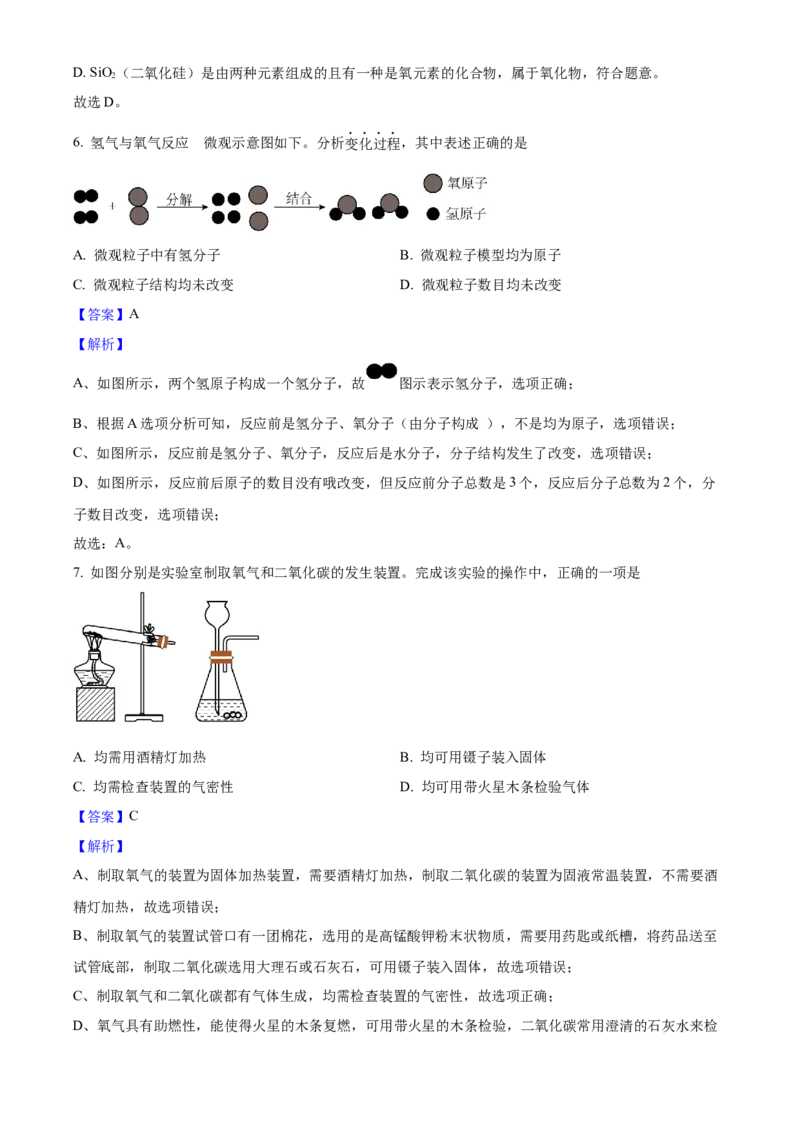
6. 氢气与氧气反应 微观示意图如下。分析变化过程,其中表述正确的是
A. 微观粒子中有氢分子 B. 微观粒子模型均为原子
C. 微观粒子结构均未改变 D. 微观粒子数目均未改变
【答案】A
【解析】
A、如图所示,两个氢原子构成一个氢分子,故 图示表示氢分子,选项正确;
B、根据A选项分析可知,反应前是氢分子、氧分子(由分子构成 ),不是均为原子,选项错误;
C、如图所示,反应前是氢分子、氧分子,反应后是水分子,分子结构发生了改变,选项错误;
D、如图所示,反应前后原子的数目没有哦改变,但反应前分子总数是3个,反应后分子总数为2个,分
子数目改变,选项错误;
故选:A。
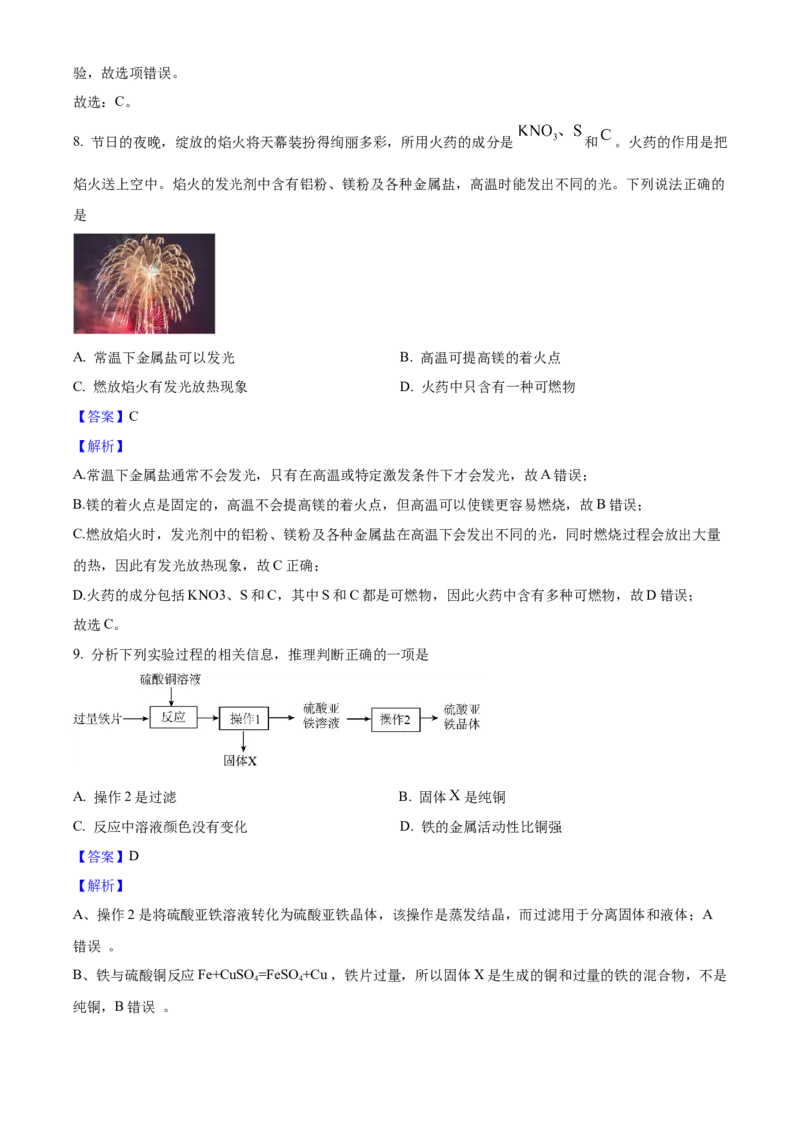
7. 如图分别是实验室制取氧气和二氧化碳的发生装置。完成该实验的操作中,正确的一项是
A. 均需用酒精灯加热 B. 均可用镊子装入固体
C. 均需检查装置的气密性 D. 均可用带火星木条检验气体
【答案】C
【解析】
A、制取氧气的装置为固体加热装置,需要酒精灯加热,制取二氧化碳的装置为固液常温装置,不需要酒
精灯加热,故选项错误;
B、制取氧气的装置试管口有一团棉花,选用的是高锰酸钾粉末状物质,需要用药匙或纸槽,将药品送至
试管底部,制取二氧化碳选用大理石或石灰石,可用镊子装入固体,故选项错误;
C、制取氧气和二氧化碳都有气体生成,均需检查装置的气密性,故选项正确;
D、氧气具有助燃性,能使得火星的木条复燃,可用带火星的木条检验,二氧化碳常用澄清的石灰水来检验,故选项错误。
故选:C。
8. 节日的夜晚,绽放的焰火将天幕装扮得绚丽多彩,所用火药的成分是 和 。火药的作用是把
焰火送上空中。焰火的发光剂中含有铝粉、镁粉及各种金属盐,高温时能发出不同的光。下列说法正确的
是
A. 常温下金属盐可以发光 B. 高温可提高镁的着火点
C. 燃放焰火有发光放热现象 D. 火药中只含有一种可燃物
【答案】C
【解析】
A.常温下金属盐通常不会发光,只有在高温或特定激发条件下才会发光,故A错误;
B.镁的着火点是固定的,高温不会提高镁的着火点,但高温可以使镁更容易燃烧,故B错误;
C.燃放焰火时,发光剂中的铝粉、镁粉及各种金属盐在高温下会发出不同的光,同时燃烧过程会放出大量
的热,因此有发光放热现象,故C正确;
D.火药的成分包括KNO3、S和C,其中S和C都是可燃物,因此火药中含有多种可燃物,故D错误;
故选C。
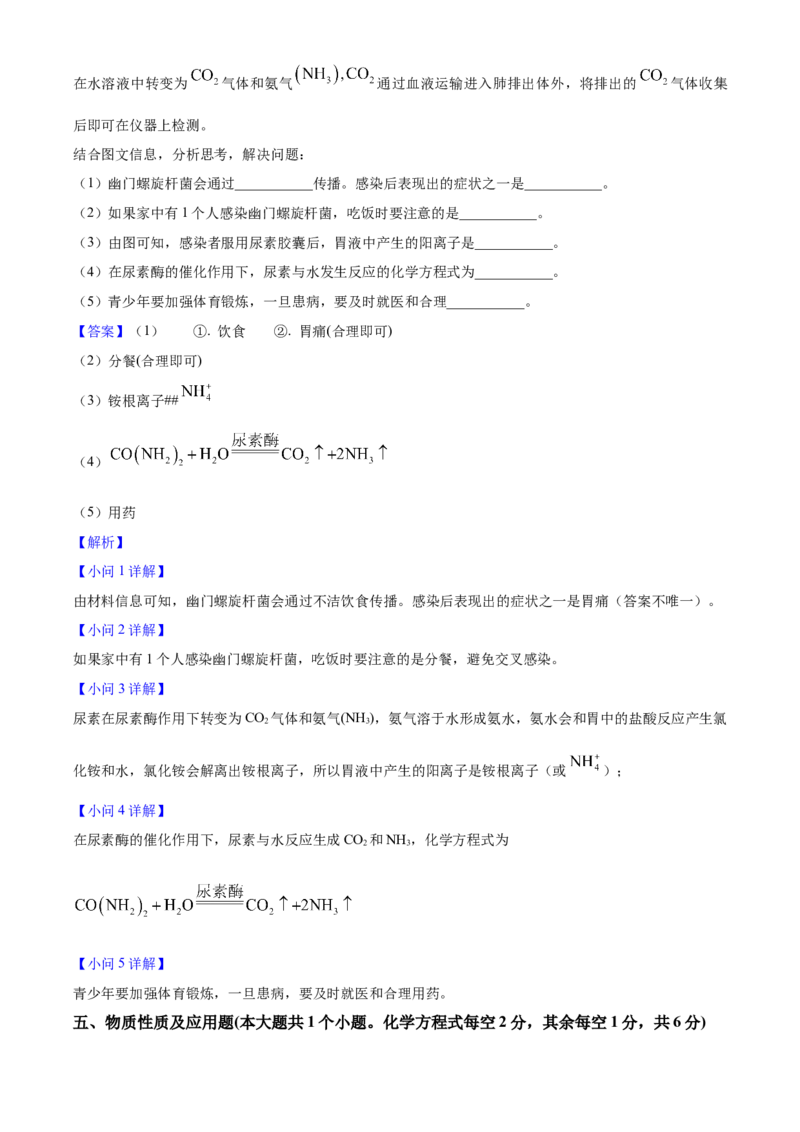
9. 分析下列实验过程的相关信息,推理判断正确的一项是
A. 操作2是过滤 B. 固体 是纯铜
C. 反应中溶液颜色没有变化 D. 铁的金属活动性比铜强
【答案】D
【解析】
A、操作2是将硫酸亚铁溶液转化为硫酸亚铁晶体,该操作是蒸发结晶,而过滤用于分离固体和液体;A
错误 。
B、铁与硫酸铜反应Fe+CuSO=FeSO+Cu ,铁片过量,所以固体X是生成的铜和过量的铁的混合物,不是
4 4
纯铜,B错误 。C、硫酸铜溶液是蓝色的,反应生成的硫酸亚铁溶液是浅绿色的,溶液颜色发生了变化。
D、铁能与硫酸铜溶液发生置换反应,根据金属活动性顺序,在金属活动性顺序里,位于前面的金属能把
位于后面的金属从它们化合物的溶液里置换出来,说明铁的金属活动性比铜强,D正确 。
故选D 。
10. 不同温度时 的溶解度如下表所示。下列分析正确的是
温度/℃ 0 10 20 30 40 50 60
31. 40.
溶解度/g 27.6 34.0 37.0 42.6 45.5
0 0
A. 20℃时, 的溶解度为34.0
B. 30℃时, 水中加入 ,所得溶液质量为
C. 40℃时, 饱和溶液的溶质质量分数为40%
D. 将 溶液由60℃冷却到50℃,可能有晶体析出
【答案】D
【解析】
A、由表格数据可知,20℃时, 的溶解度为34.0g,说法错误,不符合题意;
B、由表格数据可知,30℃时, 的溶解度为37.0g,则30℃时, 水中加入 ,最多能溶解
氯化钾,则充分溶解后所得溶液质量为 ,说法错误,不符合题意;
C、由表格数据可知,40℃时, 的溶解度为40.0g,则40℃时, 饱和溶液的溶质质量分数为
,说法错误,不符合题意;
D、将 溶液由60℃冷却到50℃,由于没有明确氯化钾溶液是否饱和,所以可能有晶体析出,说
法正确,符合题意。故选:D。
化学部分
可能用到的相对原子质量:H-1 O-16 S-32 Zn-65
三、工程、资源应用题(本大题共5个小题。化学方程式每空2分,其余每空1分,共16分)
【化学与工程】
11. 三峡工程是目前世界上规模最大的水利枢纽和清洁能源基地。作为一项伟大工程,其意义和价值体现
在防洪减灾、发电供电、生态补水、节能减排、改善通航条件和促进地方经济发展等诸多方面。
结合相关信息,完成下面小题 的问题:
(1)图1是三峡大坝。高坝根基为完整的花岗岩体,透水性极其微弱,这种地质结构的优点是
___________,大坝浇筑时,混凝土用量达2689万吨、钢材25.5万吨、钢筋29万吨,这些材料中钢筋的
作用是___________。三峡工程建设,有效地防御了___________的发生,保障了长江中下游人民生命财产
的安全。
(2)图2是三峡水力发电示意图。三峡电站是目前世界上规模最大的清洁能源基地,其能量转化方式是
___________。截至2024年12月,三峡工程累计完成发电量超过1.7万亿千瓦时,有效缓解了华中、华东
及广东、四川等地区的供电紧张局面,促进了全国电网的互联互通。通过学习我们知道,能用于发电的可
再生能源还有___________。
(3)图3是三峡景区。三峡工程实施了“两岸青绿·千里林带”建设,“千里林带”对保护生态环境所起
的作用是___________。“心驰神往山水间,醉美三峡在眼前”,游客在三峡景区进行船游活动、尽赏美
景的同时,从环保的角度应该做到___________。
(4)三峡电站的建设,相当于替代了7座260万千瓦火电站,节约了大量的标准煤,大大减少了
___________和二氧化硫等污染物的排放。生成二氧化硫的化学方程式为___________。
【答案】
(1) ①. 防止水的渗漏,增强大坝的稳定性和安全性 ②. 增强混凝土的强度 ③. 洪涝灾害
(2) ①. 水能转化为电能 ②. 太阳能、风能
(3) ①. 防止水土流失、改善空气质量 ②. 不乱扔垃圾(4) ①. CO、烟尘 ②.
【解析】
【小问1详解】
高坝根基为完整的花岗岩体,透水性极其微弱,这种地质结构的优点是防止渗漏。钢筋的作用是增强混凝
土的强度。三峡工程建设,有效地防御了洪水的发生,保障了长江中下游人民生命财产的安全;
【小问2详解】
三峡电站是目前世界上规模最大的清洁能源基地,其能量转化方式是将水能转化为电能。截至2024年12
月,三峡工程累计完成发电量超过1.7万亿千瓦时,有效缓解了华中、华东及广东、四川等地区的供电紧
张局面,促进了全国电网的互联互通。通过学习我们知道,能用于发电的可再生能源还有风能、太阳能。
【小问3详解】
三峡工程实施了“两岸青绿•千里林带”建设,“千里林带”对保护生态环境所起的作用是保持水土、净
化空气。“心驰神往山水间,醉美三峡在眼前”,游客在三峡景区进行船游活动、尽赏美景的同时,从环
保的角度应该做到不乱扔垃圾、不破坏植被。故答案为:保持水土、净化空气;不乱扔垃圾、不破坏植被。
【小问4详解】
三峡电站的建设,相当于替代了7座260万千瓦火电站,节约了大量的标准煤,大大减少了一氧化碳、烟
尘和二氧化硫等污染物的排放;煤中的硫在氧气中燃烧生成二氧化硫,化学方程式为 。
【化学与资源】
12. 我国有超过一半的地区处于严重缺水状态,故改善水资源空间分布不均、防治水环境污染和杜绝水资
源浪费等问题显得尤为重要。请联系实际,解决问题:
(1)改善水资源空间分布不均。长江流域及其以南地区,水资源量占全国80%以上,北方不足20%。我
国统筹水资源的一种做法是___________。
(2)防治水环境污染。随着工业化和城市化进程的推进,预防水体污染的措施有___________。2006年,
某船只运输浓硫酸时不慎泄漏,当地迅速采取措施,用常见的实验用品___________检测河水的酸碱度,
并用熟石灰中和水体中的硫酸,该过程发生反应的化学方程式为___________。
的
(3)杜绝水资源浪费。家庭中,用水浪费 现象有___________。因此,要从我做起,树立节约用水的意
识。
【答案】
(1)南水北调(2) ①. 污水处理达标后再排放 ②. 试纸 ③.
(3)不随手关闭水龙头、洗菜水没有二次利用
【解析】
【小问1详解】
我国统筹水资源的一种做法是南水北调;
【小问2详解】
预防水体污染的措施:污水处理达标后再排放;
用常见的实验用品 试纸检测河水的酸碱度,并用熟石灰中和水体中的硫酸,熟石灰是氢氧化钙的俗称,
氢氧化钙与硫酸反应生成硫酸钙和水,化学方程式为 ;
【小问3详解】
家庭中,用水浪费的现象有:不随手关闭水龙头、洗菜水没有二次利用等。
四、科普阅读题(本大题共1个小题。化学方程式每空2分,其余每空1分,共7分)
化学与健康
13. 幽门螺旋杆菌是一种主要寄生于人体胃部及十二指肠内的细菌。就餐时会通过饮食等途径传播,若家
中有1个人感染幽门螺旋杆菌且不分餐,其他家人就很容易被传染。当人体通过各种日常不洁饮食等途径
感染后,幽门螺旋杆菌就会在胃黏膜定植,引发一系列的健康隐患。
有些国家几乎90%的人都感染过这种细菌,感染后如不及时治疗,可能会导致胃痛、胃胀、口臭、食欲不
振等症状。
在用C-13呼吸检测幽门螺旋杆菌时,受检者要空腹口服C-13尿素胶囊,静坐约30分钟,之后将呼出的气
体吹入气袋中,交给医生检测。如果胃中有幽门螺旋杆菌,其产生的尿素酶能迅速将尿素在水溶液中转变为 气体和氨气 通过血液运输进入肺排出体外,将排出的 气体收集
后即可在仪器上检测。
结合图文信息,分析思考,解决问题:
(1)幽门螺旋杆菌会通过___________传播。感染后表现出的症状之一是___________。
(2)如果家中有1个人感染幽门螺旋杆菌,吃饭时要注意的是___________。
(3)由图可知,感染者服用尿素胶囊后,胃液中产生的阳离子是___________。
(4)在尿素酶的催化作用下,尿素与水发生反应的化学方程式为___________。
(5)青少年要加强体育锻炼,一旦患病,要及时就医和合理___________。
【答案】(1) ①. 饮食 ②. 胃痛(合理即可)
(2)分餐(合理即可)
(3)铵根离子##
(4)
(5)用药
【解析】
【小问1详解】
由材料信息可知,幽门螺旋杆菌会通过不洁饮食传播。感染后表现出的症状之一是胃痛(答案不唯一)。
【小问2详解】
如果家中有1个人感染幽门螺旋杆菌,吃饭时要注意的是分餐,避免交叉感染。
【小问3详解】
尿素在尿素酶作用下转变为CO 气体和氨气(NH ),氨气溶于水形成氨水,氨水会和胃中的盐酸反应产生氯
2 3
化铵和水,氯化铵会解离出铵根离子,所以胃液中产生的阳离子是铵根离子(或 );
【小问4详解】
在尿素酶的催化作用下,尿素与水反应生成CO 和NH ,化学方程式为
2 3
【小问5详解】
青少年要加强体育锻炼,一旦患病,要及时就医和合理用药。
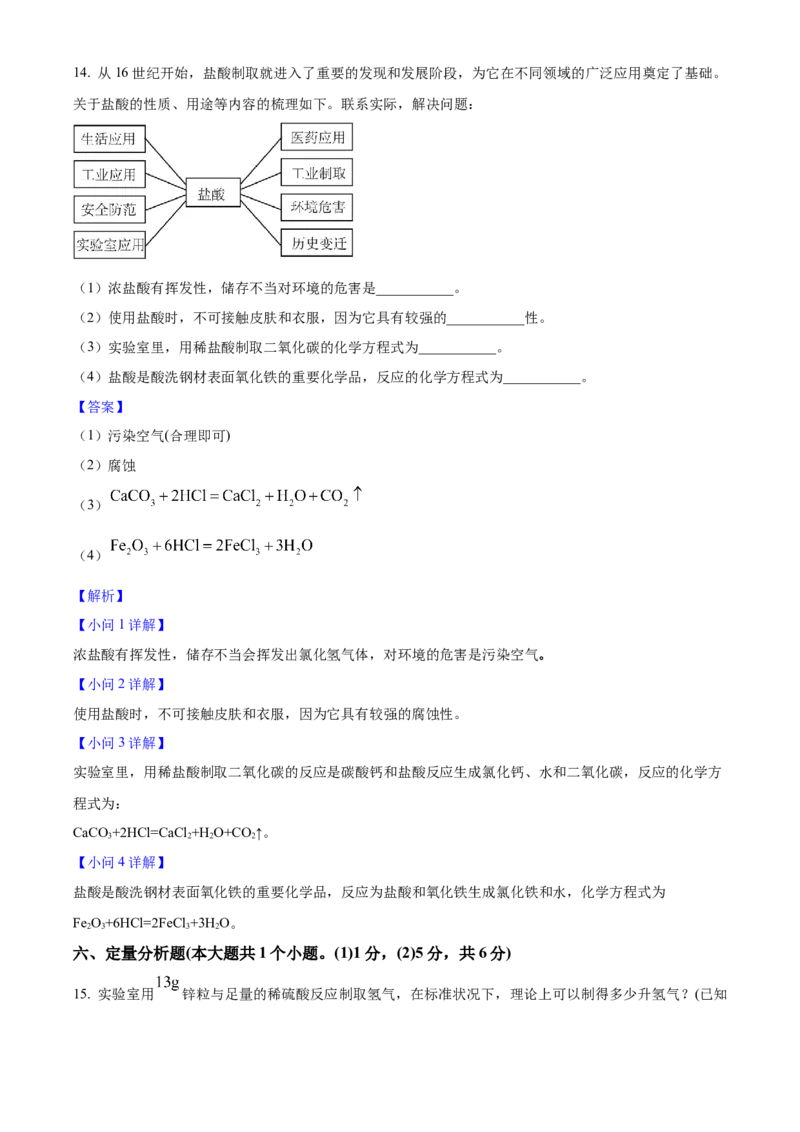
五、物质性质及应用题(本大题共1个小题。化学方程式每空2分,其余每空1分,共6分)14. 从16世纪开始,盐酸制取就进入了重要的发现和发展阶段,为它在不同领域的广泛应用奠定了基础。
关于盐酸的性质、用途等内容的梳理如下。联系实际,解决问题:
(1)浓盐酸有挥发性,储存不当对环境的危害是___________。
(2)使用盐酸时,不可接触皮肤和衣服,因为它具有较强的___________性。
(3)实验室里,用稀盐酸制取二氧化碳的化学方程式为___________。
(4)盐酸是酸洗钢材表面氧化铁的重要化学品,反应的化学方程式为___________。
【答案】
(1)污染空气(合理即可)
(2)腐蚀
(3)
(4)
【解析】
【小问1详解】
浓盐酸有挥发性,储存不当会挥发出氯化氢气体,对环境的危害是污染空气。
【小问2详解】
使用盐酸时,不可接触皮肤和衣服,因为它具有较强的腐蚀性。
【小问3详解】
实验室里,用稀盐酸制取二氧化碳的反应是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方
程式为:
CaCO +2HCl=CaCl +H O+CO↑。
3 2 2 2
【小问4详解】
盐酸是酸洗钢材表面氧化铁的重要化学品,反应为盐酸和氧化铁生成氯化铁和水,化学方程式为
Fe O+6HCl=2FeCl +3H O。
2 3 3 2
六、定量分析题(本大题共1个小题。(1)1分,(2)5分,共6分)
15. 实验室用 锌粒与足量的稀硫酸反应制取氢气,在标准状况下,理论上可以制得多少升氢气?(已知标准状况下,氢气的密度约为0.09g/L)
(1)反应前后,氢元素的化合价___________(填“改变”或“不变”)。……
(2)根据题目要求,完成计算过程(计算结果保留一位小数)。
【答案】
(1)改变
(2)解:设生成氢气的质量为
答:生成氢气的体积为 。
【解析】
【小问1详解】
硫酸中氢元素显+1价,单质中元素的化合价为0,H 属于单质,故氢元素的化合价为0,则反应前后,氢
2
元素的化合价改变。
【小问2详解】
见答案。
七、科学探究题(本大题共2个小题。化学方程式每空2分,其余每空1分,共15分)
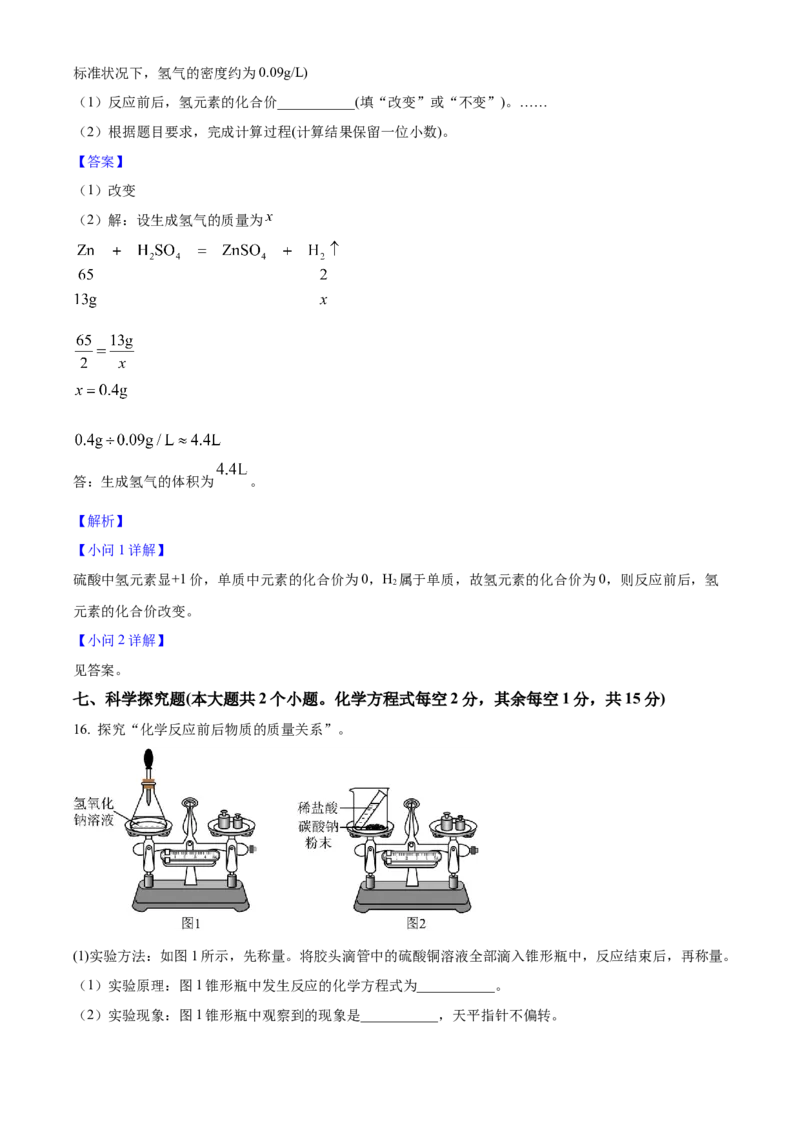
16. 探究“化学反应前后物质的质量关系”。
(1)实验方法:如图1所示,先称量。将胶头滴管中的硫酸铜溶液全部滴入锥形瓶中,反应结束后,再称量。
(1)实验原理:图1锥形瓶中发生反应的化学方程式为___________。
(2)实验现象:图1锥形瓶中观察到的现象是___________,天平指针不偏转。(3)实验结论:___________。
【问题与思考】
(4)如图2所示进行实验,反应结束后再称量,烧杯中物质的质量变化是___________。
(5)比较上述两个实验,利用图2化学反应设计实验时,应注意的问题是___________。
【答案】
(1)
(2)产生蓝色沉淀
(3)化学反应前后物质的质量相等(或不变)(合理即可)
(4)减小##变小
(5)在密闭容器中进行/有气体参加或生成的化学反应在密闭容器中进行
【解析】
【小问1详解】
图1中是氢氧化钠溶液与硫酸铜溶液反应,生成氢氧化铜蓝色沉淀和硫酸钠,化学方程式为
;
【小问2详解】
氢氧化钠与硫酸铜反应,会观察到产生蓝色沉淀,因为生成了氢氧化铜蓝色沉淀。
【小问3详解】
图1锥形瓶中氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,观察到的现象是产生蓝色沉淀,天平指
针不偏转,即化学反应前后物质的质量相等(或不变)(合理即可) 。
【小问4详解】
稀盐酸和碳酸钠反应生成二氧化碳气体,反应过程中二氧化碳气体逸出,烧杯中的物质质量减少,导致天
平不平衡,则反应结束后再称量,烧杯中物质的质量变化是减小。
【小问5详解】
图2实验因有气体生成且逸出,导致质量变化不能验证质量守恒定律。所以利用有气体参与或生成的化学
反应设计实验验证质量守恒定律时,应注意在密闭装置中进行,或有气体参加或生成的化学反应在密闭容
器中进行 。
17. “基于碳中和理念设计低碳行动方案”是跨学科实践活动的一个重要内容。在老师的统一安排下,同
学们围绕以下四项任务进行方案设计,并对有关问题进行思考和探究。
任务一:理解碳中和内涵
【查阅资料】简言之,碳中和是指通过节能减排、植树造林等措施,抵消人类活动产生的 ,达到相对“零排放”。
【构建模型】固碳是实现碳中和的重要途径之一,小组同学构建的固碳模型如下:
【小组讨论】
(1)生态固碳主要依靠植物的___________实现。
(2)捕集工业排放的 制成干冰,它可用于___________。
任务二:探究二氧化碳捕集
【提出问题】氢氧化钠溶液能吸收 吗?
【进行实验】
(3)小组同学设计如下方案并完成实验。
实验步骤 实验现象 实验结论
①向盛有 气体的塑料瓶中,加入适量氢氧化钠
___________
溶液,立即旋紧瓶盖,振荡 氢氧化钠溶液能
捕集
②取少量步骤①所得溶液于试管中,滴加几滴 产生白色沉
___________,振荡 淀
【反思评价】
(4)步骤①中发生反应的化学方程式为___________。
(5)步骤②实验目的是___________。
任务三:设计低碳行动方案
【调研访谈】同学们将收集到的低碳措施整理成表。
【创意设计】
(6)在老师指导下,同学们优化方案如下:
低碳途径 个人行为 国家工程 国际合作
减少 排放 ___________ 加快能源转型 推动技术转移与共享
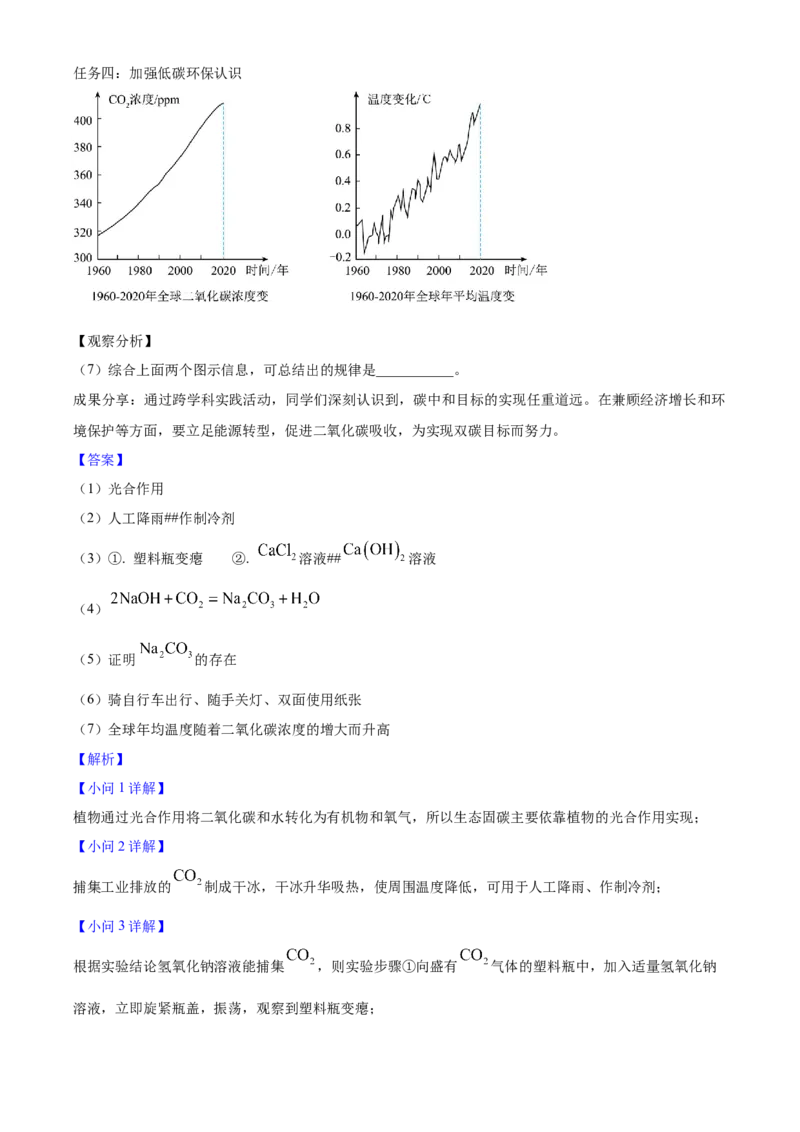
增加 吸收 种花、种树等 积极实施碳汇 多国共同参与森林保护任务四:加强低碳环保认识
【观察分析】
(7)综合上面两个图示信息,可总结出的规律是___________。
成果分享:通过跨学科实践活动,同学们深刻认识到,碳中和目标的实现任重道远。在兼顾经济增长和环
境保护等方面,要立足能源转型,促进二氧化碳吸收,为实现双碳目标而努力。
【答案】
(1)光合作用
(2)人工降雨##作制冷剂
(3)①. 塑料瓶变瘪 ②. 溶液## 溶液
(4)
(5)证明 的存在
(6)骑自行车出行、随手关灯、双面使用纸张
(7)全球年均温度随着二氧化碳浓度的增大而升高
【解析】
【小问1详解】
植物通过光合作用将二氧化碳和水转化为有机物和氧气,所以生态固碳主要依靠植物的光合作用实现;
【小问2详解】
捕集工业排放的 制成干冰,干冰升华吸热,使周围温度降低,可用于人工降雨、作制冷剂;
【小问3详解】
根据实验结论氢氧化钠溶液能捕集 ,则实验步骤①向盛有 气体的塑料瓶中,加入适量氢氧化钠
溶液,立即旋紧瓶盖,振荡,观察到塑料瓶变瘪;根据实验结论氢氧化钠溶液能捕集 ,二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠能与氯化钙反
应生成碳酸钙白色沉淀,则实验步骤②取少量步骤①所得溶液于试管中,滴加几滴氯化钙溶液,观察到产
生白色沉淀;
【小问4详解】
步骤①中发生的反应是二氧化碳与氢氧化钠反应生成碳酸钠和水,化学方程式为
;
【小问5详解】
步骤②实验目的是证明 的存在;
【小问6详解】
从个人行为方面减少 排放的途径:骑自行车出行、随手关灯、双面使用纸张等;
【小问7详解】
观察两个图示可知,从 1960-2020 年,随着全球二氧化碳浓度不断升高,全球年均温度总体也呈上升趋势。
所以可总结出的规律是:全球年均温度随着二氧化碳浓度的增大而升高(答案不唯一)