文档内容
2008年全国统一高考化学试卷(全国卷Ⅰ)
一、第Ⅰ卷选择题(在每小题给出的四个选项中,只有一项是符合题目要求的.)
1.(3分)在溶液中加入足量Na O 后仍能大量共存的离子组是( )
2 2
A.NH +、Ba2+、Cl﹣、NO ﹣ B.K+、AlO ﹣、Cl﹣、SO 2﹣
4 3 2 4
C.Ca2+、Mg2+、NO ﹣、HCO ﹣ D.Na+、Cl﹣、CO 2﹣、SO 2﹣
3 3 3 3 C. D.
2.(3分)下列化合物,按其晶体的熔点由高到低排列正确的是( )
7.(3分)已知HX的酸性比HY弱,在物质的量浓度均为0.1mol•L﹣1的NaX和NaY混合溶液中,
A.SiO 、CsCl、CBr 、CF B.SiO 、CsCl、CF 、CBr
2 4 4 2 4 4
下列排序正确的是( )
C.CsCl、SiO 、CBr 、CF D.CF 、CBr 、CsCl、SiO
2 4 4 4 4 2 A.c(OH﹣)>c(HX)>c(HY)>c(H+)
3.(3分)下列各组物质不属于同分异构体的是( )
B.c(OH﹣)>c(X﹣)>c(Y﹣)>c(H+)
A.2,2﹣二甲基丙醇和2﹣甲基丁醇
C.c(OH﹣)>c(Y﹣)>c(X﹣)>c(H+)
B.邻氯甲苯和对氯甲苯
D.c(OH﹣)>c(HY)>c(HX)>c(H+)
C.2﹣甲基丁烷和戊烷
8.(3分)电解100mL含c(H+)=0.3mol/L的下列溶液,当电路中通过0.04mol电子时,理论上
D.甲基丙烯酸和甲酸丙酯
析出金属质量最大的是( )
4.(3分)下列各组给定原子序数的元素,不能形成原子数之比为1:1稳定化合物的是( )
A.0.10mol∕LAg+ B.0.20mol∕LZn2+
A.3和17 B.1和8 C.1和6 D.7和12
C.0.20mol∕LCu2+ D.0.20mol∕LPb2+
5.(3分)下列叙述中正确的是( )
A.NH 、CO、CO 都是极性分子
3 2
二、解答题(共4小题,满分60分)
B.CH 、CCl 都是含有极性键的非极性分子
4 4
9.(16分)实验室可由软锰矿(主要成分为 MnO )制备KMnO ,方法如下:软锰矿与过量固
2 4
C.HF、HCI、HBr、HI的稳定性依次增强
体KOH和KClO 在高温下反应,生成锰酸钾(K MnO )和KCl;用水溶解,滤去残渣,滤液
3 2 4
D.CS 、H O、C H 都是直线型分子
2 2 2 2
酸化后,K MnO 转变为MnO 和KMnO ;滤去MnO 沉淀,浓缩滤液,结晶得到深紫色的针状
2 4 2 4 2
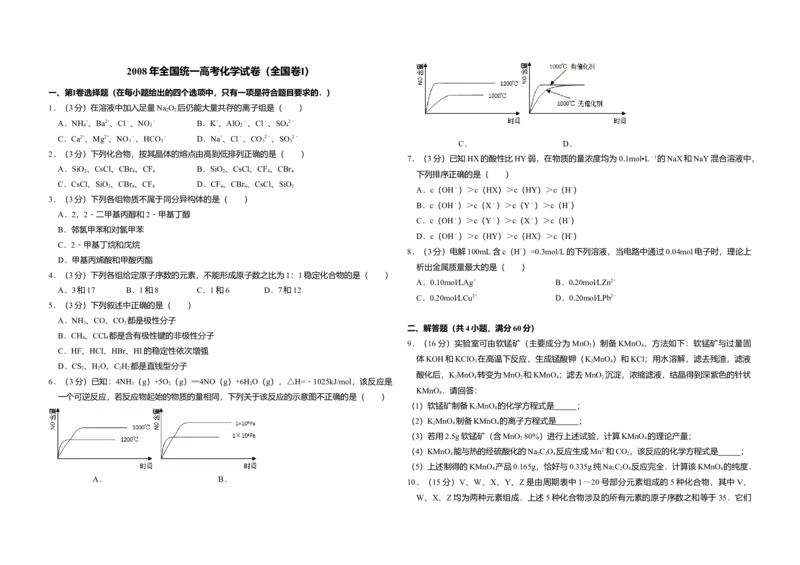
6.(3分)已知:4NH (g)+5O (g)═4NO(g)+6H O(g),△H=﹣1025kJ/mol,该反应是
3 2 2
KMnO .请回答:
4
一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是( )
(1)软锰矿制备K MnO 的化学方程式是 ;
2 4
(2)K MnO 制备KMnO 的离子方程式是 ;
2 4 4
(3)若用2.5g软锰矿(含MnO 80%)进行上述试验,计算KMnO 的理论产量;
2 4
(4)KMnO 能与热的经硫酸化的Na C O 反应生成Mn2+和CO ,该反应的化学方程式是 ;
4 2 2 4 2
(5)上述制得的KMnO 产品0.165g,恰好与0.335g纯Na C O 反应完全.计算该KMnO 的纯度.
4 2 2 4 4
A. B.
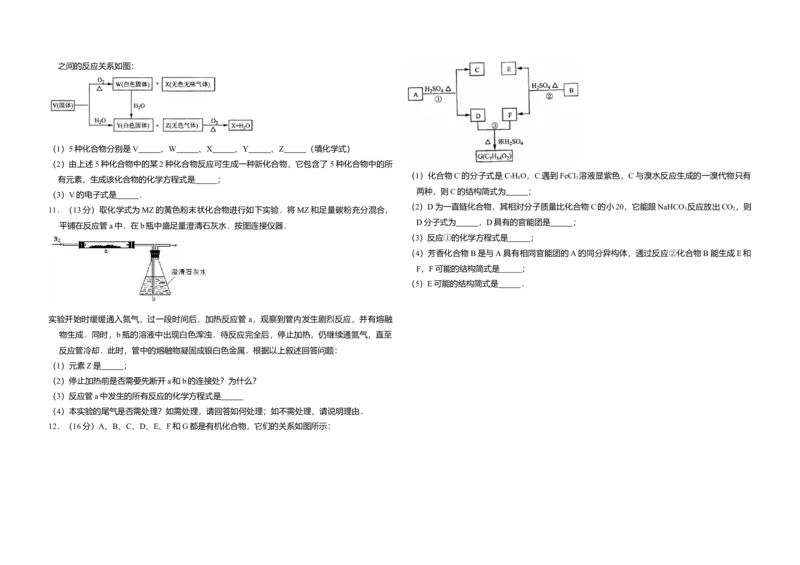
10.(15分)V、W、X、Y、Z是由周期表中 1~20号部分元素组成的 5种化合物,其中 V、
W、X、Z均为两种元素组成.上述5种化合物涉及的所有元素的原子序数之和等于 35.它们之间的反应关系如图:
(1)5种化合物分别是V 、W 、X 、Y 、Z (填化学式)
(2)由上述5种化合物中的某2种化合物反应可生成一种新化合物,它包含了 5种化合物中的所
(1)化合物C的分子式是C H O,C遇到FeCl 溶液显紫色,C与溴水反应生成的一溴代物只有
有元素,生成该化合物的化学方程式是 ; 7 8 3
两种,则C的结构简式为 ;
(3)V的电子式是 .
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO 反应放出CO ,则
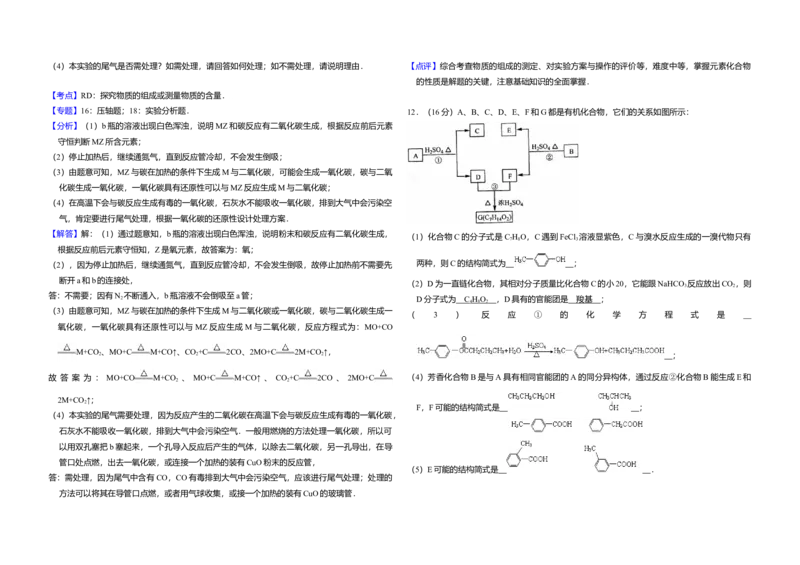
11.(13分)取化学式为MZ的黄色粉末状化合物进行如下实验.将MZ和足量碳粉充分混合, 3 2
D分子式为 ,D具有的官能团是 ;
平铺在反应管a中.在b瓶中盛足量澄清石灰水.按图连接仪器.
(3)反应①的化学方程式是 ;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和
F,F可能的结构简式是 ;
(5)E可能的结构简式是 .
实验开始时缓缓通入氮气,过一段时间后,加热反应管 a,观察到管内发生剧烈反应,并有熔融
物生成.同时,b瓶的溶液中出现白色浑浊.待反应完全后,停止加热,仍继续通氮气,直至
反应管冷却.此时,管中的熔融物凝固成银白色金属.根据以上叙述回答问题:
(1)元素Z是 ;
(2)停止加热前是否需要先断开a和b的连接处?为什么?
(3)反应管a中发生的所有反应的化学方程式是
(4)本实验的尾气是否需处理?如需处理,请回答如何处理;如不需处理,请说明理由.
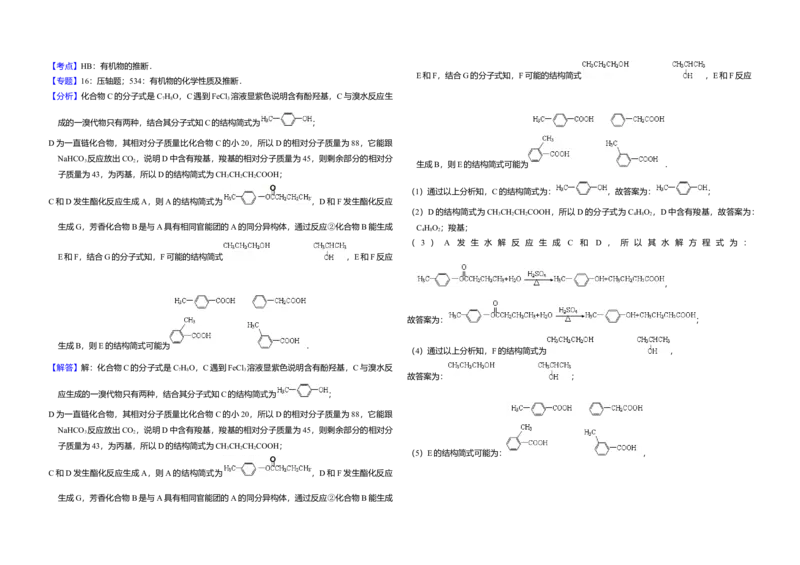
12.(16分)A、B、C、D、E、F和G都是有机化合物,它们的关系如图所示:晶体熔沸点高低的因素分析.
【解答】解:SiO 为原子晶体,CsCl为离子晶体,不同晶体的熔点:一般为原子晶体>离子晶体
2008 年全国统一高考化学试卷(全国卷Ⅰ) 2
>金属晶体>分子晶体,
参考答案与试题解析
则SiO 熔点最高,其次为CsCl,CBr 和CF 都为分子晶体,分子的相对分子质量越大,分子间作
2 4 4
用力越强,熔点越高,
一、第Ⅰ卷选择题(在每小题给出的四个选项中,只有一项是符合题目要求的.)
则熔点:CBr >CF ,
4 4
1.(3分)在溶液中加入足量Na O 后仍能大量共存的离子组是( )
2 2
固有:SiO >CsCl>CBr >CF ,
2 4 4
A.NH +、Ba2+、Cl﹣、NO ﹣ B.K+、AlO ﹣、Cl﹣、SO 2﹣
4 3 2 4
故选:A。
C.Ca2+、Mg2+、NO ﹣、HCO ﹣ D.Na+、Cl﹣、CO 2﹣、SO 2﹣
3 3 3 3
【点评】本题考查晶体的类型与熔沸点的比较,题目难度不大,解答该类题目时要首先判断晶体
的类型,晶体类型相同时,要注意晶体结构是否相似,把握影响晶体熔沸点的因素.
【考点】DP:离子共存问题;GF:钠的重要化合物.
菁优网版权所有
【专题】516:离子反应专题.
3.(3分)下列各组物质不属于同分异构体的是( )
【分析】Na O 具有强氧化性,与水反应生成OH﹣,溶液中加入足量Na O 后仍能大量共存,说明
2 2 2 2
A.2,2﹣二甲基丙醇和2﹣甲基丁醇
溶液中离子不与Na O 或OH﹣反应,且离子之间不发生任何反应.
2 2
B.邻氯甲苯和对氯甲苯
【解答】解:A.NH +与OH﹣反应而不能大量共存,故A错误;
4
C.2﹣甲基丁烷和戊烷
B.在碱性条件下,离子之间不发生任何反应,可大量共存,故B正确;
D.甲基丙烯酸和甲酸丙酯
C.Mg2+与OH﹣反应,Ca2+、HCO ﹣与OH﹣反应生成沉淀而不能大量共存,故C错误;
3
D.SO 2﹣具有还原性,可与Na O 发生氧化还原反应,故D错误。
3 2 2
【考点】I4:同分异构现象和同分异构体.
菁优网版权所有
故选:B。
【专题】532:同分异构体的类型及其判定.
【点评】本题考查离子共存问题,题目难度不大,本题注意把握题中所给信息,把握离子的性质
【分析】分子式相同,结构不同的化合物互为同分异构体.据此判断.
易错点为D,注意SO 2﹣具有还原性,可与Na O 发生氧化还原反应.
3 2 2 【解答】解:A、2,2﹣二甲基丙醇和2﹣甲基丁醇,分子式相同,含有相同数目的羟基,结构不
同,互为同分异构体,故A正确;
2.(3分)下列化合物,按其晶体的熔点由高到低排列正确的是( )
B、邻氯甲苯和对氯甲苯,分子式相同,结构不同,互为同分异构体,故B正确;
A.SiO 、CsCl、CBr 、CF B.SiO 、CsCl、CF 、CBr
2 4 4 2 4 4
C、2﹣甲基丁烷和戊烷,分子式相同,结构不同,互为同分异构体,故C正确;
C.CsCl、SiO 、CBr 、CF D.CF 、CBr 、CsCl、SiO
2 4 4 4 4 2
D、甲基丙烯酸和甲酸丙酯,分子式不同,不是同分异构体,故D错误。
故选:D。
【考点】9G:晶体的类型与物质熔点、硬度、导电性等的关系.
菁优网版权所有 【点评】本题考查同分异构体的概念与区别,难度不大,关键根据名称写出分子式进行判断.
【专题】51D:化学键与晶体结构.
【分析】不同晶体的熔点:一般为原子晶体>离子晶体>金属晶体>分子晶体;相同晶体从影响
4.(3分)下列各组给定原子序数的元素,不能形成原子数之比为1:1稳定化合物的是( )A.3和17 B.1和8 C.1和6 D.7和12 D、H O是V型分子,CS 、C H 都是直线型分子,故D错误。
2 2 2 2
故选:B。
【考点】8G:原子结构与元素的性质. 【点评】本题考查了分子极性的判断、氢化物的稳定性、分子的空间构型等知识点,难度不大,
菁优网版权所有
【专题】51B:原子组成与结构专题;51C:元素周期律与元素周期表专题. 明确分子是否极性的判断方法.
【分析】根据元素序数判断元素种类,结合元素的化合价判断.
【解答】解:A.原子序数为为3的元素为Li,原子序数为17的元素为Cl,可形成LiCl,故A不 6.(3分)已知:4NH (g)+5O (g)═4NO(g)+6H O(g),△H=﹣1025kJ/mol,该反应是
3 2 2
选; 一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是( )
B.原子序数为为1的元素为H,原子序数为8的元素为O,可形成H O ,故B不选;
2 2
C.原子序数为为1的元素为H,原子序数为6的元素为C,可形成C H ,故C不选;
2 2
D.原子序数为为7的元素为N,原子序数为12的元素为Mg,可形成Mg N ,故D选。
3 2
故选:D。
A.
【点评】本题考查原子结构与元素的性质,题目难度不大,注意常见元素形成的化合物的种类.
5.(3分)下列叙述中正确的是( )
A.NH 、CO、CO 都是极性分子
3 2
B.CH 、CCl 都是含有极性键的非极性分子
4 4
B.
C.HF、HCI、HBr、HI的稳定性依次增强
D.CS 、H O、C H 都是直线型分子
2 2 2 2
【考点】76:非金属在元素周期表中的位置及其性质递变的规律;98:判断简单分子或离子的构
型;9P:极性分子和非极性分子.
菁优网版权所有
【专题】51D:化学键与晶体结构. C.
【分析】A、分子中正负电荷重心不重叠的为极性分子.
B、非极性分子有两类,一是非金属单质,二是结构对称的分子,分子中正负电荷重心重叠.
C、非金属的非金属性越强,氢化物的稳定性越强.
D、根据分子的空间构型判断.
【解答】解:A、CO 的正负电荷重心重叠,属于非极性分子,故A错误。
2 D.
B、CH 、CCl 的正负电荷重心重叠,属于非极性分子,但存在的化学键是极性键,故B正确。
4 4
C、F、CI、Br、I的非金属逐渐减弱,所以HF、HCI、HBr、HI的稳定性逐渐减弱,故C错误。【考点】CI:体积百分含量随温度、压强变化曲线. 解显碱性,
菁优网版权所有
【专题】16:压轴题;51E:化学平衡专题. 存在X﹣+H O HX+OH﹣、Y﹣+H O HY+OH﹣,
2 2
【分析】由4NH (g)+5O (g)=4NO(g)+6H O(g)△H=﹣1025kJ/mol知,该反应是一个反 则c(OH﹣)>c(HX)>c(HY)>c(H+),
3 2 2 ⇌ ⇌
应前后气体体积增大的放热反应,升高温度,化学平衡向吸热方向移动,增大压强平衡向气体 且水解的程度不大,所以c(Y﹣)>c(X﹣)>c(OH﹣)>c(H+),
体积减小的方向移动,催化剂能改变化学反应速率但不影响化学平衡. 故选:A。
【解答】解:A、该反应是一个反应前后气体体积增大的放热反应,升高温度,平衡向逆反应方 【点评】本题考查离子浓度大小的比较,明确酸性越弱,盐的水解程度越大是解答本题的关键,
向移动,导致一氧化氮的含量减少,故A正确。 并注意离子的水解程度来解答即可,题目难度不大。
B、该反应是一个反应前后气体体积增大的放热反应,增大压强平衡向逆反应方向移动,导致一
氧化氮的含量减少,故B正确。 8.(3分)电解100mL含c(H+)=0.3mol/L的下列溶液,当电路中通过0.04mol电子时,理论上
C、该反应是一个反应前后气体体积增大的放热反应,升高温度,平衡向逆反应方向移动,导致 析出金属质量最大的是( )
一氧化氮的含量减少,故C错误。 A.0.10mol∕LAg+ B.0.20mol∕LZn2+
D、催化剂能改变化学反应速率但不影响化学平衡,正催化剂能加快反应速率缩短反应到达平衡 C.0.20mol∕LCu2+ D.0.20mol∕LPb2+
的时间,故D正确。
故选:C。 【考点】DI:电解原理.
菁优网版权所有
【点评】本题以图象为载体考查了外界条件对化学平衡的影响,难度不大,明确催化剂能改变化 【专题】16:压轴题;51I:电化学专题.
学反应速率但不影响化学平衡.
【分析】在电解池中,阴极上阳离子的放电顺序是:银离子>铜离子>氢离子,只有放电顺序在
H+前的才析出金属,根据电极反应结合电子守恒来计算即可.
7.(3分)已知HX的酸性比HY弱,在物质的量浓度均为0.1mol•L﹣1的NaX和NaY混合溶液中, 【解答】解:Zn2+和Pb2+的放电顺序都在H+后面,所以含有这两种阳离子的盐溶液中,阴极上放
下列排序正确的是( ) 出H 2 ,而含有银离子和铜离子这两种阳离子的盐溶液中,Ag和Cu金属先在阴极析出。
A.c(OH﹣)>c(HX)>c(HY)>c(H+) B.c(OH﹣)>c(X﹣)>c(Y﹣)>c A、0.10mol∕LAg+在氢离子之前放电,金属银的质量是 0.1mol/L×0.1L×108g/mol=1.08g;
(H+) B、Zn2+的放电顺序在H+后面,所以含有这种阳离子的盐溶液中,阴极上放出H
2
,不会析出金属;
C.c(OH﹣)>c(Y﹣)>c(X﹣)>c(H+) D.c(OH﹣)>c(HY)>c(HX)>c C、铜离子先放电,100mL0.20mol∕LCu2+就会得到 0.04mol 电子,所以析出金属铜的质量为:
(H+)
×0.04mol×64g/mol=1.28g;
D、Pb2+的放电顺序在H+后面,所以含有这种阳离子的盐溶液中,阴极上放出H ,不会析出金属。
2
【考点】DN:离子浓度大小的比较.
菁优网版权所有
所以析出金属质量最大的是0.20mol∕LCu2+。
【专题】16:压轴题;51H:盐类的水解专题.
故选:C。
【分析】HX的酸性比HY弱,则NaX的水解程度大于NaY的水解程度,且强碱弱酸盐水解显碱
【点评】本题考查学生电解池上阴极上离子的放电顺序并结合电子守恒来计算析出金属的质量,
性,以此来解答。
综合性较强,难度较大.
【解答】解:由HX的酸性比HY弱,则NaX的水解程度大于NaY的水解程度,且强碱弱酸盐水+2H O,
2
二、解答题(共4小题,满分60分) 故答案为:3MnO 2﹣+4H+═MnO ↓+2MnO ﹣+2H O;
4 2 4 2
9.(16分)实验室可由软锰矿(主要成分为 MnO )制备KMnO ,方法如下:软锰矿与过量固
2 4 (3)由3MnO +6KOH+KClO 3K MnO +KCl+3H O、3MnO 2﹣+4H+═MnO ↓+2MnO ﹣+2H O
2 3 2 4 2 4 2 4 2
体KOH和KClO 在高温下反应,生成锰酸钾(K MnO )和KCl;用水溶解,滤去残渣,滤液
3 2 4
可知,反应物和生成物间的计量关系为:
酸化后,K MnO 转变为MnO 和KMnO ;滤去MnO 沉淀,浓缩滤液,结晶得到深紫色的针状
2 4 2 4 2
MnO →K MnO →KMnO
KMnO .请回答: 2 2 4 4
4
87 158×
(1)软锰矿制备K MnO 的化学方程式是 3MnO + 6KOH + KClO 3K MnO + KC l + 3H O ;
2 4 2 3 2 4 2
2.5×80% x
(2)K MnO 制备KMnO 的离子方程式是 3MnO 2﹣ + 4H + ═ MnO ↓ + 2MnO ﹣ + 2H O ;
2 4 4 4 2 4 2
(3)若用2.5g软锰矿(含MnO 80%)进行上述试验,计算KMnO 的理论产量;
2 4 x= ,
(4)KMnO 能与热的经硫酸化的 Na C O 反应生成 Mn2+和 CO ,该反应的化学方程式是
4 2 2 4 2
答:KMnO 的理论产量是2.4g;
4
2KMnO + 5N a C O + 8H SO K SO + 2MnSO + 5N a SO + 10CO ↑ + 8H O ;
4 2 2 4 2 4 2 4 4 2 4 2 2 ( 4 ) 由 KMnO 能 与 热 的 经 硫 酸 化 的 Na C O 反 应 生 成 Mn2+ 和 CO , 则 反 应 为
4 2 2 4 2
(5)上述制得的KMnO 产品0.165g,恰好与0.335g纯Na C O 反应完全.计算该KMnO 的纯度.
4 2 2 4 4
2KMnO +5Na C O +8H SO K SO +2MnSO +5Na SO +10CO ↑+8H O,
4 2 2 4 2 4 2 4 4 2 4 2 2
【考点】5A:化学方程式的有关计算;B1:氧化还原反应.
菁优网版权所有 故答案为:2KMnO +5Na C O +8H SO K SO +2MnSO +5Na SO +10CO ↑+8H O;
4 2 2 4 2 4 2 4 4 2 4 2 2
【专题】515:氧化还原反应专题.
【分析】(1)根据反应物与生成物来书写反应方程式; ( 5 ) 设 该 KMnO 的 纯 度 为 y , 根 据 2KMnO +5Na C O +8H SO
4 4 2 2 4 2 4
(2)根据反应物与生成物来书写反应方程式;
K SO +2MnSO +5Na SO +10CO ↑+8H O可知,
2 4 4 2 4 2 2
(3)利用化学反应方程式及二氧化锰的质量代入计算;
KMnO ﹣﹣﹣Na C O
(4)根据KMnO 能与热的经硫酸化的Na C O 反应生成Mn2+和CO ,并利用质量守恒定律来书 4 2 2 4
4 2 2 4 2
写反应方程式;
×158 134
(5)利用(4)中的化学反应方程式及恰好与0.335g纯Na C O 反应完全来计算.
2 2 4
【解答】解:(1)由软锰矿与过量固体KOH和KClO 在高温下反应,生成锰酸钾(K MnO )和 0.165×y 0.335
3 2 4
KCl,则反应为3MnO +6KOH+KClO 3K MnO +KCl+3H O, y= ,
2 3 2 4 2
故答案为:3MnO
2
+6KOH+KClO
3
3K
2
MnO
4
+KCl+3H
2
O; 答:该KMnO
4
的纯度为95.8%.
【点评】本题考查化学反应方程式的书写及有关氧化还原反应的计算,明确反应物与生成物及物
(2)由滤液酸化后,K MnO 转变为MnO 和KMnO ,则反应为3MnO 2﹣+4H+═MnO ↓+2MnO ﹣
2 4 2 4 4 2 4
质之间的关系是解答的关键,难度不大.(2)包含了5种化合物中的所有元素的物质是碳酸氢钙,氢氧化钙和过量二氧化碳反应生成碳酸
10.(15分)V、W、X、Y、Z是由周期表中 1~20号部分元素组成的 5种化合物,其中 V、 氢钙,反应方程式为:
W、X、Z均为两种元素组成.上述5种化合物涉及的所有元素的原子序数之和等于 35.它们 Ca(OH) +2CO =Ca(HCO ) ;
2 2 3 2
之间的反应关系如图: 故答案为:Ca(OH) +2CO =Ca(HCO ) ;
2 2 3 2
(3)碳化钙是离子化合物,其电子式为: ;
故答案为: .
【点评】本题考查元素化合物的特性和反应,用框图设问可以考查学生正向思维、逆向思维、发
散和收敛思维,能根据题眼正确判断化合物是解本题的关键,很多学生在做推断题时只考虑无
机物不考虑有机物,导致错误推断,难度较大.
(1)5种化合物分别是V CaC 、W CaO 、X CO 、Y Ca ( OH ) 、Z C H (填
2 2 2 2 2
化学式)
11.(13分)取化学式为MZ的黄色粉末状化合物进行如下实验.将MZ和足量碳粉充分混合,
(2)由上述5种化合物中的某2种化合物反应可生成一种新化合物,它包含了 5种化合物中的所
平铺在反应管a中.在b瓶中盛足量澄清石灰水.按图连接仪器.
有元素,生成该化合物的化学方程式是 Ca ( OH ) + 2CO =Ca ( HCO ) ;
2 2 3 2
(3)V的电子式是 .
【考点】GS:无机物的推断.
菁优网版权所有
【专题】11:推断题.
【分析】无色气体Z能燃烧生成水和无色无味气体 X,V、W、X、Z均为两种元素组成,根据元
素守恒知,Z含有H元素,应该是烃,固体C和水反应生成Y和烃,碳化钙和水反应生成氢氧
实验开始时缓缓通入氮气,过一段时间后,加热反应管 a,观察到管内发生剧烈反应,并有熔融
化钙和乙炔,所以V是碳化钙,Y是氢氧化钙,Z是乙炔;
物生成.同时,b瓶的溶液中出现白色浑浊.待反应完全后,停止加热,仍继续通氮气,直至
加热条件下,碳化钙和氧气反应生成氧化钙和二氧化碳,所以W是氧化钙,X是二氧化碳.
反应管冷却.此时,管中的熔融物凝固成银白色金属.根据以上叙述回答问题:
【解答】解:无色气体Z能燃烧生成水和无色无味气体 X,V、W、X、Z均为两种元素组成,根
(1)元素Z是 氧 ;
据元素守恒知,Z含有H元素,应该是烃,固体C和水反应生成Y和烃,碳化钙和水反应生成
(2)停止加热前是否需要先断开a和b的连接处?为什么?
氢氧化钙和乙炔,所以V是碳化钙,Y是氢氧化钙,Z是乙炔;
(3)反应管 a中发生的所有反应的化学方程式是 MO + CO M + CO 、 MO + C M + CO↑ 、
加热条件下,碳化钙和氧气反应生成氧化钙和二氧化碳,所以W是氧化钙,X是二氧化碳. 2
(1)通过以上分析知,V、W、X、Y、Z分别是CaC 、CaO、CO 、Ca(OH) 、C H ;
2 2 2 2 2
CO + C 2CO 、 2MO + C 2M + CO ↑
故答案为:CaC 、CaO、CO 、Ca(OH) 、C H ; 2 2
2 2 2 2 2(4)本实验的尾气是否需处理?如需处理,请回答如何处理;如不需处理,请说明理由. 【点评】综合考查物质的组成的测定、对实验方案与操作的评价等,难度中等,掌握元素化合物
的性质是解题的关键,注意基础知识的全面掌握.
【考点】RD:探究物质的组成或测量物质的含量.
菁优网版权所有
【专题】16:压轴题;18:实验分析题. 12.(16分)A、B、C、D、E、F和G都是有机化合物,它们的关系如图所示:
【分析】(1)b瓶的溶液出现白色浑浊,说明MZ和碳反应有二氧化碳生成,根据反应前后元素
守恒判断MZ所含元素;
(2)停止加热后,继续通氮气,直到反应管冷却,不会发生倒吸;
(3)由题意可知,MZ与碳在加热的条件下生成M与二氧化碳,可能会生成一氧化碳,碳与二氧
化碳生成一氧化碳,一氧化碳具有还原性可以与MZ反应生成M与二氧化碳;
(4)在高温下会与碳反应生成有毒的一氧化碳,石灰水不能吸收一氧化碳,排到大气中会污染空
气,肯定要进行尾气处理,根据一氧化碳的还原性设计处理方案.
【解答】解:(1)通过题意知,b瓶的溶液出现白色浑浊,说明粉末和碳反应有二氧化碳生成,
(1)化合物C的分子式是C H O,C遇到FeCl 溶液显紫色,C与溴水反应生成的一溴代物只有
7 8 3
根据反应前后元素守恒知,Z是氧元素,故答案为:氧;
(2),因为停止加热后,继续通氮气,直到反应管冷却,不会发生倒吸,故停止加热前不需要先 两种,则C的结构简式为 ;
断开a和b的连接处,
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO 反应放出CO ,则
3 2
答:不需要;因有N 不断通入,b瓶溶液不会倒吸至a管;
2 D分子式为 C H O ,D具有的官能团是 羧基 ;
4 8 2
(3)由题意可知,MZ与碳在加热的条件下生成M与二氧化碳或一氧化碳,碳与二氧化碳生成一
( 3 ) 反 应 ① 的 化 学 方 程 式 是
氧化碳,一氧化碳具有还原性可以与 MZ 反应生成 M与二氧化碳,反应方程式为:MO+CO
M+CO 、MO+C M+CO↑、CO +C 2CO、2MO+C 2M+CO ↑,
2 2 2 ;
故 答 案 为 : MO+CO M+CO 、 MO+C M+CO↑ 、 CO +C 2CO 、 2MO+C (4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和
2 2
2M+CO ↑;
2
F,F可能的结构简式是 ;
(4)本实验的尾气需要处理,因为反应产生的二氧化碳在高温下会与碳反应生成有毒的一氧化碳,
石灰水不能吸收一氧化碳,排到大气中会污染空气.一般用燃烧的方法处理一氧化碳,所以可
以用双孔塞把b塞起来,一个孔导入反应后产生的气体,以除去二氧化碳,另一孔导出,在导
管口处点燃,出去一氧化碳,或连接一个加热的装有CuO粉末的反应管,
(5)E可能的结构简式是 .
答:需处理,因为尾气中含有CO,CO有毒排到大气中会污染空气,应该进行尾气处理;处理的
方法可以将其在导管口点燃,或者用气球收集,或接一个加热的装有CuO的玻璃管.【考点】HB:有机物的推断.
菁优网版权所有
E和F,结合G的分子式知,F可能的结构简式 ,E和F反应
【专题】16:压轴题;534:有机物的化学性质及推断.
【分析】化合物C的分子式是C H O,C遇到FeCl 溶液显紫色说明含有酚羟基,C与溴水反应生
7 8 3
成的一溴代物只有两种,结合其分子式知C的结构简式为 ;
D为一直链化合物,其相对分子质量比化合物 C的小20,所以D的相对分子质量为88,它能跟
NaHCO 反应放出CO ,说明D中含有羧基,羧基的相对分子质量为45,则剩余部分的相对分
3 2
生成B,则E的结构简式可能为 .
子质量为43,为丙基,所以D的结构简式为CH CH CH COOH;
3 2 2
(1)通过以上分析知,C的结构简式为: ,故答案为: ;
C和D发生酯化反应生成A,则A的结构简式为 ,D和F发生酯化反应
(2)D的结构简式为CH CH CH COOH,所以D的分子式为C H O ,D中含有羧基,故答案为:
3 2 2 4 8 2
生成G,芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成 C H O ;羧基;
4 8 2
( 3 ) A 发 生 水 解 反 应 生 成 C 和 D , 所 以 其 水 解 方 程 式 为 :
E和F,结合G的分子式知,F可能的结构简式 ,E和F反应
,
故答案为: ;
生成B,则E的结构简式可能为 .
(4)通过以上分析知,F的结构简式为 ,
【解答】解:化合物C的分子式是C H O,C遇到FeCl 溶液显紫色说明含有酚羟基,C与溴水反
7 8 3
故答案为: ;
应生成的一溴代物只有两种,结合其分子式知C的结构简式为 ;
D为一直链化合物,其相对分子质量比化合物 C的小20,所以D的相对分子质量为88,它能跟
NaHCO 反应放出CO ,说明D中含有羧基,羧基的相对分子质量为45,则剩余部分的相对分
3 2
子质量为43,为丙基,所以D的结构简式为CH CH CH COOH;
3 2 2
(5)E的结构简式可能为: ,
C和D发生酯化反应生成A,则A的结构简式为 ,D和F发生酯化反应
生成G,芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成故答案为: .
【点评】本题考查有机物推断,根据题给信息、正推和逆推相结合的方法进行分析解答,同分异
构体的推断是本题的难点,注意不仅有位置异构,还有官能团异构,为易错点.