文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点提分训练(十一)金属活动性顺序
一、选择题
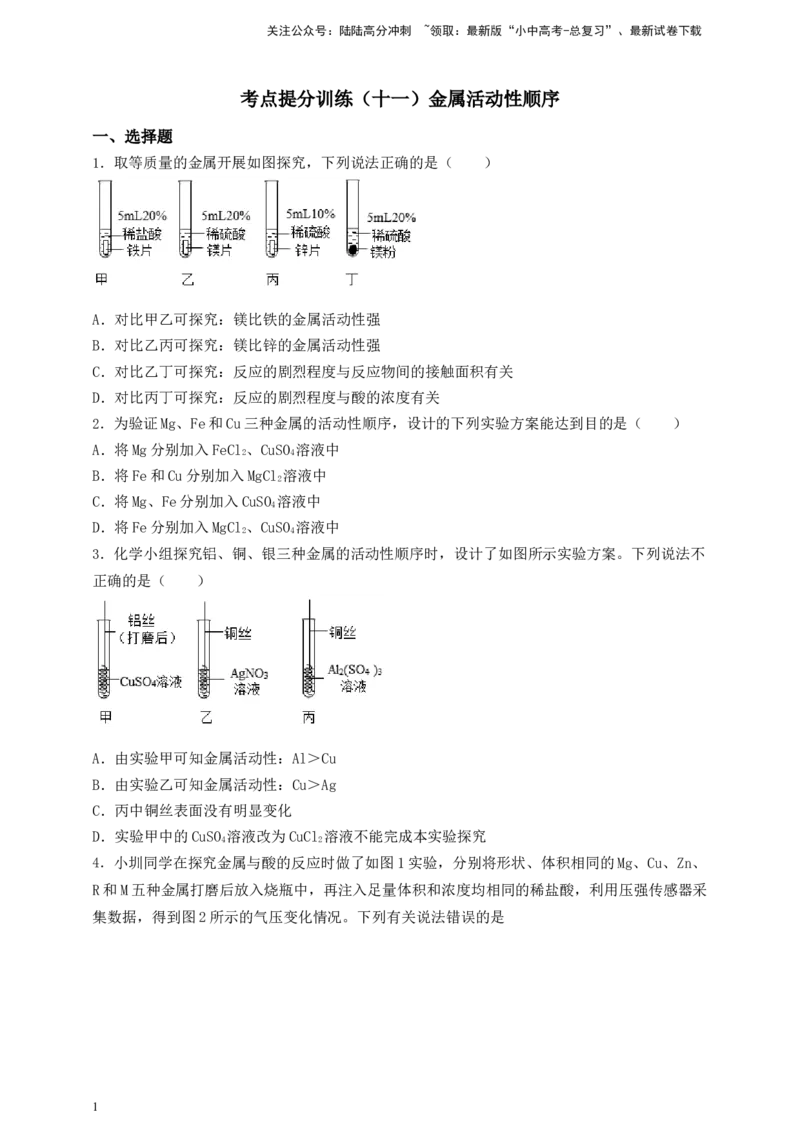
1.取等质量的金属开展如图探究,下列说法正确的是( )
A.对比甲乙可探究:镁比铁的金属活动性强
B.对比乙丙可探究:镁比锌的金属活动性强
C.对比乙丁可探究:反应的剧烈程度与反应物间的接触面积有关
D.对比丙丁可探究:反应的剧烈程度与酸的浓度有关
2.为验证Mg、Fe和Cu三种金属的活动性顺序,设计的下列实验方案能达到目的是( )
A.将Mg分别加入FeCl、CuSO 溶液中
2 4
B.将Fe和Cu分别加入MgCl 溶液中
2
C.将Mg、Fe分别加入CuSO 溶液中
4
D.将Fe分别加入MgCl、CuSO 溶液中
2 4
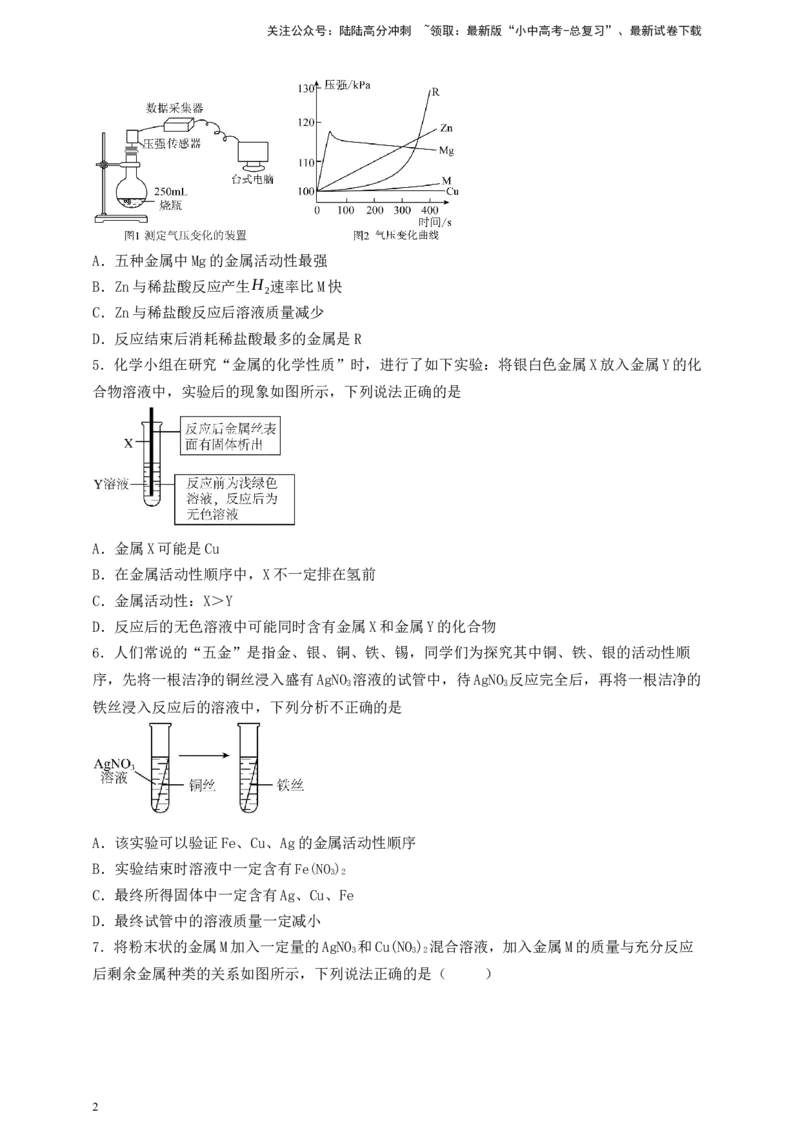
3.化学小组探究铝、铜、银三种金属的活动性顺序时,设计了如图所示实验方案。下列说法不
正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.丙中铜丝表面没有明显变化
D.实验甲中的CuSO 溶液改为CuCl 溶液不能完成本实验探究
4 2
4.小圳同学在探究金属与酸的反应时做了如图1实验,分别将形状、体积相同的Mg、Cu、Zn、
R和M五种金属打磨后放入烧瓶中,再注入足量体积和浓度均相同的稀盐酸,利用压强传感器采
集数据,得到图2所示的气压变化情况。下列有关说法错误的是
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.五种金属中Mg的金属活动性最强
B.Zn与稀盐酸反应产生H 速率比M快
2
C.Zn与稀盐酸反应后溶液质量减少
D.反应结束后消耗稀盐酸最多的金属是R
5.化学小组在研究“金属的化学性质”时,进行了如下实验:将银白色金属X放入金属Y的化
合物溶液中,实验后的现象如图所示,下列说法正确的是
A.金属X可能是Cu
B.在金属活动性顺序中,X不一定排在氢前
C.金属活动性:X>Y
D.反应后的无色溶液中可能同时含有金属X和金属Y的化合物
6.人们常说的“五金”是指金、银、铜、铁、锡,同学们为探究其中铜、铁、银的活动性顺
序,先将一根洁净的铜丝浸入盛有AgNO 溶液的试管中,待AgNO 反应完全后,再将一根洁净的
3 3
铁丝浸入反应后的溶液中,下列分析不正确的是
A.该实验可以验证Fe、Cu、Ag的金属活动性顺序
B.实验结束时溶液中一定含有Fe(NO)
3 2
C.最终所得固体中一定含有Ag、Cu、Fe
D.最终试管中的溶液质量一定减小
7.将粉末状的金属M加入一定量的AgNO 和Cu(NO) 混合溶液,加入金属M的质量与充分反应
3 3 2
后剩余金属种类的关系如图所示,下列说法正确的是( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.金属活动性:Cu>M>Ag
B.加入ag金属M,充分反应后剩余的金属是Cu
C.加入bg金属M,充分反应后溶液中含有Cu(NO)
3 2
D.加入cg金属M,充分反应后溶液中含有2种溶质
二、实验探究题
8.对金属活动性顺序的研究历程,极大的促进了化学科学的发展。
(1)I、初识金属活动性顺序
1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。
若用锡、银、铁三种金属重温实验,则会“消失”的金属有 。
(2)II、再探金属活动性顺序
1766年卡文迪许用金属与酸反应制取了一种可燃性气体,他称之为“可燃空气”,为探索金属
活动性顺序打开了新思路。上述“可燃空气”指的是 。
(3)某金属粉末含有Mg、Al、Cu中的一种或几种,取24g该金属粉末与足量稀盐酸反应产生
2g气体,则该金属粉末的组成情况有 种。
(4)Ⅲ、确定金属活动性顺序
1865年贝开托夫经过大量的实验得出了金属活动性规律。
利用上述规律,用废弃的白铜可以回收铜、镍(Ni)两种金属,已知白铜是铜、镍合金。
①先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气
泡产生,且锌粉与稀硫酸反应更剧烈,说明镍的金属活动性比锌 (填“强”或
“弱”)。资料显示,镍与稀硫酸反应有NiSO 生成。
4
②设计如下实验流程回收铜和镍。
固体A是 ,操作1的名称是 ,溶液B中,生成镍反应的化学
方程式 。
③用20%的稀硫酸处理上述废弃的白铜粉末,若理论上恰好消耗9.8t稀硫酸,则产生氢气的质
量是 。
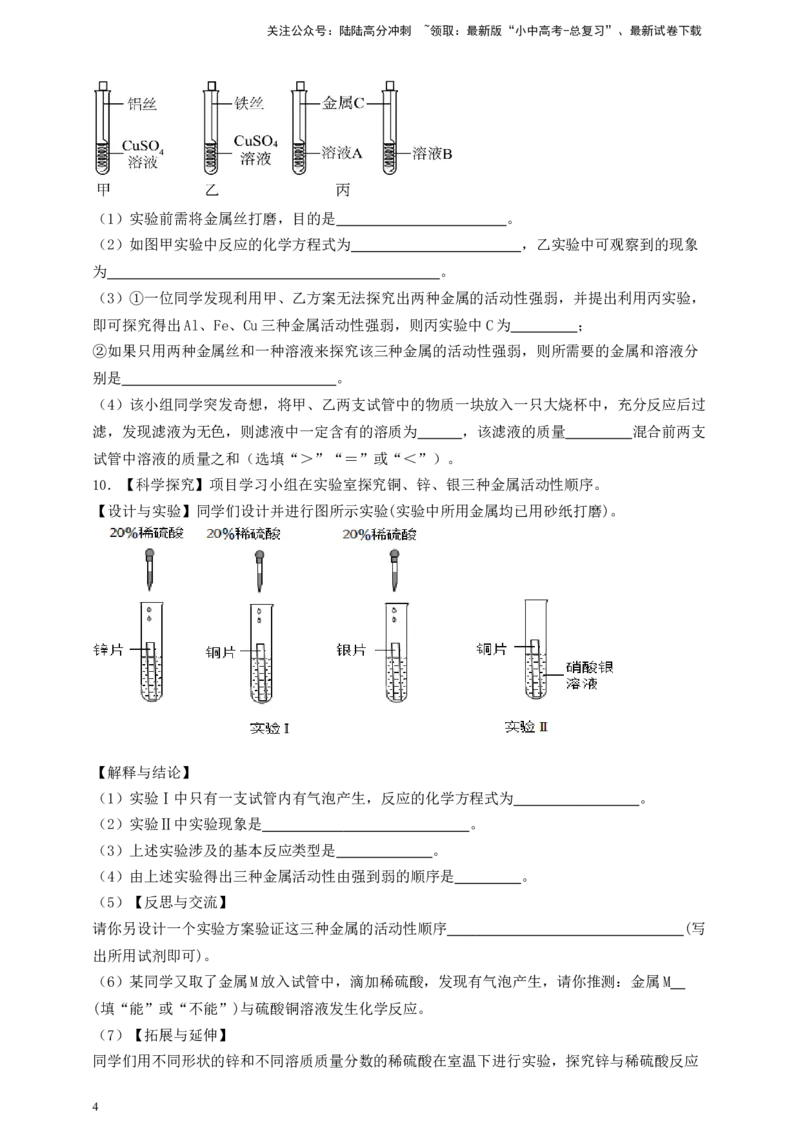
9.为探究Al、Fe、Cu的金属活动性强弱,某兴趣小组做了如下实验如图:
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)实验前需将金属丝打磨,目的是 。
(2)如图甲实验中反应的化学方程式为 ,乙实验中可观察到的现象
为 。
(3)①一位同学发现利用甲、乙方案无法探究出两种金属的活动性强弱,并提出利用丙实验,
即可探究得出Al、Fe、Cu三种金属活动性强弱,则丙实验中C为 ;
②如果只用两种金属丝和一种溶液来探究该三种金属的活动性强弱,则所需要的金属和溶液分
别是 。
(4)该小组同学突发奇想,将甲、乙两支试管中的物质一块放入一只大烧杯中,充分反应后过
滤,发现滤液为无色,则滤液中一定含有的溶质为 ,该滤液的质量 混合前两支
试管中溶液的质量之和(选填“>”“=”或“<”)。
10.【科学探究】项目学习小组在实验室探究铜、锌、银三种金属活动性顺序。
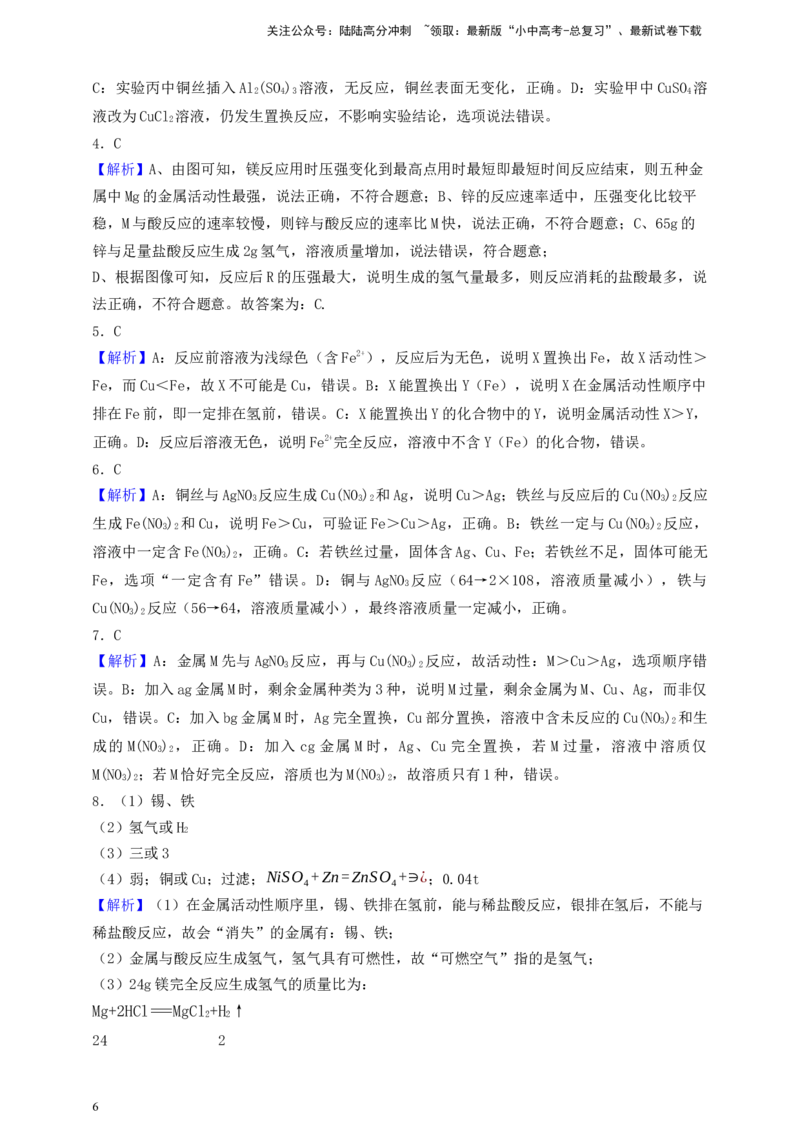
【设计与实验】同学们设计并进行图所示实验(实验中所用金属均已用砂纸打磨)。
【解释与结论】
(1)实验Ⅰ中只有一支试管内有气泡产生,反应的化学方程式为 。
(2)实验Ⅱ中实验现象是 。
(3)上述实验涉及的基本反应类型是 。
(4)由上述实验得出三种金属活动性由强到弱的顺序是 。
(5)【反思与交流】
请你另设计一个实验方案验证这三种金属的活动性顺序 (写
出所用试剂即可)。
(6)某同学又取了金属M放入试管中,滴加稀硫酸,发现有气泡产生,请你推测:金属M
(填“能”或“不能”)与硫酸铜溶液发生化学反应。
(7)【拓展与延伸】
同学们用不同形状的锌和不同溶质质量分数的稀硫酸在室温下进行实验,探究锌与稀硫酸反应
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
快慢的影响因素,实验记录表:
实验 硫酸的溶质质量分(均 锌的形状(均取 氢气的体积(mL)(均收集
编号 取20mL) 1g) 3分钟)
① 20% 锌粒 31.7
② 20% 锌片 50.9
③ 30% 锌粒 61.7
④ 30% 锌片 79.9
①②对比说明 ;要比较不同溶质质量分数的稀硫酸对反应快
慢的影响,应选择的实验编号是 。由此得出不同形状的锌和不同溶质质量分数
的稀硫酸都会影响反应快慢。
答案解析
1.C
【解析】A.甲和乙中,除了金属种类不同外,酸的种类不同,不能用于探究镁比铁的金属活动
性强,故A不符合题意;B.乙和丙中,除了金属种类不同外,酸的浓度不同,不能用于探究镁
比锌的金属活动性强,故B不符合题意;C.乙和丁中,除了镁片和镁粉(即反应物的接触面
积)不同外,其它条件均相同,根据等质量的镁粉反应的比镁片剧烈,可探究反应的剧烈程度
与反应物间的接触面积有关,故C符合题意;D.丙和丁中,除了酸的浓度不同,金属的种类也
不同,不能用于探究反应的剧烈程度与酸的浓度有关,故D不符合题意;故答案为:C。
2.D
【解析】A、将Mg加入FeCl 溶液中,Mg和FeCl 反应生成Fe和MgCl,从而证明Mg>Fe。将Mg
2 2 2
加如CuSO 溶液中,Mg和CuSO 反应生成Cu和MgSO,从而证明Mg>Cu,但是无法验证Fe和Cu
4 4 4
金属活动性强弱,该方案不能达到目的,故A不符合题意;B、将Fe和Cu分别加入MgCl 溶液
2
中, Fe、Cu均不能与MgCl 反应,证明Mg的金属活动性大于Fe和Cu,但是无法验证Fe和Cu
2
金属活动性强弱,该方案不能达到目的,故B不符合题意;
C、将Mg、Fe分别加入CuSO 溶液中,Mg、Fe均能与CuSO 反应,证明Mg、Fe的金属活动性大
4 4
于Cu,但是无法验证,Mg和Fe金属活动性强弱,该方案不能达到目的,故C不符合题意;D、
将Fe分别加入MgCl、CuSO 溶液中 ,Fe不能与MgCl 反应,说明Mg>Fe,Fe能与CuSO 反应,
2 4 2 4
说明Fe>Cu,从而证明 Mg、Fe和Cu三种金属的活动性顺序为Mg>Fe>Cu,该方案能达到目
的,故D符合题意;故答案为:D。
3.D
【解析】A:实验甲中铝丝插入CuSO 溶液,铝表面析出红色固体,说明Al>Cu,正确。
4
B:实验乙中铜丝插入AgNO 溶液,铜表面析出银白色固体,溶液变蓝,说明 Cu>Ag,正确。
3
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C:实验丙中铜丝插入Al (SO ) 溶液,无反应,铜丝表面无变化,正确。D:实验甲中CuSO 溶
2 4 3 4
液改为CuCl 溶液,仍发生置换反应,不影响实验结论,选项说法错误。
2
4.C
【解析】A、由图可知,镁反应用时压强变化到最高点用时最短即最短时间反应结束,则五种金
属中Mg的金属活动性最强,说法正确,不符合题意;B、锌的反应速率适中,压强变化比较平
稳,M与酸反应的速率较慢,则锌与酸反应的速率比M快,说法正确,不符合题意;C、65g的
锌与足量盐酸反应生成2g氢气,溶液质量增加,说法错误,符合题意;
D、根据图像可知,反应后R的压强最大,说明生成的氢气量最多,则反应消耗的盐酸最多,说
法正确,不符合题意。故答案为:C.
5.C
【解析】A:反应前溶液为浅绿色(含Fe2+),反应后为无色,说明X置换出Fe,故X活动性>
Fe,而Cu<Fe,故X不可能是Cu,错误。B:X能置换出Y(Fe),说明X在金属活动性顺序中
排在Fe前,即一定排在氢前,错误。C:X能置换出Y的化合物中的Y,说明金属活动性X>Y,
正确。D:反应后溶液无色,说明Fe2+完全反应,溶液中不含Y(Fe)的化合物,错误。
6.C
【解析】A:铜丝与AgNO 反应生成Cu(NO ) 和Ag,说明Cu>Ag;铁丝与反应后的Cu(NO ) 反应
3 3 2 3 2
生成Fe(NO ) 和Cu,说明Fe>Cu,可验证Fe>Cu>Ag,正确。B:铁丝一定与Cu(NO ) 反应,
3 2 3 2
溶液中一定含Fe(NO ) ,正确。C:若铁丝过量,固体含Ag、Cu、Fe;若铁丝不足,固体可能无
3 2
Fe,选项“一定含有 Fe”错误。D:铜与 AgNO 反应(64→2×108,溶液质量减小),铁与
3
Cu(NO ) 反应(56→64,溶液质量减小),最终溶液质量一定减小,正确。
3 2
7.C
【解析】A:金属M先与AgNO 反应,再与Cu(NO ) 反应,故活动性:M>Cu>Ag,选项顺序错
3 3 2
误。B:加入ag金属M时,剩余金属种类为3种,说明M过量,剩余金属为M、Cu、Ag,而非仅
Cu,错误。C:加入bg金属M时,Ag完全置换,Cu部分置换,溶液中含未反应的Cu(NO ) 和生
3 2
成的 M(NO ) ,正确。D:加入 cg 金属 M 时,Ag、Cu 完全置换,若 M 过量,溶液中溶质仅
3 2
M(NO ) ;若M恰好完全反应,溶质也为M(NO ) ,故溶质只有1种,错误。
3 2 3 2
8.(1)锡、铁
(2)氢气或H
2
(3)三或3
(4)弱;铜或Cu;过滤;NiSO +Zn=ZnSO +∋¿;0.04t
4 4
【解析】(1)在金属活动性顺序里,锡、铁排在氢前,能与稀盐酸反应,银排在氢后,不能与
稀盐酸反应,故会“消失”的金属有:锡、铁;
(2)金属与酸反应生成氢气,氢气具有可燃性,故“可燃空气”指的是氢气;
(3)24g镁完全反应生成氢气的质量比为:
Mg+2HCl=MgCl +H ↑
2 2
24 2
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
24g 2g
24g铝完全反应生成氢气的质量为:
2Al+6HCl=2AlCl +3H ↑
3 2
54 6
24G 2.67G
铜和稀盐酸不反应,24g该金属粉末与足量稀盐酸反应产生2g气体,故该金属粉末可能只含
镁,也可能是铝和铜的混合物,也可能是镁、铝、铜的混合物,故组成情况有三种;
(4)①先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都
有气泡产生,说明在金属活动性顺序里,锌、镍均排在氢前,锌粉与稀硫酸反应更剧烈,说明
镍的金属活动性比锌弱;②白铜是铜、镍合金,加入过量稀硫酸,镍和稀硫酸反应生成硫酸镍
和氢气,铜和稀硫酸不反应,故固体A为铜;操作1实现了固液分离,是过滤;溶液B中,生
成 镍 的 反 应 为 锌 和 硫 酸 镍 反 应 生 成 硫 酸 锌 和 镍 , 该 反 应 的 化 学 方 程 式 为 :
Zn+NiSO =Ni+ZnSO 。
4 4
9.(1)除去金属表面氧化物
(2)2Al+3CuSO =3Cu+Al (SO ) ;铁丝表面有红色固体析出,溶液由蓝色逐渐变为浅绿色
4 2 4 3
(3)Fe、Al、Cu、FeSO (合理即可)
4
(4)Al (SO ) ;<
2 4 3
10.(1)Zn+HSO=ZnSO+H↑
2 4 4 2
(2)铜片表面有银白色固体生成,溶液由无色变成蓝色
(3)置换反应
(4)锌铜银
(5)锌片、硫酸铜溶液、银片(合理即可)
(6)能
(7)在其他条件相同时,锌与稀硫酸接触面积越大,反应速率越快;①③或②④
【解析】通过实验1是比较锌能与酸反应且有大量气泡产生,而铜、银不能与酸反应,铜和银
表面没有气泡产生,该实验说明锌比氢活泼,铜、银没有氢活泼;实验2可以观察到红色的铜
表面有银白色的金属银析出,溶液由无色变成蓝色,则证明铜比银活泼。
(1) 实验Ⅰ中放有锌的试管内有气泡产生,该反应的化学方程式为: Zn+HSO=ZnSO+H↑ 。
2 4 4 2
(2)实验Ⅱ中实验现象是铜片表面有银白色固体生成,溶液由无色变成蓝色。(3)金属的活
泼性顺序的实验验证都是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,
属于置换反应。故答案为:置换反应。(4)由上述实验得出三种金属活动性由强到弱的顺序是
锌、铜、银。(5)验证锌、铜、银的活泼性顺序的实验可以选择铁、银单质和硫酸铜溶液,或
者选择硫酸亚铁溶液、硝酸银溶液和金属铜可以一次性的鉴别出锌比铜活泼,铜比银活泼。
(6)某同学又取了金属M放入试管中,滴加稀硫酸,发现有气泡产生,则金属M是比氢活泼的
金属有铁、镁等,且比铜活泼,能置换出溶液中的铜离子。
(7)根据实验分析数据表可知,反应物的浓度越大反应速度越快,反应物的接触面积越大反应
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
速度越快。①②对比说明在其他条件相同时,锌与稀硫酸接触面积越大,反应速率越快 ;要比
较不同溶质质量分数的稀硫酸对反应快慢的影响,应选择的实验编号是①③或者是②④。由此
得出不同形状的锌和不同溶质质量分数的稀硫酸都会影响反应快慢。
8