文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点提分训练(十五)酸的化学性质
一、选择题
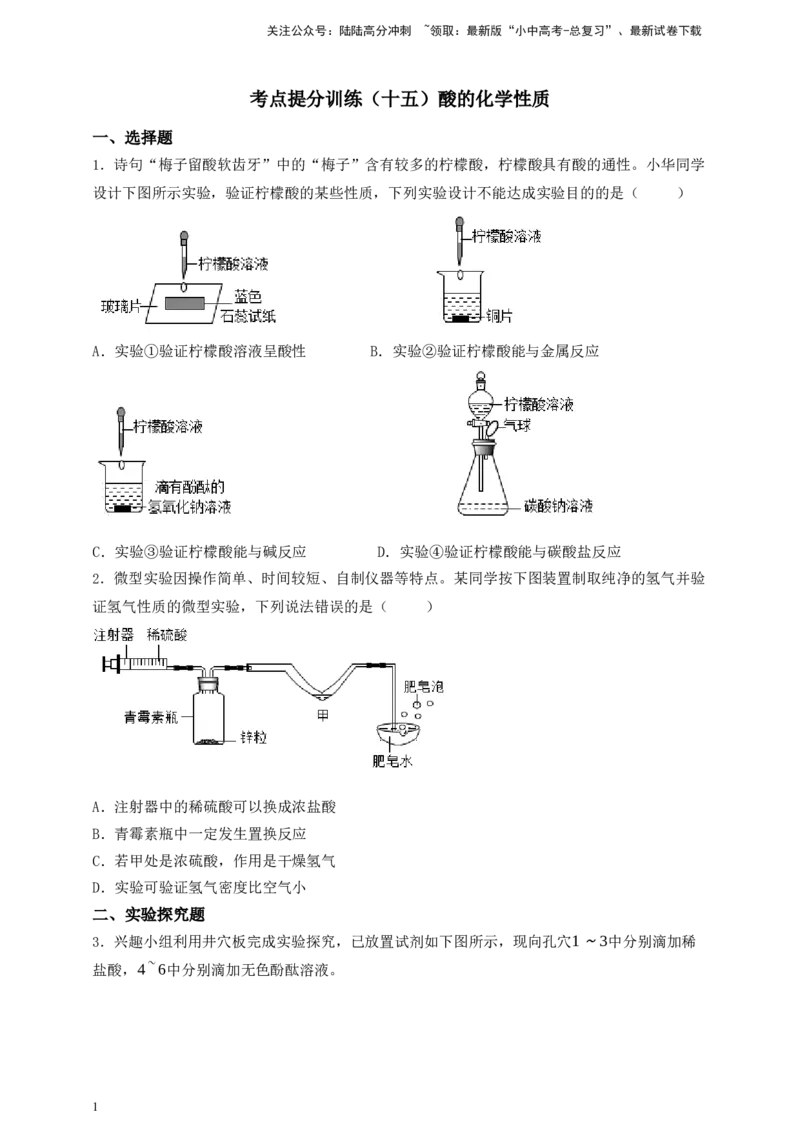
1.诗句“梅子留酸软齿牙”中的“梅子”含有较多的柠檬酸,柠檬酸具有酸的通性。小华同学
设计下图所示实验,验证柠檬酸的某些性质,下列实验设计不能达成实验目的的是( )
A.实验①验证柠檬酸溶液呈酸性 B.实验②验证柠檬酸能与金属反应
C.实验③验证柠檬酸能与碱反应 D.实验④验证柠檬酸能与碳酸盐反应
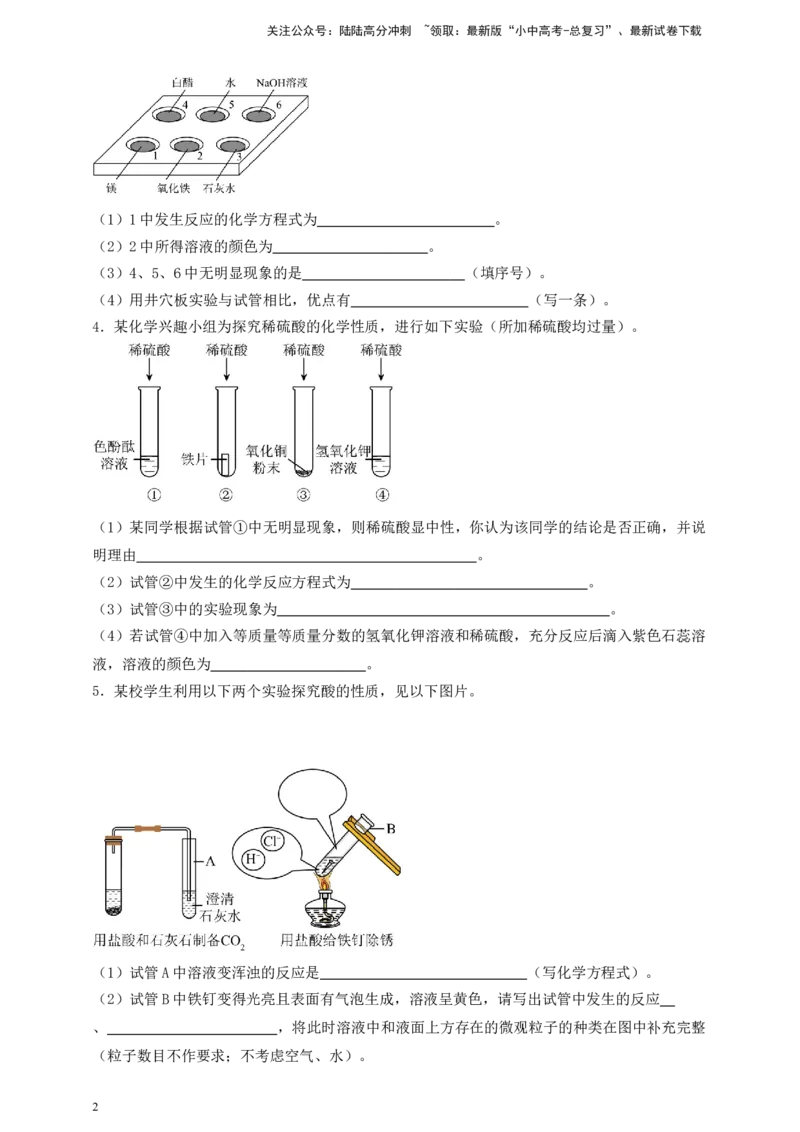
2.微型实验因操作简单、时间较短、自制仪器等特点。某同学按下图装置制取纯净的氢气并验
证氢气性质的微型实验,下列说法错误的是( )
A.注射器中的稀硫酸可以换成浓盐酸
B.青霉素瓶中一定发生置换反应
C.若甲处是浓硫酸,作用是干燥氢气
D.实验可验证氢气密度比空气小
二、实验探究题
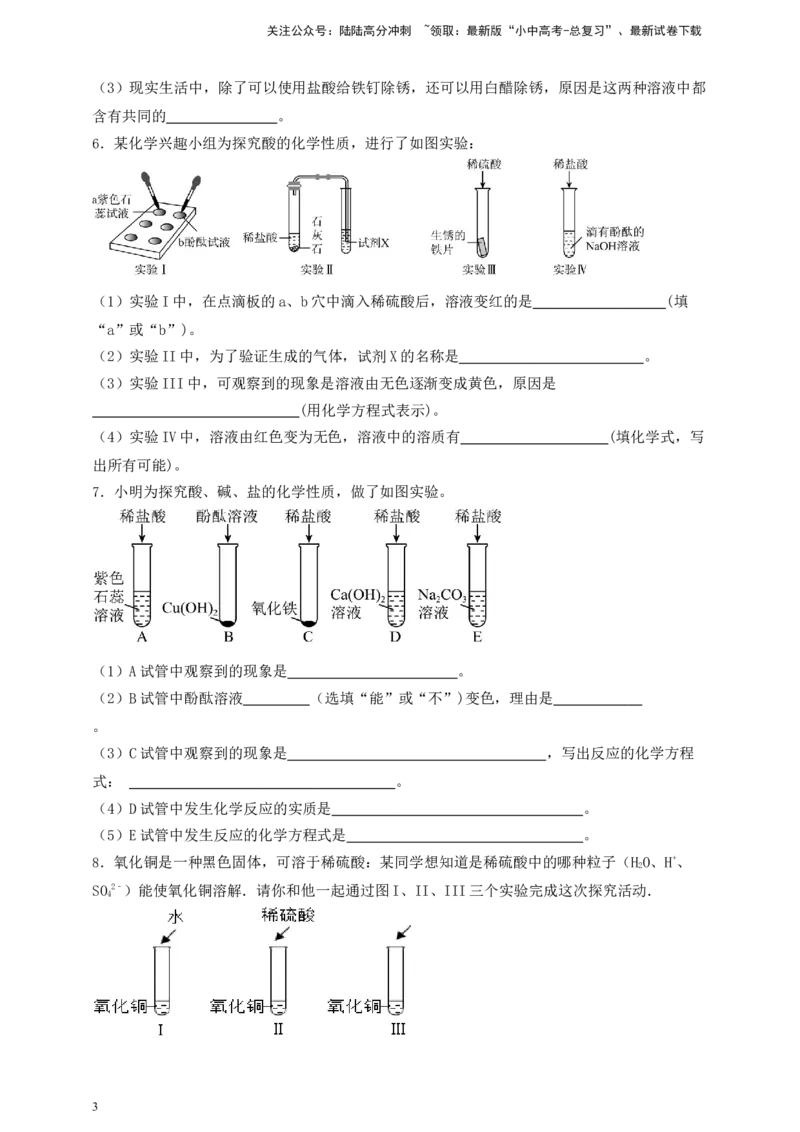
3.兴趣小组利用井穴板完成实验探究,已放置试剂如下图所示,现向孔穴1~3中分别滴加稀
盐酸,4~6中分别滴加无色酚酞溶液。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)1中发生反应的化学方程式为 。
(2)2中所得溶液的颜色为 。
(3)4、5、6中无明显现象的是 (填序号)。
(4)用井穴板实验与试管相比,优点有 (写一条)。
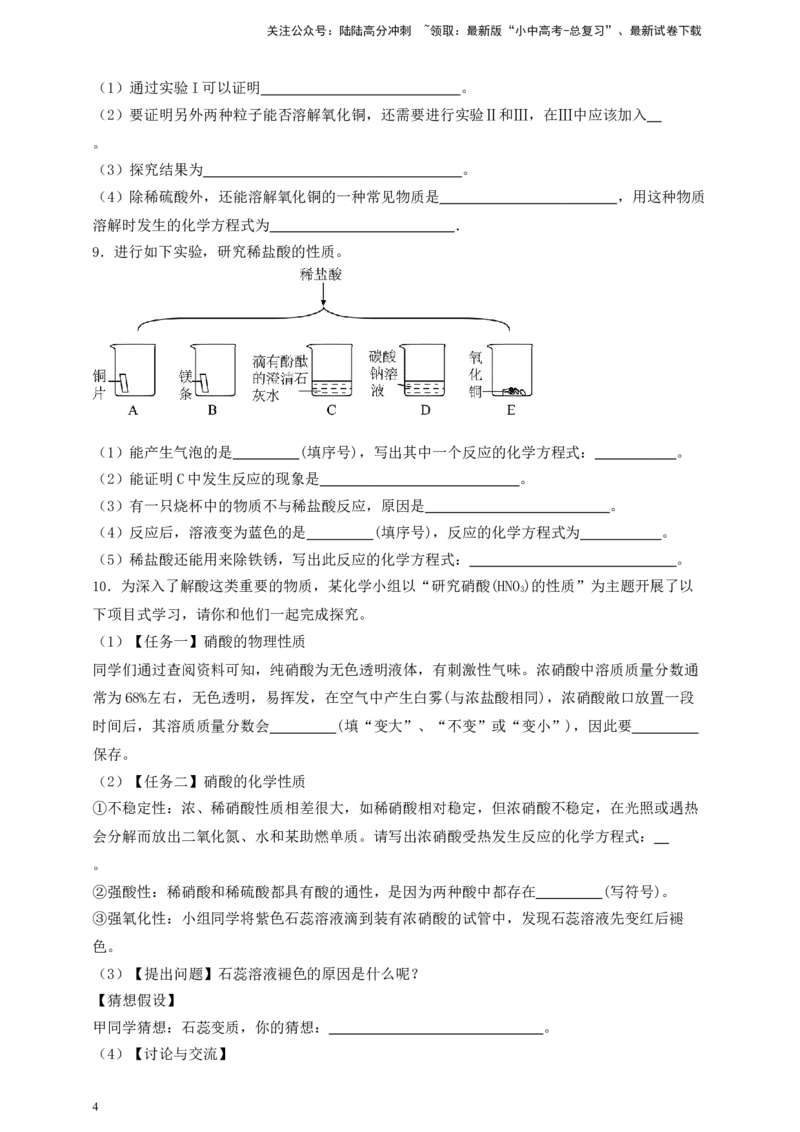
4.某化学兴趣小组为探究稀硫酸的化学性质,进行如下实验(所加稀硫酸均过量)。
(1)某同学根据试管①中无明显现象,则稀硫酸显中性,你认为该同学的结论是否正确,并说
明理由 。
(2)试管②中发生的化学反应方程式为 。
(3)试管③中的实验现象为 。
(4)若试管④中加入等质量等质量分数的氢氧化钾溶液和稀硫酸,充分反应后滴入紫色石蕊溶
液,溶液的颜色为 。
5.某校学生利用以下两个实验探究酸的性质,见以下图片。
(1)试管A中溶液变浑浊的反应是 (写化学方程式)。
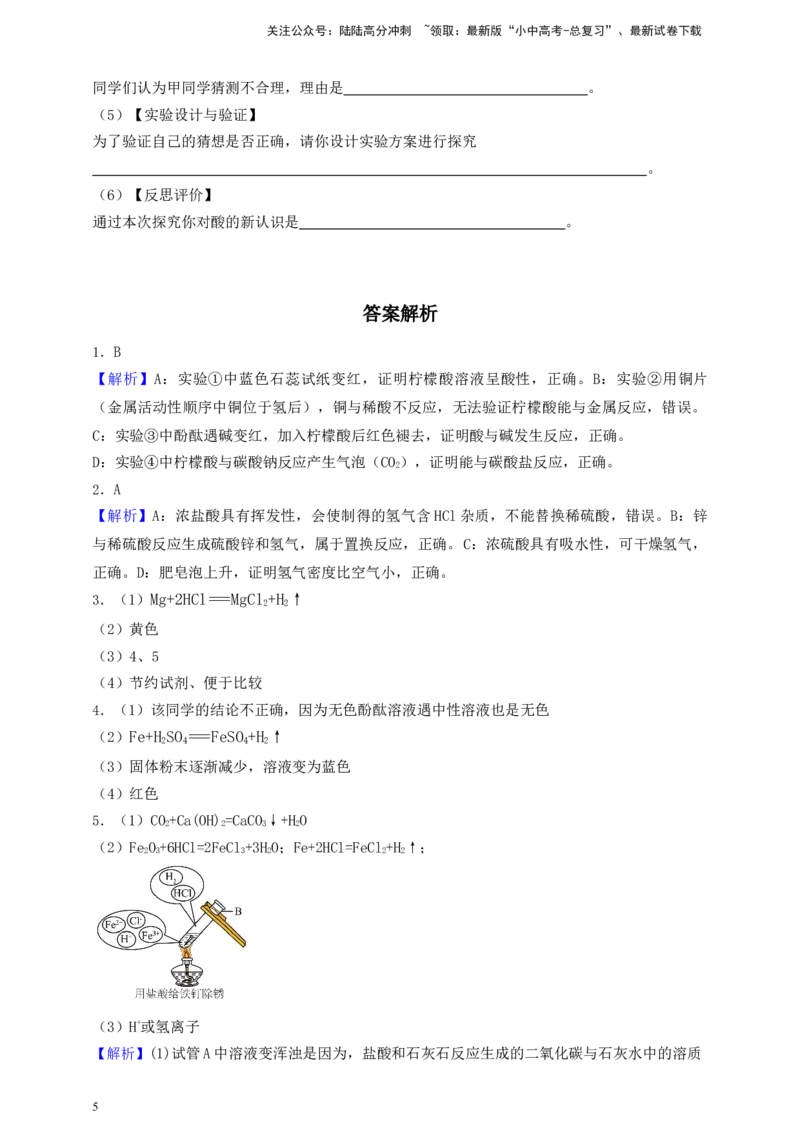
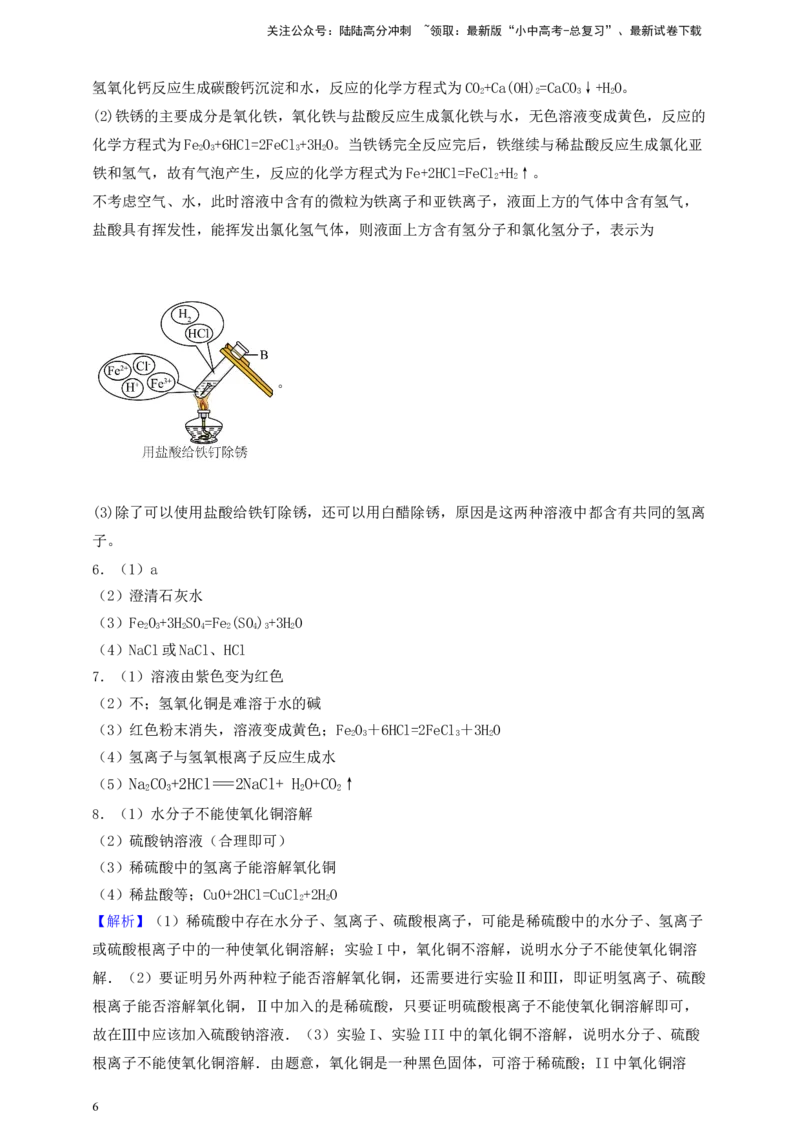
(2)试管B中铁钉变得光亮且表面有气泡生成,溶液呈黄色,请写出试管中发生的反应
、 ,将此时溶液中和液面上方存在的微观粒子的种类在图中补充完整
(粒子数目不作要求;不考虑空气、水)。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)现实生活中,除了可以使用盐酸给铁钉除锈,还可以用白醋除锈,原因是这两种溶液中都
含有共同的 。
6.某化学兴趣小组为探究酸的化学性质,进行了如图实验:
(1)实验I中,在点滴板的a、b穴中滴入稀硫酸后,溶液变红的是 (填
“a”或“b”)。
(2)实验II中,为了验证生成的气体,试剂X的名称是 。
(3)实验III中,可观察到的现象是溶液由无色逐渐变成黄色,原因是
(用化学方程式表示)。
(4)实验IV中,溶液由红色变为无色,溶液中的溶质有 (填化学式,写
出所有可能)。
7.小明为探究酸、碱、盐的化学性质,做了如图实验。
(1)A试管中观察到的现象是 。
(2)B试管中酚酞溶液 (选填“能”或“不”)变色,理由是
。
(3)C试管中观察到的现象是 ,写出反应的化学方程
式: 。
(4)D试管中发生化学反应的实质是 。
(5)E试管中发生反应的化学方程式是 。
8.氧化铜是一种黑色固体,可溶于稀硫酸:某同学想知道是稀硫酸中的哪种粒子(HO、H+、
2
SO2﹣)能使氧化铜溶解.请你和他一起通过图I、II、III三个实验完成这次探究活动.
4
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)通过实验I可以证明 。
(2)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入
。
(3)探究结果为 。
(4)除稀硫酸外,还能溶解氧化铜的一种常见物质是 ,用这种物质
溶解时发生的化学方程式为 .
9.进行如下实验,研究稀盐酸的性质。
(1)能产生气泡的是 (填序号),写出其中一个反应的化学方程式: 。
(2)能证明C中发生反应的现象是 。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是 。
(4)反应后,溶液变为蓝色的是 (填序号),反应的化学方程式为 。
(5)稀盐酸还能用来除铁锈,写出此反应的化学方程式: 。
10.为深入了解酸这类重要的物质,某化学小组以“研究硝酸(HNO)的性质”为主题开展了以
3
下项目式学习,请你和他们一起完成探究。
(1)【任务一】硝酸的物理性质
同学们通过查阅资料可知,纯硝酸为无色透明液体,有刺激性气味。浓硝酸中溶质质量分数通
常为68%左右,无色透明,易挥发,在空气中产生白雾(与浓盐酸相同),浓硝酸敞口放置一段
时间后,其溶质质量分数会 (填“变大”、“不变”或“变小”),因此要
保存。
(2)【任务二】硝酸的化学性质
①不稳定性:浓、稀硝酸性质相差很大,如稀硝酸相对稳定,但浓硝酸不稳定,在光照或遇热
会分解而放出二氧化氮、水和某助燃单质。请写出浓硝酸受热发生反应的化学方程式:
。
②强酸性:稀硝酸和稀硫酸都具有酸的通性,是因为两种酸中都存在 (写符号)。
③强氧化性:小组同学将紫色石蕊溶液滴到装有浓硝酸的试管中,发现石蕊溶液先变红后褪
色。
(3)【提出问题】石蕊溶液褪色的原因是什么呢?
【猜想假设】
甲同学猜想:石蕊变质,你的猜想: 。
(4)【讨论与交流】
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
同学们认为甲同学猜测不合理,理由是 。
(5)【实验设计与验证】
为了验证自己的猜想是否正确,请你设计实验方案进行探究
。
(6)【反思评价】
通过本次探究你对酸的新认识是 。
答案解析
1.B
【解析】A:实验①中蓝色石蕊试纸变红,证明柠檬酸溶液呈酸性,正确。B:实验②用铜片
(金属活动性顺序中铜位于氢后),铜与稀酸不反应,无法验证柠檬酸能与金属反应,错误。
C:实验③中酚酞遇碱变红,加入柠檬酸后红色褪去,证明酸与碱发生反应,正确。
D:实验④中柠檬酸与碳酸钠反应产生气泡(CO ),证明能与碳酸盐反应,正确。
2
2.A
【解析】A:浓盐酸具有挥发性,会使制得的氢气含HCl杂质,不能替换稀硫酸,错误。B:锌
与稀硫酸反应生成硫酸锌和氢气,属于置换反应,正确。C:浓硫酸具有吸水性,可干燥氢气,
正确。D:肥皂泡上升,证明氢气密度比空气小,正确。
3.(1)Mg+2HCl=MgCl +H ↑
2 2
(2)黄色
(3)4、5
(4)节约试剂、便于比较
4.(1)该同学的结论不正确,因为无色酚酞溶液遇中性溶液也是无色
(2)Fe+H SO =FeSO +H ↑
2 4 4 2
(3)固体粉末逐渐减少,溶液变为蓝色
(4)红色
5.(1)CO+Ca(OH)=CaCO↓+HO
2 2 3 2
(2)FeO+6HCl=2FeCl+3HO;Fe+2HCl=FeCl+H↑;
2 3 3 2 2 2
(3)H+或氢离子
【解析】(1)试管A中溶液变浑浊是因为,盐酸和石灰石反应生成的二氧化碳与石灰水中的溶质
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为CO+Ca(OH)=CaCO↓+HO。
2 2 3 2
(2)铁锈的主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁与水,无色溶液变成黄色,反应的
化学方程式为FeO+6HCl=2FeCl+3HO。当铁锈完全反应完后,铁继续与稀盐酸反应生成氯化亚
2 3 3 2
铁和氢气,故有气泡产生,反应的化学方程式为Fe+2HCl=FeCl+H↑。
2 2
不考虑空气、水,此时溶液中含有的微粒为铁离子和亚铁离子,液面上方的气体中含有氢气,
盐酸具有挥发性,能挥发出氯化氢气体,则液面上方含有氢分子和氯化氢分子,表示为
。
(3)除了可以使用盐酸给铁钉除锈,还可以用白醋除锈,原因是这两种溶液中都含有共同的氢离
子。
6.(1)a
(2)澄清石灰水
(3)FeO+3HSO=Fe(SO)+3HO
2 3 2 4 2 4 3 2
(4)NaCl或NaCl、HCl
7.(1)溶液由紫色变为红色
(2)不;氢氧化铜是难溶于水的碱
(3)红色粉末消失,溶液变成黄色;FeO+6HCl=2FeCl+3HO
2 3 3 2
(4)氢离子与氢氧根离子反应生成水
(5)Na CO +2HCl=2NaCl+ H O+CO ↑
2 3 2 2
8.(1)水分子不能使氧化铜溶解
(2)硫酸钠溶液(合理即可)
(3)稀硫酸中的氢离子能溶解氧化铜
(4)稀盐酸等;CuO+2HCl=CuCl+2HO
2 2
【解析】(1)稀硫酸中存在水分子、氢离子、硫酸根离子,可能是稀硫酸中的水分子、氢离子
或硫酸根离子中的一种使氧化铜溶解;实验I中,氧化铜不溶解,说明水分子不能使氧化铜溶
解.(2)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,即证明氢离子、硫酸
根离子能否溶解氧化铜,Ⅱ中加入的是稀硫酸,只要证明硫酸根离子不能使氧化铜溶解即可,
故在Ⅲ中应该加入硫酸钠溶液.(3)实验I、实验III中的氧化铜不溶解,说明水分子、硫酸
根离子不能使氧化铜溶解.由题意,氧化铜是一种黑色固体,可溶于稀硫酸;II中氧化铜溶
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
解,说明稀硫酸中的氢离子使氧化铜溶解.(4)根据所学知识可以判断稀盐酸等也可以使氧化
铜溶解.氧化铜与稀盐酸反应生成氯化铜和水,反应的化学方程式为:CuO+2HCl=CuCl+2HO.
2 2
故答案为:(1)水分子不能使氧化铜溶解;(2)硫酸钠溶液(合理即可);(3)稀硫酸中的
氢离子能溶解氧化铜;(4)稀盐酸等;CuO+2HCl=CuCl+2HO.
2 2
9.(1)B、D;Mg+2HCl=MgCl +H ↑
2 2
(2)溶液红色消失
(3)铜的活动顺序排在氢后
(4)E;CuO+2HCl=CuCl+2HO.
2 2
(5)Fe O +6HCl=2FeCl +3H O
2 3 3 2
10.(1)变小;密封
Δ
(2)4HNO (浓)¿2H O+4NO ↑+O ↑;H+
3 2 2 2
¿
(3)浓硝酸的强氧化性使其褪色
(4)紫色石蕊溶液刚开始时变成红色
(5)分别取2mL稀硝酸于A试管和浓硝酸于B试管中,依次滴加相同滴数的紫色石蕊溶液,A
中溶液变红,不褪色,B 中溶液先变红后褪色,证明石蕊褪色原因是浓硝酸的强氧化性使其褪
色
(6)酸的浓度会影响酸的化学性质
【解析】(1)根据题意,浓硝酸易挥发,浓硝酸敞口放置一段时间后, 会挥发出硝酸气体,
溶质质量分数会变小;为了防止浓硝酸挥发,浓硝酸应密封保存;
(2)①由题意可知,浓硝酸在光照或遇热会分解而放出二氧化氮、水和某助燃单质,氧气具有
Δ
助燃性因此该单质为氧气,反应的化学方程式为4HNO (浓)¿2H O+4NO ↑+O ↑;
3 2 2 2
¿
②稀硝酸具有酸的通性,是因为稀硝酸溶液中存在氢离子,故填:H+;
(3)浓硝酸具有很强的氧化性, 也能使紫色石蕊溶液褪色,故填:浓硝酸的强氧化性使其褪
色;
(4)同学们认为甲同学猜测不合理, 理由是紫色石蕊溶液滴到装有浓硝酸的试管中,发现石
蕊溶液先变红后褪色,说明紫色石蕊没有变质,故填:紫色石蕊溶液刚开始时变成红色;
(5)验证猜想可:分别取2mI稀硝酸于A试管和浓硝酸于B试管中,依次滴加相同滴数的紫色
石蕊溶液,A中溶液变红,不褪色,B中溶液先变红后褪色,证明石蕊褪色原因是浓硝酸的强氧
化性使其褪色,故填:分别取2mL稀硝酸于A试管和浓硝酸于B试管中,依次滴加相同滴数的
紫色石蕊溶液,A中溶液变红,不褪色,B中溶液先变红后褪色,证明石蕊褪色原因是浓硝酸的
强氧化性使其褪色;
(6)通过本次探究可发现酸的浓度会影响酸的化学性质,如:稀硝酸不能使变红的石蕊褪色,
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
浓硝酸可使变红的石蕊又褪色,故填:酸的浓度会影响酸的化学性质。
8