文档内容
2022 届高三化学二轮复习氯气及氯的化合物必刷卷
一、选择题(共17题)
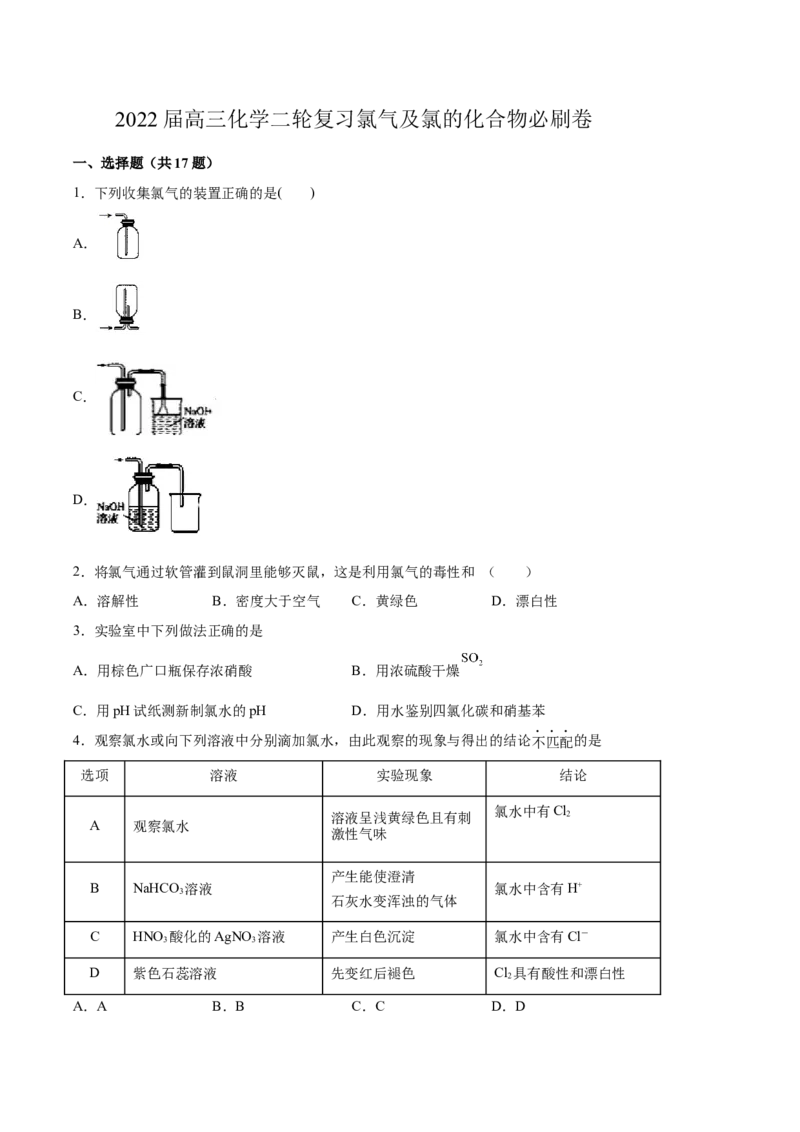
1.下列收集氯气的装置正确的是( )
A.
B.
C.
D.
2.将氯气通过软管灌到鼠洞里能够灭鼠,这是利用氯气的毒性和 ( )
A.溶解性 B.密度大于空气 C.黄绿色 D.漂白性
3.实验室中下列做法正确的是
A.用棕色广口瓶保存浓硝酸 B.用浓硫酸干燥
C.用pH试纸测新制氯水的pH D.用水鉴别四氯化碳和硝基苯
4.观察氯水或向下列溶液中分别滴加氯水,由此观察的现象与得出的结论不匹配的是
选项 溶液 实验现象 结论
氯水中有Cl
溶液呈浅黄绿色且有刺 2
A 观察氯水
激性气味
产生能使澄清
B NaHCO 溶液 氯水中含有H+
3
石灰水变浑浊的气体
C HNO 酸化的AgNO 溶液 产生白色沉淀 氯水中含有Cl-
3 3
D 紫色石蕊溶液 先变红后褪色 Cl 具有酸性和漂白性
2
A.A B.B C.C D.D5.下列不属于氧化还原反应的是
A. B.
C. D.
6.2020年春节前后,新冠病毒肆虐全球,防控疫情已成为国际首要大事。按照以往对冠状病毒的经验,
乙醚、75%乙醇、含氯的消毒剂、过氧乙酸等均可有效灭活病毒,下列有关说法错误的是
A.因乙醇易燃,不可使用酒精溶液大面积对室内空气进行消毒
B.次氯酸钠具有一定的腐蚀性和刺激性,使用时需带手套,并稀释使用
C.过氧乙酸(CHCOOOH)用于杀灭病毒是因为其含有羧基
3
D.不能将“84消毒液”和洁厕灵混合进行环境消毒
7.下列实验仪器或装置的选择正确的是
A B C D
收集 CO 除去Cl 中的 HCl 配制 20.00mL0.1 mol∙L−1NaCO 溶液 制取乙炔
2 2 2 3
A.A B.B C.C D.D
8.钛合金被誉为二十一世纪的金属,具有广泛的用途。金属钛可用下列方法提炼:
①TiO +2C+2Cl TiCl +2CO②TiCl +2Mg 2MgCl +Ti
2 2 4 4 2
对上述两个反应,下列有关叙述正确的是
A.反应①中Cl 是还原剂 B.反应①中碳元素被还原
2
C.②中钛元素被氧化 D.反应②中TiCl 是氧化剂
4
9.下列反应属于氧化还原反应的是
A.CaCO CaO+CO ↑ B.Fe O+3CO 2Fe+3CO
3 2 2 3 2
C.CaO+H O=Ca(OH) D.NaO+2HCl= 2NaCl+H O
2 2 2 210.下列常用消毒剂中,其消毒原理与其它三种不同的是
A.医用酒精 B.双氧水
C.84消毒液 D.漂粉精
11.下列描述的过程不属于化学变化的是
A.氧气在放电的条件下变成臭氧 B.加热胆矾得白色无水硫酸铜
C.古书中记载“…,煮海为盐” D.漂粉精久置于空气中后会变硬
12.南方洪灾后,为确保“大灾之后无大疫”,防疫人员可以喷洒“含氯消毒液”(成分为次氯酸钠)进
行消毒。关于该消毒剂的说法错误的是( )
A.“含氯消毒液”中的次氯酸钠是弱电解质
B.加少量盐酸可以提高“含氯消毒液”中次氯酸含量
C.“含氯消毒液”具有的强氧化性能够有效地杀死病毒
D.“含氯消毒液”应密闭保存,防止与空气反应
13.下列有关试剂的保存方法,错误的是
A.漂白粉密封保存于阴凉干燥的地方 B.少量的金属钠保存在煤油中
C.盛装NaOH溶液的试剂瓶用橡皮塞 D.新制的氯水保存在无色试剂瓶中
14.在淀粉碘化钾溶液中加入少量次氯酸钠溶液,振荡,溶液变蓝。在上述溶液中加入足量的亚硫酸钠溶
液,蓝色逐渐消失。下列判断错误的是( )
A.氧化性:ClO->SO 2->I
4 2
B.漂白粉溶液可使淀粉碘化钾试纸变蓝
C.向新制氯水中加入足量亚硫酸钠溶液,氯水褪色
D.ClO-与I-在碱性条件可以发生氧化还原反应
15.下列关于含氯消毒剂的解释不正确的是
A.84消毒液不能与洁厕灵混合使用:2H++Cl-+ClO-=Cl↑+H O
2 2
B.工业上将氯气通入澄清石灰水中制取漂白粉:2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O
2 2 2 2 2
C.氯水应避光保存的原因是:2HClO 2HCl+O ↑
2
D.向Ca(ClO) 溶液中通入适量CO 可增强漂白效果:Ca(ClO) +CO +H O=CaCO ↓+2HClO
2 2 2 2 2 3
16.甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,记录结果如下:
甲:KSO 、BaCl 、NaCl;
2 4 2
乙:NaCl、Ba(OH) 、KCO;
2 2 3
丙:HCl、KCO、NaCl;
2 3
丁:KSO 、NaCO、KCl;
2 4 2 3其中记录结果合理的是
A.甲 B.乙 C.丙 D.丁
17.下列装置或操作能达到实验目的的是
A.用装置甲制取氯气 B.用乙装置除去氯气中的HCl气体
C.用丙装置萃取溴水中的溴单质 D.用丁装置分离乙酸与乙醇
二、综合题(共5题)
18.实验室常用二氧化锰和浓盐酸反应制取氯气,化学反应方程式如下:MnO +4HCl
2
MnCl +Cl↑+2H O,将一定量的MnO 加入足量浓盐酸中,充分反应后放出6.72L(标准状况下)气体,将反
2 2 2 2
应后的溶液加水稀释至500mL。
(1)求参加反应MnO 的质量___________。
2
(2)求最终溶液中MnCl 的物质的量浓度______________。
2
19.A、B、C、D为为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为无色气体。D、E、
F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下
为液体。它们之间转化关系如下图所示(其中某些反应条件和部分反应物已略去)。
请回答下列问题:(1)写出下列物质的化学式:A_______、X_______。
(2)在反应;① ~⑦中,属于氧化还原反应的有_______个;反应⑥说明D溶液中含有_______离子。
(3)反应④的离子方程式是_______。
(4)反应⑦的化学方程式是_______。
(5)检验D的溶液中是否含有G离子的方法是_______。
(6)除去D溶液中混有的少量G的方法是_______。
20.如图,反应①为常温下的反应, 、 、 中均含有氯元素,且 中氯元素的化合价介于 和 中氯
元素的化合价之间, 在常温下为无色无味的液体, 是淡黄色固体, 为常见的无色气体。请据图回答
下列问题:
(1) 、 的化学式分别为___________、___________;
(2)写出反应①的离子方程式:___________。
(3)写出反应②的离子方程式:___________。
(4)已知 是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列
问题。
①将 通入紫色石蕊溶液中,观察到的现象是___________。请写出 与水反应的离子方程式:
___________。
② 可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是___________(用化学方程式表示)。
21.高铁酸钾(KFeO)具有强氧化性,可作为水处理剂和高容量电池材料。工业上生产高铁酸钾的工艺
2 4
流程如下:
已知KFeO 具有下列性质:①可溶于水,微溶于KOH溶液,难溶于异丙醇;②在0℃-5℃,强碱性溶液
2 4
中比较稳定;③在Fe3+和Fe(OH) 催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成
3Fe(OH) 和O
3 2
请完成下列填空:
(1)已知Cl 与KOH在低温下可制得KClO,请写出化学反应方程式____________。
2
(2)在“反应液Ⅰ”中加KOH固体的目的是____________________。
(3)生产KFeO 的化学反应方程式为________________,制备KFeO 时,须将Fe(NO ) 溶液缓慢滴加到
2 4 2 4 3 3
碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是___________________。
(4)请补充完整由“反应液Ⅱ”得到KFeO 晶体的实验步骤。(可选用的试剂:NaOH溶液、KOH溶液、
2 4
蒸馏水和异丙醇)
① 向反应液Ⅱ中加入饱和________,在冰水浴中静置结晶后过滤,得KFeO 粗产品;
2 4
② 将KFeO 粗产品溶解在___________中,再次在冰水浴中静置结晶后过滤,得到较纯净的KFeO;
2 4 2 4
③ 将KFeO 晶体再用少量__________洗涤,低温真空干燥,得到高铁酸钾成品。
2 4
(5)从“反应液Ⅱ”中分离出KFeO 晶体后,可以得到的副产品有_________(写化学式)。
2 4
22.请分析下列氧化还原反应,该反应为实验室用MnO 和浓盐酸(注意不是稀盐酸)反应制备Cl
2 2
MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
①用单线桥法表示出电子转移方向和数量___________。
②该反应的氧化剂是___________。
③HCl在该反应中体现的化学性质有___________、___________。
④实验测定,当MnO 足量时,无论如何控制条件,用含146gHCl的浓盐酸参与反应,得到的氯气始终小
2
于71g,产生该现象的一个原因是HCl易挥发,另一个原因可能是___________参考答案
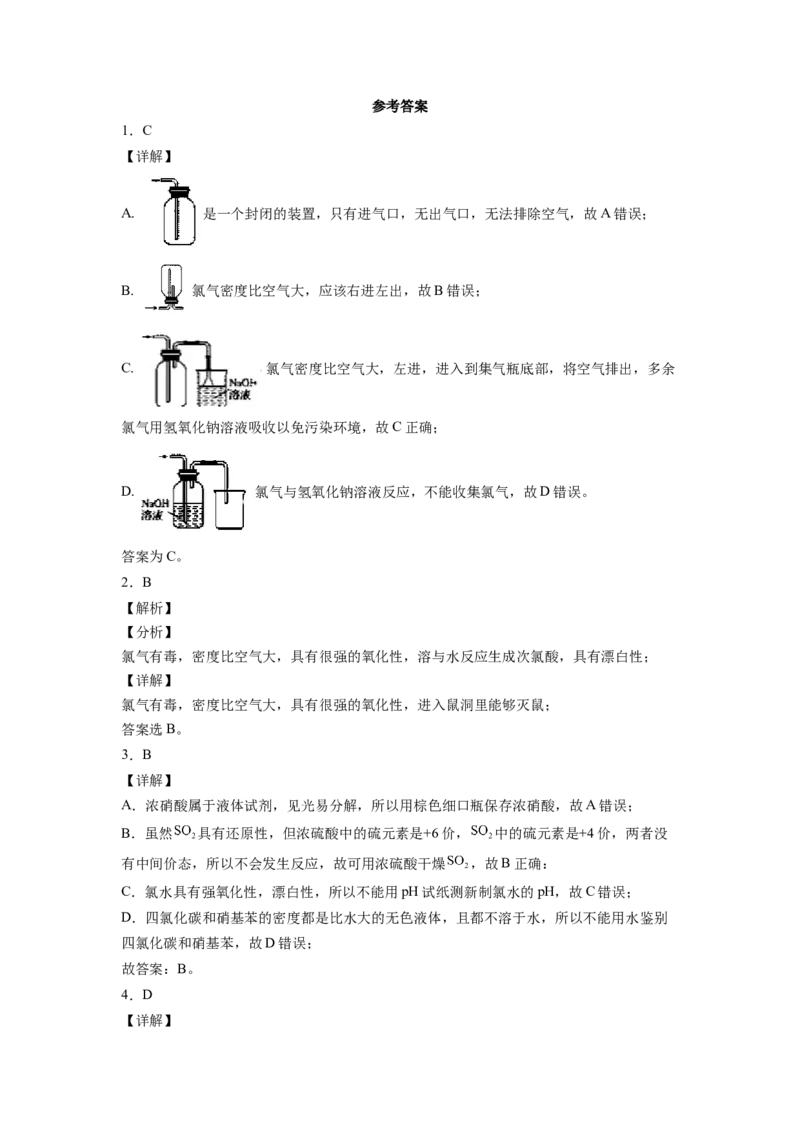
1.C
【详解】
A. 是一个封闭的装置,只有进气口,无出气口,无法排除空气,故A错误;
B. 氯气密度比空气大,应该右进左出,故B错误;
C. 氯气密度比空气大,左进,进入到集气瓶底部,将空气排出,多余
氯气用氢氧化钠溶液吸收以免污染环境,故C正确;
D. 氯气与氢氧化钠溶液反应,不能收集氯气,故D错误。
答案为C。
2.B
【解析】
【分析】
氯气有毒,密度比空气大,具有很强的氧化性,溶与水反应生成次氯酸,具有漂白性;
【详解】
氯气有毒,密度比空气大,具有很强的氧化性,进入鼠洞里能够灭鼠;
答案选B。
3.B
【详解】
A.浓硝酸属于液体试剂,见光易分解,所以用棕色细口瓶保存浓硝酸,故A错误;
B.虽然 具有还原性,但浓硫酸中的硫元素是+6价, 中的硫元素是+4价,两者没
有中间价态,所以不会发生反应,故可用浓硫酸干燥 ,故B正确:
C.氯水具有强氧化性,漂白性,所以不能用pH试纸测新制氯水的pH,故C错误;
D.四氯化碳和硝基苯的密度都是比水大的无色液体,且都不溶于水,所以不能用水鉴别
四氯化碳和硝基苯,故D错误;
故答案:B。
4.D
【详解】A.氯水中含有Cl,所以溶液呈浅黄绿色且有刺激性气味,故A正确;
2
B.NaHCO 溶液滴加氯水,产生能使澄清石灰水变浑浊的气体,是二氧化碳,说明氯水中
3
有酸性物质,即含有H+,故B正确;
C.溶液与HNO 酸化的AgNO 溶液反应产生白色沉淀,只能是氯离子与银离子反应得到
3 3
AgCl白色沉淀,说明氯水中含有Cl−,故C正确;
D. Cl 与水反应生成HCl和具有强氧化性的HClO,溶液呈酸性并具有强氧化性,能使石蕊
2
试液先变红后褪色,表现出HCl的酸性和HClO的漂白性,而不是氯气,故D错误;
5.D
【详解】
A.该反应中Zn和H元素化合价发生变化,属于氧化还原反应,故A不选;
B.该反应中W和H元素化合价发生变化,属于氧化还原反应,故B不选;
C.该反应中O和Cl元素化合价发生变化,属于氧化还原反应,故C不选;
D.该反应中没有元素化合价发生变化,属于氧化还原反应,故D选;
故选D。
6.C
【详解】
A.酒精可使蛋白质发生变性,可用于消毒,且易燃烧,则不可使用酒精溶液大面积对室
内空气进行消毒,故A正确;
B.次氯酸钠具有腐蚀性和刺激性,可杀菌消毒,且使用时需带手套,并稀释使用,减少
对人体的危害,故B正确;
C.过氧乙酸含过氧键,具有强氧化性,用于杀灭病毒,与含羧基无关,故C错误;
D.“84消毒液”和洁厕灵混合可发生反应产生氯气,则不能混合使用进行环境消毒,故
D正确;故答案选C。
7.D
【详解】
A.二氧化碳密度比空气大,应该用向上排空气法,故A错误;
B.除去Cl 中的 HCl ,应长进短出,故B错误;
2
C.应该使用容量瓶先配制配制 50mL 0.1 mol∙L−1NaCO 溶液,再取出20mL,故C错误;
2 3
D.广口瓶中放入电石,漏斗中装入饱和食盐水,发生反应生成乙炔,故D正确。
综上所述,答案为D。
8.D
【详解】
A.反应①中Cl 的化合价由0降低到-1价,被还原,是氧化剂 ,故A错误;
2
B.反应①中碳元素由0价升高到+2价,被氧化,故B错误;
C.②中钛元素由+4价降低到0价,被还原,故C错误;
D.反应②中TiCl 中Ti的化合价由+4价降低到0价,被还原,是氧化剂,故D正确;
4故选D。
9.B
【分析】
反应中存在含元素化合价变化的反应为氧化还原反应,不含元素化合价变化的反应为非氧
化还原反应。
【详解】
A.CaCO CaO+CO ↑中各元素化合价都没有发生变化,不属于氧化还原反应,故A不选;
3 2
B.Fe O+3CO 2Fe+3CO ,Fe、C元素化合价发生变化,属于氧化还原反应,故B选;
2 3 2
C.反应CaO+H O=Ca(OH) 中各元素化合价都没有发生变化,不属于氧化还原反应,故C
2 2
不选;
D.NaO+2HCl= 2NaCl+H O中各元素化合价都没有发生变化,不属于氧化还原反应,故D
2 2
不选;
故选B。
10.A
【详解】
A.酒精的分子具有很大的渗透能力,它能穿过细菌表面的膜,打入细菌的内部,使构成
细菌生命基础中的蛋白质分子结构改变,引起使其蛋白质变性,与氧化还原无关,消毒原
理与其他三种不同,故A符合;
B. 双氧水具有强氧化性,消毒原理与氧化还原有关,消毒原理与其他二种相同,故B不
符;
C. 84消毒液的消毒原理与氧化还原有关,消毒原理与其他二种相同,故C不符;
D. 漂粉精可以生成具有强氧化性的次氯酸,消毒原理与氧化还原有关,消毒原理与其他
二种相同,故D不符;
故选A。
11.C
【详解】
A选项,氧气在放电的条件下变成臭氧,有新物质生成,因此发生了化学变化,故A属于
化学变化;
B选项,加热胆矾得白色无水硫酸铜,由CuSO ∙5H O变为了CuSO ,失去结晶水,因此是
4 2 4
化学变化,故B属于化学变化;
C选项,古书中记载“…,煮海为盐”仅仅是蒸发了海水,没有发生化学变化,故C不属
于化学变化;
D选项,漂粉精久置于空气中后会变硬,漂粉精中的有效成分次氯酸钙和空气中的二氧化
碳和水反应生成了碳酸钙,因此发生了化学变化,故D属于化学变化;
综上所述,答案为C。12.A
【详解】
A.次氯酸钠易溶于水完全电离,属于强电解质,故A错误;
B. 次氯酸钠溶液中存在水解平衡:ClO-+H
2
O⇌HClO+OH-,加少量盐酸,减小c(OH-),
平衡右移,HClO浓度增大,故B正确;
C.NaClO具有强氧化性,可以使蛋白质变性,能够有效地杀死病毒,故C正确;
D.碳酸的酸性大于次氯酸,因此次氯酸钠溶液与二氧化碳反应生成次氯酸,次氯酸见光或
受热易分解,漂白作用减弱或失去,因此“含氯消毒液”应密闭保存,故D正确;
故答案选A。
13.D
【解析】
【详解】
A、漂白粉有效成分为Ca(ClO),Ca(ClO) 和空气中水分、CO 反应生成HClO,次氯
2 2 2
酸见光受热易分解,故在阴凉干燥处保存,说法正确;
B、钠的密度大于煤油,煤油能隔绝空气,防止钠与氧气反应,说法正确;
C、试剂瓶瓶口是磨制口,SiO 外露,与NaOH反应生成硅酸钠,硅酸钠具有黏合性,把
2
玻璃塞和瓶体黏合在一起,故说法正确;
D、氯水的成分Cl、HClO、HCl,其中HClO见光受热易分解,保存在棕色试剂瓶中,故
2
说法错误。
答案选D。
14.A
【解析】
【详解】
A.根据题意可知次氯酸钠将碘化钾氧化为单质碘,所以氧化性:ClO->I,碘单质将亚
2
硫酸钠氧化为硫酸钠,所以氧化性:I>SO 2-,故氧化性顺序:ClO->I>SO 2-,选项A
2 4 2 4
错误;
B.次氯酸钠将碘化钾氧化为单质碘,所以漂白粉溶液(成分中含有次氯酸钙)也能将碘
化钾氧化为单质碘,而使淀粉碘化钾试纸变蓝,选项B正确;
C.氧化性顺序:ClO->I>SO 2-,所以次氯酸钠可以将亚硫酸钠氧化,氯水褪色,选项
2 4
C正确;
D.次氯酸钠溶液水解显碱性,次氯酸在碱性溶液中具有强氧化性,能把碘离子氧化为单
质碘,选项D正确。
答案选A。
15.B
【详解】
A.84消毒液不能与洁厕灵混合使用的原因是2H++Cl-+ClO-=Cl↑+H O,生成有污染的氯气,
2 2
且降低消毒能力,故A正确;B.工业上是将氯气通入石灰乳制漂白粉,而不是澄清石灰水,故B错误;
C.因HClO不稳定,见光分解生成HCl和O,则氯水应避光保存,故C正确;
2
D.碳酸的酸性比HClO酸性强,向Ca(ClO) 溶液中通入适量CO 可提高HClO的浓度,增
2 2
强漂白效果,故D正确;
故答案为B。
16.D
【详解】
A、甲会形成BaSO 沉淀而不能共存,A错误;
4
B、乙会形成BaCO 沉淀而不能共存,B错误;
3
C、丙会产生CO 气体而不能共存,C错误;
2
D、丁的各物质彼此不会反应,可以共存,D正确;
故合理选项为D。
17.C
【详解】
A.浓盐酸和二氧化锰的应在加热条件下进行,常温下二者不反应,不能制备氯气,故A
错误;
B.氯气和HCl气体都与氢氧化钠溶液反应,应用饱和食盐水除杂,故B错误;
C.溴易溶于苯而不易溶于水,故可用丙装置萃取溴水中的溴单质,C正确;
D.温度计用于测量馏分的温度,温度计水银球应位于蒸馏烧瓶的支管口附近,故D错误;
故选C。
18.26.1g 0.6mol/L
【详解】
(1)二氧化锰与浓盐酸反应生成氯气,则6.72L(标准状况下)气体为0.3mol的氯气,根据方
程式可知,生成0.3mol氯气,需要二氧化锰0.3mol,质量=0.3mol×87g/mol=26.1g;
(2)根据Mn原子守恒,MnCl 的物质的量为0.3mol,则浓度为0.3mol÷500mL=0.6mol/L。
2
19.Fe HCl 5 Fe3+ 2Fe3++Fe=3Fe2+ 3Fe+4HO(g) Fe O+4H
2 3 4 2
取少量D的溶液,向其中加入几滴酸性KMnO 溶液,若紫红色褪去,则含有Fe2+,若紫红
4
色不褪去,则不含Fe2+。(或用六氰合铁酸钾) 向混合液中通入足量的氯气(或加入足量
的HO)
2 2
【分析】
A为固体,B为黄绿色气体,说明B为Cl,D与F反应得到血红色溶液,结合转化关系可
2
知,固体A为Fe,D为FeCl ,F为KSCN,由D与G之间的相互转化,可知G为FeCl ,
3 2
Fe与无色气体C反应得到E,E与X反应得到D、G、H,且X常温下是无色气体,其水溶
液是一种强酸,E为黑色固体,H在常温下为液体,可推知C为O,E为Fe O,X为
2 3 4
HCl,H为HO,据此解答。
2【详解】
(1)由上述分析可知,A为Fe,X为HCl,故答案为Fe;HCl;
(2)在反应①~⑦中,①为铁和氯气发生的氧化还原反应,②为铁和氧气发生的氧化还原反
应,③为四氧化三铁和盐酸发生的复分解反应,不是氧化还原反应,④为氯化铁和铁发生
的氧化还原反应,⑤为氯化亚铁和氯气发生的氧化还原反应,⑥是氯化铁和硫氰酸盐发生
的复分解反应,不是氧化还原反应,反应⑦是铁与水在高温下的置换反应,是氧化还原反
应,所以属于氧化还原反应的有①②④⑤⑦,共5个,反应⑥遇KSCN溶液呈血红色,说
明D溶液中有Fe3+,故答案为5;Fe3+;
(3)反应④的离子方程式是:2Fe3++Fe=3Fe2+,故答案为2Fe3++Fe=3Fe2+;
(4)反应⑦是铁在水蒸气中发生的反应生成四氧化三铁和氢气,反应的化学方程式为:
3Fe+4H O(g) Fe O+4H ,故答案为3Fe+4H O(g) Fe O+4H ;
2 3 4 2 2 3 4 2
(5)检验FeCl 溶液中是否有FeCl 的方法是:向溶液中滴加高锰酸钾溶液,看紫色高锰酸钾
3 2
溶液是否褪色,如果褪色则说明溶液有亚铁离子,否则没有,故答案为向溶液中滴加高锰
酸钾溶液,看紫色高锰酸钾溶液是否褪色,如果褪色则说明溶液有亚铁离子,若紫红色不
褪去,则不含Fe2+;
(6)除去FeCl 溶液中混有的少量FeCl 的方法是:向混合溶液中通入足量的氯气,故答案为
3 2
向混合溶液中通入足量的氯气。
20.
(1)
(2)
(3)
(4) 紫色试液先变红色,后又褪色
;
【分析】
E在常温下为无色无味的液体,应为HO,F为淡黄色粉末,应为NaO,则G为O,B为
2 2 2 2
NaOH,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,应为Cl 和
2
NaOH的反应,生成NaCl和NaClO,结合物质的性质作答即可。
(1)
由以上分析可知,A为Cl,G为O,故答案为:O、Cl;
2 2 2 2
(2)
由以上分析可知,A为Cl,B为NaOH,所以反应①的离子方程式为:
2
,故答案为: ;
(3)反应②为过氧化钠和水的反应,离子方程式为 ,故答
案为: ;
(4)
①氯气和水反应生成盐酸和次氯酸,发生Cl
2
+H
2
O⇌HCl+HClO,盐酸具有酸性,可使紫色
石蕊试液变红,生成的次氯酸具有漂白性,可使溶液褪色,故答案为:紫色试液先变红色,
后又褪色; ;
②氯气和氢氧化钙反应生成漂白粉,有效成分为Ca(ClO) ,在空气中与二氧化碳、水反应
2
生成不稳定的次氯酸,次氯酸见光分解,涉及反应为
; ,故答案为:
; 。
21.Cl+2KOH=KCl+KClO+H O 为下一步反应提供反应物,与反应液中过量的氯气继
2 2
续反应,生成更多的KClO 2Fe(NO )+3KClO+10KOH=2K FeO+6KNO+3KCl+
3 3 2 4 3
5HO 减少KFeO 在过量Fe3+作用下的分解(或KFeO 在低温、强碱性溶液中比较稳
2 2 4 2 4
定等) KOH溶液 KOH溶液 异丙醇 KNO、KCl
3
【详解】
试题分析:通过对KFeO 制备过程的研究,考查氧化还原反应方程式的书写和配平,以及
2 4
考生对化学实验设计的理解。解答过程中需要仔细读懂题目中对于未知知识的介绍,并且
能够合理加以运用。
解析:流程中物质转化关系如下:
(1)根据已知,Cl 与KOH在低温下的反应类似与Cl 与NaOH在低温下的反应。答案:
2 2
Cl+2KOH=KCl+KClO+H O
2 2
(2)第一步中氯气过量,则第二步KOH是为了将氯气反应完全,同时生成的KClO也是
以下反应的氧化剂,可以使氯气得到充分利用。答案:与反应液中过量的氯气继续反应,
生成更多的KClO,提高氯气的利用率,为下一步反应提供反应物。
(3)K2FeO4是KClO与F3(NO3)3通过氧化还原反应得到的,则有Fe(NO )+
3 3
KClO→K FeO,再充分考虑溶液呈碱性配平反应得到答案。
2 4
答案:2Fe(NO )+3KClO+10KOH=2K FeO+6KNO+3KCl+5HO
3 3 2 4 3 2根据已知,“已知KFeO 具有下列性质:②在0℃-5℃,强碱性溶液中比较稳定;③在
2 4
Fe3+和Fe(OH) 催化作用下发生分解”,所以缓慢加入的Fe(NO ) 可以迅速完全反应,避免
3 3 3
Fe3+催化KFeO 的分解,搅拌则可以使反应可能释放的热量尽快散失,避免溶液的温度升
2 4
高导致的产品分解。答案:减少KFeO 在过量Fe3+作用下的分解(或KFeO 在低温、强碱
2 4 2 4
性溶液中比较稳定等)
(4)此段为KFeO 的分离提纯。①考虑到静置过程中可能导致有更多的KFeO 水解,所
2 4 2 4
以应当加入KOH已知其水解,而加入NaOH会使结晶时产生钠盐沉淀。答案:KOH溶液。
②粗产品再此溶解时也容易水解,同理应当加入KOH溶液。答案:KOH溶液。
③由于KFeO 可溶于水,为了避免溶解损失,所以采用异丙醇洗涤,因为KFeO 难溶于
2 4 2 4
异丙醇。答案:异丙醇。
(5)根据(3)中反应原理,分离出KFeO 晶体后,剩余物主要是KNO 和KCl。答案:
2 4 3
KNO 和KCl。
3
22. MnO 酸性 还原性
2
盐酸浓度变稀,稀盐酸与MnO 不反应
2
【详解】
①MnO 生成氯化锰,锰元素降低两价,HCl(浓)生成氯气,氯元素升高两价,故MnO 与
2 2
HCl(浓)加热反应用单线桥法表示电子转移方向和数量为
,故答案为:
;
②氧化剂为价态降低的反应物,MnO 锰元素价态降低,故MnO 为氧化剂,故答案为:
2 2
MnO ;
2
③HCl在该反应中一部分价态不变生成氯化锰,体现酸性,一部分价态升高生成氯气,体
现还原性,故HCl在该反应中体现的化学性质有酸性、还原性,故答案为:酸性、还原性;
④浓盐酸与MnO 反应生成Cl 的过程中,随着反应的进行,HCl不断被消耗,且部分HCl
2 2
挥发,反应中有水生成,这些因素都导致盐酸浓度变稀,稀盐酸与MnO 不反应。故答案
2
为:盐酸浓度变稀,稀盐酸与MnO 不反应。
2