文档内容
2022 届高三化学二轮复习硫及其化合物专项练习
一、选择题(共17题)
1.无论在化学实验室还是在家中进行实验或探究活动都必须注意安全。下列实验操作正确的是
A.为防止试管破裂,加热固体时试管口一般要略低于试管底
B.不慎将酒精洒到桌面上引起着火,应立即用较多的水浇灭
C.白磷在空气中易自燃,用剩的白磷可溶解于CS 后倒入垃圾箱
2
D.配制HSO 溶液时,先在量筒中加一定体积的水,再在搅拌下慢慢加入浓HSO
2 4 2 4
2.下列说法正确的是
A.从性质的角度分类,SO 和NO 都属于酸性氧化物
2 2
B.从在水中是否发生电离的角度,SO 和NO 都属于电解质
2 2
C.从元素化合价的角度分类,SO 和NO 都既可作氧化剂又可作还原剂
2 2
D.从对大气及环境影响和颜色的角度,SO 和NO 都是大气污染物,都是有色气体
2 2
3.在强酸性溶液中,可以大量共存的离子组是
A.Ba2+、Na+、 、ClO- B.K+、Na+、 、
C.Na+、Cl-、 、K+ D.Na+、K+、 、
4.下列说法中正确的是( )
A.非金属单质燃烧时火焰均为无色
B.NaCl与NaCO 灼烧时火焰颜色相同
2 3
C.焰色反应均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色
5.下列气体中,不会造成空气污染的是
A.N B.SO C.CO D.NO
2 2 2
6.下列气体排放到空气中,会导致酸雨的是
A.CH B.NH C.SO D.N
4 3 2 2
7.下列说法正确的是
A.对煤进行分馏可以得到许多芳香族化合物
B.点燃爆竹后,硫燃烧生成SO,汽车尾气排放的SO 都会引起酸雨
3 2
C.“光化学烟雾”“臭氧空洞”“硝酸型酸雨”的形成都与氮氧化合物有关
D.绚丽缤纷的烟花中添加了含有铁、铂、钾、钙、铜等金属化合物
8.下列有关物质性质与用途对应关系正确的是A.SO 具有还原性,可用于纸浆漂白
2
B.Al O 是两性氧化物,可用作耐高温材料
2 3
C.SiO 熔点高、硬度大,可用于制光导纤维
2
D.液氨汽化时要吸收大量热,可用作制冷剂
9.某气体的水溶液呈酸性,该气体能使酸性高锰酸钾溶液褪色,也能使溴水褪色并出现浑浊,该气体是
A.HBr B.SO C.HS D.CO
2 2 2
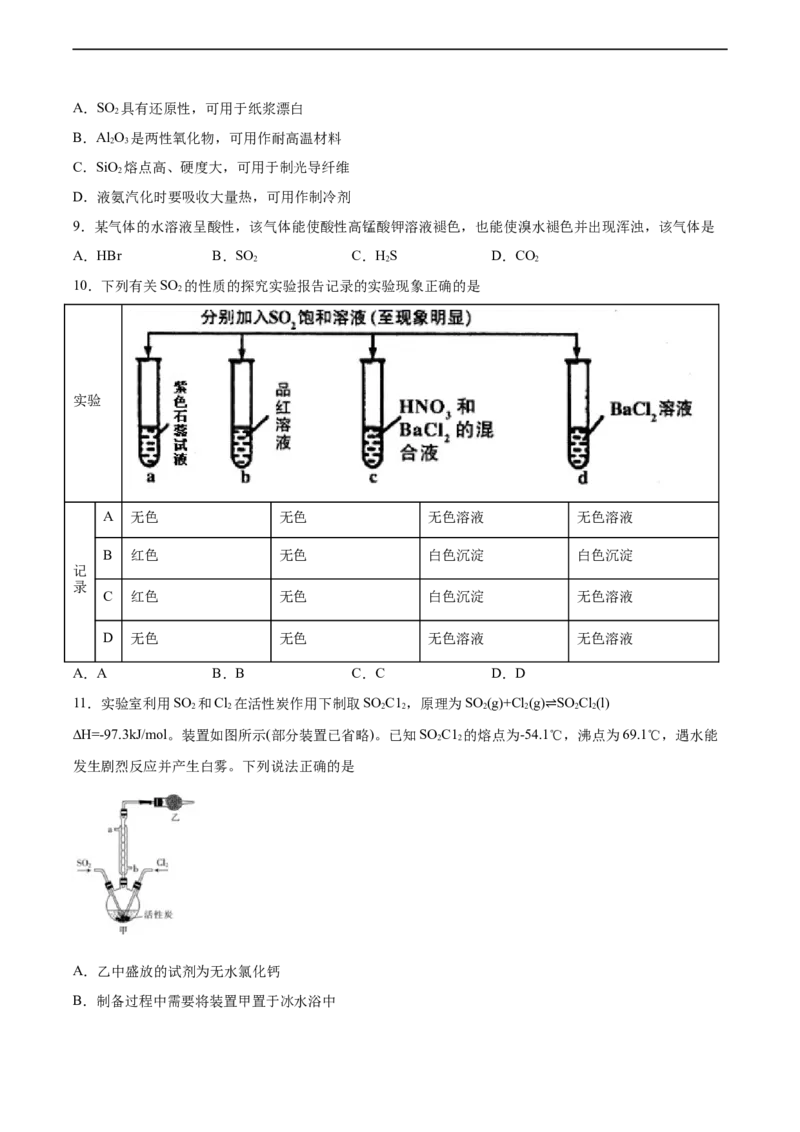
10.下列有关SO 的性质的探究实验报告记录的实验现象正确的是
2
实验
A 无色 无色 无色溶液 无色溶液
B 红色 无色 白色沉淀 白色沉淀
记
录
C 红色 无色 白色沉淀 无色溶液
D 无色 无色 无色溶液 无色溶液
A.A B.B C.C D.D
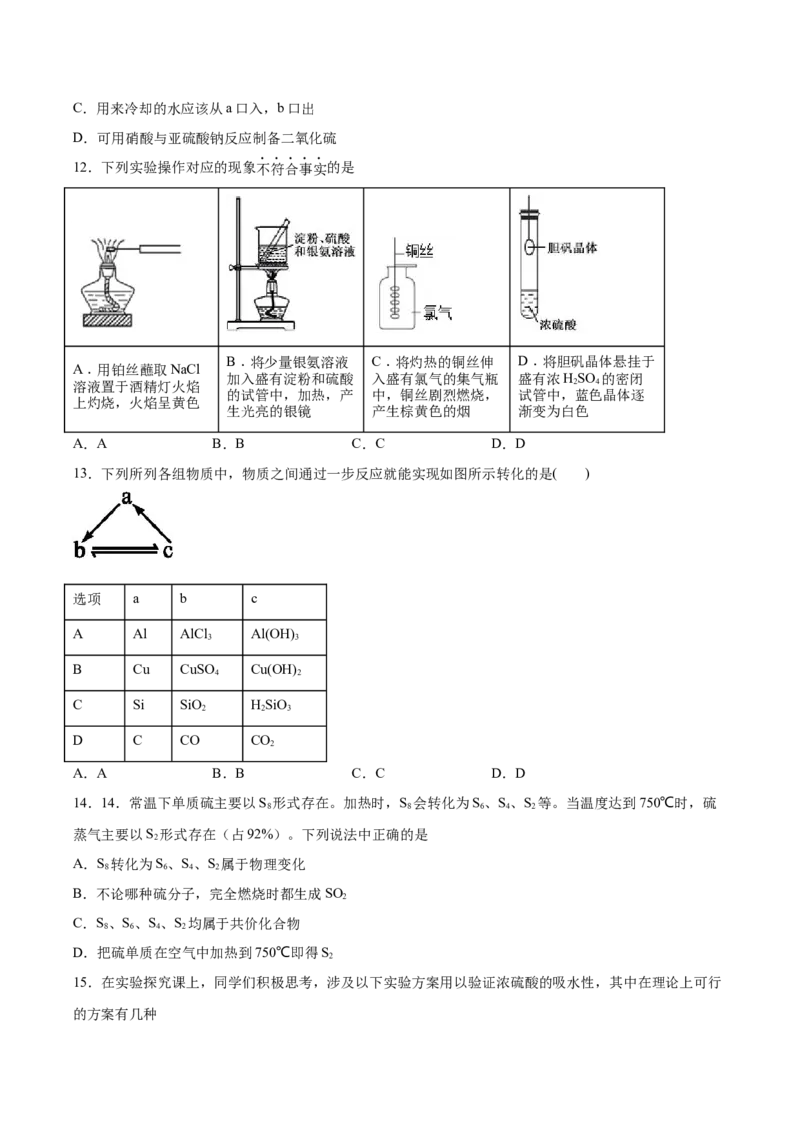
11.实验室利用SO 和Cl 在活性炭作用下制取SO C1 ,原理为SO (g)+Cl (g) SO Cl(l)
2 2 2 2 2 2 2 2
∆H=-97.3kJ/mol。装置如图所示(部分装置已省略)。已知SO C1 的熔点为-54.1⇌℃,沸点为69.1℃,遇水能
2 2
发生剧烈反应并产生白雾。下列说法正确的是
A.乙中盛放的试剂为无水氯化钙
B.制备过程中需要将装置甲置于冰水浴中C.用来冷却的水应该从a口入,b口出
D.可用硝酸与亚硫酸钠反应制备二氧化硫
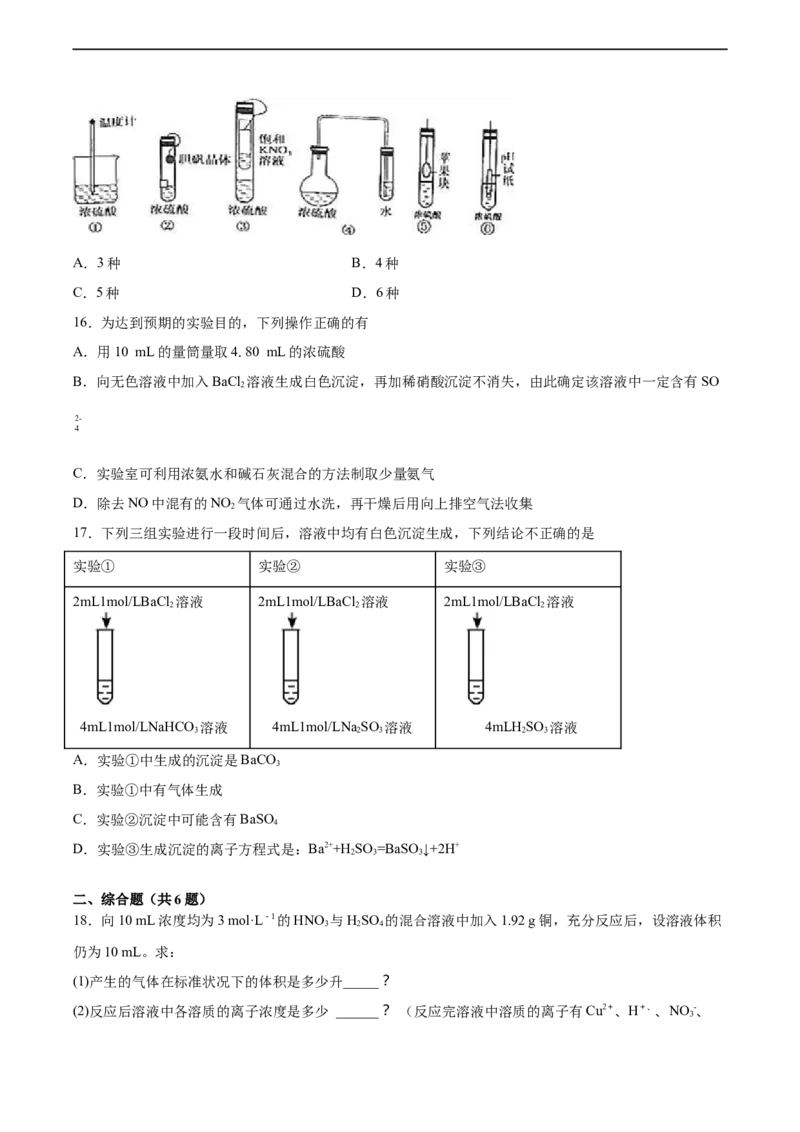
12.下列实验操作对应的现象不符合事实的是
B.将少量银氨溶液 C.将灼热的铜丝伸 D.将胆矾晶体悬挂于
A.用铂丝蘸取NaCl
加入盛有淀粉和硫酸 入盛有氯气的集气瓶 盛有浓HSO 的密闭
溶液置于酒精灯火焰 2 4
的试管中,加热,产 中,铜丝剧烈燃烧, 试管中,蓝色晶体逐
上灼烧,火焰呈黄色
生光亮的银镜 产生棕黄色的烟 渐变为白色
A.A B.B C.C D.D
13.下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
选项 a b c
A Al AlCl Al(OH)
3 3
B Cu CuSO Cu(OH)
4 2
C Si SiO HSiO
2 2 3
D C CO CO
2
A.A B.B C.C D.D
14.14.常温下单质硫主要以S 形式存在。加热时,S 会转化为S、S、S 等。当温度达到750℃时,硫
8 8 6 4 2
蒸气主要以S 形式存在(占92%)。下列说法中正确的是
2
A.S 转化为S、S、S 属于物理变化
8 6 4 2
B.不论哪种硫分子,完全燃烧时都生成SO
2
C.S、S、S、S 均属于共价化合物
8 6 4 2
D.把硫单质在空气中加热到750℃即得S
2
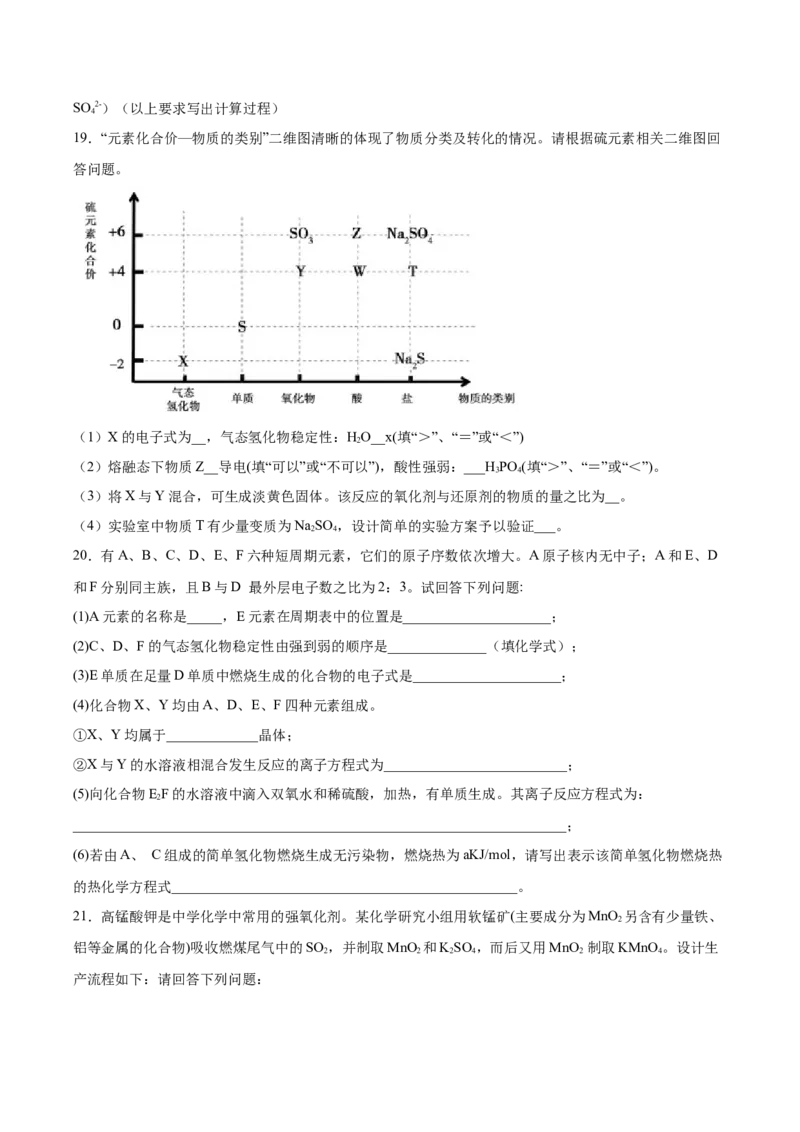
15.在实验探究课上,同学们积极思考,涉及以下实验方案用以验证浓硫酸的吸水性,其中在理论上可行
的方案有几种A.3种 B.4种
C.5种 D.6种
16.为达到预期的实验目的,下列操作正确的有
A.用10 mL的量筒量取4.80 mL的浓硫酸
B.向无色溶液中加入BaCl 溶液生成白色沉淀,再加稀硝酸沉淀不消失,由此确定该溶液中一定含有SO
2
C.实验室可利用浓氨水和碱石灰混合的方法制取少量氨气
D.除去NO中混有的NO 气体可通过水洗,再干燥后用向上排空气法收集
2
17.下列三组实验进行一段时间后,溶液中均有白色沉淀生成,下列结论不正确的是
实验① 实验② 实验③
2mL1mol/LBaCl 溶液 2mL1mol/LBaCl 溶液 2mL1mol/LBaCl 溶液
2 2 2
4mL1mol/LNaHCO 溶液 4mL1mol/LNa SO 溶液 4mLH SO 溶液
3 2 3 2 3
A.实验①中生成的沉淀是BaCO
3
B.实验①中有气体生成
C.实验②沉淀中可能含有BaSO
4
D.实验③生成沉淀的离子方程式是:Ba2++H SO =BaSO ↓+2H+
2 3 3
二、综合题(共6题)
18.向10 mL浓度均为3 mol·L-1的HNO 与HSO 的混合溶液中加入1.92 g铜,充分反应后,设溶液体积
3 2 4
仍为10 mL。求:
(1)产生的气体在标准状况下的体积是多少升_____?
(2)反应后溶液中各溶质的离子浓度是多少 ______? (反应完溶液中溶质的离子有Cu2+、H+、、NO -、
3SO 2-)(以上要求写出计算过程)
4
19.“元素化合价—物质的类别”二维图清晰的体现了物质分类及转化的情况。请根据硫元素相关二维图回
答问题。
(1)X的电子式为__,气态氢化物稳定性:HO__x(填“>”、“=”或“<”)
2
(2)熔融态下物质Z__导电(填“可以”或“不可以”),酸性强弱:___HPO (填“>”、“=”或“<”)。
3 4
(3)将X与Y混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为__。
(4)实验室中物质T有少量变质为NaSO ,设计简单的实验方案予以验证___。
2 4
20.有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子;A和E、D
和F分别同主族,且B与D 最外层电子数之比为2:3。试回答下列问题:
(1)A元素的名称是_____,E元素在周期表中的位置是_____________________;
(2)C、D、F的气态氢化物稳定性由强到弱的顺序是______________(填化学式);
(3)E单质在足量D单质中燃烧生成的化合物的电子式是_____________________;
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于_____________晶体;
②X与Y的水溶液相混合发生反应的离子方程式为__________________________;
(5)向化合物EF的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为:
2
______________________________________________________________________;
(6)若由A、 C组成的简单氢化物燃烧生成无污染物,燃烧热为aKJ/mol,请写出表示该简单氢化物燃烧热
的热化学方程式_________________________________________________。
21.高锰酸钾是中学化学中常用的强氧化剂。某化学研究小组用软锰矿(主要成分为MnO 另含有少量铁、
2
铝等金属的化合物)吸收燃煤尾气中的SO ,并制取MnO 和KSO ,而后又用MnO 制取KMnO 。设计生
2 2 2 4 2 4
产流程如下:请回答下列问题:20℃时,
相关物质的溶解度数据见下表:
(1)若将SO 气体通入下列溶液中,溶液不会褪色的是___。
2
A.紫色石蕊试液 B.品红溶液 C.新制氯水 D.酸性高锰酸钾溶液
(2)用 MnCO 除去液体中的 Fe3+时发生的离子方程式__________。
3
(3)步骤④中应在______中熔化;
A.瓷坩埚 B.铁坩埚 C.石英坩埚 D.蒸发皿
当溶液调 pH达10~11时,停止通入 CO。若 CO 过多,会造成的后果是:______。
2 2
(4)在此生产流程中,可循环使用的物质是(填名称)________。
步骤⑤中发生反应的化学方程式为_________;
步骤⑤之后,趁热过滤的理由是________。
22.已知元素X位于Y的下一周期,X、Y的原子序数均不大于20。某含氧酸盐甲的化学式为XYO。回
3
答下列问题:
(1)常温下X的单质能与水发生反应,395℃时,甲能发生分解反应生成两种盐,其中一种是含Y元素的无
氧酸盐,则X在周期表中的位置是___________,甲发生分解反应的化学方程式是___________。
(2)若甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体,则:
①甲为___________(填化学式)。该气体能使酸性高锰酸钾溶液褪色,反应的离子方程式为___________。
②X、Y形成的简单离子的半径从大到小的顺序为___________(用离子符号表示)。
(3)若甲能与盐酸反应,生成无色无味的气体乙,则:
①乙的电子式为___________。
②在水中持续加热甲,生成一种更难溶的物质并逸出气体乙,该反应的化学方程式为___________。
23.利用太阳能分解水制备氢气的示意图如图。回答下列问题:
(1)基态硫原子核外电子占据的原子轨道数为___。
(2)碘与氯同主族,碘元素在周期表中的位置是___。
(3)写出反应I的离子方程式:__。
(4)I 在CCl 中的溶解度比在水中的大,其原因是___。
2 4
(5)常温下,可用干燥的铁制容器储运浓硫酸,原因是__。这是利用了浓硫酸的___(填“脱水”“酸”或“强氧
化”)性。参考答案
1.A
【详解】
A.在对试管内的固体药品加热时,固体药品存放时因受潮而含有少量水或受热时生成的
水会在管口液化为液体,此时如果试管口高于试管底部,水则会流向试管底(倒流),而
使试管受热不均匀而炸裂,故A正确;
B.不慎将酒精洒到桌面上引起着火,应立即用湿抹布盖灭,故B错误;
C.白磷在空气中易自燃,用剩的白磷倒入垃圾箱会引发火灾,故C错误;
D.稀释浓HSO 时,先在烧杯中加一定量的水,边搅拌边慢慢加入浓HSO ,玻璃棒不断
2 4 2 4
搅拌,不能在量筒中进行稀释操作,故D错误。
故选:A。
2.C
【详解】
A.SO 属于酸性氧化物,NO 不属于酸性氧化物,A项错误;
2 2
B.SO 和NO 均属于非电解质,他们在水中并不会电离,熔融状态也不会电离,B项错误;
2 2
C.SO 中的S元素属于中间价态,NO 中的N元素也属于中间价态,所以都既可作氧化剂,
2 2
也可作还原剂,C项正确;
D.SO 是无色气体,NO 才有颜色,D项错误;
2 2
答案选C。
3.C
【分析】
强酸溶液中含大量的H+。
【详解】
A.H+和ClO-反应生成HClO而不能大量共存,A不满足题意;
B.SiO2-和H+反应生成HSiO 而不能大量共存,B不满足题意;
3 2 3
C.H+、Na+、Cl-、 、K+之间不能发生反应,能大量共存,C满足题意;
D. 、 、H+之间发生氧化还原反应而不能大量共存,D不满足题意。
答案选C。
4.B
【详解】
A.硫在空气中燃烧,火焰呈淡蓝色,故A错误;
B.因焰色反应是元素的性质,只要含有的金属元素相同,无论是单质还是化合物灼烧时火
焰颜色都相同,故B正确;
C.只有钾的焰色反应的观察需要透过蓝色钴玻璃滤去黄光,故C错误;
D.焰色反应是元素的性质,金属单质和金属形成的化合物灼烧时都会发生焰色反应,故D
错误;故答案选B。
5.A
【详解】
A.N 是一种无色无味的气体,是空气主要成分之一,对人体和环境无害,故A不会造成
2
空气污染;
B.SO 无色,有强烈刺激性的有毒气体,是造成酸雨的主要气体之一,是大气污染物之一,
2
故B会造成空气污染;
C.CO是一种无色、无臭、无刺激性的有毒气体,若局部污染严重,对人群健康有一定危
害,属于空气污染物,故C会造成空气污染;
D.NO 是红棕色的刺激性气味的气体,是造成酸雨的气体之一,吸入二氧化氮气体会对
2
人体呼吸道造成损害,属于空气污染物,故D会造成空气污染;
答案选A。
6.C
【详解】
A.CH 与水不反应,不能导致酸雨发生,故A错误;
4
B. 氨气的水溶液显碱性,所以不会造成酸雨,故B错误;
C. 二氧化硫与水反应生成亚硫酸,亚硫酸被氧气氧化为硫酸,使雨水酸性增强,导致酸
雨发生,故C正确;
D.N 与水不反应,不能导致酸雨发生,故D错误。
2
答案选C。
7.C
【详解】
煤的干馏可以得到炉煤气、煤焦油和焦炭,煤焦油分馏可得到芳香族化合物,A错误;硫
燃烧只能生成SO,不能生成SO,B错误;以一氧化氮和二氧化氮为主的氮氧化物是形成
2 3
“光化学烟雾”“硝酸型酸雨”的形成的一个重要原因, 一氧化氮也能被臭氧氧化,可以
造成“臭氧空洞”, C正确;部分金属有焰色反应,而铁、铂等金属在灼烧时,没有焰色
反应,D错误;正确选项C。
8.D
【详解】
A. SO 可用于纸浆漂白是因为其具有漂白性,故A错误;
2
B. 氧化铝可用作耐高温材料是因为其熔点高,与其两性无关,故B错误;
C. 二氧化硅具有良好光学特性,可以用来制作光导纤维, 与其熔点高、硬度大无关,故
C错误;
D. 液氨汽化时可以吸收大量热,使周围环境的温度降低,可用作制冷剂,故D正确;
答案选D。
9.C
【分析】某气体的水溶液呈酸性,该气体能使酸性高锰酸钾溶液褪色,说明该气体是酸性气体而且
有还原性,也能使溴水褪色并出现浑浊,说明与溴水反应产生难溶性的物质。
【详解】
A.HBr有酸性 ,能够使酸性高锰酸钾溶液褪色,但是不能使溴水褪色并出现浑浊,错误;
B.SO 有酸性 ,能够使酸性高锰酸钾溶液褪色,但是不能使溴水褪色并出现浑浊,错误;
2
C.HS有酸性 ,能够使酸性高锰酸钾溶液褪色,也能使溴水褪色并出现难溶于水的S单
2
质而使溶液变浑浊,正确;
D.CO 有酸性 ,不能够使酸性高锰酸钾溶液褪色,也不能使溴水褪色并出现浑浊,错误。
2
故选C。
10.C
【详解】
a.a中二氧化硫与水反应生成亚硫酸,遇紫色的石蕊试液变红色,SO 的漂白性不能使指
2
示剂褪色,a中呈现红色;
b.b中通入SO ,由于二氧化硫具有漂白性,能够使品红褪色,所以b中溶液变为无色;
2
c.c中通入SO ,由于二氧化硫具有还原性,能够被硝酸氧化生成硫酸根离子,硫酸根离
2
子与钡离子反应生成硫酸钡沉淀,所以c中产生白色沉淀;
d.d中通入SO ,由于二氧化硫与水反应生成亚硫酸,亚硫酸酸性弱于盐酸,所以二氧化
2
硫与氯化钡溶液不反应,所以d中不会产生白色沉淀;
答案为C。
11.B
【分析】
SO C1 的熔沸点低、易挥发,根据装置图可知,三颈烧瓶上方的冷凝管的作用是使挥发的
2 2
产物冷凝回流,由于会有一部分SO 和Cl 通过冷凝管逸出,SO 和Cl 都会污染空气,故
2 2 2 2
乙装置应使用碱性试剂,SO C1 遇水能发生剧烈反应并产生白雾,乙中盛放碱石灰,吸收
2 2
未反应完的二氧化硫、氯气,防止污染空气,并吸收空气中的水蒸气,防止水蒸气进入甲
中导致SO Cl 水解。
2 2
【详解】
A.乙的作用是吸收未反应完的二氧化硫、氯气,防止污染空气,并吸收空气中的水蒸气,
防止水蒸气进入甲中导致SO Cl 水解,故乙中盛放的试剂应该是碱石灰,无水氯化钙只能
2 2
吸收水,A选项错误;
B.根据题目中热化学方程式可知,∆H<0,则该反应为放热反应,降低温度使平衡正向移
动,有利于提高SO Cl 产率,B选项正确;
2 2
C.冷凝水应从冷凝管的下口进,上口出,故用来冷却的水应该从b口入,a口出,C选项
错误;
D.硝酸具有氧化性,能把二氧化硫氧化成硫酸,故不可用硝酸与亚硫酸钠反应制备二氧
化硫,D选项错误;答案选B。
12.B
【详解】
A.钠的焰色为黄色,用铂丝蘸取NaCl溶液置于酒精灯火焰上灼烧,火焰呈黄色,故A正
确;
B.淀粉在硫酸在催化剂时水解为葡萄糖,碱性条件下,银氨溶液和葡萄糖发生银镜反应,
将少量银氨溶液加入盛有淀粉和硫酸的试管中,加热,不能产生银镜,故B错误;
C.将灼热的铜丝伸入盛有氯气的集气瓶中,发生反应 ,现象是铜丝剧烈
燃烧,产生棕黄色的烟,故C正确;
D.浓硫酸具有吸水性,能使胆矾失去结晶水,将胆矾晶体悬挂于盛有浓HSO 的密闭试
2 4
管中,蓝色晶体逐渐变为白色,故D正确;
选B。
13.D
【详解】
A.Al(OH) 不能通过一步反应转化为Al,故A不选;
3
B.Cu(OH) 不能通过一步反应转化为Cu,故B不选;
2
C.SiO 不能通过一步反应生成HSiO,HSiO 也不能通过一步反应生成Si,故C不选;
2 2 3 2 3
D.C在O 中不完全燃烧得CO,CO燃烧得CO,Mg与CO 反应得到C,CO 与C反应生
2 2 2 2
成CO,故D选;
故选D。
14.B
【解析】试题分析:A、S 转化为S、S、S 有新物质生成,属于化学变化,错误,不选
8 6 4 2
A;B、硫完全燃烧都生成二氧化硫,正确,选B;C、都是单质,错误,不选C;D、硫单
质在空气中加热能和氧气反应,错误,不选D。
考点:硫的性质
15.C
【详解】
试题分析:①浓硫酸吸收空气中的水放热,温度计温度升高,故可从温度计读数来验证,
故①正确;②浓硫酸吸水,胆矾失去结晶水,变为白色的无水硫酸铜粉末,能够证明浓硫
酸的吸水性,故②正确;③浓硫吸水,饱和硝酸钾溶液中析出晶体硝酸钾,能证明浓硫酸
吸水性,故③正确;④浓硫酸吸水,试管中的水减少,证明浓硫酸具有吸水性,故④正确;
⑤鲜苹果块含水,浓硫酸吸水,苹果块变干;,故⑤正确;⑥浓硫酸具有脱水性,能够使
pH试纸碳化,不能证明其吸水性,故⑥错误;故选项C正确。
考点:考查浓硫酸的吸水性等知识。
16.C
【详解】A.量筒的精确度为0.1mL,可用10mL的量筒量取4.8mL的浓硫酸,故A错误;
B.检验SO 的操作先加HCl,再加氯化钡溶液;若用稀硝酸酸化,如果含有亚硫酸根离子,
也会被氧化为硫酸根离子,故B错误;
C.碱石灰溶解会放热,氧化钙能够与水反应,浓氨水和碱石灰混合,会有氨气生成,能用
于制备氨气,故C正确;
D.NO能与空气中的氧气反应,不能用排空气法收集NO,应该用排水法,故D错误。
故答案选C。
17.D
【分析】
此题根据实验现象,作出合理的推测和解释,考查无机物之间的反应。实验①BaCl 溶液
2
滴入NaHCO 溶液,若产生白色沉淀,则为BaCO ;实验②BaCl 溶液滴入NaSO 溶液,
3 3 2 2 3
若产生白色沉淀,可能是BaSO 或BaSO;实验③BaCl 溶液滴入HSO 溶液,BaCl 与
3 4 2 2 3 2
HSO 不能反应得到沉淀,若有白色沉淀产生,则可能是由于HSO 已被氧化成HSO 。
2 3 2 3 2 4
【详解】
A.实验①中HCO -发生电离,得到H+、CO2-,Ba2+与CO2-结合生成沉淀BaCO ,A正确;
3 3 3 3
B.实验①中随着Ba2+与CO2-结合生成沉淀BaCO ,HCO -电离程度增大,溶液中H+浓度增
3 3 3
大,H+与HCO -结合产生CO 气体,B正确;
3 2
C. BaCl 溶液滴入NaSO 溶液,产生白色沉淀,可能是直接反应生成BaSO,也可能是
2 2 3 3
NaSO 被氧化生成的NaSO 与氯化钡反应得到BaSO,C正确;
2 3 2 4 4
D. BaCl 与HSO 不能反应得到沉淀,若有白色沉淀产生,则可能是由于HSO 已被氧化成
2 2 3 2 3
HSO ,则生成沉淀的离子方程式是:Ba2++SO2-=BaSO ↓,D错误;
2 4 4 4
答案选D。
18.0.448 L Cu2+:3 mol·L-1 H+:1 mol·L-1 NO -:1 mol·L-1 SO 2-:3 mol·L-1
3 4
【分析】
根据铜与稀硝酸反应的离子反应过程分析解答。
【详解】
(1)n(Cu)= =0.03mol,n(H+)
=3mol•L-1×0.01L×1+3mol•L-1×0.01L×2=0.09mol,n(NO -)=3mol•L-1×0.01L=0.03mol,根据
3
离子反应方程式:3Cu+8H++2NO-=3 Cu2++2NO↑+4HO 可知,Cu完全反应,H+和NO -过
3 2 3
量,由反应的离子方程式可知:n(NO)=0.03mol×2÷3=0.02mol, V(NO)
=0.02mol×22.4L/mol=0.448L;
故答案为0.448 L;
(2) 由离子方程式可知1.92 g Cu为0.03 mol,反应中消耗H+ 0.08 mol,消耗NO - 0.02
3
mol,生成Cu2+ 0.03 mol,可得:c(Cu2+)=0.03mol÷0.01L=3 mol·L-1,反应后c(H+)=
(0.09mol-0.08mol) ÷0.01L=1 mol·L-1,反应后n(NO -)=0.03-0.02=0.01mol,故c(NO -)=
3 30.01mol÷0.01L=1 mol·L-1,因为SO 2-没有参加反应,故SO 2-的离子浓度仍为3 mol·L-1。
4 4
故答案为Cu2+:3 mol·L-1,H+:1 mol·L-1,NO -:1 mol·L-1,SO 2-:3 mol·L-1。
3 4
19. > 不可以 > 1:2 取少量样品制成溶液,加入盐酸酸化的
氯化钡溶液,观察,若有白色沉淀生成,证明变质
【分析】
由图X中硫显-2价,X为HS;Y中硫显+4价,Y为SO ,W中S显+4价,W为HSO ,
2 2 2 3
Z中硫显+6价,Z为HSO ,T中硫显+4价,T为NaSO 。
2 4 2 3
【详解】
(1)X为HS,X的电子式为 ,非金属性O>S,气态氢化物稳定性:HO>HS,
2 2 2
故答案为: ;>;
(2)Z为HSO ,由分子构成,熔融态下不能电离成自由移动的离子,熔融态下物质Z不
2 4
可以导电,非金属性S>P,酸性强弱:HSO >HPO 。故答案为:不可以;>;
2 4 3 4
(3)X为HS;Y为SO ,将X与Y混合,可生成淡黄色固体,反应方程式为SO +
2 2 2
2HS=3S↓+2HO,该反应的氧化剂为SO ,还原剂为HS,氧化剂与还原剂的物质的量之
2 2 2 2
比为1:2。故答案为:1:2;
(4)实验室中物质NaSO 有少量变质为NaSO ,设计实验验证时,要用足量的盐酸除去
2 3 2 4
NaSO :取少量样品制成溶液,加入盐酸酸化的氯化钡溶液,观察,若有白色沉淀生成,
2 3
证明变质,故答案为:取少量样品制成溶液,加入盐酸酸化的氯化钡溶液,观察,若有白
色沉淀生成,证明变质。
20.氢 第三周期ⅠA族 HO>NH >HS Na+ Na+ 离子 H+
2 3 2
+HSO -=HO+SO ↑ S2-+HO+2H+==S↓+2HO NH (g) + 3/4O (g) =1/2N(g) +
3 2 2 2 2 2 3 2 2
3/2H O(l) H=-aKJ/mol
2
【分析】
△
A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子,A
为H;A和E同主族,结合原子序数可知E为Na;B与D最外层电子数之比为2:3,由原
子序数可知,二者都处于第二周期,故B、D原子最外层电子数分别为4、6,可推知B为
C元素、D为O元素,则C为N元素;D和F同主族,则F为S元素。
【详解】
(1)由分析可知,A为氢元素;E为Na元素,处于周期表中第三周期ⅠA族;
(2)非金属性O>N>S,N、O、S元素氢化物的稳定性HO>NH >HS;
2 3 2
(3)Na单质在足量氧气中燃烧生成NaO,其电子式为: ;
2 2
(4)化合物X、Y均由H、O、Na、S四种元素组成,分别为NaHSO、NaHSO 中的一种,
3 4
①NaHSO、NaHSO 均属于离子化合物;
3 4
②X与Y的水溶液相混合发生反应的离子方程式为:H++HSO -=H O+SO ↑;
3 2 2(5)化合物NaS的水溶液中滴入双氧水和稀硫酸,加热,生成单质为S,同时生成水,
2
其反应离子方程式为:S2-+H O+2H+ S↓+2HO;
2 2 2
(6)若由A、C组成的简单氢化物为氨气,氨气燃烧生成无污染物,该产物应该为氮气,
氨气的燃烧热为aKJ·mol-1,则氨气燃烧热的热化学方程式为:NH (g) + 3/4O (g) =1/2N(g)
3 2 2
+ 3/2HO(l) H=-aKJ/mol。
2
21.A 3MnCO +2Fe3++3H O=3Mn2++2Fe(OH) ↓+3CO ↑ B CO 与KCO 反应生成
△ 3 2 3 2 2 2 3
KHCO ,结晶时会同一起结晶析出,降低产品的纯度 MnO 、CO、KMnO
3 2 2 4
3KMnO +2CO =2KMnO +2K CO+MnO↓ 防止KMnO 结晶析出,提高 KMnO 的产量
2 4 2 4 2 3 2 4 4
【分析】
(1)根据SO 的性质分析判断;
2
(2)MnCO 与溶液中的H+发生反应,使溶液中Fe3+形成Fe(OH) 沉淀而除去;
3 3
(3)KOH是碱,能够与SiO 在高温下反应,据此分析;
2
根据KCO 与CO 及HO反应转化为KHCO 分析;
2 3 2 2 3
(4)根据反应流程分析判断物质及反应的方程式。
【详解】
(1)A.SO 与溶液中的水反应产生HSO ,HSO 是酸,具有酸的通性,可以使紫色石蕊试液
2 2 3 2 3
变为红色,不褪色,A符合题意;
B.SO 具有漂白性,能够使品红溶液的红色褪去,B不符合题意;
2
C.新制氯水中含有HClO,HClO是具有强氧化性的物质,可以将有色物质氧化变为无色,
因此具有漂白作用,C不符合题意;
D.酸性高锰酸钾溶液具有强的氧化性,SO 具有还原性,二者发生氧化还原反应而使溶液
2
的紫色褪去,D不符合题意;
故合理选项是A;
(2)MnCO 与溶液中的H+发生反应,使溶液中c(OH-)增大,导致溶液中Fe3+形成Fe(OH) 沉
3 3
淀而除去,则用MnCO 除去液体中的Fe3+时发生的离子方程式为:3MnCO +2Fe3+
3 3
+3H O=3Mn2++2Fe(OH) ↓+3CO ↑;
2 3 2
(3)KOH是碱,在高温下能够与SiO 反应,所以不能使用含有SiO 的容器反应;
2 2
A.瓷坩埚中含有SiO,不能熔化KOH,A不符合题意;
2
B.铁坩埚中不含有SiO,与Fe不能反应,可以熔化KOH,B符合题意;
2
C.石英坩埚主要成分是SiO,与KOH在高温下反应,所以不能熔化KOH,C不符合题意;
2
D.蒸发皿主要成分是硅酸盐,其中含有SiO,可以与KOH在高温下发生反应,不能在高
2
温下熔融KOH,D不符合题意;
故合理选项是B;
向含有KOH的溶液中通入CO 气体,调整溶液的pH至10~11,二者反应产生KCO 和水,
2 2 3
若通入CO 过多,则又会发生反应:KCO+CO +H O=2KHCO ,结晶时会同KMnO 一起
2 2 3 2 2 3 4
结晶析出,降低产品的纯度;(4)向软锰矿(主要成分为MnO )浆中加入稀硫酸,并通入SO 气体,发生氧化还原反应产生
2 2
MnSO ,向该酸性溶液中加入MnCO ,消耗溶液中的H+,使溶液中的Fe3+、Al3+形成
4 3
Fe(OH) 、Al(OH) 沉淀而除去,MnCO 与H+反应,产生Mn2+和CO,向MnSO 溶液中加
3 3 3 2 4
入KMnO 溶液,发生氧化还原反应产生MnO ,向其中再加入KOH、KClO,发生氧化还
4 2 3
原反应,产生KMnO ,向该碱性溶液中通入CO,调整溶液的pH至10~11,KOH与CO
2 4 2 2
反应产生KCO,KMnO 发生歧化反应产生KMnO 、MnO ,CO 转化为MnCO ,所以在
2 3 2 4 4 2 2 3
该流程中,能够循环利用的物质有MnO 、CO、KMnO ;
2 2 4
步骤⑤中KMnO 在CO 存在条件下,发生歧化反应产生KMnO 、MnO ,发生反应的化学
2 4 2 4 2
方程式为3KMnO +2CO =2KMnO +2K CO+MnO↓;
2 4 2 4 2 3 2
步骤⑤之后,要趁热过滤,这是由于温度高,KMnO 的溶解度大,温度降低,KMnO 的溶
4 4
解度降低,导致KMnO 的产量降低,高温过滤就可以防止KMnO 结晶析出,从而提高
4 4
KMnO 的产量。
4
22.第四周期IA族 4KClO 3KClO+KCl CaSO 5SO +2 +
3 4 3 2
2HO=4H++2Mn2++5 r(S2-)>r(Ca2+) MgCO +HO Mg(OH)
2 3 2 2
+CO↑
2
【分析】
XYO 为含氧酸盐,可知X为金属元素,Y为非金属元素。若Y为第二周期非金属元素,
3
则X为第三周期元素Na或Mg或Al。若Y为第三周期非金属元素,则X为第四周期元素
K或Ca。据此分析:
【详解】
(1) 常温下X的单质能与水反应,则X可能为Na或K或Ca。若X为Na,根据XYO 可知
3
Y为N元素,则甲为NaNO ,NaNO 高温分解不可能产生两种盐;若X为K,根据化学式
3 3
可知Y为Cl,甲为KClO,其化合价为+5价,因为Cl的最高化合价为+7,最低为-1价,
3
加热分解可生成两种盐,符合题意;若X为Ca则Y只能为S,甲为CaSO,而CaSO 加热
3 3
被氧化而不会生成两种盐,综上可知X为K元素,Y为Cl元素。K位于第四周期IA族;
KClO 中Cl化合价为+5价,加热分解可生成两种盐,其一为无氧酸盐,则为KCl,根据氧
3
化还原反应化合价有升有降,另一种产物必然为KClO ,高温分解的化学方程式为:
4
4KClO 3KClO+KCl;
3 4
(2) ①甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体,气体为SO ,可知甲
2
中含 ,X元素一定为Ca,Y元素为S,即甲为CaSO。SO 具有还原性,与KMnO 发
3 2 4
生氧化还原反应,离子方程式为:5SO +2 +2HO=4H++2Mn2++5 ;
2 2
②Ca2+和S2-电子层结构相同,当电子层结构相同时,原子序数大的粒子半径反而小,所以
两种离子的半径大小为:r(S2-)>r(Ca2+);(3) 若甲能与盐酸反应,生成无色无味的气体乙,则甲中含 ,乙为CO,则Y为C元
2
素,X为Mg。
①由上分析知乙为CO,其电子式为 。
2
②MgCO 微溶于水,电离出的Mg2+和CO2-能够发生水解,加热促使水解平衡正向移动,
3 3
最终生成Mg(OH) 和CO,化学方程式为:MgCO +HO Mg(OH) +CO↑。
2 2 3 2 2 2
23.9 第五周期第ⅦA族 SO +I +2H O=4 +2 + I 和CCl 都是非极性分
2 2 2 2 4
子,水是极性分子,根据相似相容原理,极性溶质易溶于极性溶剂,非极性溶质易溶于非
极性溶剂 铁与浓硫酸接触,表面形成致密的氧化膜,发生钝化现象 体现浓硫酸的
强氧化性
【分析】
根据硫原子的核外电子排布式写出基态硫原子核外电子占据的原子轨道数;根据碘与氯同
主族判断碘在周期表的位置;反应I是二氧化硫、碘和水生成盐酸和硫酸,写出离子方程
式;根据相似相容原理分析;根据铁与浓硫酸的钝化分析,据此分析。
【详解】
(1)基态硫原子的核外电子排布式为:1s22s22p63s23p4,s能级有一个轨道,p能级有3个轨道,
基态硫原子的核外电子占据的原子轨道数为1+1+3+1+3=9;
(2)碘与氯同主族,氯位于第三周期第ⅦA族,碘元素在周期表中的位置是第五周期第ⅦA
族;
(3)反应I是二氧化硫、碘和水生成盐酸和硫酸,离子方程式:SO +I +2H O=4 +2 +
2 2 2
;
(4)I 在CCl 中的溶解度比在水中的大,其原因是I 和CCl 都是非极性分子,水是极性分子,
2 4 2 4
根据相似相容原理,极性溶质易溶于极性溶剂,非极性溶质易溶于非极性溶剂;
(5)常温下,可用干燥的铁制容器储运浓硫酸,原因是铁与浓硫酸接触,表面形成致密的氧
化膜,发生钝化现象,这是利用了浓硫酸的强氧化性。