文档内容
第 7 讲 离子反应 离子方程式
复习目标 1.了解电解质的概念,了解强电解质和弱电解质的概念。2.理解电解质在水中
的电离以及电解质溶液的导电性。3.了解离子反应的概念、离子反应发生的条件,能正确书
写离子方程式并能进行有关计算。
考点一 电解质及电离
1.电解质及其分类
答案 ①电离 ②强电解质 ③强酸 ④强碱 ⑤弱电解质 ⑥弱酸 ⑦弱碱 ⑧水溶液
⑨熔融
2.电解质的电离
3.电离方程式的书写原则
(1)原子守恒、电荷守恒。
(2)连接符号:强电解质用“===”,弱电解质用“”。
(3)多元弱酸分步书写,多元弱碱一步完成。
4.依据元素周期表,熟记常见的强电解质和弱电解质
ⅠA:除LiOH外其余都是强碱。
ⅡA:除Mg(OH) 、Be(OH) 外其余都是强碱。
2 2
ⅢA:Al(OH) 是两性氢氧化物,即可看作弱碱,也可看作弱酸。
3
ⅣA:HCO、HSiO 均为弱酸。
2 3 2 3ⅤA:强酸:HNO;中强酸:HNO、HPO ;NH ·H O为弱碱。
3 2 3 4 3 2
ⅥA:强酸:HSO ;弱酸:HSO 、HS。
2 4 2 3 2
ⅦA:强酸:HCl、HBr、HI、HClO 等;
4
弱酸:HF、HClO等。
过渡元素中常见的弱碱:Fe(OH) 、Fe(OH) 、Cu(OH) 、Zn(OH) 等,它们也都难溶于水。
3 2 2 2
注意 盐不论难溶、易溶,绝大多数都是强电解质。
(1)NaCl溶液在电流的作用下电离成钠离子和氯离子(×)
错因: NaCl 溶液在电流的作用下发生氧化还原反应 。
(2)强电解质都是离子化合物,弱电解质都为共价化合物(×)
错因: 如 HC l 是强电解质,但是共价化合物, Pb(CH COO) 是离子化合物,但为弱电解质。
3 2
(3)强电解质溶液的导电性比弱电解质溶液的导电性强(×)
错因:导电性的强弱与离子浓度及离子所带电荷数有关,而与电解质的强弱无关。
(4)CO 、NH 溶于水能导电,所以二者为电解质(×)
2 3
错因:CO 、 NH 均为非电解质,它们溶于水生成的物质 H CO 、 NH ·H O 是弱电解质 。
2 3 2 3 3 2
现有 12 种物质:① Al ②稀硝酸 ③ HNO ④液氨 ⑤ CO ⑥空气 ⑦ NaCl
3 2
⑧CaCO ⑨NaHCO ⑩乙醇 ⑪Al O ⑫石墨
3 3 2 3
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 混合物
(2) 电解质,但熔融状态下并不导电
(3) 电解质,熔融状态能导电
(4) 电解质,但难溶于水
(5) 非电解质
(6) 既不是电解质,也不是非电解质,但本身能导电
答案 (1)②⑥ (2)③ (3)⑦⑧⑨⑪ (4)⑧⑪
(5)④⑤⑩ (6)①⑫
(1)单质和混合物既不是电解质也不是非电解质,如Cu、NaCl溶液。
(2)电解质不一定能导电,如固态NaCl、液态HCl等;能导电的物质不一定是电解质,如铁、
铝等金属单质。
(3)本身电离而导电的化合物才是电解质。如CO 、SO 、NH 的水溶液能导电,但均是非电
2 2 3
解质。(4)电解质的强弱与电解质溶液导电能力的强弱、溶解性的大小没有直接关系。如碳酸钙,
其溶解性小,溶液导电性差,但其属于强电解质。
1.分类书写电离方程式
(1)强电解质
①Ba(OH) :Ba(OH) == = Ba 2 + + 2OH - ;
2 2
②BaSO:BaSO == = Ba 2 + + SO ;
4 4
③KAl(SO ):KAl(SO ) == = K + + Al 3 + + 2SO 。
4 2 4 2
(2)弱电解质
①NH ·H O:NH ·H ONH+OH-;
3 2 3 2
②HCO:HCOH++HCO、HCOH++CO;
2 3 2 3
③Al(OH) 双向电离:AlO+H++HOAl(OH) Al 3 + + 3OH - 。
3 2 3
酸式电离 碱式电离
(3)酸式盐
①NaHSO 溶于水:NaHSO===Na++H++SO;
4 4
②NaHSO 熔融:NaHSO===Na++HSO;
4 4
③NaHCO 溶于水:NaHCO ===Na++HCO、HCOH++CO。
3 3
2.有八种离子:H+、Na+、Ba2+、Ca2+、OH-、Cl-、SO、CO。
(1)由两种离子相结合形成的物质中,属于酸的是__________,属于难溶盐的是_________。
(2)写出以上离子组成的弱电解质的电离方程式:____________________________________。
答案 (1)HCl、HSO 、HCO BaSO、BaCO 、CaCO
2 4 2 3 4 3 3
(2)H OH++OH-、HCOH++HCO、HCOH++CO
2 2 3
电离方程式书写的思维模型考点二 离子反应和离子方程式书写的基本方法
1.离子反应
(1)概念:有离子参加或有离子生成的反应统称为离子反应。
(2)条件
在稀HSO 中分别加入下列物质,能发生反应的请写出有关反应的离子方程式:
2 4
A.加入BaCl 溶液:Ba2++SO===BaSO↓;
2 4
B.加入CHCOONa溶液:CHCOO-+H+===CHCOOH;
3 3 3
C.加入NaCO 溶液:CO+2H+===CO↑+HO;
2 3 2 2
D.加入Zn粒:Zn+2H+===H↑+Zn2+;
2
E.加入NaOH溶液:H++OH-===HO。
2
从A~E可知离子反应发生的条件:①生成难溶的物质、②生成难电离的物质、③生成易挥
发的物质、④发生氧化还原反应。
(3)离子反应的本质
A~E中,混合后溶液中SO的物质的量减少的是A(填字母,下同);H+的物质的量减少的
是BCDE;因此离子反应的本质是溶液中某些离子的物质的量的减少。
2.离子方程式
(1)离子方程式:用实际参加反应的离子符号来表示反应的式子。
(2)离子方程式的意义
离子方程式不仅可以表示某一个具体的化学反应,还可以表示同一类型的离子反应。
(3)根据离子反应的实质直接书写
如CuSO 溶液与Ba(OH) 溶液反应的离子方程式的书写步骤:
4 2
①首先分析出溶液中反应物电离出的离子有Cu2+、SO、Ba2+、OH-;②然后分析哪些离子
能相互结合,Cu2+与OH-反应生成Cu(OH) ,SO与Ba2+反应生成BaSO ;③最后根据离子
2 4
的个数比配平方程式,得Cu2++SO+Ba2++2OH-===Cu(OH) ↓+BaSO↓。
2 4
3.电解质的“拆分”原则
(1)易溶的强电解质(强酸、强碱、大多数可溶性盐)写成离子形式。
①常见的强酸、弱酸
强酸 HNO、HSO 、HClO、HCl、HBr、HI
3 2 4 4
弱酸 HCO、HSiO、CHCOOH、HC O、HClO、HF、HS、HSO
2 3 2 3 3 2 2 4 2 2 3
注意 浓盐酸、浓硝酸在离子方程式中可拆,浓硫酸一般不拆。
②常见的强碱、弱碱
强碱 NaOH、KOH、Ca(OH) 、Ba(OH)
2 2弱碱 NH ·H O、Mg(OH) 、Fe(OH)
3 2 2 3
③酸式盐
a.弱酸的酸式酸根离子不能拆开,如HCO、HS-、HSO等;
b.强酸的酸式酸根离子(如HSO)在水溶液中写成拆分形式,如NaHSO 应写成Na+、H+和
4
SO;而在熔融状态下HSO不能拆开,应写成Na+和HSO。
(2)固体之间的反应、浓硫酸(或浓磷酸)与固体之间的反应,不能电离出离子,所以不写离子
方程式。如:
Ca(OH) (s)+2NH Cl(s)=====CaCl (s)+2NH ↑+2HO。
2 4 2 3 2
题组一 基本反应离子方程式的书写
1.(1)完成下列反应的离子方程式,注意难溶、气体、难电离微粒的书写形式。
①氧化镁溶于稀硫酸
MgO+2H+===HO+Mg2+。
2
②AlCl 溶液中滴加过量的氨水
3
Al3++3NH ·H O===Al(OH) ↓+3NH。
3 2 3
③将浓硝酸滴到CaCO 固体上
3
CaCO +2H+===Ca2++HO+CO↑。
3 2 2
④小苏打溶液与乙酸溶液混合
HCO+CHCOOH===CHCOO-+HO+CO↑。
3 3 2 2
⑤向NaHSO 溶液中加入过量NaHSO 溶液
3 4
HSO+H+===HO+SO ↑。
2 2
(2)按要求完成下列反应的离子方程式,注意微溶物质、NH与碱反应的条件。
①澄清石灰水中加入稀盐酸
OH-+H+===HO。
2
②石灰乳与NaCO 溶液反应
2 3
Ca(OH) +CO===CaCO +2OH-。
2 3
③NaSO 溶液与AgNO 溶液混合
2 4 3
SO+2Ag+===Ag SO ↓。
2 4
④NH Cl与NaOH两稀溶液混合
4
NH+OH-===NH ·H O。
3 2
(3)完成下列教材中重要氧化还原反应的离子方程式,注意单质、氧化物、浓“盐酸、硝酸、
硫酸”的书写形式。
①过氧化钠溶于水2NaO+2HO===4Na++4OH-+O↑。
2 2 2 2
②FeCl 腐蚀铜箔
3
2Fe3++Cu===2Fe2++Cu2+。
③用MnO 与浓盐酸共热制Cl
2 2
MnO +4H++2Cl-=====Mn2++Cl↑+2HO。
2 2 2
④用NaOH吸收Cl
2
Cl+2OH-===Cl-+ClO-+HO。
2 2
⑤铜分别溶于浓、稀硝酸
Cu+4H++2NO===Cu2++2NO ↑+2HO;
2 2
3Cu+8H++2NO===3Cu2++2NO↑+4HO。
2
⑥铜加热条件下与浓硫酸反应:
Cu+2HSO (浓)=====Cu2++SO+SO ↑+2HO。
2 4 2 2
1.离子方程式书写的关键
2.特殊情况的处理
(1)微溶物作为产物视为沉淀,作为反应物处理如下:
(2)铵根离子与碱的反应
题组二 多重反应离子方程式的书写
2.完成下列反应的离子方程式
(1)Ba(OH) 溶液与HSO 溶液混合
2 2 4
Ba2++2OH-+2H++SO===BaSO↓+2HO。
4 2(2)Ba(OH) 溶液与(NH )SO 溶液混合
2 4 2 4
Ba2++2OH-+2NH+SO===BaSO↓+2NH ·H O。
4 3 2
(3)CuSO 溶液与Ba(OH) 溶液混合
4 2
Cu2++SO+Ba2++2OH-===Cu(OH) ↓+BaSO↓。
2 4
(4)Fe O 溶于HI溶液中
2 3
Fe O+6H++2I-===2Fe2++3HO+I。
2 3 2 2
(5)FeO溶于稀HNO 中
3
3FeO+10H++NO===3Fe3++NO↑+5HO。
2
多重反应离子方程式书写时的注意点
两种电解质溶液混合,至少电离出两种阴离子和两种阳离子,这四种(或更多种)离子之间都
能两两结合成难电离(或难溶)的物质或后续离子之间的氧化还原反应,这样的离子反应称为
多重反应。在写这类反应的离子方程式时易丢失其中的一组反应。
题组三 离子反应过程中溶液导电性变化的判断
3.下列几种导电性变化图像,把符合要求的图像序号填在相应的题目后面的括号中。
(1)向HSO 溶液中加入等体积、等物质的量浓度的Ba(OH) 溶液( )
2 4 2
(2)向HS溶液中通入Cl 直至过量( )
2 2
(3)向AgNO 溶液通入少量HCl( )
3
(4)向氨水中通入HCl直至过量( )
(5)向NaOH溶液中通入少量Cl( )
2
(6)向饱和石灰水中不断通入CO( )
2
答案 (1)D (2)B (3)C (4)B (5)C (6)A
解析 (1)H+与OH-中和生成极弱电解质水,Ba2+与SO结合成难溶BaSO ,溶液中自由移
4
动的离子浓度降低。(2)和(4)都是因发生离子反应,使弱电解质生成强电解质,自由移动的
离子浓度增加。(3)和(5)虽然发生了离子反应,但自由移动离子的浓度未发生改变。(6)开始
阶段CO 与Ca(OH) 反应生成CaCO 沉淀,离子浓度降低至Ca(OH) 完全反应后,继续通入
2 2 3 2CO,CO 和HO与CaCO 反应生成可溶性的Ca(HCO ),自由移动的离子浓度又增加。
2 2 2 3 3 2
(1)电解质溶液的导电原理
电解质电离出的阴、阳离子在外加电场作用下,发生定向移动实现导电过程,一般情况下,
自由移动离子的浓度越大,所带的电荷数越多,电解质溶液的导电能力越强。
(2)同一温度下,强电解质溶液(a),弱电解质溶液(b),金属导体(c),三者的导电能力相同,
若升高温度,它们的导电能力大小顺序为b>a>c。
1.下列说法正确的一组是( )
①不溶于水的盐都是弱电解质 ②可溶于水的盐都是强电解质 ③0.5 mol·L-1一元酸溶液
中H+浓度为0.5 mol·L-1 ④强酸溶液中的H+浓度不一定大于弱酸溶液中的H+浓度 ⑤电
解质溶液导电的原因是溶液中有自由移动的阴、阳离子 ⑥熔融的电解质都能导电
A.①③⑤⑥ B.只有④⑤ C.②④⑤⑥ D.只有③⑥
答案 B
解析 不溶于水的盐不一定是弱电解质,如BaSO 难溶于水,但溶于水的部分完全电离,是
4
强电解质,故①错误;电解质的强弱与溶解性无关,可溶于水的盐可能是弱电解质,如醋酸
铅,故②错误;0.5 mol·L-1一元酸溶液中的H+浓度不一定为0.5 mol·L-1,如醋酸,故③错
误;强酸溶液中的H+浓度不一定大于弱酸溶液中的H+浓度,H+浓度与酸的浓度、分子中
氢离子的个数以及电离程度有关,故④正确;电解质溶液导电的原因是溶液中有自由移动的
阴、阳离子,故⑤正确;酸在熔融态时均不导电,只有溶于水时才导电,故⑥错误;正确的
有④⑤。
2.将NaCl溶于水配成1 mol·L-1的溶液,溶解过程如图所示。下列说法正确的是( )
A.a离子为Cl-,b离子为Na+
B.溶液中含有N 个水合Na+
A
C.溶液中存在NaClNa++Cl-
D.NaCl溶解过程需要在容量瓶中进行答案 A
解析 钠离子核外有2个电子层,氯离子有3个电子层,即氯离子半径大于钠离子,a离子
为Cl-,b离子为Na+,A正确;题目中没有说明溶液的体积,无法计算溶质的物质的量,
即无法判断溶液中水合Na+的个数,B错误;氯化钠是强电解质,全部电离,电离方程式为:
NaCl===Na++Cl-,C错误;容量瓶是精密仪器,不能用于溶解,NaCl溶解需要在烧杯中
进行,D错误。
3.下列说法正确的是( )
A.三氧化硫的水溶液能导电,所以三氧化硫是电解质
B.自由移动离子数目多的电解质溶液导电能力一定强
C.NaHSO 在水溶液及熔融状态下均可电离出Na+、H+、SO
4
D.NH 属于非电解质,但其水溶液能够导电
3
答案 D
解析 三氧化硫本身不能电离出离子,SO 是非电解质,A错误;离子数目多的溶液中,离
3
子浓度不一定大,离子所带电荷数不一定多,其导电能力不一定强,B错误;NaHSO 在熔
4
融状态下只能电离出Na+、HSO,C错误;NH 是非电解质,但其溶于水后可形成电解质
3
NH ·H O,溶液能导电,D正确。
3 2
4.下列物质在指定条件下电离方程式书写正确的是( )
A.NaCO 溶于水:NaCO===Na+CO
2 3 2 3
B.Al(OH) 酸式电离:Al(OH) ===H++AlO+HO
3 3 2
C.NaHS溶于水HS-的电离:HS-+HOHS+OH-
2 2
D.NaHSO 加热熔化:NaHSO(熔融)===Na++HSO
4 4
答案 D
解析 A项,应为NaCO===2Na++CO;B项,应用可逆号;C项,是HS-的水解方程式。
2 3
5.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系
如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应的离子方程式书
写正确的是( )
A.OH-+HCl===HO+Cl- B.Ca(OH) +Cu2+===Ca2++Cu(OH)
2 2 2
C.Fe+Cu2+===Cu+Fe2+ D.Fe+2H+===Fe3++H↑
2
答案 C
解析 稀盐酸和石灰水发生中和反应,反应的离子方程式应为H++OH-===HO,A项错误;
2氯化铜和澄清石灰水反应生成氢氧化铜沉淀,反应的离子方程式为 Cu2++2OH-
===Cu(OH) ↓,B项错误;铁与氯化铜溶液发生置换反应,生成氯化亚铁和铜,反应的离
2
子方程式为Fe+Cu2+===Fe2++Cu,C项正确;铁为活泼金属,与稀盐酸发生置换反应生成
Fe2+和氢气,离子方程式为Fe+2H+===Fe2++H↑,D项错误。
2
6.(2020·湖南株洲二中模拟)下列解释事实的离子方程式正确的是( )
A.石灰水表面漂着的“白膜”可用醋酸溶解:CaCO +2H+===Ca2++CO↑+HO
3 2 2
B.NH HSO 溶液呈酸性的主要原因是NH+HO===NH ·H O+H+
4 4 2 3 2
C.盐碱地(含较多NaCl、NaCO)中加入石膏,降低土壤的碱性:Ca2++CO===CaCO ↓
2 3 3
D.漂白粉溶液在空气中失效:Ca2++2ClO-+CO+HO===2HClO+CaCO ↓
2 2 3
答案 D
解析 石灰水表面漂着的“白膜”为碳酸钙,用醋酸溶解的离子方程式为 CaCO +
3
2CHCOOH===2CHCOO-+Ca2++HO+CO↑,A项错误;NH HSO 溶液呈酸性的主要原
3 3 2 2 4 4
因是NH HSO ===NH+H++SO,B项错误;漂白粉溶液在空气中失效,是Ca(ClO) 与空气
4 4 2
中的二氧化碳、水反应,离子方程式为Ca2++2ClO-+CO +HO===2HClO+CaCO ↓,D
2 2 3
项正确。
7.(2020·泰安市高三模拟)下列离子方程式正确的是( )
A.MnO 与浓盐酸反应:MnO +4HCl(浓)=====Mn2++Cl↑+2HO+2Cl-
2 2 2 2
B.向Ba(OH) 溶液中滴加NaHSO 溶液,至混合溶液恰好为中性:
2 4
Ba2++2OH-+2H++SO===BaSO↓+2HO
4 2
C.向次氯酸钙溶液中通入SO :Ca2++2ClO-+SO +HO===CaSO↓+2HClO
2 2 2 3
D.FeCl 溶液与Cu的反应:Cu+Fe3+===Cu2++Fe2+
3
答案 B
解析 向Ba(OH) 溶液中滴加NaHSO 溶液,至混合溶液恰好为中性,要求氢氧根和氢离子
2 4
物质的量相等,氢氧化钡和硫酸氢钠的物质的量的比为1∶2,选项B正确;次氯酸有强氧
化性,可以将+4价硫氧化为+6价,选项C错误;离子方程式的电荷不守恒,选项D错误。
8.下列实验过程中产生的现象与图形相符合的是( )
A.稀硫酸滴加到Ba(OH) 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
2
B.铁粉加到一定量CuSO 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
4
C.CO 通入一定量NaOH溶液中(横坐标是CO 的体积,纵坐标为溶液的导电能力)
2 2
D.稀盐酸滴加到一定量NaOH溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
答案 A
解析 滴入的硫酸与氢氧化钡反应,生成硫酸钡沉淀和水,溶液中离子浓度减小,导电能力下降,恰好完全反应导电性变为零,再随着稀硫酸的滴入,溶液导电能力增加,直到变为定
值,故A正确;铁粉加到一定量CuSO 溶液中发生反应Fe+CuSO ===FeSO +Cu,根据方
4 4 4
程式知每当消耗56 g铁,生成64 g固体铜,所以固体的质量一直在增加,而图像中的固体
的质量先变小后变大,故B错误;CO 通入一定量NaOH溶液中,发生的化学反应是CO +
2 2
2NaOH===NaCO +HO、NaCO +HO+CO===2NaHCO ,根据方程式知钠离子浓度基本
2 3 2 2 3 2 2 3
不变,所以导电能力基本不变,故C错误;HCl+NaOH===NaCl+HO,氢氧化钠和氯化钠
2
都是强电解质,在水中完全电离,所以钠离子的物质的量不变,而图像中的钠离子的物质的
量先变小后变大,故D错误。
9.下列离子方程式书写正确的是( )
A.钠与水反应:Na+2HO===Na++2OH-+H↑
2 2
B.稀盐酸与苏打溶液反应:HCO+H+===CO↑+HO
2 2
C.向次氯酸钙溶液中通入过量二氧化碳:
Ca2++2ClO-+HO+CO===CaCO ↓+2HClO
2 2 3
D.铁盐腐蚀铜质电路板:2Fe3++Cu===2Fe2++Cu2+
答案 D
解析 不符合电子守恒、电荷守恒,离子方程式应该为:2Na+2HO===2Na++2OH-+
2
H↑,A错误;苏打是NaCO 的俗称,电离产生阴离子是CO,离子方程式应该为:CO+
2 2 3
2H+===CO↑+HO,B错误;CO 气体过量,反应产生可溶性Ca(HCO ) ,离子方程式应
2 2 2 3 2
该为:ClO-+HO+CO===HClO+HCO,C错误;反应符合事实,遵循离子方程式拆写原
2 2
则,D正确。
10.下列离子方程式书写正确的是( )
A.硫化亚铁与盐酸反应:S2-+2H+===HS↑
2
B.硫化氢气体通入氯水中:HS+Cl===2H++2Cl-+S↓
2 2
C.硫酸和氢氧化钡溶液混合:H++OH-+Ba2++SO===BaSO↓+HO
4 2
D.铁与稀硫酸反应:2Fe+6H+===2Fe3++3H↑
2
答案 B
解析 硫化亚铁是难溶性物质,在离子方程式里不能写成离子形式,故 A不选;硫化氢有
还原性,氯气有氧化性,两者会发生氧化还原反应,生成硫和氯化氢,故B选;1 mol硫酸
电离出2 mol H+和1 mol SO,1 mol氢氧化钡电离出1 mol Ba2+和2 mol OH-,所以离子方
程式中H+、OH-和水的系数均为2,即离子方程式为2H++2OH-+Ba2++SO===BaSO↓
4
+2HO,故C不选;稀硫酸的氧化性是H+体现出来的,H+的氧化性比较弱,不能把铁氧
2
化成Fe3+,只能氧化成Fe2+,故D不选。
11.向Ba(OH) 溶液中逐滴加入稀硫酸,请完成下列问题:
2
(1)写出反应的离子方程式:______________________________________________________。
(2)下列三种情况下,离子方程式与(1)相同的是______(填字母)。A.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至溶液显中性
4 2
B.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至SO恰好完全沉淀
4 2
C.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至过量
4 2
若在A项所得溶液中,继续滴加Ba(OH) 溶液,此步反应的离子方程式为:____________。
2
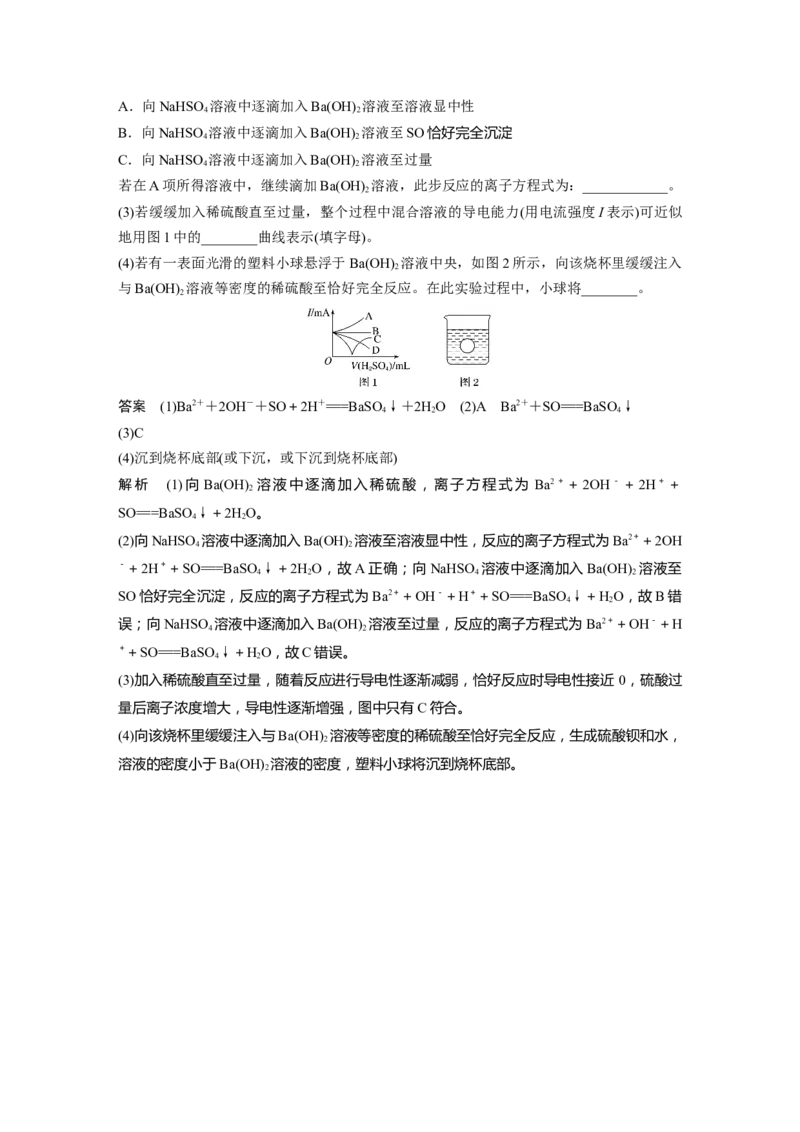
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似
地用图1中的________曲线表示(填字母)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH) 溶液中央,如图2所示,向该烧杯里缓缓注入
2
与Ba(OH) 溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将________。
2
答案 (1)Ba2++2OH-+SO+2H+===BaSO↓+2HO (2)A Ba2++SO===BaSO↓
4 2 4
(3)C
(4)沉到烧杯底部(或下沉,或下沉到烧杯底部)
解析 (1)向 Ba(OH) 溶液中逐滴加入稀硫酸,离子方程式为 Ba2++2OH-+2H++
2
SO===BaSO↓+2HO。
4 2
(2)向NaHSO 溶液中逐滴加入Ba(OH) 溶液至溶液显中性,反应的离子方程式为Ba2++2OH
4 2
-+2H++SO===BaSO↓+2HO,故A正确;向NaHSO 溶液中逐滴加入Ba(OH) 溶液至
4 2 4 2
SO恰好完全沉淀,反应的离子方程式为Ba2++OH-+H++SO===BaSO↓+HO,故B错
4 2
误;向NaHSO 溶液中逐滴加入Ba(OH) 溶液至过量,反应的离子方程式为Ba2++OH-+H
4 2
++SO===BaSO↓+HO,故C错误。
4 2
(3)加入稀硫酸直至过量,随着反应进行导电性逐渐减弱,恰好反应时导电性接近 0,硫酸过
量后离子浓度增大,导电性逐渐增强,图中只有C符合。
(4)向该烧杯里缓缓注入与Ba(OH) 溶液等密度的稀硫酸至恰好完全反应,生成硫酸钡和水,
2
溶液的密度小于Ba(OH) 溶液的密度,塑料小球将沉到烧杯底部。
2