文档内容
第 26 讲 常见非金属及其化合物重难点再落实
一、非金属及其化合物之间的转化
1.碳、硅及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①Si和NaOH溶液的反应
Si+2OH-+HO===SiO+2H↑;
2 2
②SiO 和NaOH溶液的反应
2
SiO+2OH-===SiO+HO;
2 2
③SiO 和C的反应
2
SiO+2C=====Si+2CO↑;
2
④SiO 和氢氟酸的反应
2
SiO+4HF===SiF↑+2HO;
2 4 2
⑤向NaSiO 溶液中通入过量CO 气体
2 3 2
SiO+2CO+2HO===HSiO↓+2HCO;
2 2 2 3
⑥Mg在CO 中燃烧
2
2Mg+CO=====2MgO+C;
2
⑦向澄清石灰水中通入少量CO 气体
2
Ca2++2OH-+CO===CaCO ↓+HO;
2 3 2
⑧向澄清石灰水中通入过量CO 气体
2
OH-+CO===HCO;
2
⑨除去CO 中的CO
2
CO+CuO=====CO+Cu;
2
⑩生产普通玻璃的原理NaCO+SiO=====NaSiO+CO↑、
2 3 2 2 3 2
CaCO +SiO=====CaSiO +CO↑。
3 2 3 2
2.氯气及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①Cl 和HO的反应
2 2
Cl+HOH++Cl-+HClO;
2 2
②Cl 和NaOH溶液的反应
2
Cl+2OH-===Cl-+ClO-+HO;
2 2
③Cl 和石灰乳的反应
2
Cl+Ca(OH) ===Ca2++Cl-+ClO-+HO;
2 2 2
④把Cl 通入NaSO 溶液中
2 2 3
Cl+SO+HO===SO+2H++2Cl-;
2 2
⑤将Cl 和SO 混合通入HO中
2 2 2
SO +Cl+2HO===4H++2Cl-+SO;
2 2 2
⑥将Cl 通入氢硫酸溶液中
2
Cl+HS===S↓+2H++2Cl-;
2 2
⑦将浓盐酸和MnO 混合加热
2
MnO +4H++2Cl-=====Mn2++Cl↑+2HO;
2 2 2
⑧电解饱和食盐水
2Cl-+2HO=====Cl↑+H↑+2OH-;
2 2 2
⑨将浓盐酸与漂白液混合
Cl-+ClO-+2H+===Cl↑+HO;
2 2
⑩将浓盐酸与KClO 溶液混合
3
6H++5Cl-+ClO===3Cl↑+3HO;
2 2
⑪向KMnO 固体滴加浓盐酸
4
2MnO+16H++10Cl-===2Mn2++5Cl↑+8HO;
2 2⑫向漂白粉溶液中通入少量CO 气体
2
Ca2++2ClO-+CO+HO===CaCO ↓+2HClO。
2 2 3
3.硫及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①S溶于热的烧碱溶液生成两种钠盐
3S+6OH-=====2S2-+SO+3HO;
2
②把HS气体通入CuSO 溶液中
2 4
HS+Cu2+===CuS↓+2H+;
2
③NaS溶液在空气中放置变浑浊
2
2S2-+O+2HO===2S↓+4OH-;
2 2
④铜丝在硫蒸气中燃烧
2Cu+S=====Cu S;
2
⑤将SO 气体通入氢硫酸中
2
SO +2HS===3S↓+2HO;
2 2 2
⑥把HS气体通入FeCl 溶液中
2 3
HS+2Fe3+===S↓+2Fe2++2H+;
2
⑦SO 通入足量的澄清石灰水中
2
SO +Ca2++2OH-===CaSO↓+HO;
2 3 2
⑧SO 通入溴水中,使溴水褪色
2
SO +Br +2HO===SO+2Br-+4H+;
2 2 2
⑨用足量氨水吸收SO 尾气
2
2NH ·H O+SO ===2NH+SO+HO;
3 2 2 2
○Cu和浓硫酸的反应
Cu+2HSO (浓)=====CuSO +SO ↑+2HO;
2 4 4 2 2
⑪C和浓硫酸的反应
C+2HSO (浓)=====CO↑+2SO ↑+2HO;
2 4 2 2 2
⑫把浓HSO 滴到NaSO 固体上
2 4 2 3HSO (浓)+NaSO ===NaSO +HO+SO ↑。
2 4 2 3 2 4 2 2
4.氮及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①N 和H 的反应
2 2
N+3H2NH ;
2 2 3
②把NH 通入水中
3
NH +HONH ·H ONH+OH-;
3 2 3 2
③实验室利用NH Cl固体、Ca(OH) 固体混合加热制备NH
4 2 3
2NH Cl+Ca(OH) =====2NH ↑+2HO+CaCl ;
4 2 3 2 2
④NH 的催化氧化
3
4NH +5O=====4NO+6HO;
3 2 2
⑤NH HCO 溶液中加入过量稀NaOH溶液
4 3
NH+HCO+2OH-===NH ·H O+CO+HO;
3 2 2
⑥NO 溶于水
2
3NO +HO===2H++2NO+NO;
2 2
⑦NO 被烧碱溶液吸收生成两种钠盐
2
2NO +2OH-===NO+NO+HO;
2 2
⑧物质的量之比为1∶1的NO和NO 混合气体恰好被烧碱溶液吸收生成一种钠盐
2
NO+NO +2OH-===2NO+HO;
2 2
⑨Cu和稀HNO 的反应
3
3Cu+8H++2NO===3Cu2++2NO↑+4HO;
2
⑩Cu和浓HNO 的反应
3
Cu+4H++2NO===Cu2++2NO ↑+2HO;
2 2
⑪Fe和过量稀HNO 的反应
3
Fe+4H++NO===Fe3++NO↑+2HO;
2
⑫C和浓HNO 的反应
3
C+4H++4NO=====CO↑+4NO ↑+2HO;
2 2 2
⑬浓硝酸见光分解
4HNO=====4NO ↑+O↑+2HO。
3 2 2 2二、新型无机框图推断题
1.熟记典型物质
(1)金属及其化合物:Na、NaO、NaCO、NaHCO ;Al、Al O、Al(OH) ;Fe、FeCl 等。
2 2 2 3 3 2 3 3 3
(2)非金属及其化合物:C、CO;Si、SiO;Cl、HClO;S、SO 、HSO ;N、NO 、NH 、
2 2 2 2 2 4 2 2 3
HNO 等。
3
2.重要物质的物理性质
(1)有色气体:NO (红棕色)、Cl(黄绿色);无色、刺激性气味的气体:SO 、NH 、HCl。
2 2 2 3
(2)溶液中的有色物质:Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(棕黄色)、MnO[紫(红)色]。Br 在水
2
中显黄(橙)色,在有机溶剂中显橙(红)色;I 在水中显黄(褐)色,在有机溶剂中显紫(红)色。
2
(3)有色固体:(淡)黄(棕)色固体:NaO 、S、FeS 、FeCl ;黑色固体:MnO 、C、CuO、
2 2 2 3 2
FeO、Fe O;紫(黑)色固体:KMnO 、I;(紫)红色固体:Cu。
3 4 4 2
(4)有色沉淀:①白色沉淀:HSiO 、AgCl、BaSO(不溶于酸)、BaSO 、Mg(OH) 、
2 3 4 3 2
Al(OH) 、BaCO 、CaCO 、CaSO 、MgCO 等;②红褐色沉淀:Fe(OH) ;③蓝色沉淀:
3 3 3 4 3 3
Cu(OH) ;④黑(褐)色沉淀:CuS、FeS。
2
3.既能与强酸溶液反应又能与强碱溶液反应的物质
(1)金属单质:Al。
(2)两性物质:两性氧化物如Al O,两性氢氧化物如Al(OH) ,以及氨基酸等。
2 3 3
(3)弱酸弱碱盐:如(NH )CO、CHCOONH 等。
4 2 3 3 4
(4)弱酸的酸式盐:如NaHCO 、Ca(HCO )、NaHSO 等。
3 3 2 3
4.熟悉常见的转化关系
(1)直线型转化关系
A――→B――→C
①X为O
2
Na―→NaO―→NaO
2 2 2
N―→NO―→NO 或NH ―→NO―→NO
2 2 3 2
S―→SO ―→SO 或HS―→SO ―→SO
2 3 2 2 3
C―→CO―→CO 或CH―→CO―→CO
2 4 2
醇―→醛―→羧酸
②X为CO
2
NaOH――→NaCO――→NaHCO
2 3 3
③X为强酸,如HCl
NaAlO ――→Al(OH) ――→AlCl
2 3 3
NaCO――→NaHCO ――→CO
2 3 3 2
④X为强碱,如NaOHAlCl ――→Al(OH) ――→NaAlO
3 3 2
(2)交叉型转化
(3)三角型转化
(4)注意反应形式与物质的关系,特别是置换反应
①金属―→金属:金属+盐―→盐+金属,铝热反应。
②金属―→非金属:活泼金属+HO(或H+)―→H,2Mg+CO=====2MgO+C。
2 2 2
③非金属―→非金属:2F +2HO===4HF+O ,2C+SiO=====Si+2CO↑,C+
2 2 2 2
HO(g)=====CO+H,X+HS===2HX+S↓。
2 2 2 2
④非金属―→金属:用H、C冶炼金属。
2
题组一 常见的物质转化关系
1.(2020·贵州模拟)在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A.粗硅――→SiCl ――→Si
4
B.Mg(OH) ――→MgCl (aq)――→Mg
2 2
C.Fe O――→FeCl (aq)――→无水FeCl
2 3 3 3
D.S――→SO ――→HSO
3 2 4
答案 A
解析 B项,电解熔融的MgCl 可制得镁,电解MgCl 溶液:MgCl +2HO=====Mg(OH) ↓
2 2 2 2 2
+H↑+Cl↑,错误;C项,FeCl 溶液蒸干过程中发生反应:FeCl +3HO=====Fe(OH) ↓
2 2 3 3 2 3
+3HCl↑,错误;D项,硫燃烧不能生成SO ,错误。
3
2.纯净物X、Y、Z转化关系如下图所示,下列判断正确的是( )A.X可能是金属铜 B.Y不可能是氢气
C.Z可能是氯化钠 D.Z可能是三氧化硫
破题要领 将选项物质代入看能否实现箭头方向的转化。
答案 A
解析 A项,若X是Cu,Y是Cl ,Cu在Cl 中燃烧生成CuCl ,电解CuCl 溶液生成Cu和
2 2 2 2
Cl,符合图中转化关系,正确;B项,若X是Cl,Y是H,H 在Cl 中燃烧生成HCl,HCl
2 2 2 2 2
溶于水生成盐酸,电解盐酸则生成H 和Cl ,也符合图中转化关系,错误;C项,若Z是氯
2 2
化钠,则X、Y分别是Na和Cl 中的一种,电解氯化钠水溶液生成的是H、Cl、NaOH,不
2 2 2
符合图中转化关系,错误;D项,若Z是SO ,而X、Y 分别是O 和SO 中的一种,SO 溶
3 2 2 3
于水生成硫酸,电解硫酸溶液实质是电解水,产生H 和O,不符合图中转化关系,错误。
2 2
3.甲、乙、丙、丁四种物质存在如下转化关系:
甲――→丙――→丁
(1)若甲、乙均为空气的主要成分,甲所含元素的简单阴离子的结构示意图为__________。
(2)若乙是生活中常见的金属单质,丙→丁的离子方程式为____________________________。
(3)若丙既能与强酸又能与强碱反应,则丙的化学式为____________(任写1种)。
答案 (1) (2)2Fe3++Fe===3Fe2+
(3)Al(OH) (或NaHCO )
3 3
4.单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备。其中X为Z的氧
化物;Y为氢化物,分子结构与甲烷相似。回答下列问题:
――→――→――→
(1) 能 与 X 发 生 化 学 反 应 的 酸 是 ________ ; 由 X 制 备 MgZ 的 化 学 方 程 式 为
2
______________________________________________________________________________。
(2)由MgZ生成Y的化学方程式为_________________________________________________,
2
Y分子的电子式为______________________________________________________________。
(3)Z、X中共价键的类型分别是__________、________。
破题要领——提取关键信息
关键信息 信息的分析与迁移
① 作半导体材料的单质常见物质是硅
② 硅的氧化物只有SiO
2
③ 类比甲烷的化学式确定Y为SiH
4
答案 (1)氢氟酸(HF) SiO+4Mg=====2MgO+MgSi
2 2(2)Mg Si+4HCl===2MgCl +SiH↑
2 2 4
(3)非极性键 极性键
解析 根据题意,单质Z为半导体材料,则Z是Si元素;其氧化物为二氧化硅,SiO 可与
2
氢氟酸反应;根据流程图可知,二氧化硅与Mg反应生成MgSi,MgSi与盐酸反应生成的
2 2
Y为氢化物,分子结构与甲烷相似,则Y的分子式是SiH,加热分解可得到Si单质。
4
不能一步实现的反应归纳
(1)H S(或S)不能一步转化为SO 。
2 3
(2)N (或NH )不能一步转化为NO 。
2 3 2
(3)SiO 不能与水反应生成HSiO。
2 2 3
(4)Fe O、Al O、CuO等不溶性金属氧化物都不能一步生成相应的氢氧化物。
2 3 2 3
题组二 “归中”转化关系
5.(2020·福州高三模拟)已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同
一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的HO已略去)。
2
请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、
用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式是__________;工业上
制取A的离子方程式为__________________________________________________________。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的
化学方程式为___________________________________________________________________。
(3)若 D 是氯碱工业的主要产品之一,B 物质具有两性,则反应②的离子方程式是
______________________________________________________________________________。
(4)若 A、C、D 都是常见气体,C 是导致酸雨的主要气体,则反应③的化学方程式为
______________________________________________________________________________。
某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起
始 一 段 时 间 内 , 酸 雨 的 pH 呈 减 小 趋 势 , 用 离 子 方 程 式 解 释 原 因 :
___________________________
_______________________________________________________________________________
。
答案 (1)FeCl 2Cl-+2HO=====2OH-+Cl↑+H↑
3 2 2 2
(2)4NH +5O=====4NO+6HO
3 2 2(3)Al(OH) +OH-===AlO+2HO
3 2
(4)2H S+SO ===3S↓+2HO
2 2 2
2HSO +O===4H++2SO
2 3 2
解析 (1)氯气常用于自来水消毒,则A为Cl ;铁是使用最广泛的金属单质,D是铁,则B
2
为FeCl ,C是FeCl 。
3 2
(2)碱性气体为NH ,汽车尾气中遇空气会变色的气体是NO。
3
(3)常见的两性物质是Al O 和Al(OH) ,D、C分别为NaOH和NaAlO ,故B为Al(OH) 。
2 3 3 2 3
(4)导致酸雨的主要气体是SO ,A与SO 均含有硫元素,且二者反应生成硫单质,故 A为
2 2
HS。酸雨的主要成分是HSO ,在放置过程中被氧化为HSO ,酸性增强。
2 2 3 2 4
常见的“归中”转化关系
(1)非氧化还原反应
①Al3++AlO―→Al(OH) 。
3
②CO+CO―→HCO。
2
(2)氧化还原反应
①Cl-+ClO-――→Cl。
2
②S2-+SO――→S。
③HS+SO ―→S。
2 2
④NH +NO―→N。
3 x 2
⑤Fe3++Fe―→Fe2+。
题组三 实验流程中的物质推断
6.已知有以下物质相互转化。
试回答下列问题:
(1)B的化学式为__________,D的化学式为__________________________________________。
(2)由E转变成F的化学方程式为___________________________________________________
_______________________________________________________________________________
。
(3)用KSCN溶液鉴别G溶液的离子方程式为________________________________________
______________________________________________________________________________;
向G溶液中加入A,反应的离子方程式为___________________________________________
_______________________________________________________________________________。
答案 (1)FeCl KCl
2
(2)4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
(3)Fe3++3SCN-===Fe(SCN) 2Fe3++Fe===3Fe2+
3
解析 由白色沉淀E置于空气中转化为红褐色沉淀F,可见E为Fe(OH) ,F为Fe(OH) ,G
2 3
为FeCl ,从而推断出A为Fe,B为FeCl ;焰色反应呈紫色,说明溶液中含有K+,从而确
3 2
定C为KOH。(1)B的化学式为FeCl ,D的化学式为KCl。(2)由E转变成F的化学方程式为
2
4Fe(OH) +O +2HO===4Fe(OH) 。(3)用KSCN溶液鉴别FeCl 溶液的离子方程式为Fe3++
2 2 2 3 3
3SCN-===Fe(SCN) ;向FeCl 溶液中加入铁,反应的离子方程式为2Fe3++Fe===3Fe2+。
3 3
题组四 化工生产流程中的物质推断
7.(2020·兰州质检)以黄铜矿(主要成分为CuFeS ,含少量杂质SiO 等)为原料,进行生物炼
2 2
铜,同时得到副产品绿矾(FeSO ·7H O)。其主要工艺流程如图所示:
4 2
已知:部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表所示:
沉淀物 Cu(OH) Fe(OH) Fe(OH)
2 3 2
开始沉淀pH 4.7 2.7 7.6
完全沉淀pH 6.7 3.7 9.6
(1)反应Ⅰ的化学方程式为______________________________________________________。
反应物中Fe元素被________(填“氧化”或“还原”),其目的是_____________________。
(2)试剂a是________,具体操作为________________________________________________,
目的是________________________________________________________________________。
(3)反应Ⅲ的离子方程式为________________________________________________________。
试剂c参与反应的离子方程式分别为______________________________________________、
______________________________________________________________________________。
答案 (1)4CuFeS +2HSO +17O===4CuSO +2Fe (SO ) +2HO 氧化 将Fe元素氧化成
2 2 4 2 4 2 4 3 2
Fe3+易于利用其水解生成Fe(OH) 沉淀而达到分离
3
(2)CuO[或Cu(OH) 、CuCO 、Cu (OH) CO 等] 加入试剂调节pH至3.7~4.7之间 使Fe3+
2 3 2 2 3
形成Fe(OH) 沉淀,防止生成Cu(OH) 沉淀
3 2
(3)Cu2++Fe===Cu+Fe2+ Fe+2H+===Fe2++H↑
2
Fe(OH) +3H+===Fe3++3HO
3 2无论推断题属于哪种形式,均遵循这样的推断思路:迅速浏览、整体扫描、产生印象、寻找
“突破口”,突破口由点到面、随时检验,注意联系、大胆假设、全面分析(正推或逆推),
验证确认。解题的关键是仔细审题,依物质的特性或特征转化来确定“突破口”,顺藤摸瓜,
进而完成全部未知物的推断。我们可以将推断题的解题方法及推理过程表示如下:
推断题――→――→――→结论―→验证
1.下列有关说法正确的是( )
A.工业上以氯气和澄清石灰水为原料制取漂白粉
B.为方便运输可用钢瓶储存液氯和浓硫酸
C.使用蒸发皿灼烧Fe(OH) 至分解
3
D.将SO 和Cl 按等物质的量比通入品红溶液中,品红很快褪色
2 2
答案 B
2.(2020·济南调研)化学与人类社会生产、生活密切相关。下列说法正确的是( )
A.误食重金属盐引起人体中毒,可喝大量的食盐水解毒
B.燃料的脱硫脱氮、SO 的回收利用和NO 的催化转化都是减少酸雨产生的措施
2 x
C.碳酸钡可用于胃肠X射线造影检查
D.生石灰可用作食品抗氧化剂
答案 B
解析 重金属盐引起人体中毒,用豆浆解毒,故A错误;SO 和NO 是形成酸雨的主要物质,
2 x
减少它们的排放可减少酸雨的产生,故 B正确;碳酸钡能与胃酸反应,引起中毒,故 C错
误;生石灰不能作食品抗氧化剂,而是作干燥剂,故D错误。
3.有如下转化关系(其他产物及反应所需条件均已略去)。
――→――→――→――→――→
以下推断错误的是( )
A.当X是盐酸时,则F是稀硝酸
B.当X是氢氧化钠时,则F可能是稀硝酸
C.当X是氢氧化钠时,B与Cl 反应可能有白烟现象
2
D.当X是氢氧化钠时,B可能使酸性高锰酸钾溶液褪色
答案 A
解析 当X是盐酸时,A是金属或金属氧化物,金属或金属氧化物和酸反应生成盐B,如果
盐B能和氯气反应生成C,则C也是盐,且是高价盐,C和氧气不反应,所以不能最后生成
硝酸,故 A 错误;NH Cl――→NH ――→N――→NO――→NO ――→HNO ,故 B 正确;2NH +
4 3 2 2 3 3
3Cl===6HCl+N ,生成的 HCl 会和过量的 NH 反应,产生白烟,故 C 正确;
2 2 3HS――→NaS――→S――→SO ――→SO ――→HSO ,NaS能被酸性KMnO 溶液氧化,使酸性高锰
2 2 2 3 2 4 2 4
酸钾溶液褪色,故D正确。
4.化学美无处不在。下图是物质间发生化学反应的颜色变化,其中X是( )
A.稀盐酸 B.稀硫酸
C.硫酸钠溶液 D.碳酸钠溶液
答案 B
解析 稀盐酸不与Ba(NO ) 反应,A项不符合;硫酸钠、碳酸钠都不能与CuO、Fe反应,
3 2
C、D项都不符合。
5.臭氧已成为夏季空气污染的元凶,地表产生臭氧的机理如图所示。设N 代表阿伏加德罗
A
常数的值。下列说法正确的是( )
A.该过程中,O 是催化剂
3
B.16 g O 和O 的混合气体,所含质子数为16N
3 2 A
C.0.5 mol NO 溶于水形成1 L溶液,可得到0.5 mol·L-1的硝酸溶液
2
D.标准状况下,各5.6 L的NO和O 混合后,气体总质量为15.5 g
2
答案 D
6.某兴趣小组设计用铁粉将NO还原为N(同时生成FeO),下列说法不正确的是( )
2
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置戊中发生的化学方程式为2NO+2Fe=====2FeO+N
2
C.装置丁的作用是除去挥发出来的硝酸
D.装置乙的作用是干燥,防止水蒸气进入戊中干扰反应
答案 D
解析 根据实验原理利用NO被灼热的铁粉还原为N,同时生成FeO,所以首先应制备纯净
2
的干燥的NO,利用铜与稀硝酸反应生成NO,由于硝酸具有挥发性,所以制得的NO中会
混有硝酸和水蒸气,则先通过装置丁除去挥发出的HNO ,然后再通过己干燥,得到纯净干
3
燥的NO进入戊中与铁粉反应,最后处理多余的NO,又因为NaOH溶液不与NO反应,而
浓硝酸可氧化NO生成NO ,所以先通过装置乙氧化NO,后再通过装置丙吸收,故装置接
2
口的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,A正确;装置戊中NO被灼热的
铁粉还原为N ,同时生成FeO,反应的化学方程式为2NO+2Fe=====2FeO+N ,B正确;
2 2
装置丁盛放的是水,其作用是除去挥发出的HNO ,C正确;装置乙盛放的是浓硝酸,可以
3
将NO氧化为NO ,便于NaOH溶液吸收,D错误。
2
7.漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为Ca(ClO) ,相应的生产流程如下。
2
下列说法错误的是( )
A.①中电解饱和食盐水制氯气的过程中,有元素化合价发生变化
B.②中反应的化学方程式为2Cl+2Ca(OH) ===Ca(ClO) +CaCl +2HO
2 2 2 2 2
C.④中反应ClO+HO===2HClO,氯元素的价态未发生改变
2 2
D.制备漂白粉的过程中,Cl 转化为Ca(ClO) 时,Cl的原子利用率为100%
2 2
答案 D
解析 氯碱工业中电解饱和食盐水,生成氢气、氯气和氢氧化钠,氢元素和氯元素化合价发
生改变,故 A 正确;漂白粉制取的化学方程式:2Cl +2Ca(OH) ===Ca(ClO) +CaCl +
2 2 2 2
2HO,故B正确;ClO和HClO中氯元素均为+1价,氯元素的价态未发生改变,故C正确;
2 2
Cl 转化为Ca(ClO) 的同时还有CaCl 生成,Cl的原子利用率小于100%,故D错误。
2 2 2
8.碳和浓硫酸共热产生的气体X和铜与稀硝酸反应产生的气体Y同时通入盛有足量氯化钡
溶液的洗气瓶中(如图所示装置),下列有关说法错误的是( )A.洗气瓶中产生的沉淀是BaCO
3
B.洗气瓶中产生的沉淀是BaSO
4
C.在Z导管口可能有红棕色的气体出现
D.在Z导管口出现的气体中含有CO
2
答案 A
解析 因为碳酸的酸性比盐酸的酸性弱,所以在BaCl 溶液中通入CO ,不能生成BaCO 沉
2 2 3
淀,A错误;NO和洗气瓶中的O 反应生成的NO 溶于水生成HNO ,HNO 将HSO 氧化
2 2 3 3 2 3
成HSO ,因此有BaSO 沉淀生成,B正确;若O 不足,NO有剩余,则Z导管口可能出现
2 4 4 2
红棕色气体,C正确;CO 未参与反应,D正确。
2
9.汽车发动机稀燃控制系统主要工作原理是发动机在稀燃和富燃条件下交替进行,尾气中
的NO 在催化剂上反应脱除。其工作原理示意图如下:
x
下列说法不正确的是( )
A.稀燃过程中,NO发生的主要反应为2NO+O===2NO
2 2
B.稀燃过程中,NO 被吸收的反应为BaO+2NO ===Ba(NO )
2 2 3 2
C.富燃过程中,NO 被CO还原的反应为2NO +4CO===N+4CO
2 2 2 2
D.富燃过程中,CH 被O 氧化的反应为CH+(x+)O ===xCO+HO
x y 2 x y 2 2 2
答案 B
解析 该反应中只有元素化合价的升高,没有降低,不符合氧化还原反应的书写规则,故
B错误。
10.碘在地壳中主要以NaIO 的形式存在,在海水中主要以I-的形式存在,几种粒子之间有
3
如图所示关系,根据图示转化关系推测下列说法不正确的是( )
A.可用淀粉KI试纸和食醋检验加碘盐中是否含有碘
B.足量Cl 能使湿润的淀粉KI试纸变白的原因可能是5Cl+I+6HO===2HIO +10HCl
2 2 2 2 3
C.由图可知氧化性的强弱顺序为Cl>I >IO
2 2
D.途径Ⅱ中若生成1 mol I ,反应中转移的电子数为10N
2 A
答案 C
解析 加碘盐中含有IO,在酸性条件下可被I-还原生成I ,淀粉KI试纸会变蓝,A正确;
2
根据图示转化关系可知淀粉KI试纸变白的原因可能是5Cl +I +6HO===2HIO +10HCl,B
2 2 2 3正确;根据途径Ⅰ可知氧化性:Cl>I ,根据途径Ⅱ可知氧化性:IO>I ,根据途径Ⅲ可知氧
2 2 2
化性:Cl>IO,C错误;根据关系式:2IO~I ~10e-可知,若生成1 mol I ,反应中转移的
2 2 2
电子数为10N ,D正确。
A
11.合成氨及其相关工业中,部分物质间的转化关系如图所示。下列说法不正确的是( )
A.甲、乙、丙三种物质中都含有氮元素
B.反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C.Ⅵ的产物可在上述流程中被再次利用
D.Ⅴ中发生反应:NH +CO+HO+NaCl===NaHCO ↓+NH Cl
3 2 2 3 4
答案 B
解析 甲是N ,与H 化合生成NH 。反应Ⅴ是侯氏制碱法原理,丁是NaHCO ,受热分解
2 2 3 3
生成 NaCO 。NH 发生催化氧化生成 NO,NO 与 O 反应生成 NO ,NO 溶于水生成
2 3 3 2 2 2
HNO ,HNO 和NH 反应生成NH NO ,即乙是NO,丙是NO 。甲、乙、丙三种物质中都
3 3 3 4 3 2
含有氮元素,A正确;反应Ⅳ中的氧化剂和还原剂均是NO ,B错误;NaHCO 分解生成的
2 3
CO 可以循环利用,C正确。
2
12.(2018·天津,9)烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下
x
采样和检测方法。回答下列问题:
Ⅰ.采样
采样步骤:
①检验系统气密性;②加热器将烟道气加热至140 ℃;③打开抽气泵置换系统内空气;④
采集无尘、干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用为_______________________________________________。
(2)C中填充的干燥剂是____________(填序号)。
a.碱石灰 b.无水CuSO c.PO
4 2 5
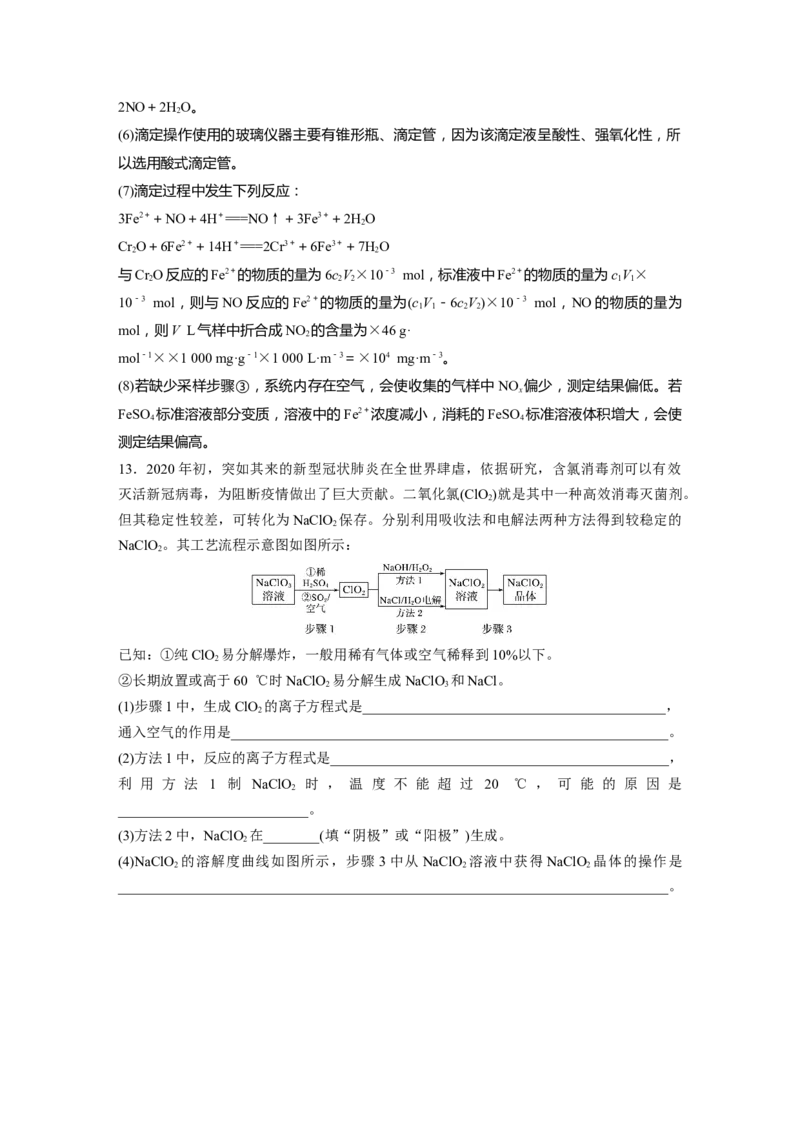
(3)用实验室常用仪器组装一套装置,其作用与D(装有碱液)相同,在虚线框中画出该装置的
示意图,标明气体的流向及试剂。(4)采样步骤②加热烟道气的目的是_______________________________________________。
Ⅱ.NO 含量的测定
x
将V L气样通入适量酸化的HO 溶液中,使NO 完全被氧化成NO,加水稀释至100.00
2 2 x
mL。量取20.00 mL该溶液,加入V mL c mol·L-1 FeSO 标准溶液(过量),充分反应后,用
1 1 4
c mol·L-1 KCr O 标准溶液滴定剩余的Fe2+,终点时消耗V mL。
2 2 2 7 2
(5)NO被HO 氧化为NO的离子方程式为_________________________________________。
2 2
(6)滴定操作使用的玻璃仪器主要有________________________________________________。
(7)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2HO
2
Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
则气样中NO 折合成NO 的含量为________ mg·m-3。
x 2
(8)判断下列情况对NO 含量测定结果的影响(填“偏高”“偏低”或“无影响”)。
x
若缺少采样步骤③,会使测定结果_______________________________________________。
若FeSO 标准溶液部分变质,会使测定结果_______________________________________。
4
答案 (1)除尘 (2)c
(3)
(4)防止NO 溶于冷凝水
x
(5)2NO+3HO===2H++2NO+2HO
2 2 2
(6)锥形瓶、酸式滴定管 (7)×104
(8)偏低 偏高
解析 (1)装置A是过滤器,装有无碱玻璃棉的作用是过滤,除去粉尘。
(2)C中填充的是干燥剂,除去HO且不能与NO 反应,所以应选有酸性、干燥能力强的
2 x
PO。
2 5
(3)D装置中装有碱液,用于除去NO,作用与实验室中的洗气瓶相同,该装置的示意图为
x
。
(4)烟道气中有水,采样步骤②加热器将烟道气加热至140 ℃的目的是防止NO 溶于冷凝水。
x
(5)NO被HO 氧化为NO,HO 的还原产物为HO,离子方程式为2NO+3HO===2H++
2 2 2 2 2 2 22NO+2HO。
2
(6)滴定操作使用的玻璃仪器主要有锥形瓶、滴定管,因为该滴定液呈酸性、强氧化性,所
以选用酸式滴定管。
(7)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2HO
2
Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
与Cr O反应的Fe2+的物质的量为6cV×10-3 mol,标准液中Fe2+的物质的量为cV×
2 2 2 1 1
10-3 mol,则与NO反应的Fe2+的物质的量为(cV -6cV)×10-3 mol,NO的物质的量为
1 1 2 2
mol,则V L气样中折合成NO 的含量为×46 g·
2
mol-1××1 000 mg·g-1×1 000 L·m-3=×104 mg·m-3。
(8)若缺少采样步骤③,系统内存在空气,会使收集的气样中NO 偏少,测定结果偏低。若
x
FeSO 标准溶液部分变质,溶液中的Fe2+浓度减小,消耗的FeSO 标准溶液体积增大,会使
4 4
测定结果偏高。
13.2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效
灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(ClO )就是其中一种高效消毒灭菌剂。
2
但其稳定性较差,可转化为NaClO 保存。分别利用吸收法和电解法两种方法得到较稳定的
2
NaClO。其工艺流程示意图如图所示:
2
已知:①纯ClO 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2
②长期放置或高于60 ℃时NaClO 易分解生成NaClO 和NaCl。
2 3
(1)步骤1中,生成ClO 的离子方程式是___________________________________________,
2
通入空气的作用是______________________________________________________________。
(2)方法1中,反应的离子方程式是________________________________________________,
利 用 方 法 1 制 NaClO 时 , 温 度 不 能 超 过 20 ℃ , 可 能 的 原 因 是
2
___________________________。
(3)方法2中,NaClO 在________(填“阴极”或“阳极”)生成。
2
(4)NaClO 的溶解度曲线如图所示,步骤3中从NaClO 溶液中获得NaClO 晶体的操作是
2 2 2
______________________________________________________________________________。(5)为测定制得的晶体中NaClO 的含量,做如下操作:
2
①称取a g样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫
酸,充分反应(已知:ClO+4I-+4H+===2HO+2I +Cl-)。将所得混合液配成100 mL待测
2 2
溶液。
②移取25.00 mL待测溶液于锥形瓶中,用b mol·L-1NaSO 标准液滴定,至滴定终点。重
2 2 3
复2次,测得消耗标准溶液的体积的平均值为c mL(已知:I +2SO===2I-+SO)。样品中
2 2 4
NaClO 的质量分数为____________(用含a、b、c的代数式表示)。
2
答案 (1)2ClO+SO ===SO+2ClO 稀释产生的ClO ,防止其分解爆炸 (2)2OH-+2ClO
2 2 2 2
+HO===2ClO+O +2HO HO 温度较高时易分解 (3)阴极 (4)加热温度至略低于60
2 2 2 2 2 2
℃,浓缩,冷却至略高于38 ℃结晶,过滤,洗涤 (5)×100%
解析 由制备流程可知,NaClO 在酸性条件下与二氧化硫发生氧化还原反应生成 ClO ,同
3 2
时得到NaHSO ,ClO 发生器中发生反应HSO +2NaClO +SO ===2ClO ↑+2NaHSO ,纯
4 2 2 4 3 2 2 4
ClO 易分解爆炸,通入足量空气稀释 ClO 以防止爆炸;方法1中发生2NaOH+2ClO +
2 2 2
HO===2NaClO +2HO+O ,根据图可看出,高于38 ℃时析出NaClO 晶体,且控制温度
2 2 2 2 2 2
低于60 ℃,减压蒸发结晶、过滤、洗涤、干燥得到 NaClO 产品;方法2中电解时阳极上
2
发生反应为 2Cl--2e-===Cl↑,阴极上发生反应为 ClO +e-===ClO,阴极上析出
2 2
NaClO,结晶、干燥得到NaClO 产品。
2 2
(5)设25.00 mL待测溶液中NaClO 的物质的量为x mol,则:
2
NaClO~2I~4SO
2 2 2
1 4
x bc×10-3
解得:x=2.5bc×10-4,m(NaClO)=×2.5bc×10-4mol×90.5 g·mol-1=9.05bc×10-2 g,则
2
a g样品中NaClO 的质量分数为×100%。
2