文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题01
1.下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其他三种归为一类的是
A.泰山墨玉 B.龙山黑陶 C.齐国刀币 D.淄博琉璃
答案:C
解析:墨玉、黑陶、琉璃均为陶瓷制品,均属于硅酸盐制品,主要成分均为硅酸盐材料,而刀
币的主要成分为青铜,故答案为:C。
2.下列物质中属于耐高温酸性氧化物的是
A. CO B. SiO C. MgO D. Na O
2 2 2
答案:B
解析:A.二氧化碳和碱反应生成盐和水,是酸性氧化物,但为分子晶体,不耐高温,A错误;
B.SiO 能跟碱反应生成盐和水:SiO+2OH-=SiO HO,所以SiO 是酸性氧化物,为共价晶
2 2 + 2 2
体,耐高温,B正确;
C.MgO能跟酸反应生成盐和水:MgO +2H+=Mg2++H O,所以MgO是碱性氧化物,;C错误;
2
D.NaO能跟酸反应生成盐和水,所以是碱性氧化物,;D错误;
2
3. 关于反应2NH OH+4Fe3+=NO↑+4Fe2++4H++HO,下列说法正确的是
2 2 2
A. 生成1molN O,转移4mol电子 B.NH OH是还原产物
2 2
C.NH OH既是氧化剂又是还原剂 D. 若设计成原电池,Fe2+为负极产物
2
答案:A
解析:A.由方程式可知,反应生成1mol一氧化二氮,转移4mol电子,故A正确;
B.由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,故B错误;
2
C.由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,铁元素的化
2
合价降低被还原,铁离子是反应的氧化剂,故C错误;
D.由方程式可知,反应中铁元素的化合价降低被还原,铁离子是反应的氧化剂,若设计成原
电池,铁离子在正极得到电子发生还原反应生成亚铁离子,亚铁离子为正极产物,故D错误;
4.下列反应的离子方程式不正确的是
A. Cl 通入氢氧化钠溶液:Cl+2OH-=Cl-+ClO-+HO
2 2 2
B. 氧化铝溶于氢氧化钠溶液:Al O+2OH-=2AlO+HO
2 3 2
C. 过量CO 通入饱和碳酸钠溶液:2Na++CO CO+HO =2NaHCO ↓
2 + 2 2 3
D. H SO 溶液中滴入氯化钙溶液:SO Ca2+=CaSO↓
2 3 + 3
答案:D解析:A.Cl 通入氢氧化钠溶液中反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:
2
Cl+2OH-=Cl-+ClO-+HO,选项A正确;
2 2
B.氧化铝溶于氢氧化钠溶液生成偏铝酸钠和水,反应的离子方程式为:Al O+2OH-=2AlO
2 3
+HO,选项B正确;
2
C.过量CO 通入饱和碳酸钠溶液反应产生碳酸氢钠晶体,反应的离子方程式为:2Na++CO
2 +
CO+HO =2NaHCO ↓,选项C正确;
2 2 3
D.HSO 溶液中滴入氯化钙溶液,因亚硫酸酸性弱于盐酸,不能发生反应,选项D不正确;
2 3
5.材料是人类赖以生存和发展的物质基础,下列材料主要成分属于有机物的是
A. 石墨烯 B. 不锈钢 C. 石英光导纤维 D. 聚酯纤维
答案:D
解析:A.石墨烯是一种由单层碳原子构成的平面结构新型碳材料,为碳的单质,属于无机物,
A不符合题意;
B.不锈钢是Fe、Cr、Ni等的合金,属于金属材料,B不符合题意;
C.石英光导纤维的主要成分为SiO,属于无机非金属材料,C不符合题意;
2
D.聚酯纤维俗称“涤纶”,是由有机二元酸和二元醇缩聚而成的聚酯经纺丝所得的合成纤维,
属于有机物,D符合题意;
6.下列化学用语表示正确的是
A. H S分子的球棍模型:
2
B. AlCl 的价层电子对互斥模型:
3
C. KI的电子式:
D. CH CH(CH CH) 的名称:3−甲基戊烷
3 2 3 2
答案:D
解析:A.HS分子是“V”形结构,因此该图不是HS分子的球棍模型,故A错误;
2 2
B.AlCl 中心原子价层电子对数为3+(3-1×3)=3+0=3,其价层电子对互斥模型为平面三角
3
形,故B错误;
C.KI是离子化合物,其电子式: ,故C错误;D.CHCH(CH CH) 的结构简式为 ,其名称为3−甲基戊烷,故D正确。
3 2 3 2
7.下列反应的离子方程式正确的是
A. 碘化亚铁溶液与等物质的量的氯气:2Fe2++2I-+2Cl=2Fe3++I+4Cl-
2 2
B. 向次氯酸钙溶液通入足量二氧化碳:ClO-+CO+HO=HClO+HCO
2 2
C. 铜与稀硝酸:Cu+4H++2NO Cu2++2NO ↑+2HO
= 2 2
D. 向硫化钠溶液通入足量二氧化硫:S2-+2SO +2HO=HS+2HSO
2 2 2
答案:B
解析:A.碘化亚铁溶液与等物质的量的氯气发生反应,碘离子与氯气恰好完全反应:2I-+
Cl=I+2Cl-,故A错误;
2 2
B.向次氯酸钙溶液通入足量二氧化碳,反应生成碳酸氢钙和次氯酸:ClO-+CO+HO=
2 2
HClO+HCO B正确;
,故
C.铜与稀硝酸反应生成硝酸铜、一氧化氮和水:3Cu+8H++2NO 3Cu2++2NO ↑+4HO,故
= 2 2
C错误;
D.向硫化钠溶液通入足量二氧化硫,溶液变浑浊,溶液中生成亚硫酸氢钠:2S2-+5SO +
2
2HO=3S↓+4HSO D错误;
2 ,故
8.化学与生活密切相关,下列说法正确的是
A. 苯甲酸钠可作为食品防腐剂是由于其具有酸性
B. 豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C. SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D. 维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
答案:B
解析:A.苯甲酸钠属于强碱弱酸盐,其水溶液呈碱性,因此,其可作为食品防腐剂不是由于
其具有酸性,A说法不正确;
B.胶体具有丁达尔效应,是因为胶体粒子对光线发生了散射;豆浆属于胶体,因此,其能产
生丁达尔效应是由于胶体粒子对光线的散射,B说法正确;
C.SO 可用于丝织品漂白是由于其能与丝织品中有色成分化合为不稳定的无色物质,C说法
2
不正确;
D.维生素C具有很强的还原性,因此,其可用作水果罐头的抗氧化剂是由于其容易被氧气氧
化,从而防止水果被氧化,D说法不正确;
9.下列应用中涉及到氧化还原反应的是A. 使用明矾对水进行净化 B. 雪天道路上撒盐融雪
C. 暖贴中的铁粉遇空气放热 D. 荧光指示牌被照发光
答案:C
解析:A.使用明矾对水进行净化过程中,明矾电离出的铝离子发生水解生成氢氧化铝胶体,
氢氧化铝胶体粒子吸附水中的悬浮颗粒并沉降下来而水变得澄清,该过程中没有任何一种元素的化
合价发生变化,因此没有涉及到氧化还原反应,A不符合题意;
B.雪天道路上撒盐融雪,是因为雪遇到盐而使其熔点降低并熔化,该过程中没有任何一种元
素的化合价发生变化,因此没有涉及到氧化还原反应,B不符合题意;
C.暖贴中的铁粉遇空气放热,是因为暖贴中含有的铁粉、碳粉、氯化钠、水等物质,形成当
这些物质遇到空气后形成无数微小原电池并开始工作,化学能转化为电能,无数微小原电池堆积在
一起使得电能又转化为热能,该过程中铁元素和氧元素的化合价发生变化,因此,该过程涉及到氧
化还原反应,C符合题意;
D.荧光指示牌被照发光,是因为光被指示牌发生了反射,该过程中没有任何一种元素的化合
价发生变化,因此没有涉及到氧化还原反应,D不符合题意;
10.化学在文物的研究和修复中有重要作用。下列说法错误的是
A. 竹简的成分之一纤维素属于天然高分子
B. 龟甲的成分之一羟基磷灰石属于无机物
C. 古陶瓷修复所用的熟石膏,其成分为Ca(OH)
2
D. 古壁画颜料中所用的铁红,其成分为Fe O
2 3
答案:C
解析:A.纤维素是一种天然化合物,其分子式为(C H O),其相对分子质量较高,是一种天
6 10 5 n
然高分子,A正确;
B.羟基磷灰石又称又称羟磷灰石、碱式磷酸钙,其化学式为[Ca (PO )(OH) ],属于无机物,
10 4 6 2
B正确;
C.熟石膏是主要成分为2CaSO·H O,Ca(OH) 为熟石灰的主要成分,C错误;
4 2 2
D.Fe O 为红色,常被用于油漆、涂料、油墨和橡胶的红色颜料,俗称铁红,D正确;
2 3
11.【任务一】某小组研究NaCO 和NaHCO 的性质,实验如下:
2 3 3
现象
序号 操作
NaCO NaHCO
2 3 3在两支试管中加入1g Na CO 或
2 3 温度由17.6℃变为 温度由17.6℃变为17.2℃;
1g NaHCO 固体,再加入5mL
① 3 23.2℃;放置至室温时, 放置至室温时,试管内有少
水,振荡;将温度计分别插入其
试管内无固体 量固体残留
中
室温时,分别向①所得溶液中滴
② 溶液变红 溶液微红
入2滴酚酞溶液
(1)室温下,NaCO 的溶解度大于NaHCO 的实验证据是___________________________。
2 3 3
(2)该实验不能说明NaCO 溶液的碱性强于NaHCO 溶液,理由是___________________。
2 3 3
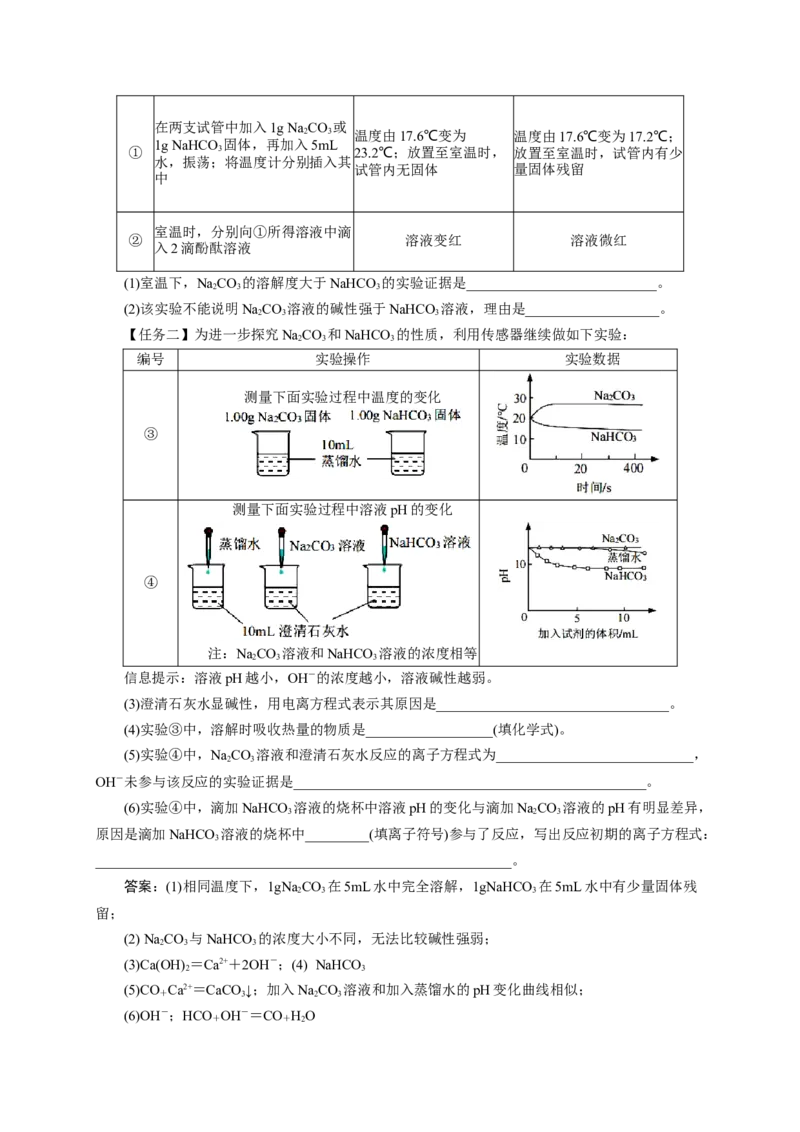
【任务二】为进一步探究NaCO 和NaHCO 的性质,利用传感器继续做如下实验:
2 3 3
编号 实验操作 实验数据
测量下面实验过程中温度的变化
③
测量下面实验过程中溶液pH的变化
④
注:NaCO 溶液和NaHCO 溶液的浓度相等
2 3 3
信息提示:溶液pH越小,OH-的浓度越小,溶液碱性越弱。
(3)澄清石灰水显碱性,用电离方程式表示其原因是_________________________________。
(4)实验③中,溶解时吸收热量的物质是__________________(填化学式)。
(5)实验④中,NaCO 溶液和澄清石灰水反应的离子方程式为____________________________,
2 3
OH-未参与该反应的实验证据是__________________________________________________。
(6)实验④中,滴加NaHCO 溶液的烧杯中溶液pH的变化与滴加NaCO 溶液的pH有明显差异,
3 2 3
原因是滴加NaHCO 溶液的烧杯中_________(填离子符号)参与了反应,写出反应初期的离子方程式:
3
___________________________________________________________。
答案:(1)相同温度下,1gNaCO 在5mL水中完全溶解,1gNaHCO 在5mL水中有少量固体残
2 3 3
留;
(2) Na CO 与NaHCO 的浓度大小不同,无法比较碱性强弱;
2 3 3
(3)Ca(OH) =Ca2++2OH-;(4) NaHCO
2 3
(5)CO Ca2+=CaCO ↓;加入NaCO 溶液和加入蒸馏水的pH变化曲线相似;
+ 3 2 3
(6)OH-;HCO OH-=CO HO
+ + 2解析:在其他条件相同的情况下,观察相同质量的碳酸钠和碳酸氢钠溶于水时能否完全溶解,
可以比较出碳酸钠与碳酸氢钠的溶解度;在相同浓度的碳酸钠、碳酸氢钠溶液相比较,碳酸钠溶液
的pH大于碳酸氢钠溶液;强碱弱酸盐水解使溶液呈碱性;比较碳酸钠、碳酸氢钠固体溶解时的温
度变化,可以判断出二者溶解时的热效应;比较观察所给图象可知,将碳酸钠、碳酸氢钠溶液中分
别滴加到澄清石灰水中,滴加碳酸钠溶液时在反应过程中,pH值几乎不变,而滴加碳酸氢钠溶液
时,pH值在逐渐减小,据此解答问题。
(1)室温下,在两支试管中加入1gNaCO 或1gNaHCO 固体,再加入5mL水,振荡,NaCO 完
2 3 3 2 3
全溶解,NaHCO 有少量固体残留,说明NaHCO 在水中溶解度小,已经达到饱和,故答案为:相
3 3
同温度下,1gNaCO 在5mL水中完全溶解,1gNaHCO 在5mL水中有少量固体残留;
2 3 3
(2)虽然所得溶液中分别滴入2滴酚酞溶液,NaCO 溶液呈红色,NaHCO 在溶液呈浅红色,前
2 3 3
者碱性强,但二者的物质的量浓度不相同,无法比较碱性强弱,故答案为:NaCO 与NaHCO 的物
2 3 3
质的量浓度不同,无法比较碱性强弱;
(3) Ca(OH) 是强电解质,溶于水的部分能够完全电离,Ca(OH) =Ca2++2OH-,故答案为:
2 2
Ca(OH) =Ca2++2OH-;
2
(4)观察任务二中所给图示温度的变化,可以发现NaCO 固体和NaHCO 固体分别溶于水,温
2 3 3
度分别升高和降低,说明NaCO 固体的溶解是放热过程,NaHCO 固体的溶解是吸热过程,故答案
2 3 3
为:NaHCO ;
3
(5) Na CO 溶液和澄清石灰水反应的离子方程式为CO Ca2+=CaCO ↓,观察所给图象可知,将
2 3 + 3
碳酸钠溶液中滴加到澄清石灰水中,溶液pH值变化与加入蒸馏水稀释时的pH变化曲线相似,故
答案为:加入NaCO 溶液和加入蒸馏水的pH变化曲线相似;
2 3
(6)滴加NaHCO 溶液的烧杯中溶液pH明显减小,说明OH-被消耗,反应初期的离子方程式
3
HCO OH-=CO HO,后再生成碳酸钙白色沉淀,故答案为:OH-;HCO OH-=CO HO。
+ + 2 + + 2
12.150mL某无色溶液中可能含有Na+、NH、Mg2+、Al3+、Fe3+、Ba2+、CO SO中的若干种,现将
、
此溶液分成三等份,进行如下实验:
①向第一份中加入足量的0.5mol·L-1-1稀盐酸,生成0.448L气体(已换算成标准状况下);
②向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体;
③向第三份中加入足量BaCl 溶液,得到沉淀6.27g,加入足量(0.5mol·L-1稀盐酸充分反应后,
2
剩余沉淀2.33g。
根据上述实验,回答下列问题:
(1)用12mol·L-1的浓盐酸配制240mL0.5mol·L-1稀盐酸,需要用量筒量取_______mL浓盐酸,若
在量取浓盐酸时俯视刻度线,则会导致配制的稀盐酸的浓度_______(填“偏高”、“偏低”或“不
变”)。
(2)实验②中生成气体的离子方程式为______________________________________。
(3)实验③中沉淀部分溶解的化学方程式为__________________________________________,剩
余沉淀的化学式为___________。(4)原溶液中c(SO)=__________mol·L-1,c(CO -1
)_______mol·L
(5)经分析,溶液中一定存在Na+,理由是__________________________________________。
答案:(1)10.4 偏低 (2)NH+OH-===NH ↑+HO
3 2
(3) BaCO +2HCl=BaCl +CO ↑+H O BaSO (4) 0.2 0.4
3 2 2 2 4
(5)经分析得知溶液中一定存在的离子有NH、CO SO,根据离子共存原则可知溶液中一定不存
、
在 Mg2+、Al3+、Fe3+、Ba2+,且硫酸根离子和碳酸根离子所带负电荷总量大于铵根离子所带正电荷
总量,只有存在钠离子,溶液才能保持电中性
解析:某无色溶液中可能含有Na+、NH、Mg2+、Al3+、Fe3+、Ba2+、CO SO中的若干种,则肯
、
定不含有色离子Fe3+;
第一份中加入足量的0.5mol·L-1-1稀盐酸,生成0.448L气体,则含有CO 3+、Ba2+;
0.02mol,不含Al
向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体,含有NH0.04mol;
向第三份中加入足量BaCl 溶液,得到沉淀6.27g,加入足量(0.5mol·L-1-1稀盐酸充分反应后,
2
剩余沉淀2.33g。则可知,同时含有CO SO,且CO :0.01mol。
、 :0.02mol、SO
(1)配置240mL溶液,需要用250mL容量瓶,所以需要盐酸=0.0104L=10.4mL,量取盐酸时,
俯视刻度线会使得取出盐酸偏少,所配置溶液浓度偏低;
(2)铵根与碱发生反应产生氨气:NH+OH-===NH ↑+HO
3 2
(3)由分析可知,溶解的物质为BaCO ,方程为:BaCO +2HCl=BaCl +CO ↑+H O,剩余物质为
3 3 2 2 2
BaSO;
4
(4)由分析可知,溶液中所含n(SO)=3×0.01mol=0.03mol,浓度为c==0.2mol·L-1;n(CO=
)
3×0.02mol=0.06mol,浓度为c==0.4mol·L-1;
(5)由上述分析可知,原溶液中含有NH:0.12mol、CO SO:0.03mol,由电荷守恒可知,
:0.06mol、
c(Na+)=0.06mol,Na+必然存在。