文档内容
课时检测(十六) 铁的化合物的制备、转化与应用
1.(2024·广东广州模拟·改编)市场出售的某种麦片中含有微量、颗粒细小的还原铁粉,在人体胃
酸(主要成分:盐酸)的作用下可发生反应对人体进行补铁,实验室模拟胃酸与该麦片反应,下列操作可
检验出反应生成补铁溶液的是( )
A.取样,加入少量KMnO 溶液
4
B.取样,加入少量KS溶液
2
C.取样,加入少量KSCN溶液
D.取样,加入少量K[Fe(CN) ]溶液
3 6
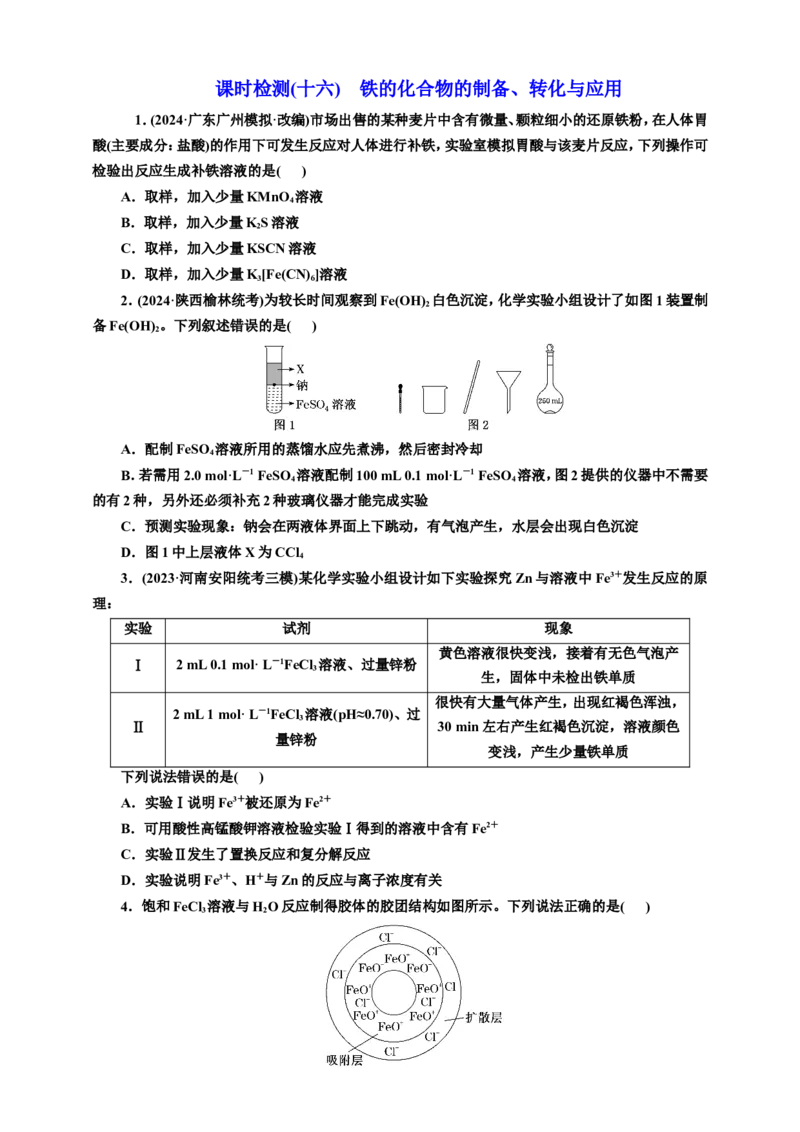
2.(2024·陕西榆林统考)为较长时间观察到Fe(OH) 白色沉淀,化学实验小组设计了如图1装置制
2
备Fe(OH) 。下列叙述错误的是( )
2
A.配制FeSO 溶液所用的蒸馏水应先煮沸,然后密封冷却
4
B.若需用2.0 mol·L-1 FeSO 溶液配制100 mL 0.1 mol·L-1 FeSO 溶液,图2提供的仪器中不需要
4 4
的有2种,另外还必须补充2种玻璃仪器才能完成实验
C.预测实验现象:钠会在两液体界面上下跳动,有气泡产生,水层会出现白色沉淀
D.图1中上层液体X为CCl
4
3.(2023·河南安阳统考三模)某化学实验小组设计如下实验探究Zn与溶液中Fe3+发生反应的原
理:
实验 试剂 现象
黄色溶液很快变浅,接着有无色气泡产
Ⅰ 2 mL 0.1 mol· L-1FeCl 溶液、过量锌粉
3
生,固体中未检出铁单质
很快有大量气体产生,出现红褐色浑浊,
2 mL 1 mol· L-1FeCl 溶液(pH≈0.70)、过
3
Ⅱ 30 min 左右产生红褐色沉淀,溶液颜色
量锌粉
变浅,产生少量铁单质
下列说法错误的是( )
A.实验Ⅰ说明Fe3+被还原为Fe2+
B.可用酸性高锰酸钾溶液检验实验Ⅰ得到的溶液中含有Fe2+
C.实验Ⅱ发生了置换反应和复分解反应
D.实验说明Fe3+、H+与Zn的反应与离子浓度有关
4.饱和FeCl 溶液与HO反应制得胶体的胶团结构如图所示。下列说法正确的是( )
3 2A.反应的离子方程式为Fe3++3HO=====Fe(OH) ↓+3H+
2 3
B.FeCl 溶液能使血液凝聚,是因为FeCl 溶液是电解质,血液是胶体
3 3
C.Fe(OH) 胶体带正电,在盛有Fe(OH) 胶体的U形管中插入石墨电极后通电,阴极周围颜色加
3 3
深
D.Fe(OH) 受热分解可得一种碱性氧化物——FeO
3 2 3
5.(2023·浙江1月选考)探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案 现象 结论
往FeCl 溶液中加入Zn 短时间内无明显 Fe2+的氧化能力比
2
A
片 现象 Zn2+弱
往Fe(SO ) 溶液中滴加
2 4 3
溶液先变成血红 Fe3+与SCN-的反
B KSCN溶液,再加入少量
色后无明显变化 应不可逆
KSO 固体
2 4
将食品脱氧剂样品中的
食品脱氧剂样品中
C 还原铁粉溶于盐酸,滴加 溶液呈浅绿色
没有+3价铁
KSCN溶液
向沸水中逐滴加5~6 滴 Fe3+先水解得
溶液先变成红褐
D 饱和FeCl 溶液,持续煮 Fe(OH) 再聚集成
3 3
色再析出沉淀
沸 Fe(OH) 沉淀
3
6.一种废水处理剂可表示为MFe(SO )(OH) ,可按下列实验步骤确定其组成(气体体积在标准状
x y 4 z w
况下测定):
下列有关叙述错误的是( )
A.检验a中是否含有Fe3+可用KSCN溶液
B.气体b能使湿润的红色石蕊试纸变蓝
C.加入稀盐酸的目的是溶解其中的氢氧化物
D.若V=448,m=13.6,m=9.32,可确定该化合物为NH Fe(SO )(OH)
1 2 4 3 4 2 3
7.(2024年1月·九省联考贵州卷)高铁酸钠(Na FeO)是一种新型绿色消毒剂,主要用于饮用水处
2 4
理。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C及油脂)制备高铁酸钠的主要流程如下。下
列说法错误的是( )
废铁屑滤液滤渣
A.“碱浸”可以除去废铁屑中的油脂
B.“滤渣”的主要成分是Al和C
C.“操作Ⅰ”通入的空气可以用HO 溶液代替
2 2
D.若流程改为先“氧化”后“调pH”,可能会生成Cl
2
8.铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。琥珀酸亚铁是市场上一种常见的补铁药物,该药品不溶于水但能溶于人体中的胃酸。某同学为了检测该补铁药物中Fe2+的
存在,设计并进行了如下实验:
下列有关说法正确的是( )
A.试剂1是蒸馏水,试剂2是KSCN溶液
B.加入新制氯水后溶液中发生氧化反应生成的氧化产物使溶液变红色
C.加入试剂2后溶液中少量的Fe2+转化为Fe3+
D.一段时间后,红色溶液褪色,再加入氯水又变红色
9.Fe3+的配位化合物较稳定且应用广泛。Fe3+可与HO、SCN-、F-等配体形成使溶液呈浅紫色的
2
[Fe(H O) ]3+、红色的[Fe(SCN) ]3-、无色的[FeF ]3-配离子。某同学按如下步骤完成实验:
2 6 6 6
已知:向含Co2+的溶液中加入KSCN溶液生成蓝色的[Co(SCN) ]2-配离子;Co2+不能与F-形成
4
配离子。下列说法不正确的是( )
A.Fe第四电离能(I)大于其第三电离能(I)
4 3
B.Ⅰ中溶液呈黄色可能是由Fe3+水解产物的颜色造成的
C.可用NaF和KSCN溶液检验FeCl 溶液中是否含有Co2+
3
D.[Fe(H O) ]3+中H—O—H的键角与HO分子中H—O—H的键角相等
2 6 2
10.探究Cu与Fe(NO) 溶液的反应,进行如下实验。
3 3
实验①:向10 mL 0.2 mol·L-1Fe(NO) 溶液(pH≈1)中加入0.1 g Cu粉,振荡后静置,取上层清液,
3 3
滴加K[Fe(CN) ]溶液,有蓝色沉淀产生。6 h后,溶液由棕黄色变为蓝绿色。实验过程中未见有气泡产
3 6
生,溶液的pH几乎不变。
实验②:在密闭容器中,向10 mL 0.6 mol·L-1HNO 溶液中加入0.1 g Cu粉,10 h后溶液变为淡蓝
3
色。
实验③:在密闭容器中,向10 mL 0.6 mol·L-1HNO 溶液中分别加入0.1 g Cu粉和0.1 g FeSO 固
3 4
体,0.5 h后溶液变黄,3 h后溶液变为黄绿色。
下列说法不正确的是( )
A.实验①中发生了反应:Cu+2Fe3+===Cu2++2Fe2+
B.推测实验②的离子方程式是3Cu+2NO+8H+===3Cu2++2NO↑+4HO
2
C.对比实验①和②,①中溶解Cu的主要是NO(H+)
D.对比实验②和③,HNO 与Fe2+反应的速率大于HNO 与Cu反应的速率
3 3
11.某小组在验证反应“Fe+2Ag+===Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下:
向硝酸酸化的0.05 mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固
体,溶液呈黄色。
(1)检验产物
①取出少量黑色固体,洗涤后,_________________________________________
________________________________________________________________________(填操作和现
象),证明黑色固体中含有Ag。
②取上层清液,滴加K[Fe(CN) ]溶液,产生蓝色沉淀,说明溶液中含有________。
3 6
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理
是______________________(用离子方程式表示)。
针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液
颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
取样时间
序号 现象
/min
Ⅰ 3 产生大量白色沉淀;溶液呈红色
Ⅱ 30 产生白色沉淀,较3 min时量少;溶液红色较3 min时加深
Ⅲ 120 产生白色沉淀,较30 min时量少;溶液红色较30 min时变浅
(资料:Ag+与SCN-生成白色沉淀AgSCN)
②对Fe3+产生的原因做出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O,由于_____________________________________________
2
________________________________________________________________________(用离子方程
式表示),
可产生Fe3+;
假设c:酸性溶液中NO具有氧化性,可产生Fe3+;
假设d:根据__________________________________________________________现象,
判断溶液中存在Ag+,可产生Fe3+。
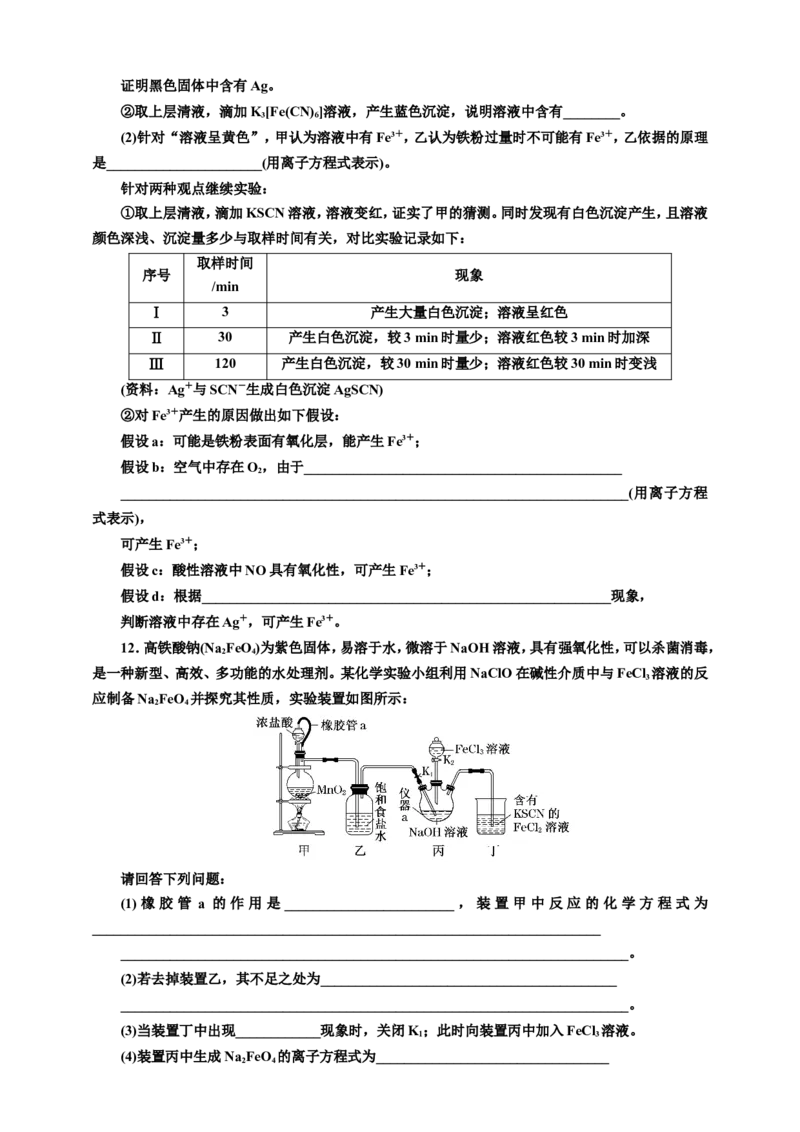
12.高铁酸钠(Na FeO)为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀菌消毒,
2 4
是一种新型、高效、多功能的水处理剂。某化学实验小组利用NaClO在碱性介质中与FeCl 溶液的反
3
应制备Na FeO 并探究其性质,实验装置如图所示:
2 4
请回答下列问题:
(1)橡胶管 a 的作用是 ________________________,装置 甲中反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)若去掉装置乙,其不足之处为__________________________________________
________________________________________________________________________。
(3)当装置丁中出现____________现象时,关闭K;此时向装置丙中加入FeCl 溶液。
1 3
(4)装置丙中生成Na FeO 的离子方程式为_________________________________
2 4________________________________________________________________________。
(5)反应后,向装置丙中加入饱和的____________(填化学式)溶液,析出紫色晶体,过滤、洗涤、干
燥。
(6)取少量Na FeO 晶体加入浑浊的泥浆水中,泥浆水很快澄清,同时产生气体。请结合化学方程
2 4
式分析Na FeO 的净水原理:_________________________________________
2 4
________________________________________________________________________
________________________________________________________________________。
13.乳酸亚铁晶体{[CH CH(OH)COO] Fe·3HO}是一种很好的食品铁强化剂,吸收效果比无机铁
3 2 2
好,易溶于水,几乎不溶于乙醇,可由乳酸与FeCO 反应制得。
3
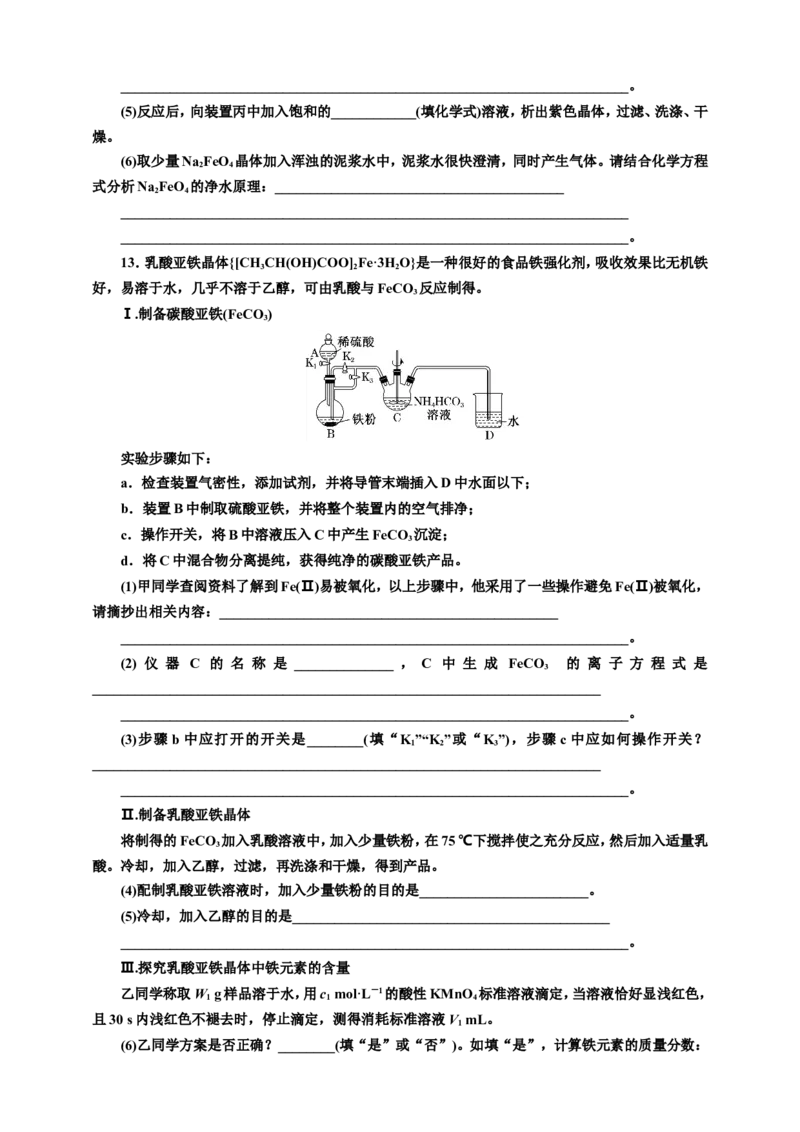
Ⅰ.制备碳酸亚铁(FeCO )
3
实验步骤如下:
a.检查装置气密性,添加试剂,并将导管末端插入D中水面以下;
b.装置B中制取硫酸亚铁,并将整个装置内的空气排净;
c.操作开关,将B中溶液压入C中产生FeCO 沉淀;
3
d.将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)甲同学查阅资料了解到Fe(Ⅱ)易被氧化,以上步骤中,他采用了一些操作避免Fe(Ⅱ)被氧化,
请摘抄出相关内容:________________________________________________
________________________________________________________________________。
(2) 仪 器 C 的 名 称 是 ______________ , C 中 生 成 FeCO 的 离 子 方 程 式 是
3
________________________________________________________________________
________________________________________________________________________。
(3)步骤 b 中应打开的开关是________(填“K”“K”或“K”),步骤 c 中应如何操作开关?
1 2 3
________________________________________________________________________
________________________________________________________________________。
Ⅱ.制备乳酸亚铁晶体
将制得的FeCO 加入乳酸溶液中,加入少量铁粉,在75 ℃下搅拌使之充分反应,然后加入适量乳
3
酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
(4)配制乳酸亚铁溶液时,加入少量铁粉的目的是________________________。
(5)冷却,加入乙醇的目的是_____________________________________________
________________________________________________________________________。
Ⅲ.探究乳酸亚铁晶体中铁元素的含量
乙同学称取W g样品溶于水,用c mol·L-1的酸性KMnO 标准溶液滴定,当溶液恰好显浅红色,
1 1 4
且30 s内浅红色不褪去时,停止滴定,测得消耗标准溶液V mL。
1
(6)乙同学方案是否正确?________(填“是”或“否”)。如填“是”,计算铁元素的质量分数:________(用含有 W 、c 、V 的代数式表示)。如填“否”,说明偏高还是偏低,理由是
1 1 1
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
课时检测(十六)
1.D 铁粉与胃酸反应,生成补铁的亚铁盐溶液,则通过检验亚铁离子是否存在即可判断是否生
成补铁溶液。Cl-会与KMnO 反应,干扰KMnO 对Fe2+的检验,A错误;过量的盐酸会影响FeS的生
4 4
成,无法确认Fe2+是否存在,B错误;能使KSCN溶液变红的是Fe3+,C错误;加入K[Fe(CN) ] 溶液,
3 6
样品中有蓝色沉淀生成,说明其中含有Fe2+,即反应生成了补铁溶液,D正确。
2.D Fe(OH) 易被氧化而变色,故要想长时间观察Fe(OH) 的白色,必须严格除氧,一方面配制
2 2
溶液的蒸馏水要煮沸,另一方面要用有机溶剂液封,A正确;配制0.1 mol·L-1 FeSO 溶液需要的玻璃
4
仪器:100 mL容量瓶、烧杯、玻璃棒、胶头滴管和量筒,不需要漏斗、250 mL容量瓶,B正确;由于反应
过程中生成气体,钠会在界面上下跳动,水层会出现白色胶状固体,C正确;所用有机溶剂必须难溶于
水且不与钠反应、密度必须比钠小,但CCl 密度大于钠,D错误。
4
3.B 实验Ⅰ黄色溶液很快变浅,固体中未检出铁单质,说明Fe3+被还原为Fe2+,选项A正确。
FeCl 溶液中的Cl-也能被酸性高锰酸钾溶液氧化,干扰Fe2+的检验,故不能用酸性高锰酸钾溶液检验
3
实验Ⅰ得到的溶液中含有Fe2+,选项B错误。FeCl 溶液中加入过量锌粉,很快有大量气体产生,是氯
3
化铁溶液水解产生的盐酸与锌粉反应产生氯化锌和氢气,反应为置换反应;出现红褐色浑浊,是氯化
铁水解生成氢氧化铁,属于复分解反应;产生少量铁单质,是锌置换出铁,属于置换反应,选项C正确。
根据题述实验可知,实验开始时Fe3+浓度较大,先与锌发生氧化还原反应生成氯化锌和氯化亚铁,当
Fe3+浓度较低,H+浓度较大时,H+与锌反应生成锌盐和氢气,故实验说明Fe3+、H+与Zn的反应与离
子浓度有关,选项D正确。
4.D 该反应生成氢氧化铁胶体,不是沉淀,离子方程式为Fe3++3HO Fe(OH) (胶体)+3H
2 3
+,A错误;FeCl 溶液是混合物,不属于电解质,FeCl 是电解质,B错误;Fe(OH) 胶体不带电,其中所
3 3 3
含的胶粒因吸附离子而带电,C错误;Fe(OH) 不稳定,受热分解生成氧化铁,氧化铁属于碱性氧化物,
3
D正确。
5.D 往FeCl 溶液中加入Zn片,发生反应Fe2++Zn===Zn2++Fe,溶液由浅绿色变为无色,Fe2
2
+的氧化能力比Zn2+强,A项错误;往Fe(SO ) 溶液中滴加KSCN 溶液,发生反应Fe3++3SCN-⥫⥬
2 4 3
Fe(SCN) ,溶液变血红色,再加入少量KSO 固体,对平衡无影响,故不能说明Fe3+与SCN-的反应不
3 2 4
可逆,B项错误;若食品脱氧剂样品中有+3价铁,铁粉与+3价铁发生反应Fe+2Fe3+===3Fe2+,滴加
KSCN 溶液,溶液呈浅绿色,C项错误;向沸水中逐滴加5~6滴饱和FeCl 溶液,继续煮沸至溶液呈红
3
褐色,得到Fe(OH) 胶体,持续煮沸,Fe(OH) 胶体发生聚沉,析出红褐色沉淀,D项正确。
3 3
6.D 可用KSCN溶液检验溶液中是否含有Fe3+,A正确;化合物与强碱反应生成气体,该气体
为氨气,氨气能使湿润的红色石蕊试纸变蓝,B正确;由于加入的是强碱Ba(OH) ,产生的沉淀c一定
2
是氢氧化铁和硫酸钡,而铁的氢氧化物溶于强酸,硫酸钡不能溶于强酸,C正确;根据给出数据,可确
定 m g 化合物中含有n(NH)==0.02 mol,n(SO)==0.04 mol,n(Fe3+)=n[Fe(OH)]= =0.04 mol,
3再根据溶液呈电中性可推知溶液中含有 n(OH-)=3n(Fe3+)+n(NH)-2n(SO)=0.04 mol×3+0.02 mol
-0.04 mol×2=0.06 mol,n(NH)∶n(Fe3+)∶n(SO)∶n(OH-)=0.02∶0.04∶0.04∶0.06=1∶2∶2∶3,
所以该化合物为NH Fe(SO )(OH) ,D错误。
4 2 4 2 3
7.B 废铁屑(主要成分为Fe,杂质有Al、C及油脂)加NaOH碱浸,可以除去废铁屑表面的油脂
和Al,过滤后滤液中含有Na[Al(OH) ]和油脂水解后形成的物质,固体中含有Fe、C,加盐酸酸浸,过
4
滤后滤渣为C,滤液为氯化亚铁溶液,通入空气Fe2+被氧化为Fe3+,加NaOH调pH为碱性,NaClO和
Fe(OH) 发生氧化还原反应得到Na FeO、NaCl,并通过结晶分离出Na FeO。根据分析,“碱浸”可
3 2 4 2 4
以除去废铁屑中的油脂,A正确;根据分析,“滤渣”的主要成分是C,B错误;根据分析,“操作Ⅰ”
目的是将Fe2+氧化为Fe3+,用HO 也可以作氧化剂,且不会引入杂质,因此通入的空气可以用HO
2 2 2 2
溶液代替,C正确;若先“氧化”,溶液为酸性,Na FeO 在酸性条件下有较强的氧化性,能将盐酸中的
2 4
Cl-氧化为Cl ,D正确。
2
8.C 该药品不溶于水,但能溶于人体中的胃酸,试剂1用于溶解样品,可以选用稀盐酸,试剂2
用于检验Fe3+,可以选用KSCN溶液,A错误;氯水氧化亚铁离子生成氧化产物铁离子呈黄色,铁离子
与硫氰根离子结合生成硫氰化铁呈红色,B错误;加入试剂2后溶液由淡黄色变为淡红色,是因为少量
的Fe2+被空气氧化转化为Fe3+,C正确;因为氯水氧化性很强,试剂2中少量的SCN-可能被过量的氯
水氧化使红色溶液褪色,故再加入KSCN溶液又变红色,D错误。
9.D Fe3+的价电子排布式为3d5,3d轨道处于半满状态,电子的能量低,失电子困难,所以Fe的
第四电离能(I)大于其第三电离能(I),A正确;[Fe(H O) ]3+使溶液呈浅紫色,而Fe3+易水解,生成红褐
4 3 2 6
色的Fe(OH) ,与浅紫色[Fe(H O) ]3+形成混合体系,使溶液呈黄色,B正确;先向溶液中加入足量的
3 2 6
NaF溶液,再加入KSCN溶液,若溶液呈蓝色,则表明含有Co2+,否则不含Co2+,C正确;[Fe(H O) ]3+
2 6
中HO分子内O原子最外层只存在一个孤电子对,对H—O—H 中O—H键的排斥作用减小,所以键
2
角比HO分子中 H—O—H 的键角大,D错误。
2
10.C 实验①中取上层清液,滴加K[Fe(CN) ]溶液,有蓝色沉淀产生,说明有亚铁离子生成;6 h
3 6
后,溶液由棕黄色变为蓝绿色,说明有铜离子生成,故发生了反应:Cu+2Fe3+===
Cu2++2Fe2+,A正确。实验②溶液变为淡蓝色,说明有铜离子生成,则推测实验②的离子方程式是
3Cu+2NO+8H+===3Cu2++2NO↑+4HO,B正确。对比实验①和②,①中溶解Cu的主要是铁离子,
2
不是硝酸根离子,C错误。对比实验②和③,③中先生成铁离子,后生成铜离子,说明HNO 与Fe2+反
3
应的速率大于HNO 与Cu反应的速率,D正确。
3
11.解析:(1)②K[Fe(CN) ]是检验Fe2+的试剂,所以产生蓝色沉淀说明溶液中含有Fe2+。(2)过量
3 6
铁粉与Fe3+反应生成Fe2+,Fe+2Fe3+===3Fe2+。O 氧化Fe2+的反应为4Fe2++O+4H+===4Fe3++
2 2
2HO。白色沉淀是AgSCN,所以实验可以说明含有Ag+,Ag+可能氧化Fe2+生成Fe3+。
2
答案:(1)①加入足量稀盐酸(或稀硫酸)酸化,固体未完全溶解 ②Fe2+
(2)Fe+2Fe3+===3Fe2+ 4Fe2++O+4H+===4Fe3++2HO
2 2
加入KSCN溶液后生成白色沉淀
12.解析:(3)若装置甲中生成的氯气将装置中的空气完全排出后,过量的氯气将丁中氯化亚铁氧
化为氯化铁,FeCl 与溶液中的硫氰化钾反应生成硫氰化铁,使溶液变为红色。(5)高铁酸钠易溶于水,
3
微溶于NaOH溶液,反应后为使高铁酸钠析出,向装置丙中加入饱和的NaOH溶液。
答案:(1)平衡气压,便于浓盐酸顺利流下
MnO +4HCl(浓)=====MnCl + Cl ↑+2HO
2 2 2 2(2)挥发出的氯化氢与氢氧化钠溶液反应,干扰Na FeO 的制备 (3)溶液变为红色
2 4
(4)3ClO-+2Fe3++10OH-===2FeO+3Cl-+5HO
2
(5)NaOH (6)Na FeO 在水中发生反应:4Na FeO +10HO===4Fe(OH) (胶体)+3O↑+
2 4 2 4 2 3 2
8NaOH,氢氧化铁胶体具有吸附性,可净水
13.解析:(3)步骤b利用生成的氢气排尽装置内的空气,应打开K 使B中反应进行,打开K 使生
1 3
成的氢气充满装置,排走空气;步骤c要使B中的硫酸亚铁溶液压入C中,应关闭K、K,一段时间后
1 3
打开K。(4)Fe2+容易被氧化成Fe3+,铁粉可将Fe3+还原成Fe2+,即加入铁粉可防止Fe(Ⅱ)被氧化。(5)
2
乳酸亚铁晶体易溶于水,几乎不溶于乙醇,故冷却,加入乙醇的目的是减小乳酸亚铁的溶解度,使之析
出,提高产量。(6)乙同学方案不正确,测定铁元素含量时只能考虑高锰酸钾与亚铁离子的反应,但乳酸
根离子也能被酸性高锰酸钾溶液氧化,从而使测得的铁元素的质量分数偏高。
答案:(1)将导管末端插入D中水面以下;将整个装置内的空气排净
(2)三颈烧瓶 Fe2++2HCO===FeCO ↓+HO+CO ↑
3 2 2
(3)K 、K 关闭K、K,一段时间后打开K
1 3 1 3 2
(4)防止Fe(Ⅱ)被氧化
(5)减小乳酸亚铁的溶解度,使之析出,提高产量
(6)否 偏高,乳酸根离子也能被酸性高锰酸钾溶液氧化,消耗更多的酸性高锰酸钾溶液,使铁元
素的质量分数偏高