文档内容
章末综合检测(八)
(时间:60分钟 分值:100分)
一、选择题(本小题包括9小题,每小题6分,共54分)
1.下列说法正确的是( )
A.将FeCl 溶液和Fe (SO ) 溶液分别加热、蒸干、灼烧,所得固体成分相同
3 2 4 3
B.配制FeSO 溶液时,将FeSO 固体溶于稀盐酸中,然后稀释至所需浓度
4 4
C.用加热的方法可以除去KSO 溶液中的Fe3+
2 4
D.洗涤油污常用热的碳酸钠溶液
解析:选D。A项,氯化铁溶液加热、蒸干、灼烧后得到氧化铁,而硫酸铁溶液加热、蒸干、
灼烧后得到的仍是硫酸铁,不正确;B项,所加酸应是稀硫酸,溶于稀盐酸引入新杂质,不正确;
C项,加热法不能除去KSO 溶液中的Fe3+,不正确。
2 4
2.化学平衡常数(K)、弱酸的电离平衡常数(K)、难溶物的溶度积常数(K )是判断物质性质
a sp
或变化的重要平衡常数。下列关于这些常数的说法中,正确的是( )
A.平衡常数的大小与温度、浓度、压强、催化剂等有关
B.当温度升高时,弱酸的电离平衡常数K 变小
a
C.K (AgCl)>K (AgI),由此可以判断AgCl(s)+ I-(aq)===AgI(s)+Cl-(aq)能够发生
sp sp
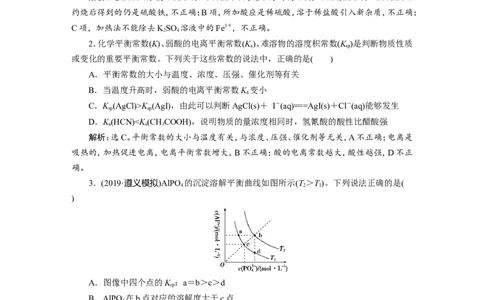
D.K(HCN)H CO>HClO
3 2 3
(2)CO>ClO->HCO>CHCOO-
3
(3)A ABCE
(4)大于 (5)③④⑤
12.(12分)(2019·杭州模拟)Ⅰ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)
和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
NaOH的物质
混合后溶液的
实验编号 HA的物质的量浓度/(mol/L) 的量浓度/
pH
(mol/L)
甲 0.1 0.1 pH=a
乙 0.12 0.1 pH=7
丙 0.2 0.1 pH>7
丁 0.1 0.1 pH=10
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?
________________________________________________________________________。
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是________(填编号)。
A.前者大 B.后者大
C.二者相等 D.无法判断
(3) 从 丙 组 实 验 结 果 分 析 , 该 混 合 溶 液 中 离 子 浓 度 由 大 到 小 的 顺 序 是
________________________________________________________________________。(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=
________mol/L。
Ⅱ.某二元酸(化学式用HB表示)在水中的电离方程式是HB===H++HB-、HB-H+
2 2
+B2-。
(5)在0.1 mol/L的NaB溶液中,下列粒子浓度关系式正确的是________。
2
A.c(B2-)+c(HB-)=0.1 mol/L
B.c(B2-)+c(HB-)+c(H B)=0.1 mol/L
2
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
解析:Ⅰ.(1)一元酸HA与NaOH等物质的量反应,HA的酸性强弱决定完全中和后盐溶
液的pH,a=7时HA为强酸,a>7时HA为弱酸。(2)根据电荷守恒,有c(Na+)+c(H+)=
c(A-)+c(OH-),因c(H+)=c(OH-),所以c(Na+)=c(A-)。(3)丙为等浓度的HA与NaA的混合
溶液,由 pH>7 知 A-水解程度大于 HA 的电离程度,离子浓度的大小关系为 c(Na+)>
c(A-)>c(OH-)>c(H+)。(4)根据电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-),推导 c(Na+)-
c(A-)=c(OH-)-c(H+)=(10-4-10-10) mol/L。
Ⅱ.(5)注意题干中的电离方程式,一级电离为完全电离,判断A项为B元素的物料守恒,C项
为溶液中的质子守恒。
答案:Ⅰ.(1)a=7时,HA是强酸;a>7时,HA是弱酸
(2)C
(3)c(Na+)>c(A-)>c(OH-)>c(H+)
(4)(10-4-10-10)
Ⅱ.(5)AC
13.(14分)按要求回答下列问题:
(1)实验室中通常用NaOH溶液进行洗气和提纯,当用100 mL 3 mol·L-1的NaOH溶液吸
收标准状况下 6.72 L SO 时,所得溶液显酸性,溶液中各离子浓度由大到小的顺序为
2
________________________________________________________________________。
(2)T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b
=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
NaOH溶液的体积/
序号 盐酸的体积/mL 溶液的pH
mL
① 20.00 0.00 8
② 20.00 20.00 6
假设溶液混合前后的体积变化忽略不计,则c为________。
A.3 B.4 C.5 D.6
(3)常温下,浓度均为0.1 mol·L-1的下列三种溶液的pH如表所示:溶质 CHCOONa NaClO NaCN
3
pH 8.8 10.3 11.1
①根据表中数据,将浓度均为0.01 mol·L-1的下列三种酸的溶液分别稀释100倍,pH变
化最小的是______。
A.HCN B.HClO C.CHCOOH
3
②根据以上数据,判断下列反应可以成立的是________。
A.CHCOOH+NaClO===HClO+CHCOONa
3 3
B.CHCOOH+NaCN===CH COONa+HCN
3 3
C.HCN+NaClO===NaCN+HClO
(4)几种离子开始沉淀时的pH如表:
离子 Fe2+ Cu2+ Mg2+
pH 7.6 5.2 10.4
当向含相同浓度Cu2+、Mg2+和Fe2+的溶液中滴加NaOH溶液时,________(填离子符号)
先沉淀,K [Fe(OH) ]________K [Mg(OH) ](填“>”“=”或“<”)。
sp 2 sp 2
解析:(1)n(NaOH)=0.1 L×3 mol·L-1=0.3 mol,n(SO )=6.72 L÷22.4 L· mol-1=0.3 mol,
2
故溶质为 NaHSO 。由于溶液显酸性,可知HSO的水解程度小于 HSO的电离程度,则
3
c(H+)>c(SO)>c(OH-),故离子浓度的大小关系为 c(Na+)>c(HSO)>c(H+)>c(SO)>
c(OH-)。
(2)根据题意可知在该温度下水的离子积常数是1×10-12,而不是1×10-14,通过①可知,
此NaOH溶液中c(OH-)=1×10-4 mol·L-1。由②可知,加入20.00 mL盐酸后溶液的pH=6,
此时恰好完全中和,则c(H+)==1×10-4 mol·L-1,则c=pH=-lg (1×10-4)=4。
(3)从盐溶液的pH可知,对应酸的电离能力(酸性强弱):CHCOOH>HClO>HCN。①0.1
3
mol·L-1的溶液稀释过程中,pH变化最小的其酸性最弱,即HCN溶液的pH变化最小,A项正
确。②根据“强酸制弱酸”原理可知A、B项正确。
(4)根据离子开始沉淀时pH可知,Cu2+最先沉淀;Fe2+、Mg2+沉淀时,溶液中OH-的浓度
分别为10-6.4 mol·L-1、10-3.6 mol·L-1,两种难溶物的离子配比相同,故Fe(OH) 的溶度积比
2
Mg(OH) 小。
2
答案:(1)c(Na+)>c(HSO)>c(H+)>c(SO)>c(OH-)
(2)B
(3)①A ②AB
(4)Cu2+ <