文档内容
专练 15 金属及其化合物的制备流程
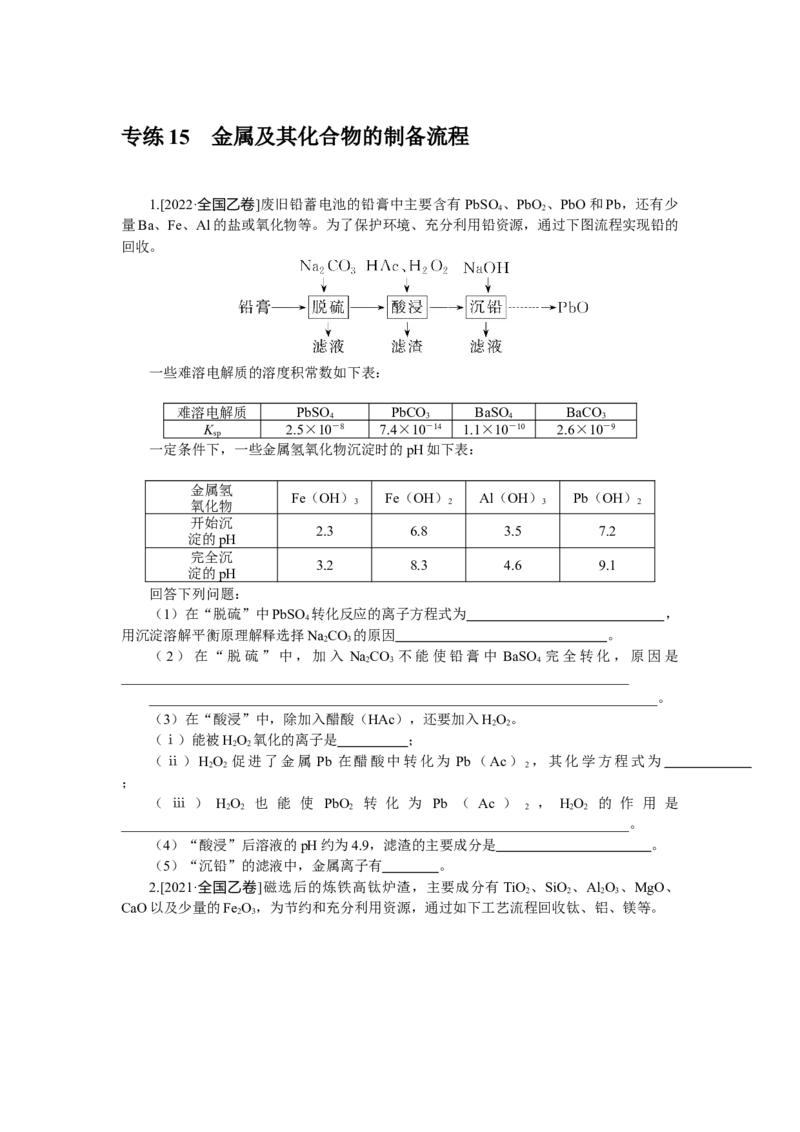
1.[2022·全国乙卷]废旧铅蓄电池的铅膏中主要含有 PbSO 、PbO 、PbO和Pb,还有少
4 2
量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的
回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢
Fe(OH) Fe(OH) Al(OH) Pb(OH)
氧化物 3 2 3 2
开始沉
2.3 6.8 3.5 7.2
淀的pH
完全沉
3.2 8.3 4.6 9.1
淀的pH
回答下列问题:
(1)在“脱硫”中PbSO 转化反应的离子方程式为 ,
4
用沉淀溶解平衡原理解释选择NaCO 的原因 。
2 3
(2)在“脱硫”中,加入 NaCO 不能使铅膏中 BaSO 完全转化,原因是
2 3 4
________________________________________________________________________
________________________________________________________________________。
(3)在“酸浸”中,除加入醋酸(HAc),还要加入HO。
2 2
(ⅰ)能被HO 氧化的离子是 ;
2 2
(ⅱ)HO 促进了金属 Pb 在醋酸中转化为 Pb(Ac) ,其化学方程式为
2 2 2
;
( ⅲ ) HO 也 能 使 PbO 转 化 为 Pb ( Ac ) , HO 的 作 用 是
2 2 2 2 2 2
________________________________________________________________________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是 。
(5)“沉铅”的滤液中,金属离子有 。
2.[2021·全国乙卷]磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、
2 2 2 3
CaO以及少量的Fe O,为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×
3.2 4.7 11.1 13.8
10-5 mol·L-1)的pH
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相
2 2 2 3 2 3
应 的 硫 酸 盐 。 写 出 Al O 转 化 为 NH Al ( SO ) 的 化 学 方 程 式
2 3 4 4 2
________________________________________________________________________。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至
11.6,依次析出的金属离子是
________________________________________________________________________。
(3)“母液①”中Mg2+浓度为 mol·L-1。
(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是 。“酸溶渣”的成分是
、 。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO·xHO沉淀,该反应
2 2
的离子方程式是
________________________________________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得 ,循环利用。
3.某研究性学习小组将一定浓度的NaCO 溶液滴入CuSO 溶液中得到蓝色沉淀。
2 3 4
甲同学认为沉淀可能是CuCO;
3
乙同学认为沉淀可能是Cu(OH);
2
丙同学认为沉淀可能是CuCO 和Cu(OH) 的混合物。[查阅资料知:CuCO 和Cu
3 2 3
(OH) 均不带结晶水,受热均易分解,各生成对应的两种氧化物]
2
Ⅰ. ( 1 ) 乙 同 学 的 观 点 , 你 认 为 其 原 理 是 ( 用 离 子 方 程 式 表 示 ) :
________________________________________________________________________。
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,检验沉淀是否洗
涤干净的方法是
________________________________________________________________________。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
(3)B装置中试剂的化学式是 ,C装置中试剂的名称是 。
(4)能证明乙同学观点正确的预期实验现象是________________________________________________________________________。
Ⅲ.若丙同学的观点正确,可利用下列装置通过实验测定其组成。
(5)实验装置的连接顺序为
________________________________________________________________________。
(6)装置C中碱石灰的作用是 ,实验开始和结束时都要通过量的空
气,请说明结束时通入过量空气的作用是
________________________________________________________________________。
(7)若沉淀样品的质量为m g,装置B质量增加了n g,则沉淀中CuCO 的质量分数
3
为 。
4.草酸亚铁晶体(FeC O·2H O)是一种浅黄色固体,难溶于水,受热易分解,是生产
2 4 2
锂电池的原材料,也常用作分析试剂及显影剂等,其制备流程如下:
(1)配制硫酸亚铁铵[(NH ) Fe(SO ) ]溶液时,需加少量硫酸,目的是
4 2 4 2
________________________________________________________________________。
(2)加热到沸腾时发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)向盛有草酸亚铁晶体的试管中滴入硫酸酸化的 KMnO 溶液,振荡,溶液变为棕
4
黄色,同时有气体生成。已知反应中MnO转化为无色的Mn2+,则该过程中被氧化的元素
是 ,若反应中消耗1 mol FeC O·2HO,则参加反应的n(KMnO )= 。
2 4 2 4
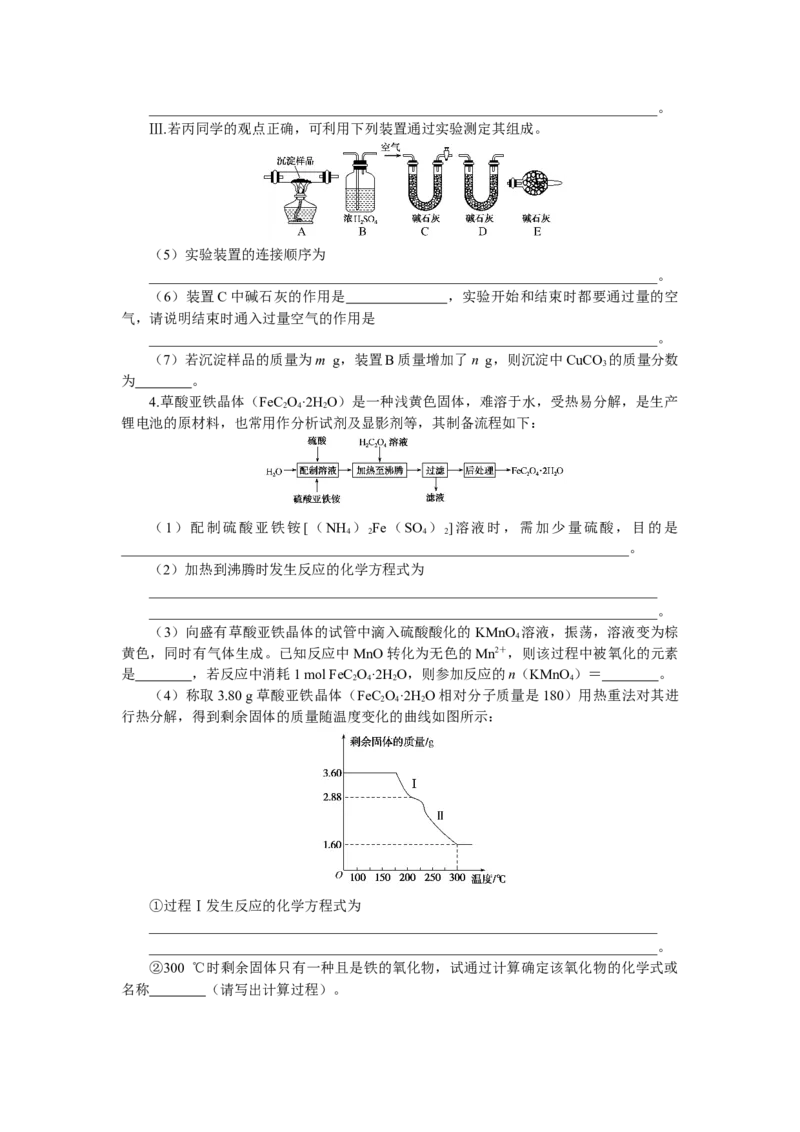
(4)称取3.80 g草酸亚铁晶体(FeC O·2H O相对分子质量是180)用热重法对其进
2 4 2
行热分解,得到剩余固体的质量随温度变化的曲线如图所示:
①过程Ⅰ发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
②300 ℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式或
名称 (请写出计算过程)。