文档内容
专练 53 实验综合应用二
1.[2022·全国乙卷]二草酸合铜(Ⅱ)酸钾{K [Cu(C O)]}可用于无机合成、功能材
2 2 4 2
料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的CuSO 溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,
4
沉淀转变成黑色,过滤。
Ⅱ.向草酸(HC O)溶液中加入适量KCO 固体,制得KHC O 和KC O 混合溶液。
2 2 4 2 3 2 4 2 2 4
Ⅲ.将Ⅱ的混合溶液加热至80~85 ℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸
钾晶体,进行表征和分析。
回答下列问题:
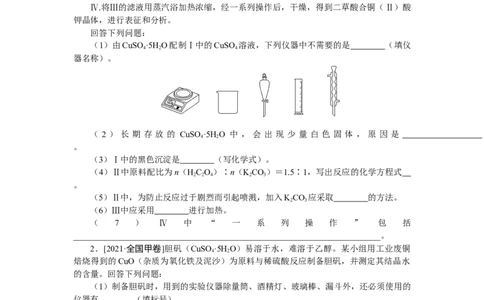
(1)由CuSO ·5H O配制Ⅰ中的CuSO 溶液,下列仪器中不需要的是 (填仪
4 2 4
器名称)。
( 2 ) 长 期 存 放 的 CuSO ·5H O 中 , 会 出 现 少 量 白 色 固 体 , 原 因 是
4 2
。
(3)Ⅰ中的黑色沉淀是 (写化学式)。
(4)Ⅱ中原料配比为n(HC O )∶n(KCO )=1.5∶1,写出反应的化学方程式
2 2 4 2 3
。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入KCO 应采取 的方法。
2 3
(6)Ⅲ中应采用 进行加热。
( 7 ) Ⅳ 中 “ 一 系 列 操 作 ” 包 括
________________________________________________________________________。
2.[2021·全国甲卷]胆矾(CuSO ·5H O)易溶于水,难溶于乙醇。某小组用工业废铜
4 2
焙烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水
的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的
仪器有 (填标号)。
A.烧杯 B.容量瓶
C.蒸发皿 D.移液管
(2)将 CuO 加入到适量的稀硫酸中,加热,其主要反应的化学方程式为
________________________________________________________________________,
与 直 接 用 废 铜 和 浓 硫 酸 反 应 相 比 , 该 方 法 的 优 点 是
________________________________________________________________________
________________________________________________________________________。
(3)待CuO完全反应后停止加热,边搅拌边加入适量 HO ,冷却后用NH ·H O调
2 2 3 2pH为3.5~4,再煮沸10 min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、
、乙醇洗涤、 ,得到胆矾。其中,控制溶液pH为3.5~4的目的是
, 煮 沸 10 min 的 作 用 是
________________________________________________________________________
________________________________________________________________________。
(4)结晶水测定:称量干燥坩埚的质量为 m ,加入胆矾后总质量为m ,将坩埚加热
1 2
至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
m 。 根 据 实 验 数 据 , 胆 矾 分 子 中 结 晶 水 的 个 数 为
3
________________________________________________________________________
________________________________________________________________________
(写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是 (填标号)。
①胆矾未充分干燥
②坩埚未置于干燥器中冷却
③加热时有少量胆矾迸溅出来
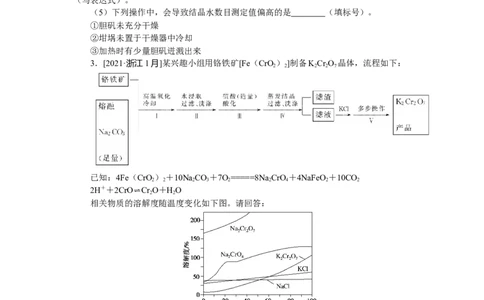
3.[2021·浙江1月]某兴趣小组用铬铁矿[Fe(CrO)]制备KCr O 晶体,流程如下:
2 2 2 2 7
已知:4Fe(CrO)+10NaCO+7O=====8NaCrO+4NaFeO +10CO
2 2 2 3 2 2 4 2 2
2H++2CrO⇌Cr
2
O+H
2
O
相关物质的溶解度随温度变化如下图。请回答:
(1)步骤Ⅰ,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是
________________________________________________________________________。
(2)下列说法正确的是 。
A.步骤Ⅱ,低温可提高浸取率
B.步骤Ⅱ,过滤可除去NaFeO 水解产生的Fe(OH)
2 3
C.步骤Ⅲ,酸化的目的主要是使NaCrO 转变为NaCr O
2 4 2 2 7
D.步骤Ⅳ,所得滤渣的主要成分是NaSO 和NaCO
2 4 2 3
(3)步骤Ⅴ,重结晶前,为了得到杂质较少的KCr O 粗产品,从下列选项中选出合
2 2 7理的操作(操作不能重复使用)并排序:溶解KCl→( )→( )→(
)→( )→重结晶。
a.50 ℃蒸发溶剂
b.100 ℃蒸发溶剂
c.抽滤
d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
f.蒸发至溶液中出现大量晶体,停止加热
(4)为了测定KCr O 产品的纯度,可采用氧化还原滴定法。
2 2 7
①下列关于滴定分析的操作,不正确的是 。
A.用量筒量取25.00 mL待测液转移至锥形瓶
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
②在接近终点时,使用“半滴操作”可提高测量的准确度。其方法是:将旋塞稍稍转
动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落, ,继续摇动锥形瓶,
观察颜色变化。(请在横线上补全操作)
(5)该小组用滴定法准确测得产品中KCr O 的质量分数为98.50%。某同学还用分光
2 2 7
光度法测定产品纯度(KCr O 溶液的吸光度与其浓度成正比例),但测得的质量分数明显
2 2 7
偏低。分析其原因,发现配制 KCr O 待测水溶液时少加了一种试剂。该试剂是
2 2 7
,添加该试剂的理由是 。