文档内容
第八篇 化学实验
专项 56 热重分析与计算
热重曲线题是实验和计算的有机融合,久考不衰。热重曲线是指在热分析过程中通过热天平而得到的试
样在加热过程中质量随温度变化的曲线。通过热重曲线的分析计算,可以了解样品在某一温度下的反应程
度及相应的物质含量等信息,是一种常用的热分析方法。热重曲线试题主要以下类型:
(1)从失重的方式来分,热重曲线类试题可分为两类:第一类试样发生分解反应,以脱水、分解等方式
失重,气氛物质不参加反应;第二类试样发生氧化、还原等反应,以氧化、还原等方式失重。当然也有试
题形式上是两者的结合,但本质上可以分步处理,故仍属于上述类型。
(2)从选试样是否已知,热重曲线类试题可分为两类:第一类以已知试样确定产物组成的目标思维法试
题;第二类以未知试样需要确定组成的逆向思维法试题。
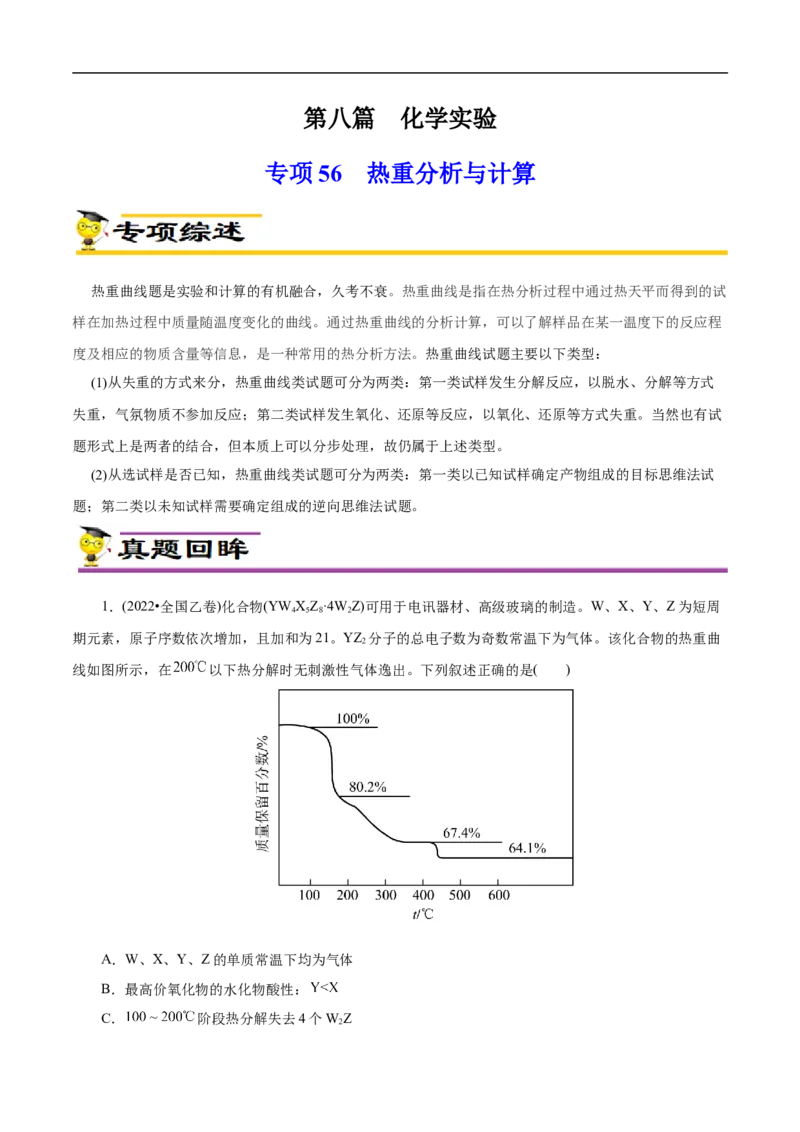
1.(2022•全国乙卷)化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
4 5 8 2
期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数常温下为气体。该化合物的热重曲
2
线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是( )
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个WZ
2D. 热分解后生成固体化合物XY
2 3
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原
4 5 8 2
子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,
则说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序
2
数依次增加,且加和为21,则X为B。A项,X(B)的单质常温下为固体,故A错误;B项,根据非金属性
越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<Y(HNO ),故B错
3 3 3
误;C项,根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段
热分解失去4个HO,则质量分数 ,则说明不是失去去4个
2
HO,故C错误;D项,化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元
2 4 5 8 2 2 3 2 3
素守恒,则得到关系式2NH B O·4H O~5B O,则固体化合物B O 质量分数为
4 5 8 2 2 3 2 3
,说明假设正确,故D正确。故选D。
2.(2022•全国甲卷)胆矾(CuSO ·5H O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的CuO (杂
4 2
质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有_______(填
标号)。
A.烧杯 B.容量瓶 C.蒸发皿 D.移液管
(2)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为_______,与直接用废铜和浓硫
酸反应相比,该方法的优点是_______。
(3)待CuO完全反应后停止加热,边搅拌边加入适量HO,冷却后用NH ·H O调pH为3.5~4,再煮沸
2 2 3 2
10min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、_______、乙醇洗涤、_______,得到
胆矾。其中,控制溶液pH为3.5~4的目的是_______,煮沸10min的作用是_______。
(4)结晶水测定:称量干燥坩埚的质量为m,加入胆矾后总质量为m,将坩埚加热至胆矾全部变为白
1 2
色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m。根据实验数据,胆矾分子中结
3
晶水的个数为_______(写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是_______(填标号)。
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少胆矾迸溅出来【答案】(1)A、C
(2)CuO+HSO CuSO +H O 不会产生二氧化硫且产生等量胆矾消耗硫酸少(硫酸利用率高)
2 4 4 2
(3)过滤 干燥 除尽铁,抑制硫酸铜水解 破坏氢氧化铁胶体,易于过滤
(4) (5)①③
【解析】(1)制备胆矾时,根据题干信息可知,需进行溶解、过滤、结晶操作,用到的实验仪器除量筒、
酒精灯、玻璃棒、漏斗外,还必须使用的仪器有烧杯和蒸发皿,A、C符合题意;(2)将CuO加入到适量的
稀硫酸中,加热,其主要反应的化学方程式为CuO+HSO CuSO +H O;直接用废铜和浓硫酸反应生成硫
2 4 4 2
酸铜与二氧化硫和水,与这种方法相比,将CuO加入到适量的稀硫酸中,加热制备胆矾的实验方案具有的
优点是:不会产生二氧化硫且产生等量胆矾消耗硫酸少(硫酸利用率高);(3) 硫酸铜溶液制硫酸铜晶体,操
作步骤有加热蒸发、冷却结晶、过滤、乙醇洗涤、干燥;CuO中含氧化铁杂质,溶于硫酸后会形成铁离子,
为使铁元素以氢氧化铁形成沉淀完全,需控制溶液pH为3.5~4,酸性环境同时还可抑制铜离子发生水解;
操作过程中可能会生成氢氧化铁胶体,所以煮沸10min,目的是破坏氢氧化铁胶体,使其沉淀,易于过滤;
(4) 称量干燥坩埚的质量为m,加入胆矾后总质量为m,将坩埚加热至胆矾全部变为白色,置于干燥器中
1 2
冷至室温后称量,重复上述操作,最终总质量恒定为m。则水的质量是(m -m)g,所以胆矾
3 2 3
(CuSO •nH O)中n值的表达式为 =n:1,解得n= ;(5) ①胆矾未充分干
4 2
燥,捯饬所测m 偏大,根据n= 可知,最终会导致结晶水数目定值偏高,符合题意;②坩埚
2
未置于干燥器中冷却,部分白色硫酸铜会与空气中水蒸气结合重新生成胆矾,导致所测m 偏大,根据n=
3
可知,最终会导致结晶水数目定值偏低,不符合题意;③加热胆矾晶体时有晶体从坩埚中溅
出,会使m 数值偏小,根据n= 可知,最终会导致结晶水数目定值偏高,符合题意;故①③
3
符合题意。
3.(2019•全国I卷)硫酸铁铵[NH Fe(SO )·xH O]是一种重要铁盐。为充分利用资源,变废为宝,在实验
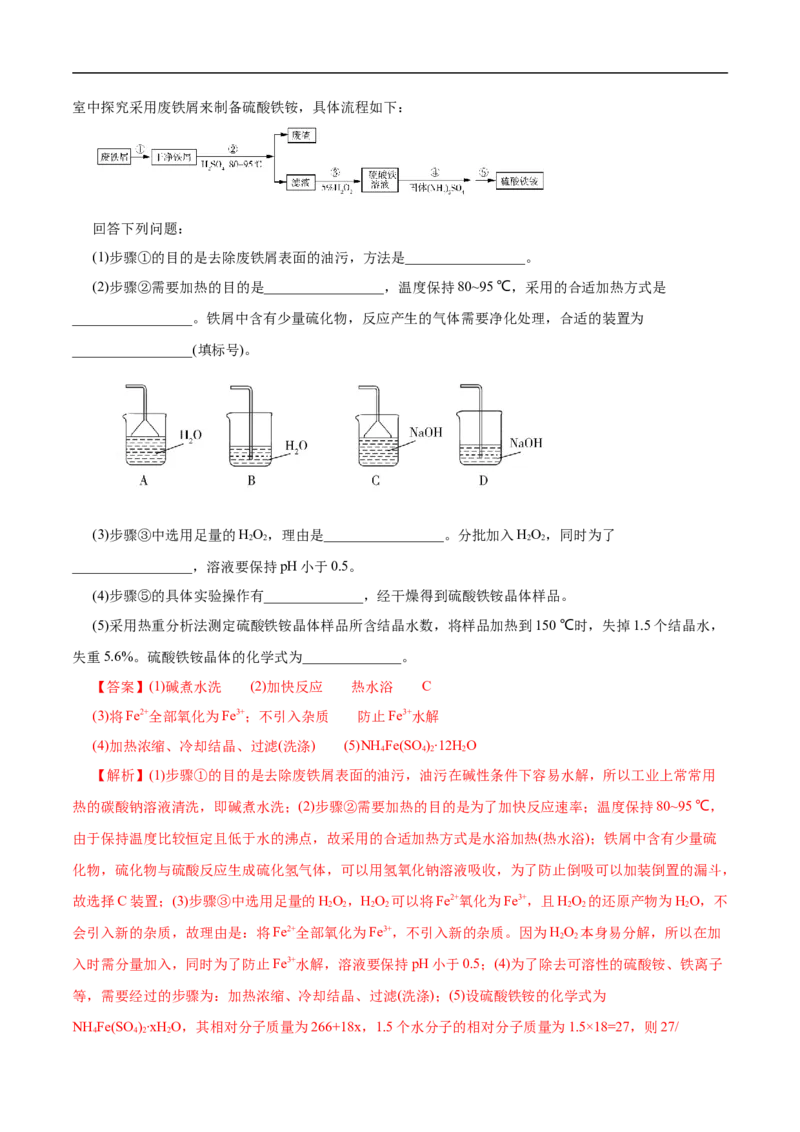
4 4 2 2室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________。
(2)步骤②需要加热的目的是_________________,温度保持80~95 ℃,采用的合适加热方式是
_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为
_________________(填标号)。
(3)步骤③中选用足量的HO,理由是_________________。分批加入HO,同时为了
2 2 2 2
_________________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,
失重5.6%。硫酸铁铵晶体的化学式为______________。
【答案】(1)碱煮水洗 (2)加快反应 热水浴 C
(3)将Fe2+全部氧化为Fe3+;不引入杂质 防止Fe3+水解
(4)加热浓缩、冷却结晶、过滤(洗涤) (5)NH Fe(SO )∙12HO
4 4 2 2
【解析】(1)步骤①的目的是去除废铁屑表面的油污,油污在碱性条件下容易水解,所以工业上常常用
热的碳酸钠溶液清洗,即碱煮水洗;(2)步骤②需要加热的目的是为了加快反应速率;温度保持80~95 ℃,
由于保持温度比较恒定且低于水的沸点,故采用的合适加热方式是水浴加热(热水浴);铁屑中含有少量硫
化物,硫化物与硫酸反应生成硫化氢气体,可以用氢氧化钠溶液吸收,为了防止倒吸可以加装倒置的漏斗,
故选择C装置;(3)步骤③中选用足量的HO,HO 可以将Fe2+氧化为Fe3+,且HO 的还原产物为HO,不
2 2 2 2 2 2 2
会引入新的杂质,故理由是:将Fe2+全部氧化为Fe3+,不引入新的杂质。因为HO 本身易分解,所以在加
2 2
入时需分量加入,同时为了防止Fe3+水解,溶液要保持pH小于0.5;(4)为了除去可溶性的硫酸铵、铁离子
等,需要经过的步骤为:加热浓缩、冷却结晶、过滤(洗涤);(5)设硫酸铁铵的化学式为
NH Fe(SO )∙xHO,其相对分子质量为266+18x,1.5个水分子的相对分子质量为1.5×18=27,则27/
4 4 2 2(266+18x)=5.6%,解得x=12,则硫酸铁铵的化学式为NH Fe(SO )∙12HO。
4 4 2 2
1.结晶水合盐受热分解步骤
加热结晶水合盐反应可分三步进行:第一步是脱去部分水,第二步是生成羟基盐或含水盐,第三步是生
成金属氧化物;如果热重实验的气氛为空气,则加热过程中可能被氧化,反应将变得更复杂一些。
2.热重曲线图的分析方法
(1)识图。识图的关键是三看:一看轴即横、纵坐标所表示的化学含义(自变量X轴和函数Y轴表示的意
义),寻找X、Y轴之间的关系,因为这是理解题意和进行正确思维的前提;二看点即曲线中的特殊点(顶
点、始点、终点、拐点、交叉点);三看线即曲线的走势(变化趋势是上升、下降、波动、正态、偏态等变
化)。
(2)析图。分析图中为什么会出现这些特殊点,曲线为什么有这样的变化趋势和走向,分析曲线变化的
因果关系;通过联想,把课本内的有关化学概念、原理、规律等与图中的曲线和相关点建立联系。
(3)用图。将相关的化学知识与图中曲线紧密结合,在头脑中构建新的曲线——知识体系,然后运用新
的曲线——知识体系揭示问题的实质,解决实际问题。
3.解题的方法思路
根据失重的质量与反应物的质量关系判断反应过程失去的元素及化合物,利用完全失去水的反应计算特
殊点。
(1)设晶体为1 mol,其质量为m。
(2)失重一般是先失水,再失非金属氧化物。
(3)计算每步固体剩余的质量(m ): ×100%=固体残留率。
余
(4)晶体中金属质量不再减少,仍在残留固体(m )中。
余
(5)失重最后一般为金属氧化物,由质量守恒得得m(O),由n(金属)∶n(O),即可求出失重后物质的化学
式。
(6)根据失重后物质的化学式,写出相应的化学方程式。
1.(2022·河南省焦作市第一中学模拟预测)研究表明NH VO 固体(固体的组成用VO·a NH ·b HO表
4 3 2 5 3 2
示)热分解得到VO 的过程可分为四步,每一步产生NH 和HO(g)的物质的量之比依次为2∶1、x∶y、
2 5 3 2
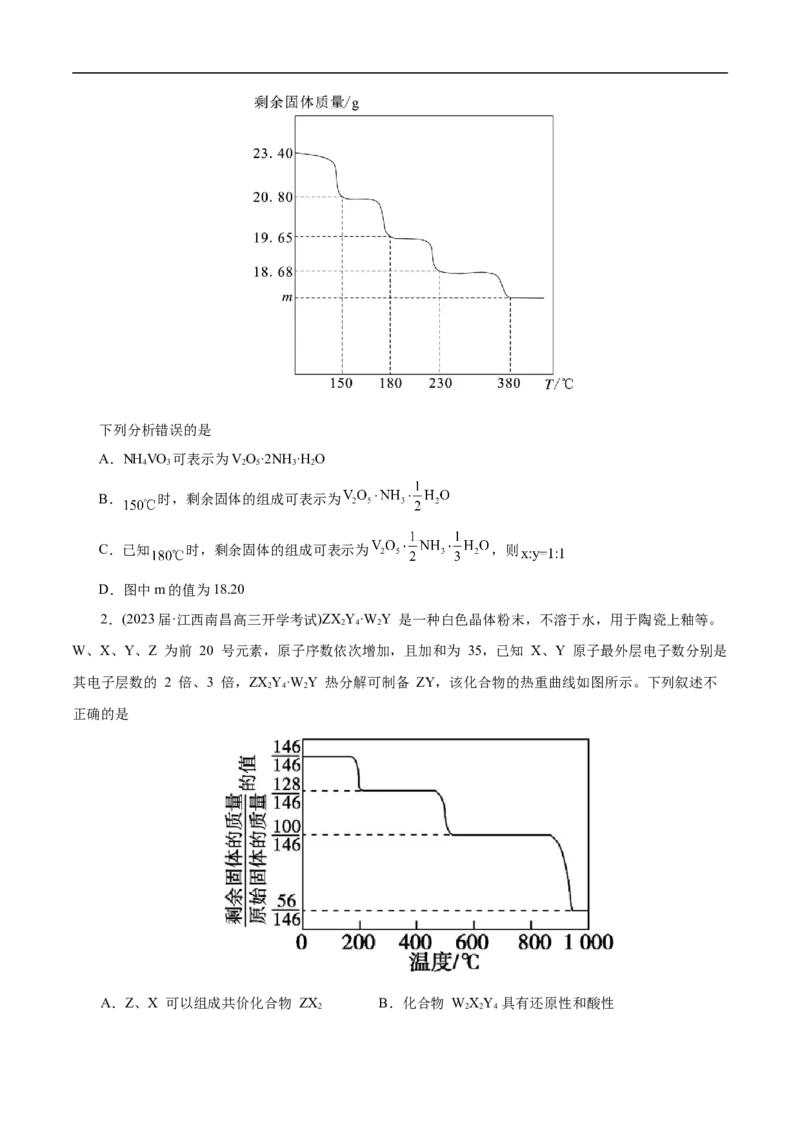
3∶2、3∶2。某实验小组取23.4gNH VO 固体进行热重分析,剩余固体的质量与温度的关系如图所示:
4 3下列分析错误的是
A.NH VO 可表示为VO·2NH ·H O
4 3 2 5 3 2
B. 时,剩余固体的组成可表示为
C.已知 时,剩余固体的组成可表示为 ,则
D.图中m的值为18.20
2.(2023届·江西南昌高三开学考试)ZXY·W Y 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。
2 4 2
W、X、Y、Z 为前 20 号元素,原子序数依次增加,且加和为 35,已知 X、Y 原子最外层电子数分别是
其电子层数的 2 倍、3 倍,ZXY·W Y 热分解可制备 ZY,该化合物的热重曲线如图所示。下列叙述不
2 4 2
正确的是
A.Z、X 可以组成共价化合物 ZX B.化合物 WXY 具有还原性和酸性
2 2 2 4C.150~200℃阶段热分解失去 WY D.400~600℃热分解后生成固体化合物 ZXY
2 3
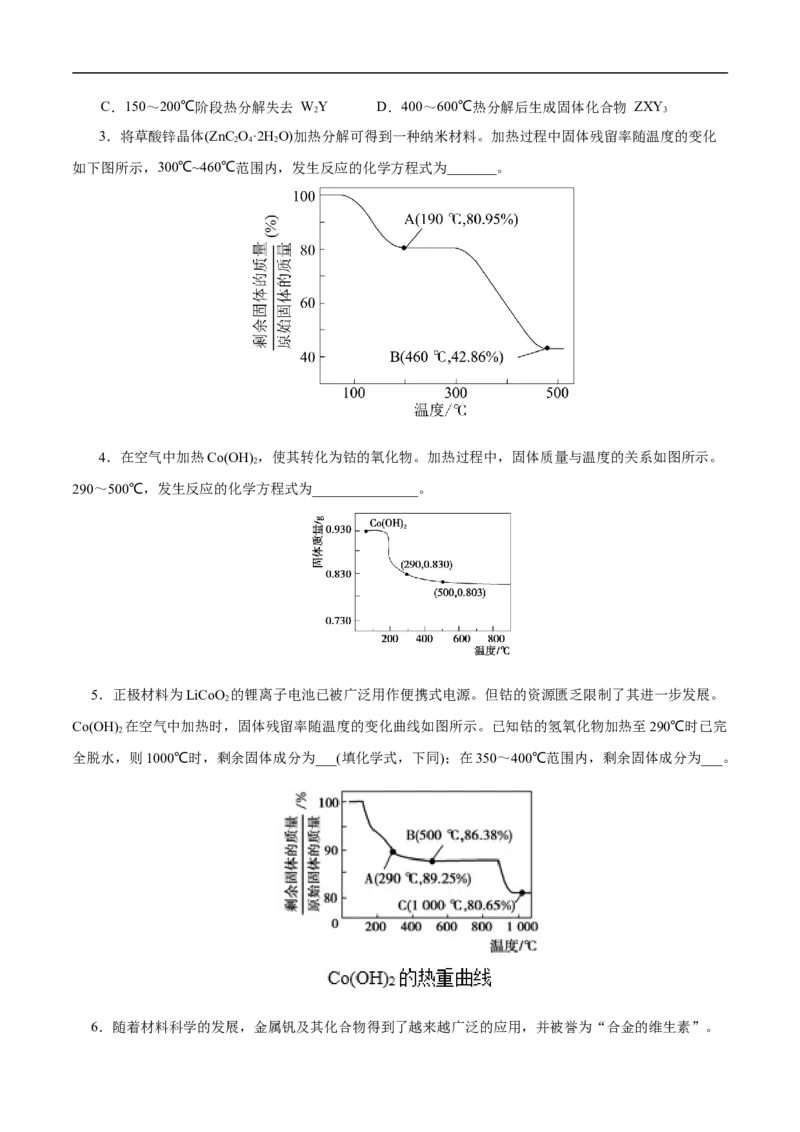
3.将草酸锌晶体(ZnC O·2H O)加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化
2 4 2
如下图所示,300℃~460℃范围内,发生反应的化学方程式为_______。
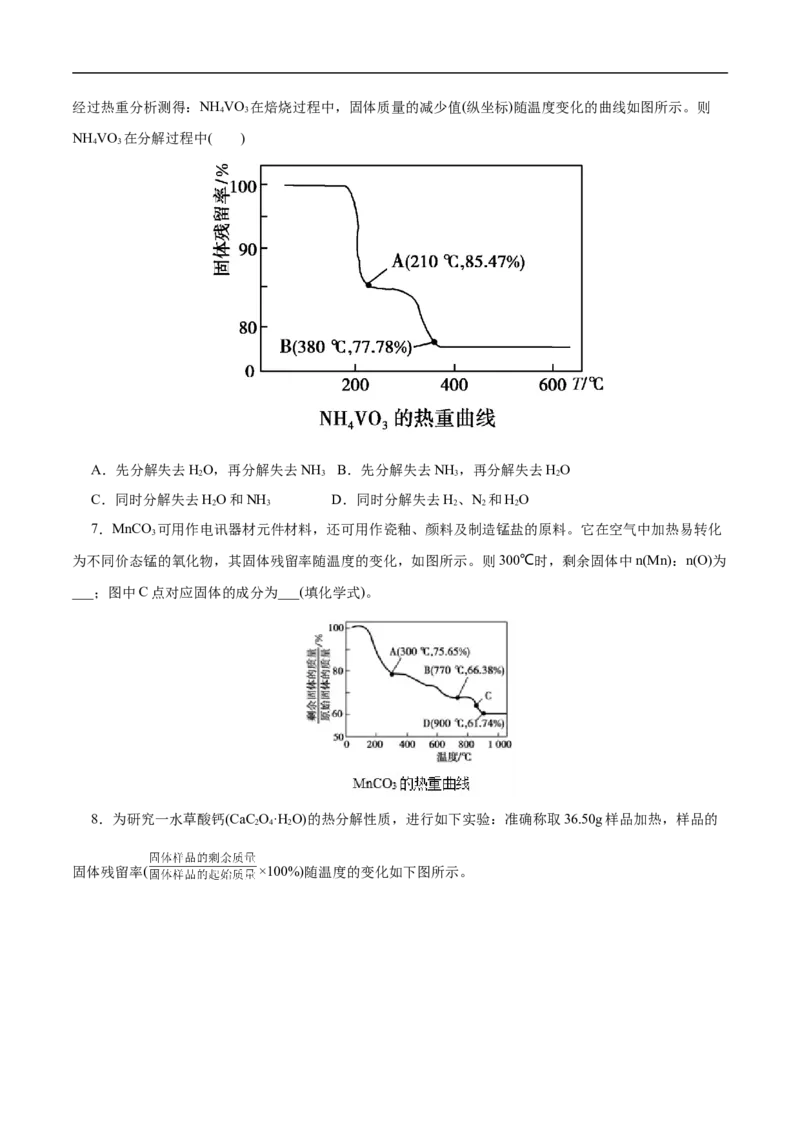
4.在空气中加热Co(OH) ,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。
2
290~500℃,发生反应的化学方程式为_______________。
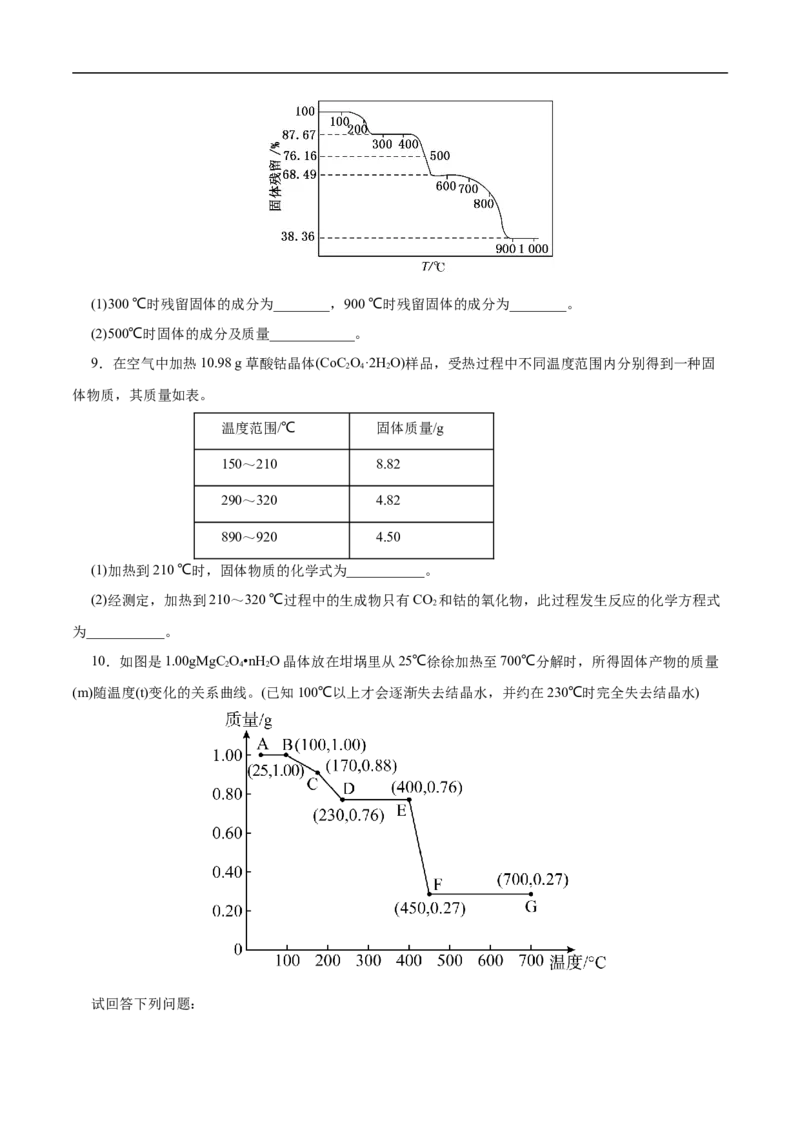
5.正极材料为LiCoO 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
2
Co(OH) 在空气中加热时,固体残留率随温度的变化曲线如图所示。已知钴的氢氧化物加热至290℃时已完
2
全脱水,则1000℃时,剩余固体成分为___(填化学式,下同);在350~400℃范围内,剩余固体成分为___。
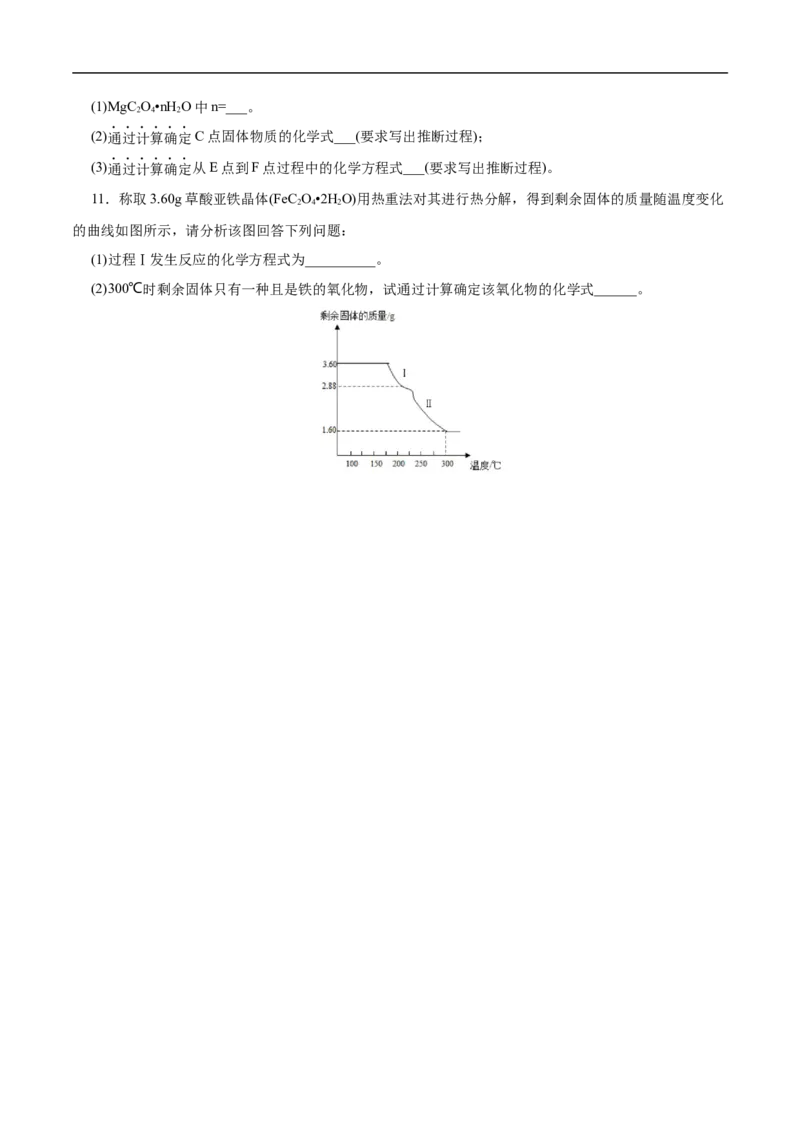
6.随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”。经过热重分析测得:NH VO 在焙烧过程中,固体质量的减少值(纵坐标)随温度变化的曲线如图所示。则
4 3
NH VO 在分解过程中( )
4 3
A.先分解失去HO,再分解失去NH B.先分解失去NH ,再分解失去HO
2 3 3 2
C.同时分解失去HO和NH D.同时分解失去H、N 和HO
2 3 2 2 2
7.MnCO 可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化
3
为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。则300℃时,剩余固体中n(Mn):n(O)为
___;图中C点对应固体的成分为___(填化学式)。
8.为研究一水草酸钙(CaC O·H O)的热分解性质,进行如下实验:准确称取36.50g样品加热,样品的
2 4 2
固体残留率( ×100%)随温度的变化如下图所示。(1)300 ℃时残留固体的成分为________,900 ℃时残留固体的成分为________。
(2)500℃时固体的成分及质量____________。
9.在空气中加热10.98 g草酸钴晶体(CoC O·2H O)样品,受热过程中不同温度范围内分别得到一种固
2 4 2
体物质,其质量如表。
温度范围/℃ 固体质量/g
150~210 8.82
290~320 4.82
890~920 4.50
(1)加热到210 ℃时,固体物质的化学式为___________。
(2)经测定,加热到210~320 ℃过程中的生成物只有CO 和钴的氧化物,此过程发生反应的化学方程式
2
为___________。
10.如图是1.00gMgC O•nH O晶体放在坩埚里从25℃徐徐加热至700℃分解时,所得固体产物的质量
2 4 2
(m)随温度(t)变化的关系曲线。(已知100℃以上才会逐渐失去结晶水,并约在230℃时完全失去结晶水)
试回答下列问题:(1)MgC O•nH O中n=___。
2 4 2
(2)通过计算确定C点固体物质的化学式___(要求写出推断过程);
(3)通过计算确定从E点到F点过程中的化学方程式___(要求写出推断过程)。
11.称取3.60g草酸亚铁晶体(FeC O•2H O)用热重法对其进行热分解,得到剩余固体的质量随温度变化
2 4 2
的曲线如图所示,请分析该图回答下列问题:
(1)过程Ⅰ发生反应的化学方程式为__________。
(2)300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式______。