文档内容
专项训练 晶胞中原子空间利用率的计算(解析版)
一、单选题
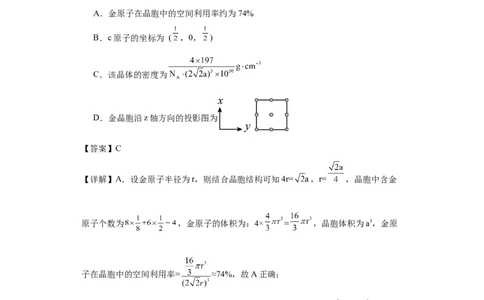
1.金的晶胞结构如图所示(假设晶胞参数为anm),下列说法错误的是
A.金原子在晶胞中的空间利用率约为74%
B.c原子的坐标为 ( ,0, )
C.该晶体的密度为
D.金晶胞沿z轴方向的投影图为
【答案】C
【详解】A.设金原子半径为r,则结合晶胞结构可知4r= ,r= ,晶胞中含金
原子个数为 ,金原子的体积为:4× = ,晶胞体积为a3,金原
子在晶胞中的空间利用率= ≈74%,故A正确;
B.a为坐标原点,c处于面心,结合晶胞结构可知c原子的坐标为 ( ,0, ),故B
正确;
C.晶胞质量为: ,晶胞体积为: nm3,则晶胞密度为
,C项错误;
资料收集整理【淘宝店铺:向阳百分百】D.金晶胞沿z轴方向投影,顶点原子均投影在正方形顶点,面心分别投影在棱心和面
心,投影图正确,故D正确;
故选:C。
2.钠元素和硒元素可组成一种对蛋白质的合成和糖代谢有保护作用的无机化合物,其
晶胞结构如图所示。已知 和 的半径分别为anm和bnm,晶胞参数为cnm。下
列有关说法错误的是
A.该晶体的化学式为
B.与 距离最近且相等的 数目为8
C.该晶胞的空间利用率为
D. 位于由 构成的四面体空隙中, 位于由 构成的六面体空隙中
【答案】B
【详解】A.由题图可知,该晶胞中 位于顶点和面心,共有 个,
位于晶胞体内,共有8个,则该晶体的化学式为 ,A正确;
B.由题图可知,与 距离最近且相等的 共有12个,B错误;
C.该晶胞的空间利用率为 ,
C正确;
D.由题给晶胞结构可知, 位于由 构成的四面体空隙中, 位于由 构成
的六面体空隙中,D正确;
故选B。
3.已知 晶体晶胞边长为a cm。将 掺杂到该晶胞中,可得到一种高性能
资料收集整理【淘宝店铺:向阳百分百】的p型太阳能电池材料,其结构单元如图所示。假定掺杂后的晶胞参数不发生变化,
下列说法正确的是
A.Li和Mg间最短距离是 cm
B.该物质的化学式为
C.若M点坐标为 ,则Li的坐标为
D.若O原子的半径为b cm,则O原子的空间利用率为
【答案】D
【详解】A.由图可知,Li原子和Mg原子间的最短距离为晶胞面对角线的一半,即
cm,A错误;
B.根据均摊法,1个晶胞中Li原子的个数为 ,Mg原子的个数为
,Ni原子的个数为 ,O原子的个数为4,因此该
物质的化学式为 ,B错误;
C.若M点坐标为 ,则Li的坐标为 ,C错误;
D.O原子的体积为 cm ,晶胞体积为 cm ,则O原子的空间利用率为
资料收集整理【淘宝店铺:向阳百分百】,D正确;
故答案选D。
4.空间利用率是指构成晶体的原子、离子或分子在整个晶体中所占有的体积百分比。
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是
A.①为简单立方堆积,③为面心立方最密堆积
B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C.晶胞中原子的配位数分别为:①6,②8,③8,④12
D.空间利用率的大小关系为:
【答案】B
【详解】A.由金属晶体的晶胞结构图,可知①为简单立方堆积、②为体心立方堆积、
③为六方最密堆积、④为面心立方最密堆积,A项错误;
B.顶点为8个晶胞共用、面为2个晶胞共用、晶胞体内原子为1个晶胞单独占有,晶
胞①中原子个数=8 =1;晶胞②中原子个数=1+8 =2;晶胞③中原子个数=1+8
=2;④中原子个数=8 +6 =4,B项正确;
C.①为简单立方堆积,配位数为6,②为体心立方堆积,配位数为8,③为六方最密
堆积,④为面心立方最密堆积,二者配位数均为12,C项错误;
D.六方最密堆积与面心立方最密堆积的空间利用率相等,简单立方堆积、体心立方
堆积不是最密堆积,空间利用率比六方最密堆积、面心立方最密堆积的小,体心立方
堆积空间利用率比简单立方堆积的高,故空间利用率的大小关系①<②<③=④,D项错
误。
答案选B。
5.亚铁氰化钾属于欧盟批准使用的食品添加剂,受热易分解: 3K[Fe(CN) ]
4 6
12KCN+Fe C+2(CN) ↑+N ↑+C,下列关于该反应说法错误的是
3 2 2
资料收集整理【淘宝店铺:向阳百分百】A.金刚石中碳原子在晶胞中的空间利用率
B.配合物K[Fe(CN) ]中配位原子是碳原子
4 6
C.(CN) 是一种与Cl 性质相似的气体,分子中每个原子都达到了8电子稳定结构,
2 2
其分子中σ键和π键数目比为 3:4
D.已知 Fe C 晶胞中每个碳原子被 6 个铁原子包围,则铁的配位数是 2
3
【答案】A
【详解】A.设晶胞的边长为a、碳原子半径为r,金刚石晶胞体对角线等于8r,则
,原子的空间利用率 ,A选项错误;
B.配合物K[Fe(CN) ]中配体为CN-,由于电负性N>C,所以C原子提供孤对电子,
4 6
即配位原子是碳原子,B选项正确;
C.(CN) 分子的结构式为N≡C—C≡N,从结构式中可以发现分子中每个原子都达到了
2
8电子稳定结构,单键为σ键,三键含有1个σ键和2个π键,因此(CN) 分子中σ键和
2
π键数目比为3:4,C选项正确;
D.Fe C的晶胞结构中碳原子的配位数为6,与碳原子紧邻的铁原子,以C原子为原点
3
建立三维坐标系,Fe原子位于坐标轴上且关于原点(碳原子)对称,6个Fe形成的空间
结构为正八面体,故C原子的配位数为6,配位数之比等于相应原子数目反比,则Fe
原子配位数为6×13=2,D选项正确;
故选A。
6.铜的晶胞结构如图所示,下列关于其晶胞的说法中错误的是
A.若晶胞的边长为a,则最近的两个铜原子的距离为
B.每个晶胞中含有4个铜原子
C.铜原子的配位数为12
D.晶胞的空间利用率为
【答案】A
资料收集整理【淘宝店铺:向阳百分百】【详解】A.晶胞边长为a,则面对角线长度为 a,铜晶胞为面心立方堆积,最近的
两个铜原子间的距离是面对角线的二分之一,即 a,故A错误;
B.在晶胞的顶点和面心各有1个铜原子,顶点上的铜原子被8个晶胞共有,面心上的
铜原子被2个晶胞共有,所以每个晶胞中含有4个铜原子,故B正确;
C.铜晶胞为面心立方最密堆积,铜原子的配位数为12,故C正确;
D.晶胞的空间利用率等于晶胞中铜原子的体积除以晶胞的体积,晶胞中有4个铜原子,
设铜原子半径为r,则铜原子的体积为 ,铜原子半径为两个铜原子间距离的一
半,则铜原子半径和晶胞边长的关系为r= a,则铜原子体积为 ,晶
胞体积为a3,所以晶胞的空间利用率= ×100%= ×100%,故D正
确;
故选A。
7.已知空间利用率是指构成晶体的原子、离子或分子在整个晶体空间中所占有的体积
百分比。下列有关说法不正确的是
A.铜碘杂化团簇分子结构如图1所示,分子间通过范德华力聚集在一起
B. 晶体的晶胞如图2所示,标记为X的 的分子坐标为
C.H原子的电子云如图3所示,H原子核外大多数电子在原子核附近运动
D.金属Cu为面心立方晶胞(如图4所示),其空间利用率约为74%
【答案】C
资料收集整理【淘宝店铺:向阳百分百】【详解】A.范德华力是分子之间普遍存在的一种相互作用力,它的本质是正负电荷
间的相互吸引,它使得许多物质能以一定的凝聚态存在,则铜碘杂化团簇分子是分子
间通过范德华力聚集在一起,A项正确;
B.根据 晶体的晶胞图示可知,标记为X的 的分子坐标为 ,B项正确;
C.H原子为单电子体系,核外只有1个电子,电子云图中的黑点不是指大多数电子在
原子核附近运动,C项错误;
D.面心立方最密堆积,空间利用率为 ,D项正确;
答案选C。
8.金刚石和C 都是由碳元素组成的重要单质,金刚石和C 分子及它们的晶胞如图所
60 60
示(已知 ≈1.732、π≈3.14):
下列说法正确的是
A.每个金刚石晶胞中含有4个碳原子
B.每个C 分子含有90个σ键
60
C.金刚石和C 晶胞中微粒间的作用力均只有共价键
60
D.每个金刚石晶胞原子的空间利用率为74.05%
【答案】B
【详解】A.根据均摊原则,每个金刚石晶胞中碳原子数为 ,故A错
误;
B.C 分子中每个C原子形成3个σ键,每个C 分子含有σ键数 ,故B正
60 60
确;
C.金刚石晶胞中微粒间的作用力均只有共价键,C 晶胞中微粒间的作用力有共价键、
60
分子间作用力,故C错误;
资料收集整理【淘宝店铺:向阳百分百】D.设晶胞的边长为a、碳原子半径为r,金刚石晶胞体对角线等于8r,则 ,原
子的空间利用率 ,故D错误;
选B。
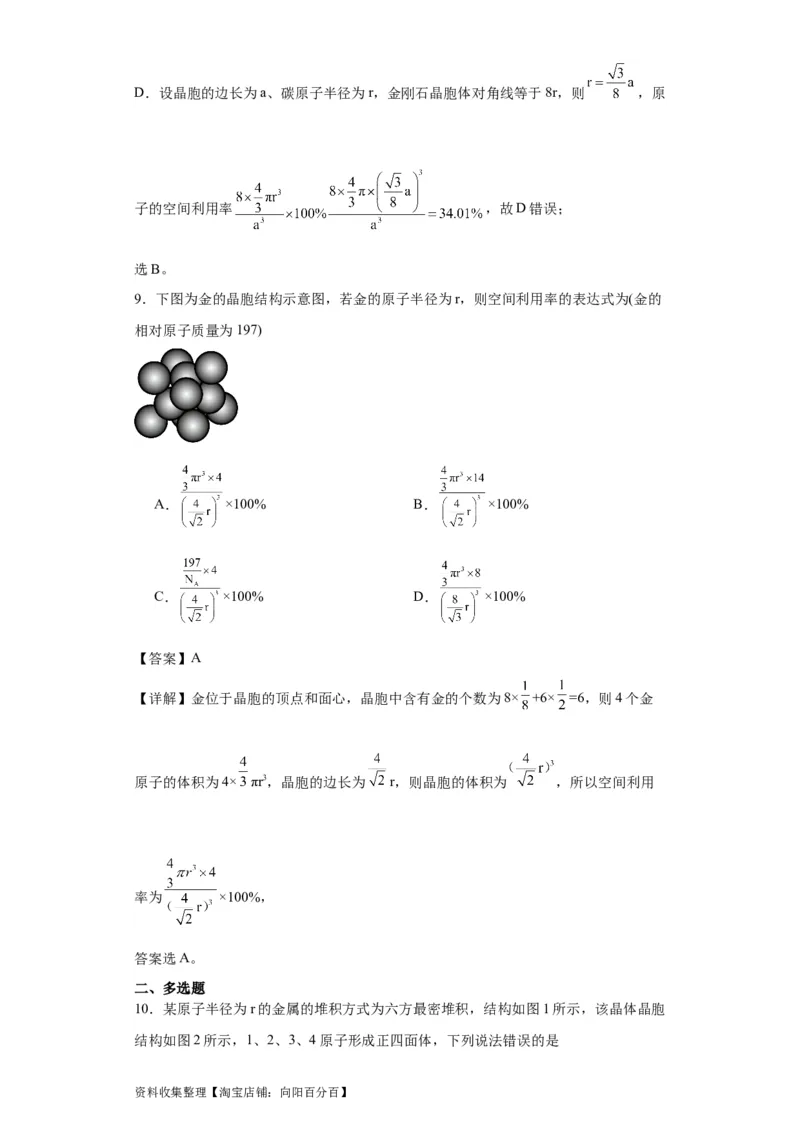
9.下图为金的晶胞结构示意图,若金的原子半径为r,则空间利用率的表达式为(金的
相对原子质量为197)
A. ×100% B. ×100%
C. ×100% D. ×100%
【答案】A
【详解】金位于晶胞的顶点和面心,晶胞中含有金的个数为8× +6× =6,则4个金
原子的体积为4× πr3,晶胞的边长为 r,则晶胞的体积为 ,所以空间利用
率为 ×100%,
答案选A。
二、多选题
10.某原子半径为r的金属的堆积方式为六方最密堆积,结构如图1所示,该晶体晶胞
结构如图2所示,1、2、3、4原子形成正四面体,下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.该晶胞中含有的金属原子数目为2 B.该晶胞的高为
C.图1结构中含4个晶胞 D.该晶胞的空间利用率为
【答案】BC
【详解】A.根据均摊原则,该晶胞中含有的金属原子数目为 ,选项
A正确;
B.原子半径为r,则底面边长为2r,则1、2、3、4原子形成正四面体的高为 ,
晶胞的高为正四面体的高的2倍,则晶胞的高为 ,选项B错误;
C.图1结构可分割为3个图2所示的3个晶胞,选项C错误;
D.该晶胞中含有2个原子,2个原子的体积为 ,晶胞的体积为
,空间利用率为 = ,选项
D正确;
答案选BC。
11.金属铁有δ、γ、α三种结构,各晶胞如图。下列说法不正确的是
A.三种晶胞中实际含有的铁原子的个数之比为2:4:1
B.三种晶胞中铁原子的配位数之比为1:3:2
C.三种晶胞密度之比为32: 37 :29
资料收集整理【淘宝店铺:向阳百分百】D.δ-Fe晶胞的空间利用率为
【答案】BC
【详解】A. 三种晶胞中实际含有的铁原子的个数之比为(8× +1):(8× +6× ):(8×
)=2:4:1,故A正确;
B. δ-Fe为体心立方堆积,以体心Fe研究可知Fe原子配位数为8,γ-Fe为面心立方堆
积,Fe原子配位数为12,α-Fe为简单立方堆积,可知Fe原子配位数为6,故δ-Fe、γ-
Fe、α-Fe两种晶胞中铁原子的配位数之比为8:12:6=4:6:3,故B错误;
C.设铁原子半径为a,根据晶胞结构图,γ-Fe晶体中晶胞的棱长为 ,δ-Fe晶体中
晶胞的棱长为 ,α-Fe晶体中晶胞的棱长为2a,所以三种晶胞的棱长之比为:2
:3 :3,原子数之比2:4:1,密度之比: = ,故
C错误;
D. δ-Fe晶胞的空间利用率为= = ,故D正确;
故选BC。
三、填空题
12.古画墨迹千年不褪色是因为常温下石墨稳定,金刚石与石墨是碳的同素异形体。
若碳原子半径为rnm,根据硬球接触模型,金刚石晶胞如图2所示,碳原子的空间利
用率为 (用含π的代数式表示);金刚石的密度为 g/cm3(用含r和N 的计算式
A
表示即可)。
资料收集整理【淘宝店铺:向阳百分百】【答案】
π×100%
【详解】
1个金刚石的晶胞中有8个碳原子,碳原子的总体积为 ,设晶胞的边长为
anm,两个碳原子最近距离是半径的2倍即2rnm,占体对角线的 ,体对角线为8r,
有 a=8r,a= nm,晶胞的体积为V=( 3nm3,碳原子的空间利用率为
= π×100%,金刚石的密度等于质量除以体积,该晶胞中有8个碳原子,
质量为 g,晶胞的体积为 = ,最终密度是
g/cm3
。
13.下图为元素周期表的部分,元素①~⑥在表中的位置如图所示。
用化学用语回答下列问题:
单质⑤的晶胞结构如图所示,平均一个晶胞中含有 个⑤原子,若⑤原子的
原子半径为r,则该晶体的空间利用率为 。(用含r的代数式表示,不必化
资料收集整理【淘宝店铺:向阳百分百】简)
【答案】
2
【详解】根据均摊原则,平均一个晶胞中含有 个Cr原子,若Cr原子的原子
半径为r,晶胞的体对角线为4r,晶胞的边长为 ,晶胞的体积为, ,则
该晶体的空间利用率为 。
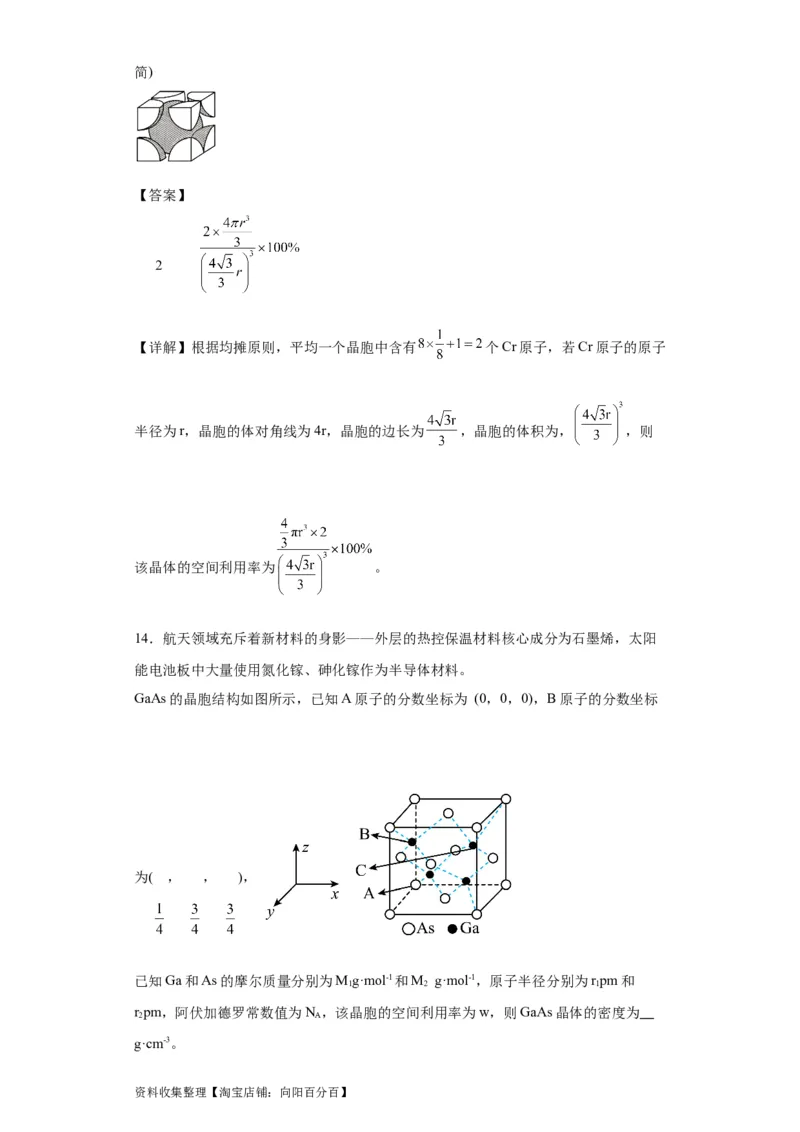
14.航天领域充斥着新材料的身影——外层的热控保温材料核心成分为石墨烯,太阳
能电池板中大量使用氮化镓、砷化镓作为半导体材料。
GaAs的晶胞结构如图所示,已知A原子的分数坐标为 (0,0,0),B原子的分数坐标
为( , , ),
已知Ga和As的摩尔质量分别为Mg·mol-1和M g·mol-1,原子半径分别为rpm和
1 2 1
rpm,阿伏加德罗常数值为N ,该晶胞的空间利用率为w,则GaAs晶体的密度为
2 A
g·cm-3。
资料收集整理【淘宝店铺:向阳百分百】【答案】
【详解】根据晶胞的结构, 原子在顶点处和面心,个数为: , 在
体心,个数为4,所以密度为: 。
15.我国科学家最近开发了 催化剂实现 制 ,为资源回收利
用提供新思路。钛晶体有两种结构,如图1和图2所示。
图1立方体结构中原子的空间利用率为 (用含 的代数式表示);图2结构
钛晶体中的原子堆积方式称为 。
【答案】
×100% 六方最密堆积
【详解】
由晶胞结构可知,图1中晶胞为体心立方堆积,处于体对角线上的钛原子紧密相切,
体对角线为钛原子的原子半径的4倍,设晶胞边长为a,则晶胞体积为a3、硼原子的原
子半径为 ,晶胞中位于顶点和体心的钛原子数目为8× +1=2,所以晶胞空间利用
率为 ×100%= ×100%;图2结构钛晶体中的原子堆积方式为六方最
资料收集整理【淘宝店铺:向阳百分百】密堆积,故答案为: ×100%;六方最密堆积。
16.铁单质的堆积方式有两种,其剖面图分别如图a、 所示。
其中属于面心立方最密堆积的是 (填“ ”或“ ”),此晶体的空间利用
率为 用含圆周率 的代数式表示
【答案】
b
【详解】
a属于体心立方,b为面心面心立方最密堆积,此晶体铁原子数为 4,晶
胞参数等于 ,则空间利用率为 ;故答案为:b; 。
17. 年 月 日神舟 号载人飞行任务取得圆满成功,高性能金属材料铝合金、
钛合金、镁合金、超强度钢等作用功不可没。
是金红石的主要成分,其晶胞结构如图所示,设 和 原子半径分别为 和
(单位: ),晶胞的长宽高分别为 、 、 (单位: ),则晶胞中原子的空间利用
率为 (列出计算表达式)。(空间利用率指构成晶体的原子、离子或分子在整
个晶体空间中所占有的体积百分比)
【答案】
资料收集整理【淘宝店铺:向阳百分百】【详解】晶胞中,黑色球数目为1+8× =2,白色球数目为2+4× =4,结合化学式
TiO 可知,黑色球为Ti、白色球为O,分子中原子总体积为4× π(r ×10-10cm)3+2×
2 O
π(r ×10-10cm)3,晶胞体积为abc cm3,晶胞中原子的空间利用率=
Ti
×100= ×100%,故
答案为: ×100%。
18.由于锂离子电池成本的日益上涨以及锂资源的不断消耗,钾离子电池成为近几年
的研究热点。锑钾(Sb-K)合金的晶胞结构如图a,图b表示晶胞的一部分。
①设1号原子的分数坐标为(0,0,0),2号原子的分数坐标为(1,1,1),则3号原子
的分数坐标为 。
②与Sb最邻近的K原子数为 ,若K原子的半径为a pm,Sb原子的半径为
b pm,则该晶体中原子的空间利用率为 (用含a、b的计算表达式表示)。
【答案】
① ( ) ② 8
【详解】①由图可知,3号原子的分数坐标为( );
②以位于顶点的Sb原子为例,与Sb最邻近的K原子位于晶胞内部(图b中位于体心
资料收集整理【淘宝店铺:向阳百分百】的K原子),共有8个; ,晶胞中含有
个K和 个Sb,因此原子体积为 ,
晶胞边长 ,则晶胞体积为 ,因此该晶体中原子的空
间利用率为 。
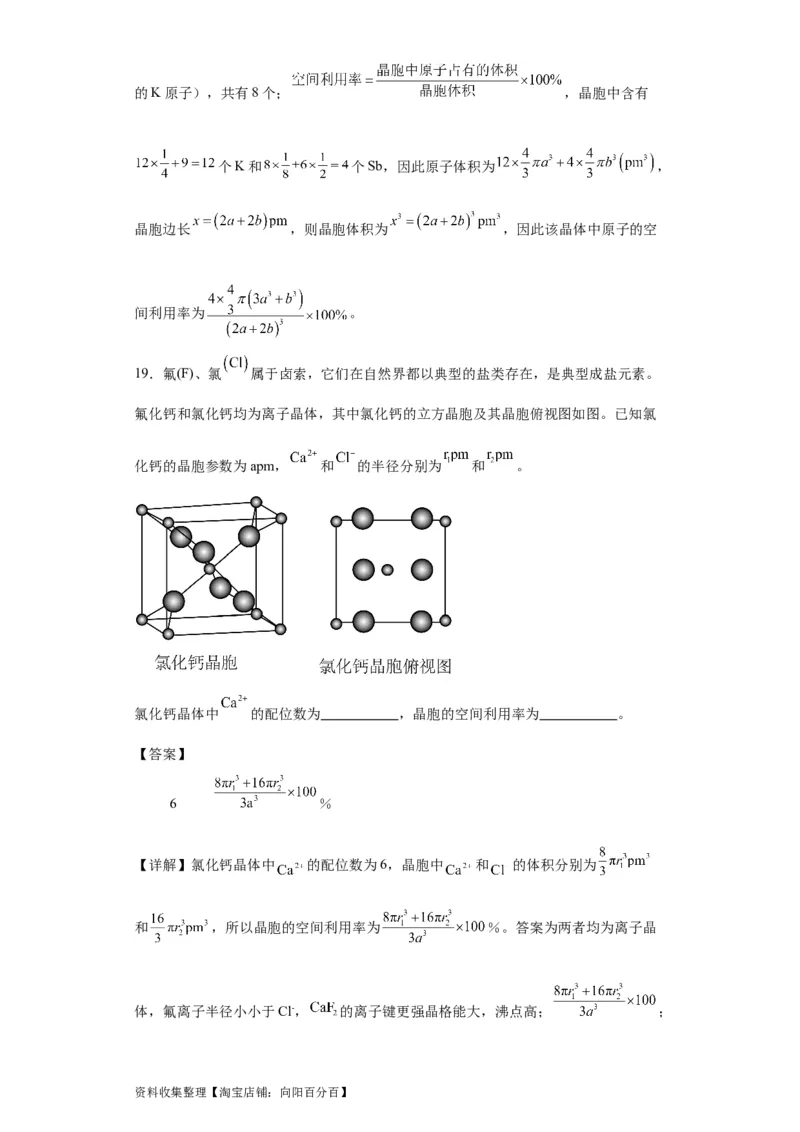
19.氟(F)、氯 属于卤索,它们在自然界都以典型的盐类存在,是典型成盐元素。
氟化钙和氯化钙均为离子晶体,其中氯化钙的立方晶胞及其晶胞俯视图如图。已知氯
化钙的晶胞参数为apm, 和 的半径分别为 和 。
氯化钙晶体中 的配位数为 ,晶胞的空间利用率为 。
【答案】
6 %
【详解】氯化钙晶体中 的配位数为6,晶胞中 和 的体积分别为
和 ,所以晶胞的空间利用率为 %。答案为两者均为离子晶
体,氟离子半径小小于Cl-, 的离子键更强晶格能大,沸点高; ;
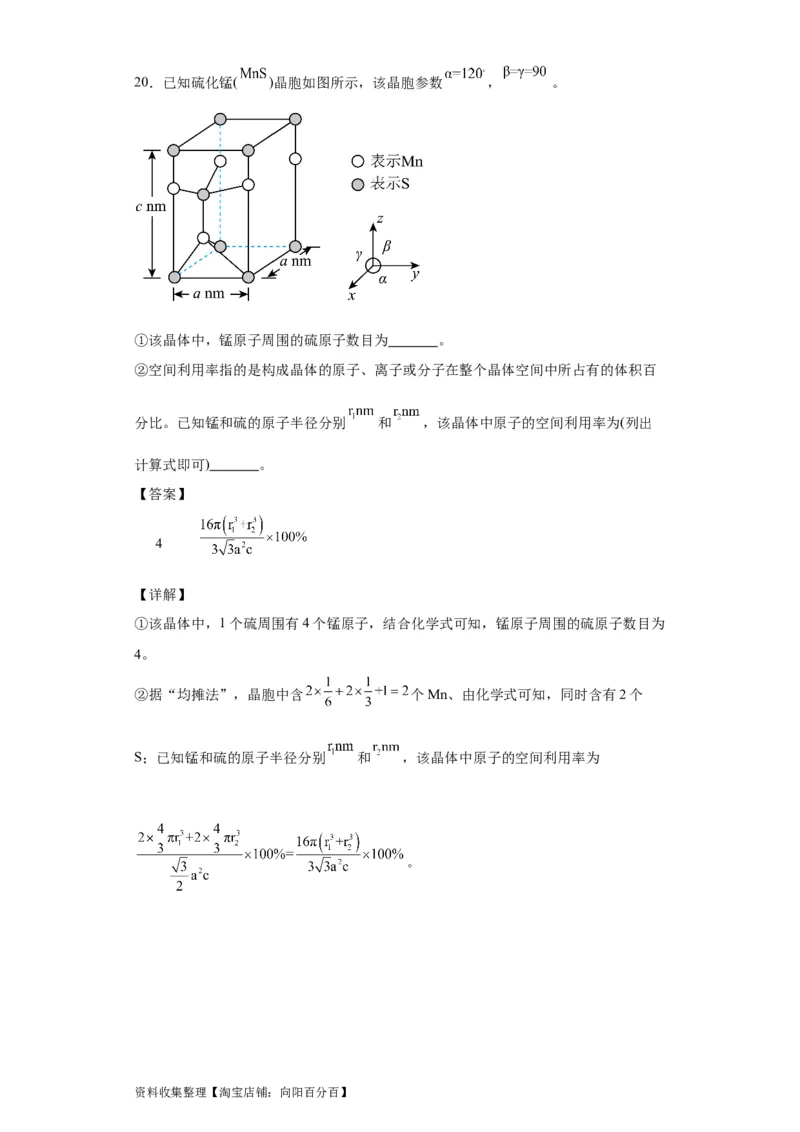
资料收集整理【淘宝店铺:向阳百分百】20.已知硫化锰( )晶胞如图所示,该晶胞参数 , 。
①该晶体中,锰原子周围的硫原子数目为 。
②空间利用率指的是构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百
分比。已知锰和硫的原子半径分别 和 ,该晶体中原子的空间利用率为(列出
计算式即可) 。
【答案】
4
【详解】
①该晶体中,1个硫周围有4个锰原子,结合化学式可知,锰原子周围的硫原子数目为
4。
②据“均摊法”,晶胞中含 个Mn、由化学式可知,同时含有2个
S;已知锰和硫的原子半径分别 和 ,该晶体中原子的空间利用率为
。
资料收集整理【淘宝店铺:向阳百分百】