文档内容
专题 02 化学计量及其应用
目录
01 模拟基础练
【题型一】不含有题干描述考查N
A
【题型二】含有题干描述考查N
A
【题型三】配制一定物质的量浓度溶液操作
【题型四】配制一定物质的量浓度的溶液的误差分析
02 重难创新练
03 真题实战练
题型一 不含有题干描述考查N
A
1.设N 为阿伏加德罗常数的值,下列说法中正确的是( )
A
A.标准状况下,22.4L正丙醇(C HO)分子中含有 的数目为8 N
3 8 A
B.24g质量分数为25%的甲醛水溶液中含有氢原子数目为2.4 N
A
C.pH=1的HSO 溶液与足量的Zn反应产生的氢气分子数目为0.05 N
2 4 A
D.0.1mol FeI 与0.1molCl 反应时,转移电子的数目为0.3 N
2 2 A
2.[真题改编] (2022·浙江省1月选考,12改编)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
3.[真题改编] (2022•海南省选择性考试,7改编)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。
N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
4.下列有关阿伏伽德罗常数(N )的叙述中正确的是( )
AA.18g液态水中含有氢键的数目为2 N
A
B.10g质量分数为46%的乙醇溶液中含有O-H键的数目为0.1 N
A
C.常温下2.7g Al加至足量的浓硝酸中,转移的电子数为0.3 N
A
D.25℃时,1L pH=2的CHCOOH溶液中, 的数目为0.01 N
3 A
5.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.电解精炼铜时,阳极质量减少 ,电路中转移电子数可能是2 N
A
B.1molCaC 晶体和1molCaH 晶体含有的离子数目均为2 N
2 2 A
C.1molHOOCCH COOH与足量乙醇在一定条件下反应,生成的酯基的数目为2 N
2 A
D. 水解能力弱于NH +,1 L1mol·L-1的NH F溶液中HF和NH +的总数大于N
4 4 4 A
题型二 含有题干描述考查N
A
6.[新考法]新制氢氧化铜和葡萄糖的反应可用来检验血糖,其反应为:
CHOH(CHOH) CHO+2Cu(OH) +NaOH CHOH(CHOH) COONa+Cu O↓+3HO,设N 为阿伏加德罗常数
2 4 2 2 4 2 2 A
的值,下列说法正确的是( )
A.18gCHOH(CHOH) CHO中含有羟基的数目为0.6 N
2 4 A
B.每消耗1mol Cu(OH) ,转移电子的数目为2 N
2 A
C.1L1mol·L-1CHOH(CHOH) COONa溶液中含有的离子数目为2 N
2 4 A
D.标准状况下,112mLH O(l)中含有的分子数目约为6.2 N
2 A
7.[新考法](2024·湖南省长沙市高三一模)磷烷(PH )是集成电路、太阳能电池等电子工业生产的原材料。
3
工业上制备PH 的反应原理为:P(s)+3NaOH(aq) +3H O(l)=PH(g)+3NaH PO (aq)。N 表示阿伏加德罗常数
3 4 2 3 2 2 A
的值,下列说法正确的是( )
A.常温下pH=13的NaOH溶液中水电离出的c(OH-)=0.1mol/L
B.3.1g白磷(P )中共价键的数目为N
4 A
C.每转移3个电子,生成 磷烷
D.0.1 mol/L的NaH PO 溶液中HPO -的数目小于0.1N
2 2 2 2 A
8.[新考法] (2024·辽宁省部分重点中学协作体高三模拟)三氟化氮(NF )在潮湿的环境中能发生反应:
3
3NF +5H O=2NO+HNO +9HF,N 代表阿伏加德罗常数的值。下列说法正确的是( )
3 2 3 A
A.生成22.4LNO,转移电子数为N
A
B.1molH O含有的中子数为10N
2 AC.1mol/L的HNO 溶液含NO -离子数为N
3 3 A
D.反应中若有1molNF 被氧化,则理论上需要分子数为2N 的氧化剂
3 A
9.[新考法] (2024·广东省佛山市二模)设N 为阿伏加德罗常数的值。制备莫尔盐
A
[(NH )Fe(SO )·6H O]用到Fe、HSO 、HO、(NH )SO 等物质,下列说法正确的是( )
4 2 4 2 2 2 4 2 4 2 4
A.1L pH=1的HSO 溶液中阳离子总数为0.1 N
2 4 A
B.标准状况下,2.24L H O所含共价键数为0.2 N
2 A
C.0.1mol/L (NH)SO 溶液中,NH +的数目为0.2 N
4 2 4 4 A
D.5.6g Fe与足量的浓硫酸反应制备FeSO ,转移的电子数为0.2 N
4 A
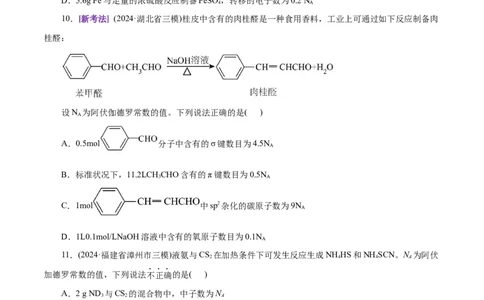
10.[新考法] (2024·湖北省三模)桂皮中含有的肉桂醛是一种食用香料,工业上可通过如下反应制备肉
桂醛:
设N 为阿伏伽德罗常数的值。下列说法正确的是( )
A
A.0.5mol 分子中含有的σ键数目为4.5N
A
B.标准状况下,11.2LCHCHO含有的π键数目为0.5N
3 A
C.1mol 中sp2杂化的碳原子数为9N
A
D.1L0.1mol/LNaOH溶液中含有的氧原子数目为0.1N
A
11.(2024·福建省漳州市三模)液氨与CS 在加热条件下可发生反应生成NH HS和NH SCN。N 为阿伏
2 4 4 A
加德罗常数的值,下列说法不正确的是( )
A.2 g ND 与CS 的混合物中,中子数为N
3 2 A
B.工业合成氨中每生成1 mol NH ,转移的电子数为3N
3 A
C.1 L0.1 mol/LNH HS溶液中,氢原子数为0.5N
4 A
D.1 mol NH SCN晶体中,σ键数目为6N
4 A
12.[新考法] (2024·青海省二模)联合制碱法利用食盐水、氨气和二氧化碳制纯碱,涉及的反应之一为
H+HO+CO+NaCl===NaHCO↓+NH Cl。设N 为阿伏加德罗常数的值。下列说法正确的是( )
3 2 2 3 4 A
A.常温常压下,11.2LCO 含氧原子的数目为N
2 A
B.0.1molNaHCO 中含离子数目为0.2N
3 AC.0.1mol·L-1 NaHCO 溶液中含 数目为0.1N
3 A
D.标准状况下,11.2LNH 通入水中,溶液中NH +数目为0.5N
3 4 A
13.(2024·广东省模拟预测)工业上监测SO 含量是否达到排放标准的化学反应原理是SO +HO+
2 2 2 2
BaCl =BaSO ↓+2HCl,用N 表示阿伏伽德罗常数的值,下列说法正确的是( )
2 4 A
A.25℃时, 的HCl溶液中含有 的数目为0.1N
A
B.生成2.33 g BaSO 沉淀时,吸收SO 的体积为0.224L
4 2
C.HO 晶体和HO晶体混合物共1 mol,则极性键数目为2N
2 2 2 A
D.此反应中,每消耗1 mol H O,转移的电子数为1N
2 2 A
14.[新题型] (2024·福建省福州市一模)25℃时,K (FePO )= 1.0×10-15。磷酸铁锂废料浸出的化学方程
sp 4
式为10LiFePO +12HCl+2NaClO=10FePO +10LiCl+Cl↑+2NaCl+6H O。N 是阿伏加德罗常数的值。下列有关
4 3 4 2 2 A
说法正确的是( )
A.18g冰晶体中含有氢键数目为4N
A
B.106.5 gNaClO 晶体中含有的σ键数目为4N
3 A
C.检测出反应液中c(PO 3-)为10-5 mol·L-1,则含有的Fe3+数目为10-10N
3 A
D.生成2.24L Cl (已折算为标准状况),转移电子数目为N
2 A
15.[新题型] (2024•河南省濮阳市第三次联考)工业上常用纯碱溶液吸收尾气中的NO、NO ,反应如
2
下:
反应1:NO+NO +Na CO=2NaNO +CO
2 2 3 2 2
反应2:2NO +Na CO=NaNO +NaNO +CO
2 2 3 2 3 2
已知:CO 与水的反应类似SO 和HO的反应。若N 代表阿伏加德罗常数的值。下列叙述正确的是(
2 2 2 A
)
A.反应1中放出2.24LCO 时,NO、NO 参与反应的总分子数为0.2N
2 2 A
B.1L0.5mol·L-1NaCO 溶液恰好完全反应时,作氧化剂的分子数为0.5N
2 3 A
C.将反应2中9.2gNO 完全反应产生的CO 通入足量水中生成的HCO 分子数为0.1N
2 2 2 3 A
D.上述制备的化工品(NaNO 、NaNO )中含N元素的质量为28g,则所含的Na+数一定为N
2 3 A
题型三 配制一定物质的量浓度溶液操作
16.配制400 mL 0.100 mol·L-1的KCl溶液,下列说法正确的是( )① ② ③ ④
A.上述实验操作步骤的正确顺序为:④①②③
B.容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
C.实验中需用的仪器有:天平、250 mL容量瓶、烧杯、玻璃棒、胶头滴管等
D.定容时,仰视容量瓶的刻度线,使配得的KCl溶液浓度偏低
17.配制0.1000 mol/L H SO 溶液250 mL,下列有关说法错误的是( )
2 4
A.在配制过程中玻璃棒的作用是搅拌和引流
B.用到的仪器有250 mL容量瓶、托盘天平、量筒、烧杯、玻璃棒和胶头滴管
C.浓硫酸稀释后,立即转移到容量瓶进行后续操作,所配溶液浓度偏高
D.定容时,液面位于容量瓶刻度线下1~2cm时,应改用胶头滴管滴加水
18.下列说法正确的是( )
A.现需480 mL 0.1 mol·L-1硫酸铜溶液,则需要称量7.68 g硫酸铜固体
B.100 g硫酸溶液的物质的量浓度为18.4 mol·L-1,用水稀释到物质的量浓度为9.2 mol·L-1,需要水
100 g
C.将10 g CuSO 溶解在90 g水中,配制质量分数为10%的CuSO 溶液
4 4
D.使用量筒量取一定体积的浓硫酸配制一定物质的量浓度的稀硫酸,将浓硫酸转移至烧杯后须用蒸
馏水洗涤量筒,并将洗涤液一并转移至烧杯
题型四 配制一定物质的量浓度的溶液的误差分析
19.配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已吸潮 B.容量瓶未干燥
C.烧杯内有少量NaOH溶液残留 D.定容时俯视液面
20.下列配制的溶液浓度偏高的是( )
A.配制盐酸用量筒量取浓盐酸时俯视刻度线
B.配制盐酸定容时,仰视容量瓶刻度线
C.称量10.6gNa CO 配制1.000mol·L-1NaCO 溶液100mL时,砝码错放左盘
2 3 2 3D.配制HSO 溶液,用浓HSO 稀释后未经冷却即注入容量瓶并定容
2 4 2 4
21.配制一定物质的量浓度溶液时,会导致所配溶液浓度偏大的操作是( )
A.在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中
B.定容摇匀后,发现液面低于刻度线,又加水到刻度
C.定容时俯视刻度线
D.用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理
22.下列对实验操作分析错误的是( )
A.配制0.1 mol·L-1 NaCl溶液时,若没有洗涤烧杯和玻璃棒,则所得溶液物质的量浓度偏低
B.NH NO 溶解吸热,若配制0.5 mol·L-1NH NO 溶液时直接将溶解后的溶液转移到容量瓶中,则所
4 3 4 3
得溶液的物质的量浓度偏高
C.配制一定物质的量浓度溶液时,若所用砝码已经生锈,则所得溶液的物质的量浓度偏高
D.配制一定物质的量浓度溶液时,若定容中不小心加水超过刻度线,立刻将超出的水吸出,则所得
溶液的物质的量浓度偏低
23.(2022·浙江省五校高三联考)N 代表阿伏伽德罗常数,下列叙述正确的是( )
A
A.1mol棱晶烷 中含有9N 个共价键
A
B.32gCu与过量I 充分反应,转移电子数为0.5N
2 A
C.标准状况下,22.4L乙烯与氧气的混合气体充分燃烧后,混合气体分子总数仍为N
A
D.密闭容器中,2molNO与1molO 充分反应,产物的分子数为2N
2 A
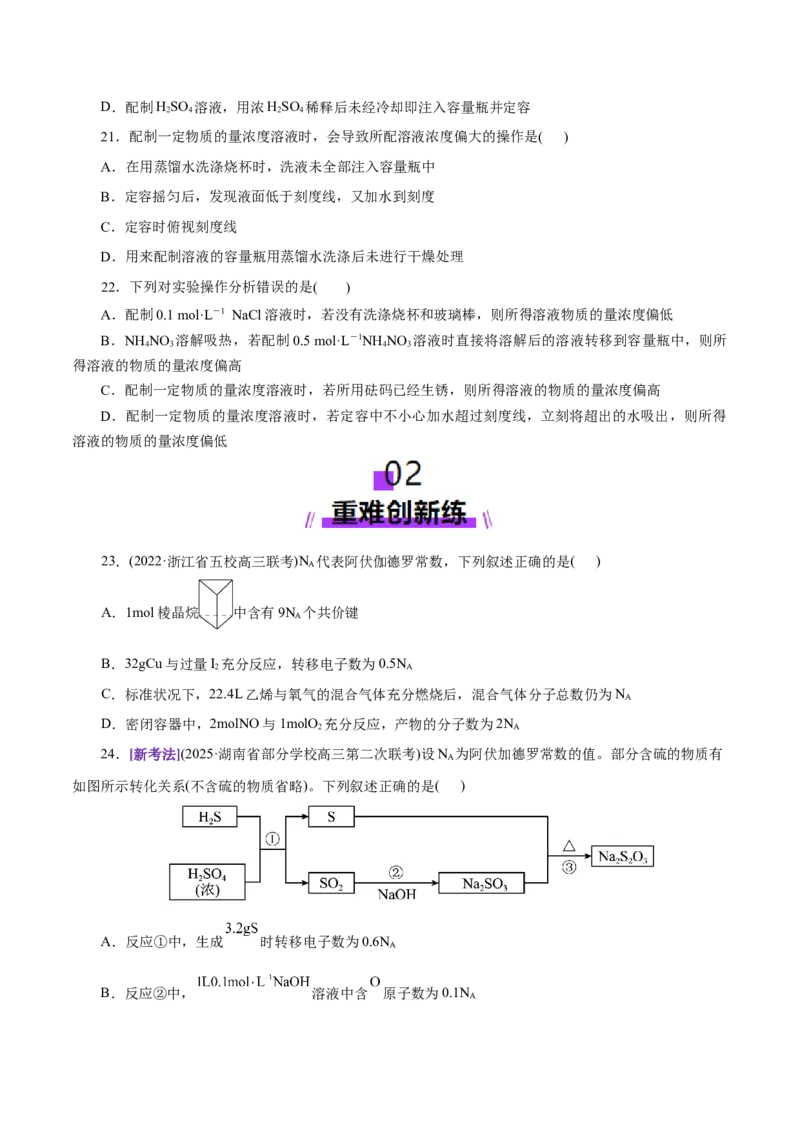
24.[新考法](2025·湖南省部分学校高三第二次联考)设N 为阿伏加德罗常数的值。部分含硫的物质有
A
如图所示转化关系(不含硫的物质省略)。下列叙述正确的是( )
A.反应①中,生成 时转移电子数为0.6N
A
B.反应②中, 溶液中含 原子数为0.1N
AC.反应②中,1L0.1mol·L-1NaSO 溶液中含阴离子数小于0.1N
2 3 A
D.反应③中,生成1molNa SO 时消耗 单质的数目为N
2 2 3 A
25.(2025·山西省晋中市平遥二中高三质检)“84”消毒液常用于杀菌、消毒。漂白等。欲用NaClO固体
准确配制480mL含NaClO25%、密度为1.19 g·cm-3的消毒液,下列说法正确的是( )
A.定容时俯视刻度线导致所配溶液浓度偏低
B.应称取142.8gNaClO固体配制该溶液
C.该“84”消毒液中NaClO的物质的量浓度约为4.0mol/L
D.所配制的 消毒液在空气中光照久置后,溶液的漂白性不变
26.工业上常用“碳氯法”制备MgCl ,原理为MgO+C+Cl MgCl +CO。N 代表阿伏加德罗常数的
2 2 2 A
值,下列叙述错误的是( )
A.反应中断裂1molCl—Cl键,转移的电子数为2N
A
B.反应中消耗6gC,生成CO的体积为11.2L(标准状况)
C.密度、体积均相同的Cl 和CO,CO的分子数更多
2
D.将MgCl 溶于水配成0.1mol·L-1MgC1 溶液,阴离子总数大于0.2N
2 2 A
27.N 是阿伏加德罗常数的值。利用反应2NH +NaClO= N H+ NaCl+ H O可制备火箭推进剂的燃料
A 3 2 4 2
NH。下列说法正确的是( )
2 4
A.0.1molNH 溶于水形成的饱和溶液中,NH +的数目为0.1N
3 4 A
B.1 L2 mol·L-1的NaClO溶液中,O原子的数目为2N
A
C.每生成11.7gNaCl,该反应转移电子数为0.4N
A
D.标准状况下,2.24L的HO中含有的质子数为1N
2 A
28.设 为阿伏加德罗常数的值。我国科学家开发的沸石分子筛催化剂,可实现甲烷在温和条件下
高选择性氧化制备高附加值的甲醇和乙酸的目的,转化关系如下:
下列说法正确的是( )
A.60g CH COOH中含 键的数目为3N
3 A
B.标准状况下,22.4LCH OH中含有的原子数为6N
3 A
C.在光照下,2molCH 和71gCl 充分反应生成CHCl分子的数目为2N
4 2 3 A
D.在浓硫酸、加热条件下,1molCH OH和足量CHCOOH充分反应生成的酯基数目为N
3 3 A
29.[新题型]设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,N(z)为微粒z的数量,N
A为阿伏加德罗常数的值。下列说法正确的是( )
A.C(石墨)+O (g)=CO (g) ΔH=-390kJ•mol-1,则1mol[ C(石墨)+ O(g)]完全燃烧放热130kJ
2 2 2
B.Cu与1mol•L-1的硝酸溶液充分反应,若生成22.4LNO气体,则转移电子数为3N
A
C.1.6g氧气含分子数为0.05N ,且平均每个O 分子的体积约为 L
A 2
D.50mL12mol·L-1盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
1.(2023•全国甲卷,10)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A. 异丁烷分子中共价键的数目为6.5N
A
B.标准状况下,2.24LSO 中电子的数目为4.00N
3 A
C. 的HSO 溶液中 的数目为0.02N
2 4 A
D. 的NaCO 溶液中CO2-的数目为1.0N
2 3 3 A
2.(2023•浙江省6月选考,7) N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.1.7gH O 中含有氧原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
3.(2023•海南卷,6)N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.2.4g镁条在空气中充分燃烧,转移的电子数目为0.2N
A
B.5.6g铁粉与0.1L1mol·L-1的HCl的溶液充分反应,产生的气体分子数目为0.1N
A
C.标准状况下,2.24LSO 与1.12LO 充分反应,生成的SO 分子数目为0.1N
2 2 3 A
D.1.7gNH 完全溶于1LHO所得溶液,NH ·H O微粒数目为0.1N
3 2 3 2 A
4.(2023•广东卷,11)设N 为阿伏加德罗常数的值。侯氏制碱法涉及NaCl 和NH Cl和NaHCO 等物
A 4 3
质。下列叙述正确的是( )
A.1mol NH Cl含有的共价键数目为5 N
4 A
B.1mol NaHCO 完全分解,得到的CO 分子数目为2 N
3 2 AC.体积为1L的1mol·L-1NaHCO 溶液中,HCO -数目为N
3 3 A
D.NaCl 和NH Cl的混合物中含1molCl-,则混合物中质子数为28 N
4 A
5.(2022•重庆卷,5)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的是(
2 2 3 A
)
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
6.(2022•全国甲卷,11)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.25℃,101kPa下, 氢气中质子的数目为2.5N
A
B.2.0L 1.0 mol/L溶液中, 的数目为2.0N
A
C.0.2mol苯甲酸完全燃烧,生成CO 的数目为1.4N
2 A
D.电解熔融CuCl ,阴极增重6.4g,外电路中通过电子的数目为0.10N
2 A
7.(2022·浙江省1月考试,12)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
8.(2022·浙江省6月考试,12)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.12 g NaHSO 中含有0.2N 个阳离子
4 A
B. 乙烷和丙烯的混合气体中所含碳氢键数为3N
A
C.8 gCH 含有中子数为3N
4 A
D.0.1mol H 和0.1mol I 于密闭容器中充分反应后, 分子总数为0.2N
2 2 A
9.(2022•辽宁省选择性考试,3)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1.8 g 18O中含有的中子数为N
A
B.28 g C H 分子中含有的 键数目为4 N
2 4 A
C.标准状况下,22.4L HCl气体中H+数目为N
A
D.pH=12的NaCO 溶液中 数目为0.01 N
2 3 A
10.(2023•辽宁省选择性考试,5)我国古代四大发明之一黑火药的爆炸反应为:
S+2KNO +3C=K S+N↑+3CO ↑。设N 为阿伏加德罗常数的值,下列说法正确的是( )
3 2 2 2 A
A.11.2LCO 含π键数目为N B.每生成2.8 g N 转移电子数目为N
2 A 2 AC.0.1molKNO 晶体中含离子数目为0.2N D.1L0.1mol·L-1KS溶液中含S2-数目为0.1N
3 A 2 A
11.(2022•福建卷,3)常温常压下,电化学还原制氨气的总反应方程式:
,设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 水中含有的孤电子对数为2N
A
B.每产生34gNH ,N 失去的电子数为6N
3 2 A
C. 氨水中,含有的NH ·H O分子数少于N
3 2 A
D.消耗11.2LN (己折算为标况)时,产生的O 分子数为0.75N
2 2 A
12.(2022•海南省选择性考试,7)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德
A
罗常数的值,下列说法正确的是( )
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
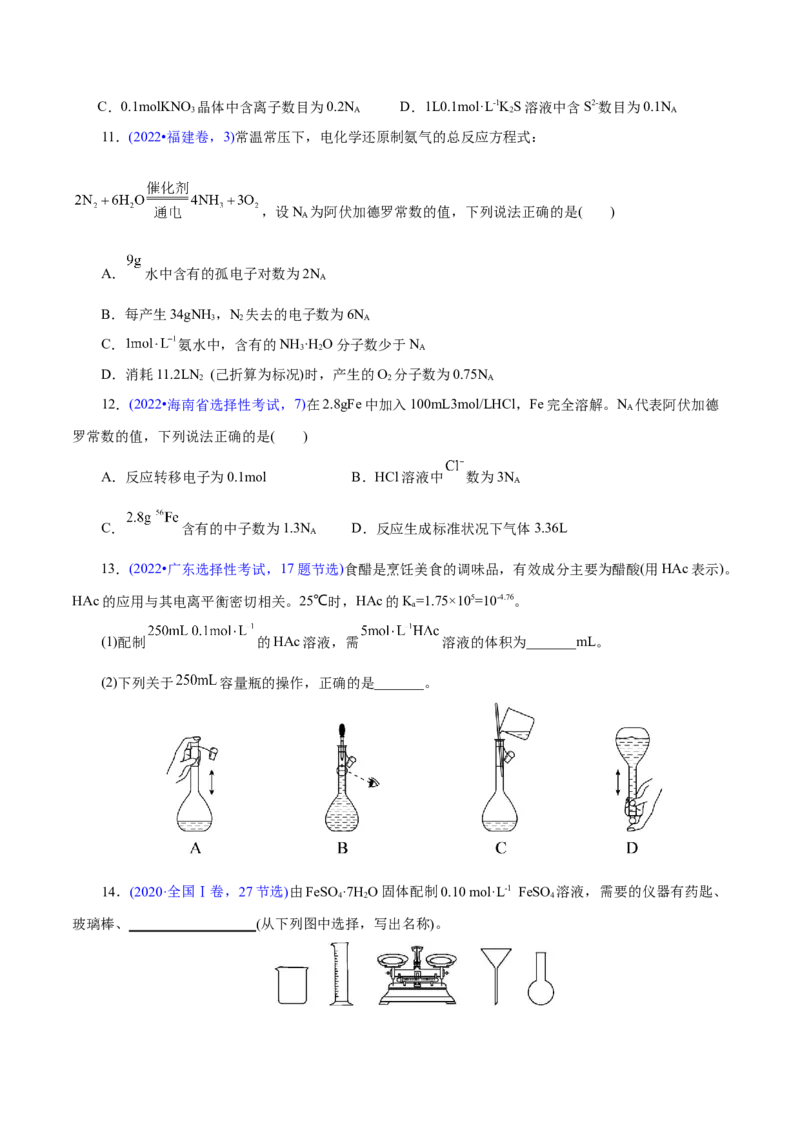
13.(2022•广东选择性考试,17题节选)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。
HAc的应用与其电离平衡密切相关。25℃时,HAc的K=1.75×105=10-4.76。
a
(1)配制 的HAc溶液,需 溶液的体积为_______mL。
(2)下列关于 容量瓶的操作,正确的是_______。
14.(2020·全国Ⅰ卷,27节选)由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需要的仪器有药匙、
4 2 4
玻璃棒、__________________(从下列图中选择,写出名称)。