文档内容
专题 08 水溶液中的离子反应与平衡
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2023·浙江省宁波市高三下学期高考模拟)常温下,K (HCOOH)=1.77×10-4,K (HCOOH)=1.75×10-
a1 a2
5,K(NH ·H O)=1.76×10-5,下列说法不正确的是( )
a 3 2
A.浓度均为0.1 mol/L的HCOONa和NH Cl溶液中阳离子的物质的量浓度之和:前者>后者
4
B.用相同浓度的NaOH溶液分别滴定等体积、pH均为3的HCOOH和CHCOOH溶液至终点,消耗
3
NaOH溶液的体积:前者<后者
C.0.2mol/L CH COONa与0.1 mol/L盐酸等体积混合后,溶液中微粒浓度:c(Na+)>c(CHCOO-)>
3 3
c(Cl-)>c(CHCOOH)>c(H+)>c(OH-)
3
D.0.2mol/L HCOONa溶液与0.1mol/L NaOH溶液等体积混合后的溶液中:c(HCOO-)+ c(OH-)=
c(HCOOH)+c(H+)
2.(2024·河南省普高联盟高三测评)常温下,NH •H O的K 约为10-5。在下列装置中存在不同pH的两
3 2 b
种溶液,溶液中离子不能穿过隔膜,分子可以自由穿过隔膜(如图所示)。已知c (NH •H O)=c
起始 3 2 平衡
(NH •H O)+c(NH )。当达到平衡时,下列叙述正确的是( )
3 2
A.溶液I中c(OH-)=c(H+)+c(NH )
B.溶液I和II中的c (NH •H O)不相等
平衡 3 2
C.溶液II中 为0.1
D.溶液I和II中c (NH •H O):c (NH •H O)=101:110
起始I 3 2 起始II 3 2
3.(2023·四川省成都市高二期末)为探究浓度对醋酸电离程度的影响,用 计测定 时不同浓度醋酸的 结果如下,下列说法正确的是( )
浓度/ 0.0010 0.010 0.020 0.10 0.20
3.88 3.38 3.23 2.88 2.83
A.实验过程中可以改用广泛 试纸
B. 溶液稀释过程中,醋酸电离程度及溶液导电性都增大
C. 时,电离常数K(CH COOH)的数量级为10-5
3
D.CHCOOH溶液稀释过程中不可能出现c(H+)>c(OH―)>c(CHCOO-)
3 3
4.(2023·江苏省徐州市高二期末)水的离子积常数随着温度的变化关系如表:
温度/℃ 25 50 75 100
K /×10-14 1.0 5.5 20.0 56.0
W
下列说法正确的是( )
A.纯水中c(H+)的大小与温度无关
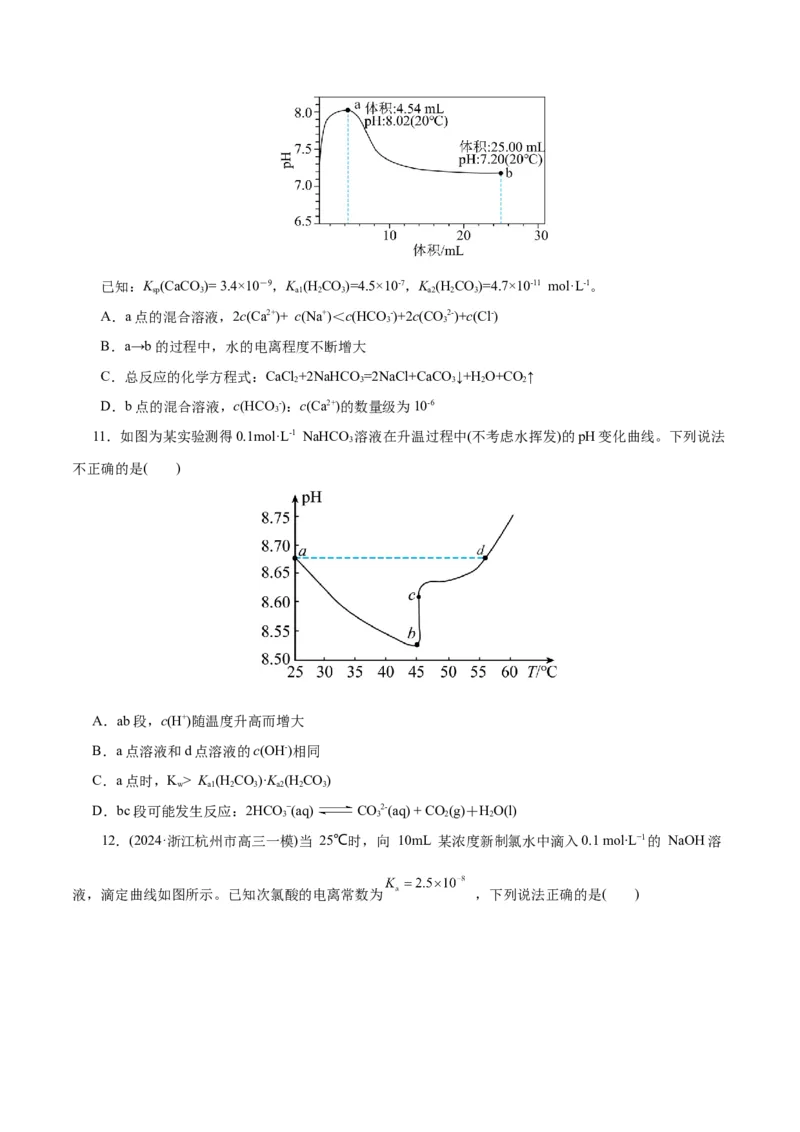
B.水的电离度a(50℃) K (H CO)·K (H CO)
w a1 2 3 a2 2 3
D.bc段可能发生反应:2HCO −(aq) CO2-(aq) + CO (g)+HO(l)
3 3 2 2
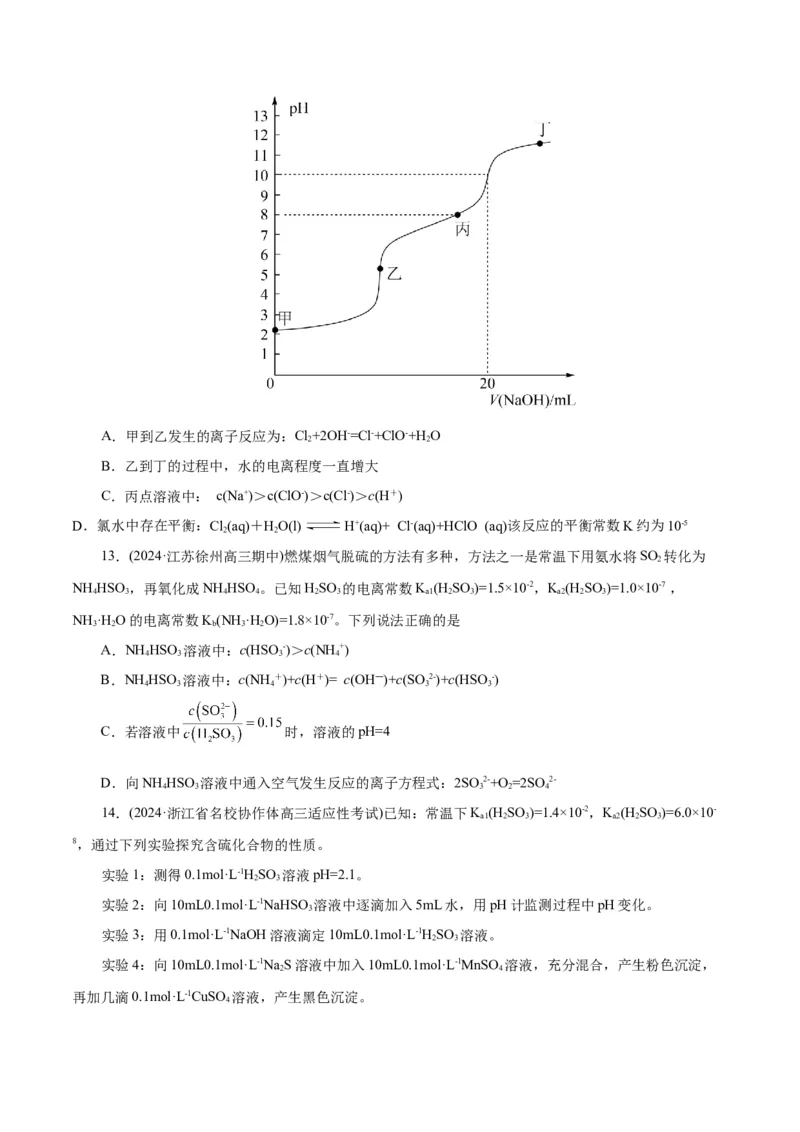
12.(2024·浙江杭州市高三一模)当 25℃时,向 10mL 某浓度新制氯水中滴入0.1 mol∙L−1的 NaOH溶
液,滴定曲线如图所示。已知次氯酸的电离常数为 ,下列说法正确的是( )A.甲到乙发生的离子反应为:Cl+2OH-=Cl-+ClO-+H O
2 2
B.乙到丁的过程中,水的电离程度一直增大
C.丙点溶液中: c(Na+)>c(ClO-)>c(Cl-)>c(H+)
D.氯水中存在平衡:Cl(aq)+HO(l) H+(aq)+ Cl-(aq)+HClO (aq)该反应的平衡常数K约为10-5
2 2
13.(2024·江苏徐州高三期中)燃煤烟气脱硫的方法有多种,方法之一是常温下用氨水将SO 转化为
2
NH HSO ,再氧化成NH HSO 。已知HSO 的电离常数K (H SO )=1.5×10-2,K (H SO )=1.0×10-7 ,
4 3 4 4 2 3 a1 2 3 a2 2 3
NH ·H O的电离常数K(NH ·H O)=1.8×10-7。下列说法正确的是
3 2 b 3 2
A.NH HSO 溶液中:c(HSO -)>c(NH +)
4 3 3 4
B.NH HSO 溶液中:c(NH +)+c(H+)= c(OH―)+c(SO 2-)+c(HSO -)
4 3 4 3 3
C.若溶液中 时,溶液的pH=4
D.向NH HSO 溶液中通入空气发生反应的离子方程式:2SO 2-+O =2SO2-
4 3 3 2 4
14.(2024·浙江省名校协作体高三适应性考试)已知:常温下K (H SO )=1.4×10-2,K (H SO )=6.0×10-
a1 2 3 a2 2 3
8,通过下列实验探究含硫化合物的性质。
实验1:测得0.1mol·L-1HSO 溶液pH=2.1。
2 3
实验2:向10mL0.1mol·L-1NaHSO 溶液中逐滴加入5mL水,用pH计监测过程中pH变化。
3
实验3:用0.1mol·L-1NaOH溶液滴定10mL0.1mol·L-1HSO 溶液。
2 3
实验4:向10mL0.1mol·L-1NaS溶液中加入10mL0.1mol·L-1MnSO 溶液,充分混合,产生粉色沉淀,
2 4
再加几滴0.1mol·L-1CuSO 溶液,产生黑色沉淀。
4下列说法不正确的是( )
A.由实验1可知:0.1mol·L-1HSO 溶液中c(SO 2-)K (CuS)
sp sp
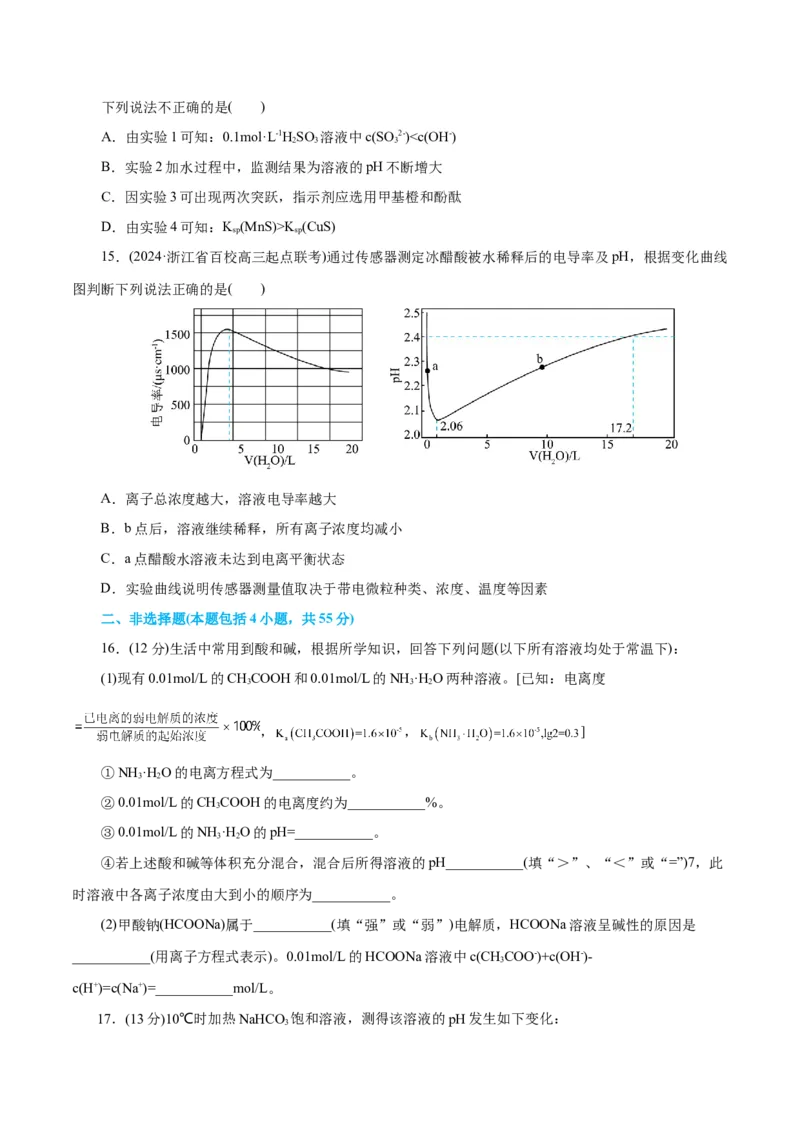
15.(2024·浙江省百校高三起点联考)通过传感器测定冰醋酸被水稀释后的电导率及pH,根据变化曲线
图判断下列说法正确的是( )
A.离子总浓度越大,溶液电导率越大
B.b点后,溶液继续稀释,所有离子浓度均减小
C.a点醋酸水溶液未达到电离平衡状态
D.实验曲线说明传感器测量值取决于带电微粒种类、浓度、温度等因素
二、非选择题(本题包括4小题,共55分)
16.(12分)生活中常用到酸和碱,根据所学知识,回答下列问题(以下所有溶液均处于常温下):
(1)现有0.01mol/L的CHCOOH和0.01mol/L的NH ·H O两种溶液。[已知:电离度
3 3 2
, , ]
①NH ·H O的电离方程式为___________。
3 2
②0.01mol/L的CHCOOH的电离度约为___________%。
3
③0.01mol/L的NH ·H O的pH=___________。
3 2
④若上述酸和碱等体积充分混合,混合后所得溶液的pH___________(填“>”、“<”或“=”)7,此
时溶液中各离子浓度由大到小的顺序为___________。
(2)甲酸钠(HCOONa)属于___________(填“强”或“弱”)电解质,HCOONa溶液呈碱性的原因是
___________(用离子方程式表示)。0.01mol/L的HCOONa溶液中c(CHCOO-)+c(OH-)-
3
c(H+)=c(Na+)=___________mol/L。
17.(13分)10℃时加热NaHCO 饱和溶液,测得该溶液的pH发生如下变化:
3温度(℃) 10 20 30 加热煮沸后冷却到50℃
pH 8.3 8.4 8.5 8.8
根据上述数据:甲同学认为,该溶液的 pH升高的原因是HCO -的水解程度增大,故碱性增强,该反
3
应的离子方程式为____________________________。乙同学认为,溶液pH升高的原因是NaHCO 受热分
3
解,生成了NaCO ,并推断NaCO 的水解程度_______(填“大于”或“小于”)NaHCO 。丙同学认为甲、
2 3 2 3 3
乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则____(填“甲”或“乙”判断正确。试
剂X是_____________(填序号)。
A.Ba(OH) 溶液 B.BaCl 溶液 C.NaOH溶液 D.澄清的石灰水
2 2
(2)将加热后的溶液冷却到 10℃,若溶液的 pH_____(填“高于”、“低于”或“等于”)8.3,则
_____(填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO 的分解温度为150℃,丙断言_____(填“甲”或“乙”)判断是错误的,理
3
由是_____________________________________________________。
18.(15分) (2024·江苏南通·高三统考期中)制备锂离子电池的正极材料的前体FePO 的一种流程如下:
4
资料:i.磷灰石的主要成分是Ca (PO )F
5 4 3
ii.Ca(HPO ) 可溶于水,CaSO·2H O微溶于水
2 4 2 4 2
iii.K (FePO )=1.3×10-22
sp 4
(1)酸浸制粗HPO
3 4
用HPO 溶液、HSO 溶液浸取磷灰石生成HF、CaSO·2H O和HPO 。
3 4 2 4 4 2 3 4
①加入HPO 溶液、HSO 溶液的顺序为 。
3 4 2 4
②写出该反应的化学方程式: 。
③“酸浸”时能否要浓盐酸代替硫酸? (判断并说明理由)。
(2)纯化制备HPO
3 4
已知纯磷酸(熔点为42℃,沸点261℃),高于100℃时会脱水生成焦磷酸。则由85%的粗磷酸纯化制纯
磷酸的实验操作为 。
(3)制备FePO
4
①已知25℃时HPO 电离平衡常数K =6.9×10-3,K =6.2×10-8,K =4.8×10-13,则NaHPO 水解平衡常
3 4 a1 a2 a3 2 4
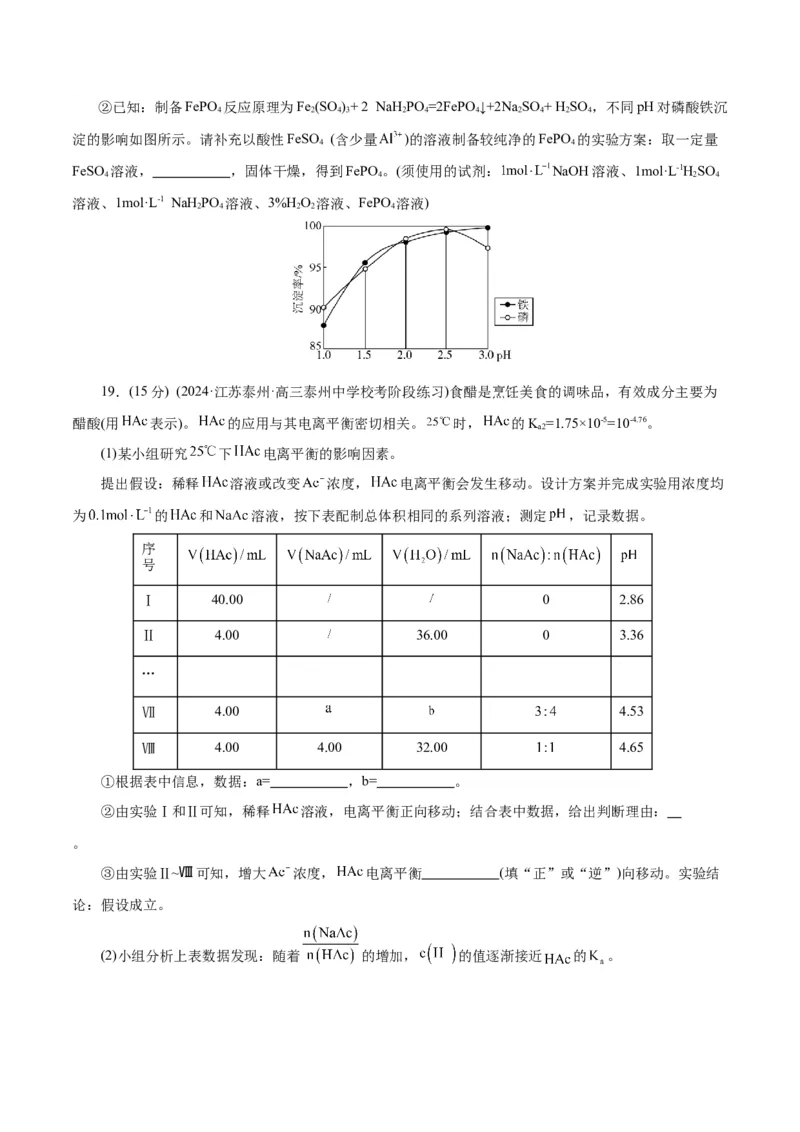
数为 (保留2位有效数字)。②已知:制备FePO 反应原理为Fe (SO )+ 2 NaH PO =2FePO ↓+2Na SO + H SO ,不同pH对磷酸铁沉
4 2 4 3 2 4 4 2 4 2 4
淀的影响如图所示。请补充以酸性FeSO (含少量 )的溶液制备较纯净的FePO 的实验方案:取一定量
4 4
FeSO 溶液, ,固体干燥,得到FePO 。(须使用的试剂: NaOH溶液、1mol·L-1HSO
4 4 2 4
溶液、1mol·L-1 NaH PO 溶液、3%H O 溶液、FePO 溶液)
2 4 2 2 4
19.(15分) (2024·江苏泰州·高三泰州中学校考阶段练习)食醋是烹饪美食的调味品,有效成分主要为
醋酸(用 表示)。 的应用与其电离平衡密切相关。 时, 的K =1.75×10-5=10-4.76。
a2
(1)某小组研究 下 电离平衡的影响因素。
提出假设:稀释 溶液或改变 浓度, 电离平衡会发生移动。设计方案并完成实验用浓度均
为 的 和 溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
序
号
Ⅰ 40.00 0 2.86
Ⅱ 4.00 36.00 0 3.36
…
Ⅶ 4.00 4.53
Ⅷ 4.00 4.00 32.00 4.65
①根据表中信息,数据:a= ,b= 。
②由实验Ⅰ和Ⅱ可知,稀释 溶液,电离平衡正向移动;结合表中数据,给出判断理由:
。
③由实验Ⅱ~Ⅷ可知,增大 浓度, 电离平衡 (填“正”或“逆”)向移动。实验结
论:假设成立。
(2)小组分析上表数据发现:随着 的增加, 的值逐渐接近 的 。查阅资料获悉:一定条件下,按 配制的溶液中, 的值等于HAc的K。
a
对比数据发现,实验Ⅷ中pH=4.65与资料数据K =10-4.76存在一定差异;推测可能由物质浓度准确程度
a2
不够引起,故先准确测定 溶液的浓度再验证。
①移取20.00 mL HAc溶液,加入2滴酚酞溶液,用 溶液滴定至 ,消
耗体积为 ,则该HAc溶液的浓度为 。
②用上述 溶液和 溶液,配制等物质的量的HAc与NaAc混合溶液,测定
pH,结果与资料数据相符。
(3)小组进一步提出:如果只有浓度均约为 的 和NaOH溶液,如何准确测定 的K?
a
小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
移取 溶液,用 溶液滴定至终点,消耗 溶液V
Ⅰ 1
mL
Ⅱ ,测得溶液的pH为4.76
实验总结得到的结果与资料数据相符,方案可行。