文档内容
专题 11 水溶液中离子反应
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
1.(2023·黑龙江省海伦市第一中学高三期中)化学用语是学习化学的工具和基础。下列化学用语正确的是(
)
A.一水合氨的电离:NH ·H O= NH ++OH-
3 2 4
B.CuS沉淀溶解平衡:CuS(s) Cu 2+(aq)+S2-(aq)
C.“铅蓄电池”放电时正极反应式:PbO +4H++2e-=Pb2++2HO
2 2
D.NaS的水解反应:S2-+2H O 2OH-+H S
2 2 2
【答案】B
【解析】A项,一水合氨为弱碱,电离时存在电离平衡,所以用“ ”; NH ·H O NH +
3 2 4
+OH-,A项错误;B项,CuS难溶于水,在水中存在溶解平衡,溶解平衡方程式为CuS(s) Cu 2+(aq)+S2-
(aq),B项正确;C项,“铅蓄电池”的正极反应式为PbO +4H++SO 2-+2e-=PbSO +2HO,C项错误;D
2 4 4 2
项,NaS分步水解,离子方程式为S2-+H O OH-+HS-,HS-+H O OH-+H S,D项错误;故选B。
2 2 2 2
2.(2023·北京市牛栏山一中高三期中)室温下,对于1L 醋酸溶液,下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为 个
3
B.加入少量CHCOONa固体后,溶液的pH升高
3
C.滴加NaOH溶液过程中,c(CHCOO-)与c(CHCOOH)之和始终为0.1mol/L
3 3
D.与NaCO 溶液反应的离子方程式为CO2-+2H+=H O+CO↑
2 3 3 2 2
【答案】B
【解析】A项, 1L 0.1mol•L-1醋酸溶液中醋酸的物质的量为0.1mol,醋酸属于弱酸,是弱电解质,在溶
液中部分电离,则CHCOO-的粒子数小于6.02×1022,A项错误;B项,加入少量CHCOONa固体后,溶液中
3 3
CHCOO-的浓度增大,根据同离子效应,会抑制醋酸的电离,溶液中的氢离子浓度减小,酸性减弱,则溶液的
3
pH升高,B项正确;C项,1L 0.1mol•L-1醋酸溶液中醋酸的物质的量为0.1mol,滴加NaOH溶液过程中,溶液
中始终存在物料守恒,n(CHCOO-)+n(CH COOH)=0.1mol,但溶液体积不确定,故二者浓度之和无法计算,C
3 3
项错误;D项,醋酸是弱电解质,离子反应中不能拆写,则离子方程式为CO2-
3
+2CH COOH=H O+CO↑+2CH COO-,D项错误;故选B。
3 2 2 3
3.(2022·安徽省六安一中高三第四次月考)已知室温下氢氟酸的电离常数K=6.6×10-4,有关下列溶液(均在
a
常温下)说法一定正确的是( )
A.pH=6的氯化铵溶液中:c(H+)=c(NH·H O)=1.0×10-6 mol·L-1
3 2B.1L pH=7的CHCOONH 溶液中,由水电离产生的H+的物质的量为
3 4
C.对NaF溶液加适量水稀释过程中,水解平衡右移,溶液碱性增强
D.向MgF 悬浊液中加少量硝酸,溶液中2c(Mg2+)=c(F-)+c(HF)
2
【答案】D
【解析】A项,pH=6的氯化铵溶液中遵循质子守恒,即c(H+)=c(NH·H O)+ c(OH-)=1.0×10-6 mol·L-1,A错
3 2
误;B项,CHCOONH 溶液的pH=7,H+ 浓度为10-7 mol·L-1,溶液中的 H+ 的物质的量等于 10−7mol;醋酸
3 4
根离子与铵根离子能同等程度促进水的电离,因此,1L该溶液中水电离产生的 H+ 的物质的量大于 10−7mol,
B错误;C项,NaF在水中的水解的离子方程式为F-+H O F-+OH-,加水会促进氟离子水解,使其平衡向
2
右移动,氢氧根离子的个数增多,但由于溶液体积变大对溶液浓度的影响更大,所以溶液的碱性减弱,C错误;
D项,MgF 悬浊液中加少量硝酸后MgF 的溶解度变大,但是不能改变原本存在的物料守恒,2c(Mg2+)=c(F-)
2 2
+c(HF),D正确;故选D。
4.(2022·辽宁省沈阳二中高三第二阶段测试)盐类水解在工农业生产和日常生活中有着广泛的应用。下列
有关应用或说法与水解无关的是( )
A.用浓氨水除去铜器表面的铜绿
B.TiO 化学性质稳定,制备时用TiCl 加入大量水,同时加热,生成物再经焙烧可得
2 4
C.配制FeCl 溶液时,先将晶体溶解在较浓的盐酸中,再加水至指定浓度
3
D.长期施用硫酸铵化肥的土壤,易变酸性,可施用适量的熟石灰
【答案】A
【解析】A项,铜绿主要成分是碱式碳酸铜,用浓氨水可将碱式碳酸铜转变成可溶性的铜氨络合物而被除,
与水解无关,故A选;B项,TiCl 中加入大量水,同时加热,促进水解,且生成HCl易挥发,则过滤,经焙
4
烧得TiO,与水解有关,故B不选;C项,将FeCl 固体溶解在较浓的盐酸中可抑制铁离子水解,再加水稀释
2 3
至所需的浓度,与水解有关,故D不选;D项,长期使用硫酸铵化肥的土壤,易变酸性,和铵根离子水解有关,
熟石灰显碱性,且价格便宜,常用来改良酸性土壤,与水解有关,故D不选;故选A。
5.(2023·浙江省名校协作体高三开学考试)下列说法正确的是( )
A.用标准盐酸溶液滴定未知浓度的NaOH溶液,若溶液久置,用甲基橙作指示剂测得结果偏低
B.常温下,等体积、等pH的稀盐酸和稀醋酸溶液中c(Cl-)= c(CHCOO-)
3
C.常温下KNO 溶液和CHCOONH 溶液pH均为7,两溶液中水的电离程度相同
3 3 4
D.如果常温下体积、浓度均为0.1mol·L-1的盐酸和醋酸溶液,分别稀释m、n倍使溶液的pH都变为5,
则m HClO,故水解程度为:NaClO> NaHCO ,故pH相等的①次氯酸钠溶液、
2 3 3
②碳酸氢钠溶液,二者的物质的量浓度关系:①<②,A正确;B项,等体积等pH的盐酸和醋酸,稀释相同
倍数后盐酸中H+浓度小于醋酸中的H+浓度,故与等量且足量的锌反应,醋酸比盐酸中更剧烈,由于醋酸的物
质的量浓度大于盐酸故醋酸产生氢气多,B错误;C项,向pH=a的盐酸中加入pH=b的氢氧化钠溶液,恰好完
全反应时,测得盐酸与氢氧化钠溶液的体积比为10:1,即10V×10-a =V× ,则a+b=15 , C错误;D项,
pH=3的HA溶液与pH=11的BOH等体积混合后溶液呈酸性,即pH<7,则BOH为强碱、HA为弱酸,D错误;
故选A。
8.(2022·上海市奉贤区高三统考)常温下,用0.1mol·L-1氨水滴定10mL浓度均为0.1mol·L-1的HCl和
CHCOOH的混合液,下列说法不正确的是( )
3
A.滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CH COO-)
3 3
B.滴加氨水到20mL的过程中,水的电离程度逐渐增大
C.当滴入20mL氨水时,c(CHCOOH)+c(H+)=c(NH·H O)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20mL,c(NH +)c(CH COO-),A正确;B项,酸或碱的电离抑制水的电离,滴加氨水时,溶液中的酸被消耗,滴加
3
到20mL时,溶液中溶质只有盐,此时水的电离程度达到最大,B正确;C项,当滴入20mL氨水时,溶质为
等物质的量的CHCOONH 和NH Cl,溶液中存在电荷守恒:c(NH +)+c(H+)=c(Cl-)+c(CH COO-)+c(OH-),存在
3 4 4 4 3
物料守恒c(CHCOOH)+c(CH COO-)+c(Cl-)=c(NH+)+c(NH·H O),二式联立可得c(CHCOOH)
3 3 4 3 2 3
+c(H+)=c(NH·H O)+c(OH-),C正确;D项,当滴入20mL氨水时,溶质为等物质的量的CHCOONH 和
3 2 3 4
NH Cl,溶液显酸性,所以要想使溶液呈中性,需要加入更多的氨水,则当溶液呈中性时,氨水滴入量大于
4
20mL,溶液中的溶质为等物质的量的CHCOONH 和NH Cl,以及少量NH ·H O,水解是微弱的,所以
3 4 4 3 2
c(NH +)>c(Cl-),D错误;故选D。
4
9.(2022·广东省广州市高三调研考试)HCOOH是最简单的羧酸,俗称蚁酸。下列叙述正确的是( )
A.pH=4的HCOOH溶液中,c(H+)=c(HCOO-)
B.pH=5的HCOOH和HCOONa混合溶液中,c(HCOO-)>c(Na+)C.0.1mol•L-1HCOONa溶液中,c(Na+)>c(OH-)>c(HCOO-)>c(H+)
D.0.1mol•L-1HCOONa溶液中,c(Na+)=c(HCOO-)+c(OH-)
【答案】B
【解析】A项,HCOOH溶液中存在HCOOH部分电离:HCOOH H++HCOO-,也有水的部分电离:
HO H++OH-,则c(H+)>c(HCOO-),故A正确;B项,HCOOH和HCOONa混合溶液pH=5说明显酸性,
2
c(H+)> c OH-),由电荷守恒:c(HCOO-)+ c OH-)= c(H+)+ c(Na+),则c(HCOO-)>c(Na+),故B正确;C项,
HCOONa溶液中存在HCOO-的水解,水解方程式:HCOO-+H O HCOOH+OH-,则溶液呈碱性,离子浓
2
度大小为:c(Na+)> c(HCOO-)>c(OH-)> c(H+),故C错误;D项,HCOONa溶液中,存在电荷守恒:c(HCOO-)+
c OH-)= c(H+)+ c(Na+),故D错误;故选B。
10.(2023·重庆南开中学高三质检)下列叙述正确的是( )
A.向含足量Mg(OH) 固体的悬浊液中加少量水,则c(Mg2+)减小
2
B.向NaHCO 溶液中加入CHCOONa固体,则c(HCO -)减小
3 3 3
C.已知KHC O 溶液呈酸性,向KC O 溶液中滴加HSO 溶液至c(K+)=4c(SO2-),则c(C O2-)>
2 4 2 2 4 2 4 4 2 4
c(H C O)
2 2 4
D.向HPO 溶液中滴加NaOH溶液至c(H PO -)=c(HPO 2-),则c(Na+)=3c(PO 3-)+ 3c(H PO -)
3 4 2 3 4 4 2 3
【答案】C
【解析】A项, 向含足量Mg(OH) 固体的悬浊液中加少量水,得到的仍为氢氧化镁饱和溶液,镁离子浓
2
度不变,A错误;B项,向NaHCO 溶液中加入CHCOONa固体,溶液碱性增强,抑制碳酸氢根的水解,且由
3 3
于碳酸的酸性比醋酸的弱,即醋酸根不能促进碳酸氢根的电离,则碳酸氢根离子浓度增大,B错误;C项,已
知KHC O 溶液呈酸性,说明草酸氢根的电离程度大于其水解程度,向KC O 溶液中滴加HSO 溶液至
2 4 2 2 4 2 4
c(K+)=4c(SO2-),即草酸钾和硫酸按照物质的量之比2:1混合,此时溶质成分为KHC O、KSO ,则c(C O2-)
4 2 4 2 4 2 4
>c(H C O),C正确;D项,根据电荷守恒:c(Na+)+c(H+)=3c(PO 3-)+2c(H PO -)+c(HPO 2-)+c(OH-)=3c(PO 3-)
2 2 4 4 2 3 4 4
+3c(H PO -)+c(OH-),此时溶液不呈中性,即氢离子和氢氧根离子浓度不相等,D错误;故选C。
2 3
11.(2022·上海市金山区高三质量监控一模)H X为二元弱酸。20℃时,向100mL0.1mol·L-1的NaX溶液中
2 2
缓慢通入HCl(忽略溶液体积变化及HX的挥发)。指定溶液中微粒的物质的量浓度关系一定正确的是( )
2
A.通入HCl前:c(X2-)>c(HX-)>c(OH-)>c(H+)
B.若通入5×10-3molHCl,溶液呈碱性,则溶液中c(X2-)=c(HX-)
C.pH=7时:溶液中c(HX-)>c(Cl-)
D.c(Cl-)=0.1mol·L-1时:c(OH-)-c(H+)=c(H X)-c(X2-)
2
【答案】D
【解析】A项,通入HCl气体之前,该溶液为NaX溶液,分步水解且程度很小,离子浓度大小关系为
2c(X2-)>c(OH-)>c(HX-)>c(H+),A错误;B项,若通入5×10-3molHCl,则反应后溶液为NaHX和NaX等浓度
2
混合的溶液,因溶液呈碱性,即HX-的电离小于X2-的水解,则溶液中c(X2-)<c(HX-),B错误;C项,电荷守
恒式c(Cl-)+2c(X2-)+c(HX-)+c(OH-)=c(Na+)+c(H+),物料守恒式c(Na+)=2c(X2-)+2c(HX-)+2c(H X),pH=7的溶液
2
c(OH-)=c(H+),三等式联立可得c(Cl-)>c(HX-),C错误;D项,c(Cl-)=0.100 mol•L-1的溶液中,c(X2-)+c(HX-)
+c(H X)=c(Cl-)=0.100mol•L-1,又根据电荷守恒式c(Cl-)+2c(X2-)+c(HX-)+c(OH-)=c(Na+)+c(H+),物料守恒式
2
c(Na+)=2c(X2-)+2c(HX-)+2c(H X)可得c(Cl-)+c(OH-)═c(H+)+c(HX-)+2c(H X),所以c(OH-)-c(H+)=c(HX-)+2c(H X)-
2 2 2
[c(X2-)+c(HX-)+c(H X)]=c(HX)-c(X2-),D正确;故选D。
2 2
12.(2023·河北省部分学校高三联考)二元弱酸是分步电离的,25℃时碳酸和氢硫酸的 如下表。
K =4.5×10-7 K =1.1×10-7
a1 a1
HCO HS
2 3 2
K =4.7×10-11 K =1.3×10-13
a2 a2
下列叙述正确的是( )
A.根据以上数据可知,NaHCO 溶液中c(CO2-)>c(H CO
3 3 2 3
B.等浓度的NaHS溶液和NaHCO 溶液等体积混合后,则c(H+)-c(OH-)= c(S2-)+c(CO2-)-c(H S)-c(H CO)
3 3 2 2 3
C.pH相同的①NaCO 溶液和②NaS溶液中的c(Na+):①<②
2 3 2
D.过量HS通入NaCO 溶液中反应的离子方程式为HS+CO2-=HS-+CO
2 2 3 2 3 2
【答案】B
【解析】A项,NaHCO 溶液中存在电离平衡和水解平衡:HCO - H++CO 2-,K= K =4.7×10-11,
3 3 3 a2
HCO -+ H O HCO+OH-,Kˊ= = = ×10-7,由此可知,CO2-是
3 2 2 3 3
电离产物,HCO 是水解产物,二者大小取决于电离和水解程度大小,即比较电离平衡常数和水解平衡常数大
2 3
小,由上可知水解平衡常数大于电离平衡常数,故水解程度大,则NaHCO 溶液中c(CO2-)<c(H CO,A项错
3 3 2 3
误;B项,二者混合后溶液中的电荷守恒为c(Na+)+c(H+)= c(HS-)+2c(S2-)+ c(HCO -)+2c(CO2-)+c(OH-),物料
3 3
守恒为c(Na+)= c(HS-)+c(S2-)+ c(H S)+c(CO2-)+c(HCO -)+c(H CO),两式相减得:c(H+)= c(S2-)+c(CO2-)
2 3 3 2 3 3
+c(OH-)-c(H S)-c(H CO),B项正确;C项,由表中数据可知,NaS溶液水解程度较大,所以pH相同的
2 2 3 2
①NaCO 溶液和②NaS溶液,NaS溶液的浓度较小,则钠离子浓度较小,即①>②,C项错误;D项,由电
2 3 2 2
离常数可知,酸性HCO>HS>HCO ->HS-,则过量HS通入NaCO 溶液中反应的离子方程式为HS+CO2-
2 3 2 3 2 2 3 2 3
=HS-+HCO-,D项错误;故选B。
3
13.(2023·江苏省苏州八校联盟、南京一中、中华中学高三联考)已知HSO 是一种二元弱酸。室温下,通
2 3过下列实验探究HSO 溶液的性质。
2 3
实验 实验操作和现象
1 用pH试纸测量0.1mol·L-1NaHSO 溶液的pH,测得pH约为5
3
向10mL0.1mol·L-1NaCO 溶液中滴加几滴0.1mol·L-1NaHSO 溶液,无明显现
2 2 3 3
象
3 向0.1mol·L-1NaHSO 溶液中加入等体积0.1mol·L-1Ba(OH) 溶液,溶液变浑浊
3 2
向10mL0.1mol·L-1NaHSO 溶液中加入等体积0.1mol·L-1氨水溶液,充分混
4 3
合,溶液pH约为9
若忽略溶液混合时的体积变化,下列说法正确的是( )
A.依据实验1可推测:K (H SO )K (H SO )<K
a1 2 3 a2 2 3 w
B.依据实验2推测:K (H SO ) <K (H CO)
a2 2 3 a1 2 3
C.依据实验3推测:K (BaSO)>2.5×10-3
sp 3
D.实验4所得溶液中存在:2c(H SO )+c(HSO -)>c(NH ·H O)
2 3 3 3 2
【答案】D
【解析】A项, 0.1mol/L亚硫酸氢钠溶液pH约为5,溶液呈酸性说明亚硫酸氢根离子的电离程度大于水
解程度,则亚硫酸氢根离子的水解常数K = <K (H SO ),所以K (H SO )K (H SO )>K ,故A错
h a2 2 3 a1 2 3 a2 2 3 w
误;B项,10mL0.1mol/L碳酸钠溶液与几滴0.1mol/L亚硫酸氢钠溶液可能反应生成碳酸氢钠和亚硫酸钠,无
法确定亚硫酸氢钠是否能与碳酸氢钠溶液反应,所以无法比较亚硫酸氢根离子和碳酸的电离程度大小,不能确
定亚硫酸的二级电离常数和碳酸一级电离常数的大小,故B错误;C项,0.1mol/L亚硫酸氢钠溶液与等体积的
0.1mol/L氢氧化钡溶液反应所得溶液中亚硫酸根离子被钡离子的浓度均为0.05mol/L,由混合后溶液变浑浊可
知,溶液中浓度熵大于亚硫酸钡的溶度积,则K (BaSO)<0.05mol/L×0.05mol/L=2.5×10−3,故C错误;D项,
sp 3
10mL0.1mol/L亚硫酸氢钠溶液与等体积的0.1mol/L氨水溶液反应得到亚硫酸钠和亚硫酸铵的混合溶液,溶液
中存在质子守恒关系2c(H SO )+c(HSO -)+c(H+)=c(OH-)+c(NH ·H O),由溶液pH约为9可知,溶液中氢氧根离
2 3 3 3 2
子浓度大于氢离子浓度,则溶液中存在2c(H SO )+c(HSO -)>c(NH ·H O),故D正确;故选D。
2 3 3 3 2
14.(2023·安徽省皖优联盟高三第二次阶段测试)一种吸收SO 再经氧化得到硫酸盐的过程如图所示。室温
2
下,用0.1 mol·L 的NaOH溶液吸收SO ,若通入SO 所引起的溶液体积变化和HO挥发可忽略,溶液中含硫
2 2 2
物种的浓度 。HSO 的电离常数分别为K =1.29×10-2,K =6.24×10-8。下列
2 3 a1 a2说法错误的是( )
A.“吸收”所得溶液中;c(Na+)+c(H+)=2c(SO 2-)+c(HSO -)+c(OH-)
3 3
B.“吸收”所得溶液中不可能存在:c(Na+)>c(H+)>c(SO 2-)>c(HSO -)>c(OH-)
3 3
C.“吸收”所得 mol·L 的溶液中:c(H SO )>c(SO 2-)
2 3 3
D.调节“吸收”所得溶液的pH约为5,“氧化”时主要发生的反应为2HSO -+O =2SO-+2H+
3 2 4
【答案】C
【解析】A项,二氧化硫被氢氧化钠吸收后可生成亚硫酸钠或亚硫酸氢钠,溶液中根据电荷守恒:c(Na+)
+c(H+)=2c(SO 2-)+c(HSO -)+c(OH-),A正确;B项,根据选项A可知,不可能存在c(Na+)>c(H+)>c(SO 2-)>
3 3 3
c(HSO -)>c(OH-),B正确;C项, mol·L-1时,投料相当于NaHSO 溶液,根据电离常数计算,电离程
3 3
度大于水解程度, c(SO 2-)>c(H SO ),C错误;D项,根据平衡常数数据可知,亚硫酸氢钠的电离大于水解,
3 2 3
溶液显酸性,所以若“吸收”所得溶液的pH约为5时,溶液中主要的阴离子为HSO - “氧化”时主要发生的
3
反应为2HSO -+O =2SO-+2H+,D正确;故选C。
3 2 4
15.(2022·江苏省如皋市高三期中调研)草酸钠(Na C O)可作为基准物质测定KMnO 溶液的浓度。测定的
2 2 4 4
方法是准确称量一定质量的草酸钠固体,加水溶解后,加入硫酸酸化,用待测KMnO 溶液进行滴定。HC O
4 2 2 4
是一种二元弱酸,C O2-能与Ca2+结合生成CaC O 沉淀。关于KMnO 溶液测定实验,下列说法正确的是
2 4 2 4 4
( )
A.应用图1所示装置及操作进行滴定
B.图2所示读数为20.5mLC.滴定时应一直保持液体匀速下滴
D.滴定时,开始溶液红色褪去较慢,一段时间后,溶液红色褪去较快,可能是生成的Mn2+对反应具有
催化作用
【答案】D
【解析】A项,酸性高锰酸钾溶液应用酸式滴定管滴定,不能用碱式滴定管,故A错误;B项,滴定管读
数精确度应保留两位小数,即0.01mL,故B错误;C项,滴定时可以先快后慢,故C错误;D项,高锰酸钾
溶液与草酸发生氧化还原反应,生成Mn2+、CO,开始时溶液红色褪去较慢,一段时间后,溶液红色褪去较
2
快,可能是生成的Mn2+对反应具有催化作用,故D正确;故选D。
16.(2022·安徽省六安一中高三第四次月考)已知:常温下,CN-的水解常数K =1.6×10-5。该温度下,将浓
h
度均为0.1 mol•L-1的HCN溶液和NaCN溶液等体积混合。下列说法正确的是( )
A.混合溶液的
B.混合液中水的电离程度小于纯水的
C.混合溶液中存在c(CN-)>c(Na+)>c(HCN)>c(OH-)>c(H+)
D.若c 盐酸与0.6 mol•L-1 NaCN溶液等体积混合后溶液呈中性,则
【答案】D
【解析】CN-的水解常数K =1.6×10-5,则HCN的电离常数是 。A项,0.1 mol•L-1的
h
HCN溶液和NaCN溶液等体积混合,CN-水解大于HCN电离,溶液呈碱性,混合溶液的pH>7,故A错误;B
项,CN-水解促进水电离、HCN电离抑制水电离,CN-水解大于HCN电离,混合液中水的电离程度大于纯水的,
故B错误;C项,CN-水解大于HCN电离,混合溶液呈碱性,混合溶液中存在c(HCN)>c(Na+)>c(CN-)>
c(OH-)>c(H+),故C错误;D项,若c mol•L-1盐酸与0.6 mol•L-1NaCN溶液等体积混合后溶液呈中性,根据电
荷守恒c(Na+)= c(CN-)+ c(Cl-),根据物料守恒,c(Na+)= c(CN-)+ c(HCN)=0.3mol/L,c(Cl-)= ,则c(HCN)=
c(Cl-)= ,根据CN-的水解常数K =1.6×10-5,则 ,c(CN-)=
h
; c(CN-)+ c(HCN)=0.3mol/L,即 + =0.3 mol/L,所以 ,故D正确;故选D。
17.(2022·山东省东明县第一中学高三期中)食盐是氯碱工业的基础原料,由于工业提纯的原因,精制食盐
中也含有少量NaSO 。探究小组同学按下列实验步骤测定精制食盐中NaSO 的含量。
2 4 2 4
已知:CrO2-+Ba2+═BaCrO↓(黄色);CrO2-+3Fe2++8H+═Cr3++3Fe3++4H O。
4 4 4 2
Ⅰ.称取精制食盐样品mg,加水溶解,加盐酸调至弱酸性,滴加过量cmol•L-1 BaCl 溶液vmL;
1 1 2 1
Ⅱ.继续滴加过量cmol•L-1KCrO 溶液vmL;
2 2 4 2
Ⅲ.过滤洗涤,滴加少许指示剂于滤液中,用cmol•L-1FeSO 溶液滴定至终点,消耗FeSO 溶液vmL。
3 4 4 3
精制食盐样品 的质量分数为( )
A. B.
C. D.
【答案】D
【解析】设NaSO 物质的量为,则SO 2-物质的量为x;Ⅰ.称取精制食盐样品mg,加水溶解,加盐酸调
2 4 4 1
至弱酸性,滴加过量cmol•L-1 BaCl 溶液vmL,发生反应Ba2++SO2-=BaSO ↓,则剩余BaCl 物质的量为
1 2 1 4 4 2
(c v×10-3-x)mol:Ⅱ.继续滴加过量cmol•L-1KCrO 溶液vmL,发生反应CrO2-+Ba2+═BaCrO↓(黄色),则剩余
1 1 2 2 4 2 4 4
CrO2-物质的量为[c v -3-(c v×10-3-x)]mol;Ⅲ.过滤洗涤,滴加少许指示剂于滤液中,用cmol•L-1FeSO 溶液滴
4 2 210 1 1 3 4
定至终点,消耗FeSO 溶液vmL,发生反应为CrO2-+3Fe2++8H+═Cr3++3Fe3++4H O,可得3[c v×10-3-(c v×10-3-
4 3 4 2 2 2 1 1
x)]mol=(c v×10-3)mol,可得x=(c v-c v+ cv)×10-3mol,精制食盐样品NaSO 的质量分数为
3 3 1 1 2 2 3 3 2 4
,故选D。
18.(2022·山西省吕粱市金科大联考)下列实验操作、现象、结论均正确的是( )
选项 实验操作 实验现象 实验结论
Fe3+能催化HO 的分
向 的FeCl,溶液中 溶液中有气泡产生 2 2
A 3 解,且HO 分解为放
FeCl 溶液颜色加深 2 2
滴入几滴 的双氧水 3 热反应B 将氯气通入FeI 淀粉溶液 混合溶液变蓝 氧化性:Cl>Fe3+>I
2 2 2
用甲基橙作指示剂,用0.1mol·L-1
C 溶液由红色变为橙色 达到滴定终点
的NaOH溶液滴定未知浓度的醋酸
向 5mL0.5mol·L-1的 NaOH 溶液中
先后滴加 0.2mol·L-1 的 MgCl 、 溶液中先生成白色沉 证明:K [Cu(OH)]<
D 2 sp 2
CuCl 溶液各5滴,观察滴加时沉 淀,后生成蓝色沉淀 K [Mg(OH)]
2 sp 2
淀的颜色
【答案】A
【解析】A项,向FeCl 溶液中滴入几滴双氧水后能明显看到气泡的产生,说明Fe3+能催化HO 的分解,
3 2 2
并且FeCl 溶液颜色加深,说明Fe3+的水解程度増大,而水解是吸热反应,说明HO 分解是放热反应,故A正
3 2 2
确;B项,向FeI 淀粉溶液中通入氯气,溶液变蓝说明有I 生成,从而证明氧化性Cl>I,但无法证明氧化性
2 2 2 2
Fe3+>I,故B错误;C项,用NaOH溶液滴定醋酸时,应该用酚酞作指示剂,故C错误;D项,在NaOH与
2
MgCl 的反应过程中,溶液中OH-过量,再滴加CuCl 溶液,剩余的OH-直接与Cu2+结合生成蓝色Cu(OH) 沉淀,
2 2 2
不能证明K [Cu(OH)]<K [Mg(OH)],故D错误;故选A。
sp 2 sp 2
19.(2022·江苏省常州市八校高三联合调研)室温下,通过下列实验探究NaHSO 溶液的性质:
3
实验 实验操作和现象
1 用pH试纸测定某NaHSO 溶液的pH,测得pH约为6
3
2 向某NaHSO 溶液中加入过量的Ba(OH) 溶液,产生白色沉淀
3 2
3 向某NaHSO 溶液中加入等体积等浓度的烧碱溶液,测得溶液pH约为9
3
4 向某苏打溶液中滴加几滴NaHSO 溶液,未观察到明显实验现象
3
下列有关说法正确的是( )
A.NaHSO 溶液中存在c(OH-)=c(H+)-c(SO 2-)+c(HSO -)
3 3 3
B.实验2反应静置后的上层清液中有c(Ba2+)×c(SO2-)>Ksp(BaSO )
3 3
C.实验3得到的溶液中有c(Na+)=c(SO2-)+c(HSO -)+c(H SO )
3 3 2 3
D.实验4中反应的离子方程式为CO2-+HSO -=HCO-+SO2-
3 3 3 3
【答案】D
【解析】A项,NaHSO 溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+2c(SO2-)+c(HSO -),物料守恒:
3 3 3
c(Na+)=c(HSO )+c(SO2-)+c(HSO -),所以有c(OH-)=c(H+)-c(SO 2-)+c(H SO ),故A错误;B项,向某NaHSO
2 3 3 3 3 2 3 3
溶液中加入过量的Ba(OH) 溶液,产生亚硫酸钡白色沉淀、氢氧化钠和水,因此反应静置后的上层清液是亚硫
2
酸钡的饱和溶液,则其中有c(Ba2+)×c(SO2-)=K (BaSO),故B错误;C项,向某NaHSO 溶液中加入等体积等
3 sp 3 3
浓度的烧碱溶液,测得溶液pH约为9,所得溶液是亚硫酸钠溶液,溶液中存在物料守恒:c(Na+)=2c(HSO )+2c(SO2-)+2c(HSO -),故C错误;D项,向某苏打溶液中滴加几滴NaHSO 溶液,碳酸钠过量,生成
2 3 3 3 3
碳酸氢钠,不会产生二氧化碳,所以未观察到明显实验现象,故D正确;故选D。
20.(2022·山东省高三第三次联考)碳酸和亚硫酸电离平衡常数(25℃)如下表所示:
名称 碳酸 亚硫酸
电离常数 K =4.4×10-7 K =4.7×10-11 K =1.3×10-2 K =6.2×10-8
1 2 1 2
下列说法正确的是( )
A.pH相同的①NaCO ②NaSO 溶液中c(Na+):①>②
2 3 2 3
B.少量CO 通入NaSO 溶液中反应的离子方程式为:CO+H O+2SO 2-=CO 2-+HSO -
2 2 3 2 2 3 3 3
C.某NaHSO 溶液pH=5,则该溶液中的c(HSO )>c(SO 2-)
3 2 3 3
D.等浓度的NaHSO 和NaHCO 等体积混合后,则c(H+)-c(OH-)= c(CO2-)-c(HCO)+ c(SO 2-)-c(HSO )
3 3 3 2 3 3 2 3
【答案】D
【解析】A项,根据电离常数可知 ,则NaCO 的水解程度大,pH相同时需要的NaCO 浓度
2 3 2 3
小,碳酸钠溶液中钠离子浓度小,①<②,故A错误﹔B项,由于酸性HCO>HSO ->HCO -,则少量CO 通入
2 3 3 3 2
NaSO 溶液,不能生成CO2-,故B错误;C项,NaHSO 溶液pH=5,则HSO -的电离程度大于其水解程度,溶
2 3 3 3 3
液中c(HSO )<c(SO 2-),故C错误;D项,等浓度的NaHSO 和NaHCO 等体积混合后,其电荷守恒为:c(H+)
2 3 3 3 3
+c(Na+)=2c(CO 2-)+c(OH-)+c(HCO-)+2 c(SO 2-)+c(HSO -) ①,物料守恒为:c(Na+)= c(HCO -)+ c(CO2-)
3 3 3 3 3 3
+c(H CO)+ c(HSO -)+ c(SO 2-)+ c(HSO ) ②;①-②得c(H+)-c(OH-)= c(CO2-)-c(HCO)+ c(SO 2-)-c(HSO ),故
2 3 3 3 2 3 3 2 3 3 2 3
D正确。故选D。
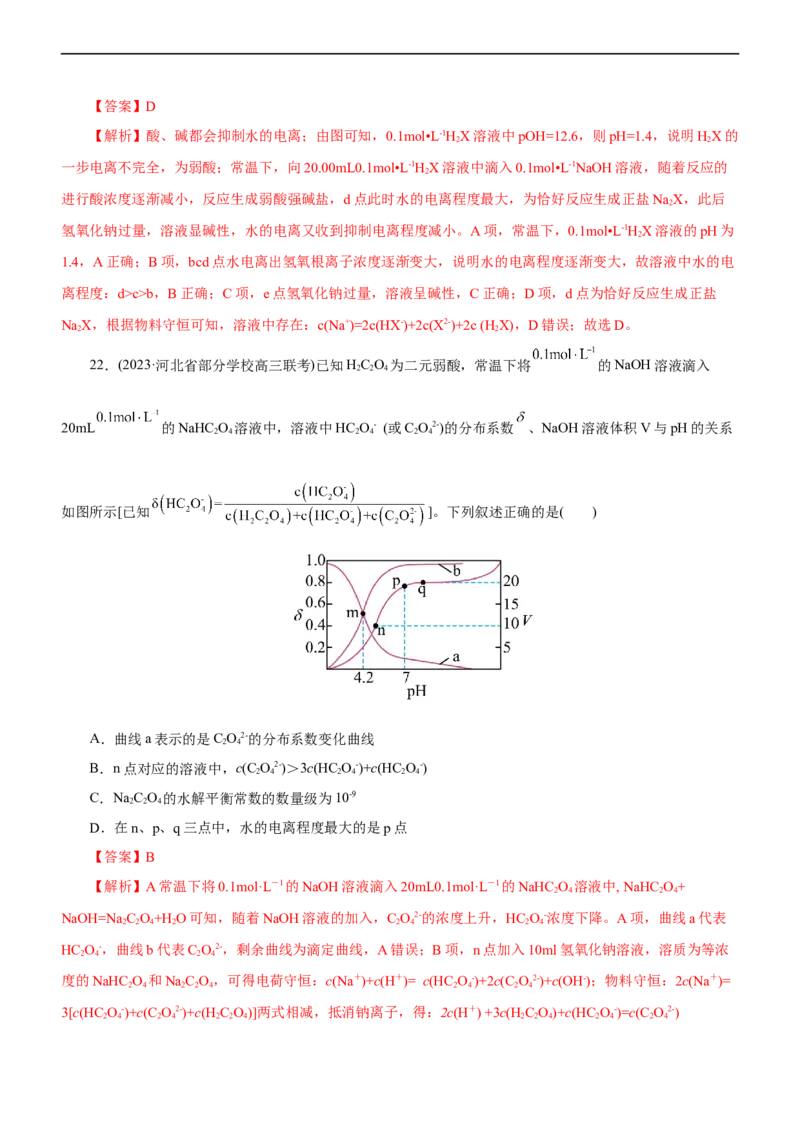
21.(2023·广东省广州三校(广大附中、铁一、广外)高三期中联考)常温下,向20.00mL0.1mol•L-1HX溶液
2
中滴入0.1mol•L-1NaOH溶液,pOH 与所加NaOH溶液体积的关系如图所示。下列说法错误的是( )
水
已知pOH=−lgc(OH-)。
A.常温下,0.1mol•L-1HX溶液的pH为1.4 B.溶液中水的电离程度:d>c>b
2
C.e点溶液呈碱性 D.d点溶液中存在:2c(Na+)=c(HX-)+c(X2-)【答案】D
【解析】酸、碱都会抑制水的电离;由图可知,0.1mol•L-1HX溶液中pOH=12.6,则pH=1.4,说明HX的
2 2
一步电离不完全,为弱酸;常温下,向20.00mL0.1mol•L-1HX溶液中滴入0.1mol•L-1NaOH溶液,随着反应的
2
进行酸浓度逐渐减小,反应生成弱酸强碱盐,d点此时水的电离程度最大,为恰好反应生成正盐NaX,此后
2
氢氧化钠过量,溶液显碱性,水的电离又收到抑制电离程度减小。A项,常温下,0.1mol•L-1HX溶液的pH为
2
1.4,A正确;B项,bcd点水电离出氢氧根离子浓度逐渐变大,说明水的电离程度逐渐变大,故溶液中水的电
离程度:d>c>b,B正确;C项,e点氢氧化钠过量,溶液呈碱性,C正确;D项,d点为恰好反应生成正盐
NaX,根据物料守恒可知,溶液中存在:c(Na+)=2c(HX-)+2c(X2-)+2c (HX),D错误;故选D。
2 2
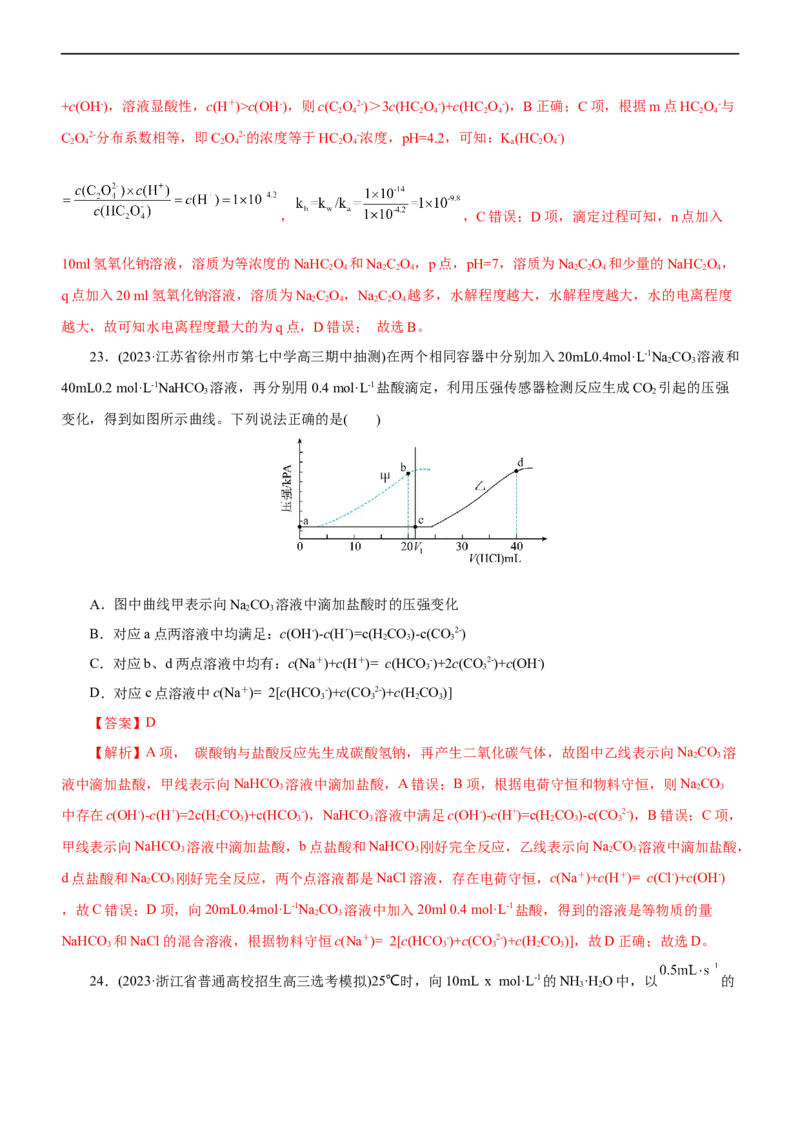
22.(2023·河北省部分学校高三联考)已知HC O 为二元弱酸,常温下将 的NaOH溶液滴入
2 2 4
20mL 的NaHC O 溶液中,溶液中HC O- (或C O2-)的分布系数 、NaOH溶液体积V与pH的关系
2 4 2 4 2 4
如图所示[已知 ]。下列叙述正确的是( )
A.曲线a表示的是C O2-的分布系数变化曲线
2 4
B.n点对应的溶液中,c(C O2-)>3c(HC O-)+c(HC O-)
2 4 2 4 2 4
C.NaC O 的水解平衡常数的数量级为10-9
2 2 4
D.在n、p、q三点中,水的电离程度最大的是p点
【答案】B
【解析】A常温下将0.1mol·L-1的NaOH溶液滴入20mL0.1mol·L-1的NaHC O 溶液中, NaHC O+
2 4 2 4
NaOH=Na C O+H O可知,随着NaOH溶液的加入,C O2-的浓度上升,HC O-浓度下降。A项,曲线a代表
2 2 4 2 2 4 2 4
HC O-,曲线b代表C O2-,剩余曲线为滴定曲线,A错误;B项,n点加入10ml氢氧化钠溶液,溶质为等浓
2 4 2 4
度的NaHC O 和NaC O,可得电荷守恒:c(Na+)+c(H+)= c(HC O-)+2c(C O2-)+c(OH-);物料守恒:2c(Na+)=
2 4 2 2 4 2 4 2 4
3[c(HC O-)+c(C O2-)+c(H C O)]两式相减,抵消钠离子,得:2c(H+) +3c(H C O)+c(HC O-)=c(C O2-)
2 4 2 4 2 2 4 2 2 4 2 4 2 4+c(OH-),溶液显酸性,c(H+)>c(OH-),则c(C O2-)>3c(HC O-)+c(HC O-),B正确;C项,根据m点HC O-与
2 4 2 4 2 4 2 4
C O2-分布系数相等,即C O2-的浓度等于HC O-浓度,pH=4.2,可知:K(HC O-)
2 4 2 4 2 4 a 2 4
, ,C错误;D项,滴定过程可知,n点加入
10ml氢氧化钠溶液,溶质为等浓度的NaHC O 和NaC O,p点,pH=7,溶质为NaC O 和少量的NaHC O,
2 4 2 2 4 2 2 4 2 4
q点加入20 ml氢氧化钠溶液,溶质为NaC O,NaC O 越多,水解程度越大,水解程度越大,水的电离程度
2 2 4 2 2 4
越大,故可知水电离程度最大的为q点,D错误; 故选B。
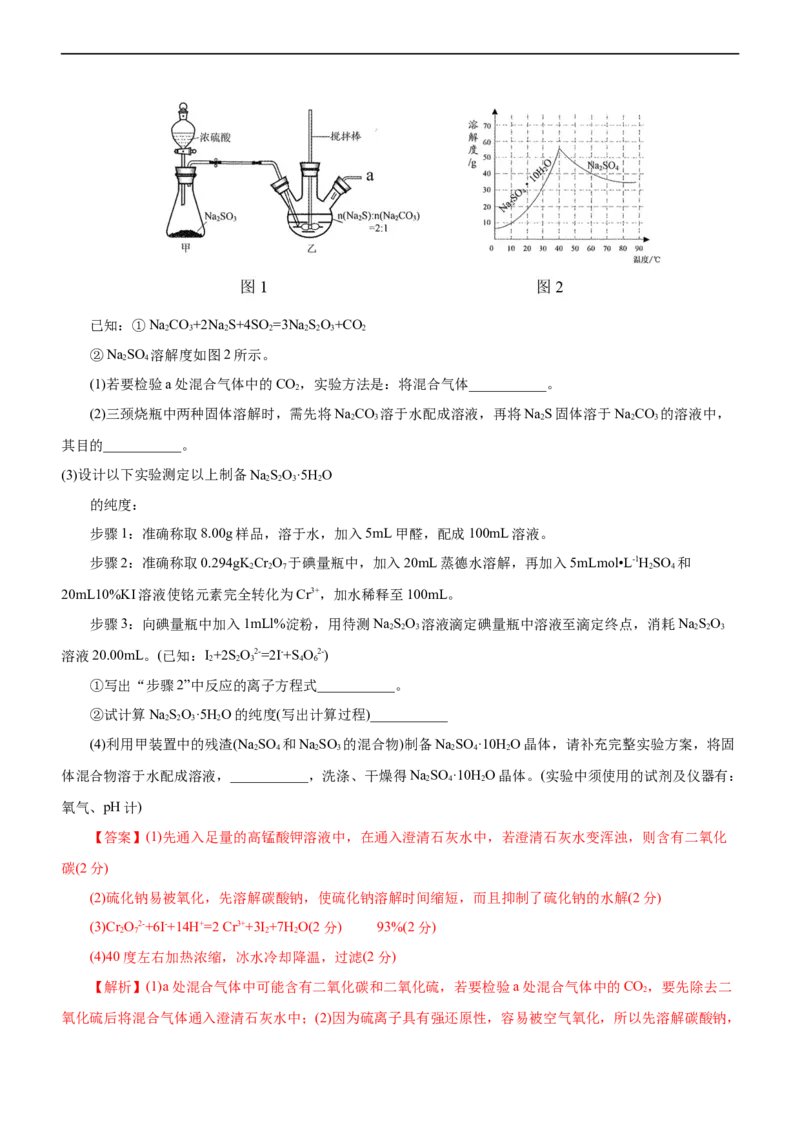
23.(2023·江苏省徐州市第七中学高三期中抽测)在两个相同容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2 mol·L-1NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,利用压强传感器检测反应生成CO 引起的压强
3 2
变化,得到如图所示曲线。下列说法正确的是( )
A.图中曲线甲表示向NaCO 溶液中滴加盐酸时的压强变化
2 3
B.对应a点两溶液中均满足:c(OH-)-c(H+)=c(H CO)-c(CO2-)
2 3 3
C.对应b、d两点溶液中均有:c(Na+)+c(H+)= c(HCO -)+2c(CO2-)+c(OH-)
3 3
D.对应c点溶液中c(Na+)= 2[c(HCO -)+c(CO2-)+c(H CO)]
3 3 2 3
【答案】D
【解析】A项, 碳酸钠与盐酸反应先生成碳酸氢钠,再产生二氧化碳气体,故图中乙线表示向NaCO 溶
2 3
液中滴加盐酸,甲线表示向NaHCO 溶液中滴加盐酸,A错误;B项,根据电荷守恒和物料守恒,则NaCO
3 2 3
中存在c(OH-)-c(H+)=2c(H CO)+c(HCO-),NaHCO 溶液中满足c(OH-)-c(H+)=c(H CO)-c(CO2-),B错误;C项,
2 3 3 3 2 3 3
甲线表示向NaHCO 溶液中滴加盐酸,b点盐酸和NaHCO 刚好完全反应,乙线表示向NaCO 溶液中滴加盐酸,
3 3 2 3
d点盐酸和NaCO 刚好完全反应,两个点溶液都是NaCl溶液,存在电荷守恒,c(Na+)+c(H+)= c(Cl-)+c(OH-)
2 3
,故C错误;D项,向20mL0.4mol·L-1NaCO 溶液中加入20ml 0.4 mol·L-1盐酸,得到的溶液是等物质的量
2 3
NaHCO 和NaCl的混合溶液,根据物料守恒c(Na+)= 2[c(HCO -)+c(CO2-)+c(H CO)],故D正确;故选D。
3 3 3 2 3
24.(2023·浙江省普通高校招生高三选考模拟)25℃时,向10mL x mol·L-1的NH ·H O中,以 的
3 2速度逐滴加入0.1 mol·L-1的HCl溶液。如图为 与时间(t)的关系图,其中一条线段为
,另一条线段为 。已知电离平衡常数K (NH ·H O)=2.0×10-5, 。
b 3 2
下列说法不正确的是( )
A.该酸碱滴定实验最宜用甲基橙作为指示剂
B.由图可推知:M点的pH约为9.3
C.使HCl溶液滴至1min时,由 可推知:
D.适当升高温度(忽略 的变化),Q点(与x轴交点)将向右移动
【答案】D
【解析】向10mL x mol·L-1的NH ·H O中,以 的速度逐滴加入0.1 mol·L-1的HCl溶液,
3 2
表示的曲线是pH变化曲线;由 知, =
;表示的线是直线。A项,恰好反应时,得到的氯化铵溶液是酸性溶液,甲基橙的变色范围
是3.1-4.4,所以强酸滴定弱碱时,最宜使用甲基橙,A项正确;B项,由图可知,M点对应p X 曲线的Q点,
2
则 = =0,代入K (NH ·H O)=2.0×10-5,解得c(OH-)=2.0×10-5,c(H+)=
b 3 20.5×10-9,此时pH=9.3,B项正确;C项,使HCl溶液滴至1min时,加入的稀盐酸的体积
是 ×60s=30mL,加入盐酸的物质的量是0.003mol,此时pH=7,此时根据电荷守恒得到
c(Cl-)=c(NH+)=0.075mol/L,根据K (NH ·H O)=2.0×10-5计算,此时c(NH ·H O)=0.000375 mol/L,再根据N原子
4 b 3 2 3 2
守恒,c (NH ·H O)=c(NH+)+ c(NH ·H O)=0.075+0.000375,再根据稀释前后物质的量不变,原来是10mL,反
总 3 2 4 3 2
应后体积为40mL,则起始时氨水的浓度是(0.075+0.000375)×4=0.3015mol/L,C项正确;D项,氨水的电离过
程是吸热过程,温度升高,利于电离方向进行,电离常数K增大。对于 =
,温度升高,K变大,碱性增强,Q点应向左移动,D项错误;故选D。
25.(2023·浙江省温州市高三第一次适应性考试)25℃时,分别向20mL浓度均1.0mol·L−1的CHCOOH、
3
CHCOONa溶液中逐滴加入浓度均1.0mol·L−1NaOH、HCl溶液VmL,溶液的pH与lgY[Y= 或
3
]的关系如图所示。下列说法不正确的是( )
A.曲线①中的Y=
B.当pH=4.74时,恒有关系:c(H+)+c(Na+)=c(OH−)+c(CH COOH)
3C.当滴入体积V=10mL时,溶液pH>4.74
D.25℃时,1.0mol·L−1的CHCOONa的pH=9.37
3
【答案】B
【解析】pH越大,H+浓度越小,从而促进CHCOOH的电离,抑制CHCOO-的水解,所以溶液中
3 3
c(CHCOOH)减小,c(CHCOO-)增大,则 增大, 减小,所以曲线①中的Y=
3 3
,②中的Y= ;pH=4.74时, = ,即
c(CHCOOH)=c(CH COO-),所以K= =c(H+)=10-4.74,K= =10-9.26。A项,根据分析可知曲
3 3 a h
线①中的Y= ,A正确;B项,据图可知pH=4.74时,c(CHCOOH)=c(CH COO-),若是
3 3
CHCOOH溶液中滴加NaOH溶液,由电荷守恒可得c(H+)+c(Na+)=c(OH−)+c(CH COOH),但若是向CHCOONa
3 3 3
溶液中滴加HCl溶液,有电荷守恒可得c(H+)+c(Na+)=c(OH−)+c(Cl-)+c(CH COOH),B错误;C项,若
3
V=10mL,则溶液中的溶质均为等物质的量的CHCOOH和CHCOONa,K>K,所以CHCOOH的电离程度
3 3 a h 3
大于CHCOO-的水解程度,所以c(CHCOOH)<c(CHCOO-),则 < ,据图可知此时
3 3 3
pH>4.74,C正确;D项,设25℃时,1.0mol·L−1的CHCOONa的溶液中c(OH-)=x,则
3
c(CHCOOH)=c(OH-)=x,K= = =10-9.26,解得x≈10-4.63mol/L,所以c(H+)=10-9.37mol/L,
3 h
pH=9.37,D正确;故选B。
二、非选择题(本题包括5小题,共50分)
26.(8分)(2022·辽宁省葫芦岛市协作校高三第二次联考)生活中常用到酸和碱,根据所学知识,回答下列
问题(以下所有溶液均处于常温下):(1)现有0.01mol/L的CHCOOH和0.01mol/L的NH ·H O两种溶液。[已知:电离度
3 3 2
, , ]
①NH ·H O的电离方程式为___________。
3 2
②0.01mol/L的CHCOOH的电离度约为___________%。
3
③0.01mol/L的NH ·H O的pH=___________。
3 2
④若上述酸和碱等体积充分混合,混合后所得溶液的pH___________(填“>”、“<”或“=”)7,此时
溶液中各离子浓度由大到小的顺序为___________。
(2)甲酸钠(HCOONa)属于___________(填“强”或“弱”)电解质,HCOONa溶液呈碱性的原因是
___________(用离子方程式表示)。0.01mol/L的HCOONa溶液中c(CHCOO-)+c(OH-)-
3
c(H+)=c(Na+)=___________mol/L。
【答案】(1)NH ·H O NH ++OH-(1分) 4(1分) 10.6(1分) = (1分) c(CHCOOH)=
3 2 4 3
c(NH +)>c(OH-)=c(H+)(1分)
4
(2)强(1分) HCCO-+H O HCOOH+OH-(1分) 0.01(1分)
2
【解析】(1)①NH ·H O-的电离方程式为NH ·H O NH ++OH-。②已知:
3 2 3 2 4
则可得 =1.6×10-5,x=4×10-4,电离度 =4%。③
则可得 =1.6×10-5,x=4×10-4,c(OH-)=4×10-4mol/L,所以pH=10.6。
④因为醋酸和氨水的电离常数相同,故等浓度等体积的醋酸和氨水混合后溶液显中性,故 pH=7,根据电
荷守恒可以推知,离子浓度大小为c(CHCOOH)= c(NH +)>c(OH-)=c(H+)。(2)甲酸钠(HCOONa)属于强电解质,
3 4
甲酸根水解显碱性,故 HCOONa 溶液呈碱性的原因是 HCCO-+H O HCOOH+OH-。根据电荷守恒
2
c(CHCOO-)+c(OH-)=c(H+)+ c(Na+),故c(CHCOO-)+c(OH-)-c(H+)=c(Na+)=0.01mol/L。
3 3
27.(10分)(2022·江苏省海门区高三第二次诊断测试)硫代硫酸钠(Na SO)俗称海波,广泛应用于照相定影
2 2 3
及纺织业等领域等。某化学实验小组用如图1装置制备NaSO·5H O。
2 2 3 2已知:①NaCO+2Na S+4SO=3Na SO+CO
2 3 2 2 2 2 3 2
②NaSO 溶解度如图2所示。
2 4
(1)若要检验a处混合气体中的CO,实验方法是:将混合气体___________。
2
(2)三颈烧瓶中两种固体溶解时,需先将NaCO 溶于水配成溶液,再将NaS固体溶于NaCO 的溶液中,
2 3 2 2 3
其目的___________。
(3)设计以下实验测定以上制备NaSO·5H O
2 2 3 2
的纯度:
步骤1:准确称取8.00g样品,溶于水,加入5mL甲醛,配成100mL溶液。
步骤2:准确称取0.294gK Cr O 于碘量瓶中,加入20mL蒸德水溶解,再加入5mLmol•L-1HSO 和
2 2 7 2 4
20mL10%KI溶液使铭元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mLl%淀粉,用待测NaSO 溶液滴定碘量瓶中溶液至滴定终点,消耗NaSO
2 2 3 2 2 3
溶液20.00mL。(已知:I+2S O2-=2I-+SO2-)
2 2 3 4 6
①写出“步骤2”中反应的离子方程式___________。
②试计算NaSO·5H O的纯度(写出计算过程)___________
2 2 3 2
(4)利用甲装置中的残渣(Na SO 和NaSO 的混合物)制备NaSO ·10H O晶体,请补充完整实验方案,将固
2 4 2 3 2 4 2
体混合物溶于水配成溶液,___________,洗涤、干燥得NaSO ·10H O晶体。(实验中须使用的试剂及仪器有:
2 4 2
氧气、pH计)
【答案】(1)先通入足量的高锰酸钾溶液中,在通入澄清石灰水中,若澄清石灰水变浑浊,则含有二氧化
碳(2分)
(2)硫化钠易被氧化,先溶解碳酸钠,使硫化钠溶解时间缩短,而且抑制了硫化钠的水解(2分)
(3)Cr O2-+6I-+14H+=2 Cr3++3I +7H O(2分) 93%(2分)
2 7 2 2
(4)40度左右加热浓缩,冰水冷却降温,过滤(2分)
【解析】(1)a处混合气体中可能含有二氧化碳和二氧化硫,若要检验a处混合气体中的CO,要先除去二
2
氧化硫后将混合气体通入澄清石灰水中;(2)因为硫离子具有强还原性,容易被空气氧化,所以先溶解碳酸钠,接着进行试验,减少硫化钠的溶解时间,而且碳酸钠水解呈碱性,还能抑制硫化钠的水解,所以需先将
NaCO 溶于水配成溶液,再将NaS固体溶于NaCO 的溶液中;(3)①“步骤2” 中准确称取0.294gK Cr O 于
2 3 2 2 3 2 2 7
碘量瓶中,加入20mL蒸德水溶解,再加入5mLmol•L-1HSO 和20mL10%KI溶液使铭元素完全转化为Cr3+,碘
2 4
离子转化为碘单质,所以离子方程式为:Cr O2-+6I-+14H+=2 Cr3++3I +7H O;②根据化学方程式Cr O2-+6I-
2 7 2 2 2 7
+14H+=2 Cr3++3I +7H O和I+2S O2-=2I-+SO2-,可推出关系式为:Cr O2-~3I ~6S O2-,m(Na SO·5H O)=
2 2 2 2 3 4 6 2 7 2 2 3 2 2 3 2
,样品中NaSO·5H O的纯度为 ;(4)由硫酸钠的溶解度
2 2 3 2
曲线图可知,NaSO ·10H O的溶解度受温度影响较大,在30度左右时溶解度最大,而且降到0度时溶解度最
2 4 2
小,故采用40度左右加热浓缩,冰水冷却降温的方法加以分离,然后过滤,冰水洗涤。
28.(12分)(2022·山东省威海市文登区教育教学研究培训中心高三期中)硫酸氧矾(VOSO)对高血糖、高血
4
症等具有一定的治疗作用。制备VOSO 的实验流程及实验装置如图(夹持及加热装置已省略)。
4
已知:草酸又名乙二酸,是一种二元有机弱酸,易溶于乙醇,可溶于水,不溶于苯,受热易分解,具有还
原性。回答下列问题:
(1)仪器c的名称为___________,在a中反应生成(VO )SO ___________(填“是”或“不是”)氧化还原反
2 2 4
应。
(2)加入草酸前,为防止草酸因反应而减少,需对反应液采取的措施为___________、___________。
(3)反应液由橙红色变为蓝黑色的反应的化学方程式为___________。
(4)硫酸氧钒中钒含量的测定:
Ⅰ.制备VOSO 溶液:称取0. 51 g VO,置于上图装置中反应,VO 全部转化为VOSO。
4 2 5 2 5 4
Ⅱ.滴定预处理:①将制得的VOSO 溶液配成250mL溶液;
4
②取25.00 mL溶液于锥形瓶中,滴加酸性高锰酸钾(可将VO2+转化为VO -)溶液至反应完全;
2
③滴加亚硝酸钠溶液反应掉过量的高锰酸钾溶液,加入2mL尿素溶液至溶液不再产生气泡。已知:尿素
不直接与亚硝酸盐反应,但可将亚硝酸转化为氮气;亚硝酸可将VO -转化为VO2+。
2
Ⅲ.滴定过程:加入10mL硫酸-磷酸混酸,调节pH=0,滴入指示剂,用0.05 mol·L−1硫酸亚铁铵标准溶液
(将VO -转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
2
步骤③中加入尿素的目的是___________;测得硫酸氧钒中钒的质量分数为___________ (保留三位有效数
字)。实验过程中,下列操作会导致所测钒含量偏低的是___________。
A.预处理过程中加入尿素的量不足
B.盛装硫酸亚铁铵标准液的滴定管未润洗
C.滴定管读数时,开始时仰视刻度线,结束时平视刻度线
D.滴定前滴定管有气泡,滴定结束后发现滴定管内无气泡
【答案】(1)球形冷凝管(1分) 不是(1分) (2)充分冷却(1分) 加适量蒸馏水稀释(1分)
(3)(VO )SO +H C O+H SO =2VOSO +2CO ↑+2H O(2分)
2 2 4 2 2 4 2 4 4 2 2
(4) 除去过量的亚硝酸钠,防止亚硝酸将VO -还原为VO2+(2分)
2
0.279或27.9% (2分) AC(2分)
【解析】(1)仪器c的名称为球形冷凝管,在a中五氧化二钒和硫酸反应生成(VO )SO ,反应前后元素化
2 2 4
合价没有改变,不是氧化还原反应。(2)草酸可溶于水,受热易分解;加入草酸前,为防止草酸因反应而减少,
需对反应液采取的措施为充分冷却、加适量蒸馏水稀释等。(3)由流程可知,反应液由橙红色变为蓝黑色的反
应为(VO )SO 在酸性溶液中和草酸反应生成VOSO,反应为:
2 2 4 4
(VO )SO +H C O+H SO =2VOSO +2CO ↑+2H O;(4)已知:尿素不直接与亚硝酸盐反应,但可将亚硝酸转化
2 2 4 2 2 4 2 4 4 2 2
为氮气;亚硝酸可将VO -转化为VO2+。故步骤③中加入尿素的目的是除去过量的亚硝酸钠,防止亚硝酸将
2
VO -还原为VO2+;1molVO 转化为VO2+转移电子1mol,1mol亚铁离子转化为铁离子转移电子1mol;根据质
2
量守恒、电子守恒,可知,则硫酸氧钒中钒的质量为 ;0.
51 g VO 全部转化为VOSO 质量为 ;故硫酸氧钒中
2 5 4
钒的质量分数为 。A项,预处理过程中加入尿素的量不足,亚硝酸可将VO -转化为
2VO2+,导致硫酸亚铁铵标准溶液用量减少,测量值偏小,符合题意;B项,盛装硫酸亚铁铵标准液的滴定管未
润洗,导致用量偏大,测量值偏大,不符合题意;C项,滴定管读数时,开始时仰视刻度线,结束时平视刻度
线,导致用量读数偏小,测量值偏小,符合题意;D项,滴定前滴定管有气泡,滴定结束后发现滴定管内无气
泡,导致用量偏大,测量值偏大,不符合题意;故选AC。
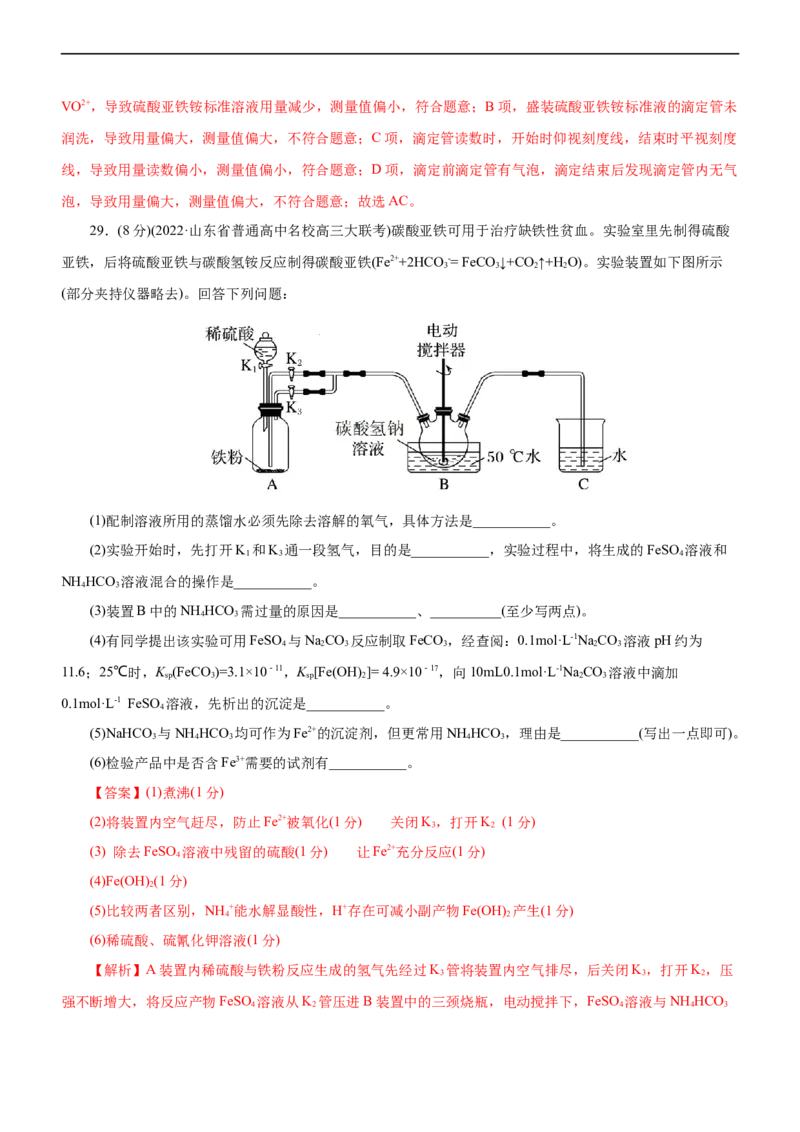
29.(8分)(2022·山东省普通高中名校高三大联考)碳酸亚铁可用于治疗缺铁性贫血。实验室里先制得硫酸
亚铁,后将硫酸亚铁与碳酸氢铵反应制得碳酸亚铁(Fe2++2HCO-= FeCO↓+CO ↑+H O)。实验装置如下图所示
3 3 2 2
(部分夹持仪器略去)。回答下列问题:
(1)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是___________。
(2)实验开始时,先打开K 和K 通一段氢气,目的是___________,实验过程中,将生成的FeSO 溶液和
1 3 4
NH HCO 溶液混合的操作是___________。
4 3
(3)装置B中的NH HCO 需过量的原因是___________、__________(至少写两点)。
4 3
(4)有同学提出该实验可用FeSO 与NaCO 反应制取FeCO,经查阅:0.1mol·L-1NaCO 溶液pH约为
4 2 3 3 2 3
11.6;25℃时,K (FeCO)=3.1×10-11,K [Fe(OH) ]= 4.9×10-17,向10mL0.1mol·L-1NaCO 溶液中滴加
sp 3 sp 2 2 3
0.1mol·L-1 FeSO 溶液,先析出的沉淀是___________。
4
(5)NaHCO 与NH HCO 均可作为Fe2+的沉淀剂,但更常用NH HCO ,理由是___________(写出一点即可)。
3 4 3 4 3
(6)检验产品中是否含Fe3+需要的试剂有___________。
【答案】(1)煮沸(1分)
(2)将装置内空气赶尽,防止Fe2+被氧化(1分) 关闭K,打开K (1分)
3 2
(3) 除去FeSO 溶液中残留的硫酸(1分) 让Fe2+充分反应(1分)
4
(4)Fe(OH) (1分)
2
(5)比较两者区别,NH +能水解显酸性,H+存在可减小副产物Fe(OH) 产生(1分)
4 2
(6)稀硫酸、硫氰化钾溶液(1分)
【解析】A装置内稀硫酸与铁粉反应生成的氢气先经过K 管将装置内空气排尽,后关闭K,打开K,压
3 3 2
强不断增大,将反应产物FeSO 溶液从K 管压进B装置中的三颈烧瓶,电动搅拌下,FeSO 溶液与NH HCO
4 2 4 4 3溶液充分反应得到碳酸亚铁产品。(1)除去水中溶解的氧气方法为:将蒸馏水煮沸后迅速冷却;(2)Fe2+容易被空
气所氧化,实验开始时,先打开K 和K 通一段氢气,可将装置内空气赶尽;A中Fe与稀硫酸反应生成FeSO
1 3 4
和H,关闭K,打开K,利用压强差使其与NH HCO 溶液混合;(3)装置B中的NH HCO 需过量,既可除去
2 3 2 4 3 4 3
FeSO 溶液中残留的硫酸,也可让Fe2+充分反应,同时NH HCO 受热易分解,过量可防止其损失;(4)析出
4 4 3
FeCO 沉淀时c(Fe2+)= = mol/L =3.1×10—10mol/L,NaCO 溶液pH约为11.6,则
3 2 3
c(OH-)=10—2.4mol/L,析出Fe(OH) 沉淀时c(Fe2+)= Ksp= = mol/L =4.9×10—
2
12.2mol/L<3.1×10—10mol/L,故Fe(OH) 先沉淀;(5)比较两者区别,NH +能水解显酸性,H+存在可减小副产物
2 4
Fe(OH) 产生;(6)取少量样品于试管中,加入适量的稀硫酸溶解,再滴入硫氰化钾溶液,若溶液不变为红色,
2
则说明产品中不含Fe3+;若溶液变为红色,则含有Fe3+,故需要用到的试剂是稀硫酸、硫氰化钾溶液。
30.(10分)(2022·安徽省百校联盟高三联考)实现变废为宝和资源的回收利用是实现“碳中和”的重要途径。
一种利用碲化亚铜废渣制备二氧化碲和单质银的工业流程如图所示:
已知:①碲化亚铜废渣的主要成分为CuTe,还含有少量Ag Te;
2 2
②二氧化碲是两性氧化物,微溶于水;
③本流程条件下,K = 1.0×10-14,K [Cu(OH)]= 2.2×10-20。
W sp 2
回答下列问题:
(1)碲(Te)是52号元素,其在元素周期表中的位置为___________,“破碎”的目的为___________。
(2)“酸浸氧化”后Te元素以TeCl 形式存在,由CuTe生成TeCl 的化学方程式为___________,双氧水实
4 2 4
际消耗量为理论消耗量的 倍,原因为___________。
(3)“碱转化除铜”时应调节溶液的 为13,此时溶液中的c(Cu2+)为___________ 。(4)“中和沉碲”时需控制溶液的 为 ,温度为 ,若溶液的 过低,将导致
___________。
(5)酸浸渣的主要成分为___________(填化学式),“还原”工序中发生的反应中氧化剂与还原剂的物质的
量之比为___________。
(6)以上述流程制得的TeO 为原料制备高纯碲单质的方法如下:将TeO 溶于NaOH溶液生成NaTeO,电
2 2 2 3
解NaTeO 溶液即可在阴极获得单质碲。若溶液中c(Na TeO)过低,在阴极会产生Te2-,生成该离子的电极反
2 3 2 3 2
应式为___________。
【答案】(1)第五周期ⅥA族(1分) 增大固体表面积,提高酸浸氧化时的反应速率(1分)
(2)CuTe+8HCl+4HO=2CuCl+TeCl+8H O(2分)
2 2 2 2 4 2
反应生成的Cu2+能催化HO 的分解反应,导致大量HO 被分解(2分)
2 2 2 2
(3)2.2×10-18(1分) (4)碲的沉淀率降低(1分)
(5)AgCl (1分) 4:1 (2分)
(6)2TeO2-+6H O+10e-=Te2-+12OH-(1分)
3 2 2
【解析】碲化亚铜废渣首先粉碎,然后用稀盐酸、双氧水分别酸浸氧化得到酸浸渣和酸浸液,酸浸渣中加
入还原剂将氯化银中的银离子还原为单质银,酸浸液中加入氢氧化钠溶液沉铜,过滤得到含碲酸钠的溶液,然
后加入稀盐酸中和沉碲得到二氧化碲。(1)碲(Te)元素的原子序数是52,在元素周期表中的位置为第五周期ⅥA
族;“破碎”的目的为增大固体表面积,提高酸浸氧化时的反应速率。(2)“酸浸氧化”后Te元素以TeCl 形式
4
存在,铜元素转化成CuCl,故生成TeCl 的化学方程式为CuTe+8HCl+4HO=2CuCl+TeCl+8H O;反应生成的
2 4 2 2 2 2 4 2
Cu2+能催化HO 的分解反应,导致大量HO 被分解,故双氧水实际消耗量比理论消耗量大。(3)溶液的pH为
2 2 2 2
13时,溶液中的c(OH-)=0.1 mol•L-1,则溶液中的 。(4)“中和沉碲”
生成TeO 反应的离子方程式为TeO2-+2H+ TeO↓+H O,由于二氧化碲是两性氧化物,若溶液pH过
2 3 2 2
低,TeO 转化为TeCl,碲的沉淀率降低。(5)氯化银不溶于水也不溶于酸,酸浸渣的主要成分为氯化银;“还
2 4
原”工序中N2H4是还原剂,失去4个电子,银离子得到1个电子,则依据电子得失守恒可知发生的反应中氧
化剂与还原剂的物质的量之比为4:1。(6)阴极发生得到电子的还原反应,则生成Te2-的电极反应式为2TeO2-
2 3
+6H O+10e-=Te2-+12OH-。
2 2