文档内容
专题 12 化学反应机理
近两年来有关反应历程和反应机理的选择题,通过构建模型,进行类比迁移考查考生的化学学科素养。反
应历程是指化学反应中的反应物转化为最终产物通过的途径,因为化学变化从根本上来说,就是旧键的破裂和
新键的生成。反应的历程能够反映出物质结构和反应能力之间的关系,从而可以加深我们对于物质运动形态的
认识。反应机理是化学中用来描述某一化学变化所经由的全部基元反应,机理详细描述了每一步转化的过程,
包括过渡态的形成,键的断裂和生成,以及各步的相对速率大小等。完整的反应机理需要考虑到反应物、催化
剂、反应的立体化学、产物以及各物质的用量。通过反应历程或机理可以帮助我们了解物质结构的知识,形成
“结构决定性质” 的观念,从宏观和微观相结合的视角分析与解决实际问题。 化学反应机理试题以图示的
形式来描述某一化学变化所经由的全部反应,就是把一个复杂反应分解成若干个反应,然后按照一定规律组合
起来,从而达到阐述复杂反应的内在联系的目的。解答时注意题干信息的理解应用,通过分析化学反应过程,
明确反应过程中催化剂的作用和能量变化、化学键的变化试题常以图像为载体,以陌生的反应历程方程式或示
意图为主要信息源,高起点(题目陌生度高,往往用词新颖) ,低落点(考查的思维简单) ,从微观视角来考查
反应机理,考查点集中在题目信息采集处理、能量、速率、平衡、结构、反应等关键考点。由于形式较新颖,
能比较好的考察学生阅读和理解题目信息能力,且考察难度、深度比较容易调控,广度易于辐射到各模块,预
计在今后几年的高考中仍会是命题热点。
1.反应机理
(1)反应机理是用来描述某反应物到反应产物所经由的全部基元反应,就是把一个复杂反应分解成若干个
基元反应,以图示的形式来描述某一化学变化所经由的全部反应,然后按照一定规律组合起来,从而阐述复杂
反应的内在联系,以及总反应与基元反应内在联系。
(2)反应机理详细描述了每一步转化的过程,包括过渡态的形成,键的断裂和生成,以及各步的相对速率
大小等。典型的是基元反应碰撞理论和基元反应过渡态理论。
(3)反应机理中包含的基元反应是单分子反应或双分子反应。完整的反应机理需要考虑到反应物、催化
剂、反应的立体化学、产物以及各物质的用量。
(4)认识化学反应机理,任何化合物的每一步反应都应该是在该条件下此类化合物的通用反应。
2.有效碰撞理论(1)化学反应发生的条件:在化学反应中,反应物分子不断发生碰撞,大多数碰撞无法发生反应,只有少
数分子的碰撞才能发生化学反应,能发生有效碰撞的分子是活化分子。普通反应物分子形成活化分子所需要的
能量叫活化能。而活化分子的碰撞也不一定都能发生有效碰撞。发生有效碰撞不仅有能量的因素,还有空间因
素,只有同时满足这两者的要求才能发生有效碰撞。
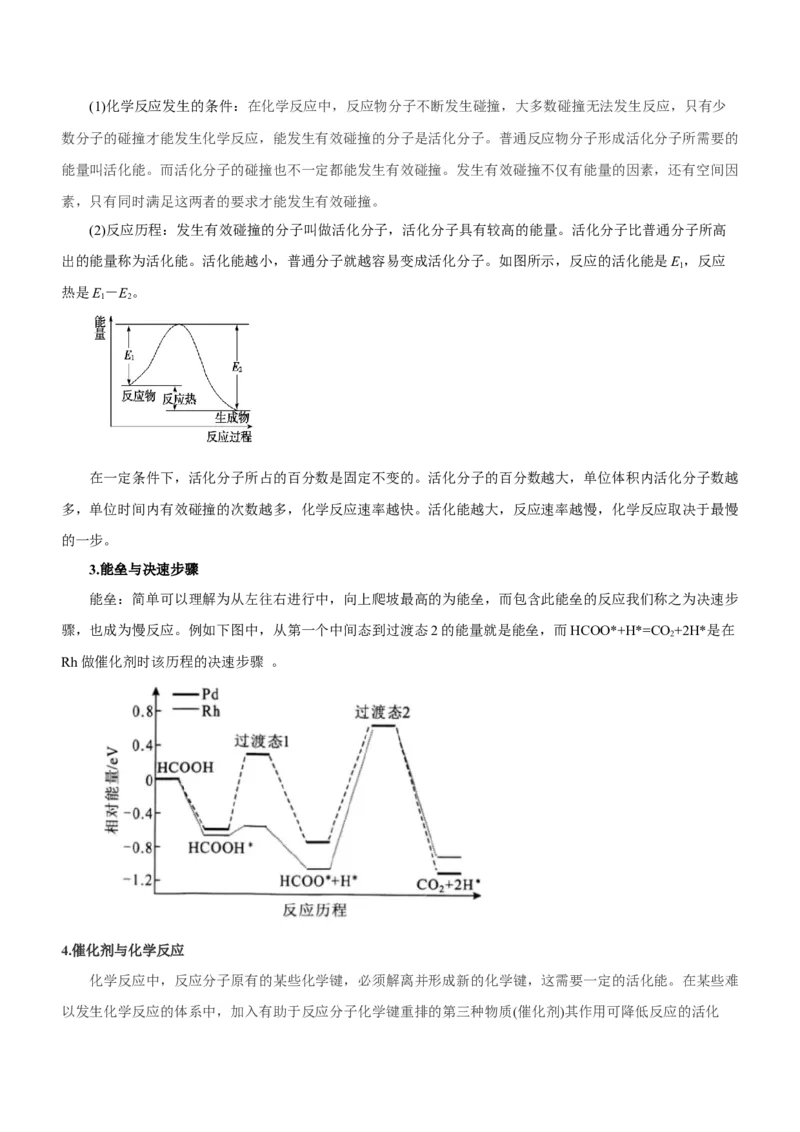
(2)反应历程:发生有效碰撞的分子叫做活化分子,活化分子具有较高的能量。活化分子比普通分子所高
出的能量称为活化能。活化能越小,普通分子就越容易变成活化分子。如图所示,反应的活化能是E,反应
1
热是E-E。
1 2
在一定条件下,活化分子所占的百分数是固定不变的。活化分子的百分数越大,单位体积内活化分子数越
多,单位时间内有效碰撞的次数越多,化学反应速率越快。活化能越大,反应速率越慢,化学反应取决于最慢
的一步。
3.能垒与决速步骤
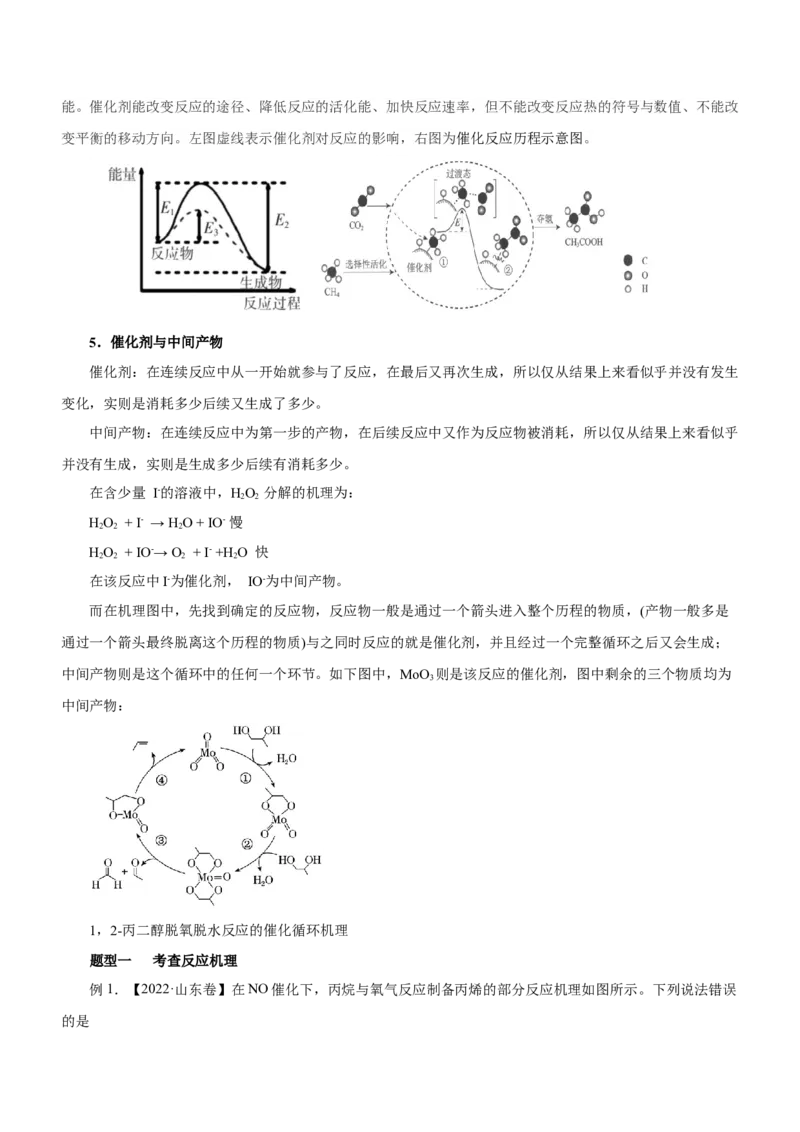
能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决速步
骤,也成为慢反应。例如下图中,从第一个中间态到过渡态2的能量就是能垒,而HCOO*+H*=CO +2H*是在
2
Rh做催化剂时该历程的决速步骤 。
4.催化剂与化学反应
化学反应中,反应分子原有的某些化学键,必须解离并形成新的化学键,这需要一定的活化能。在某些难
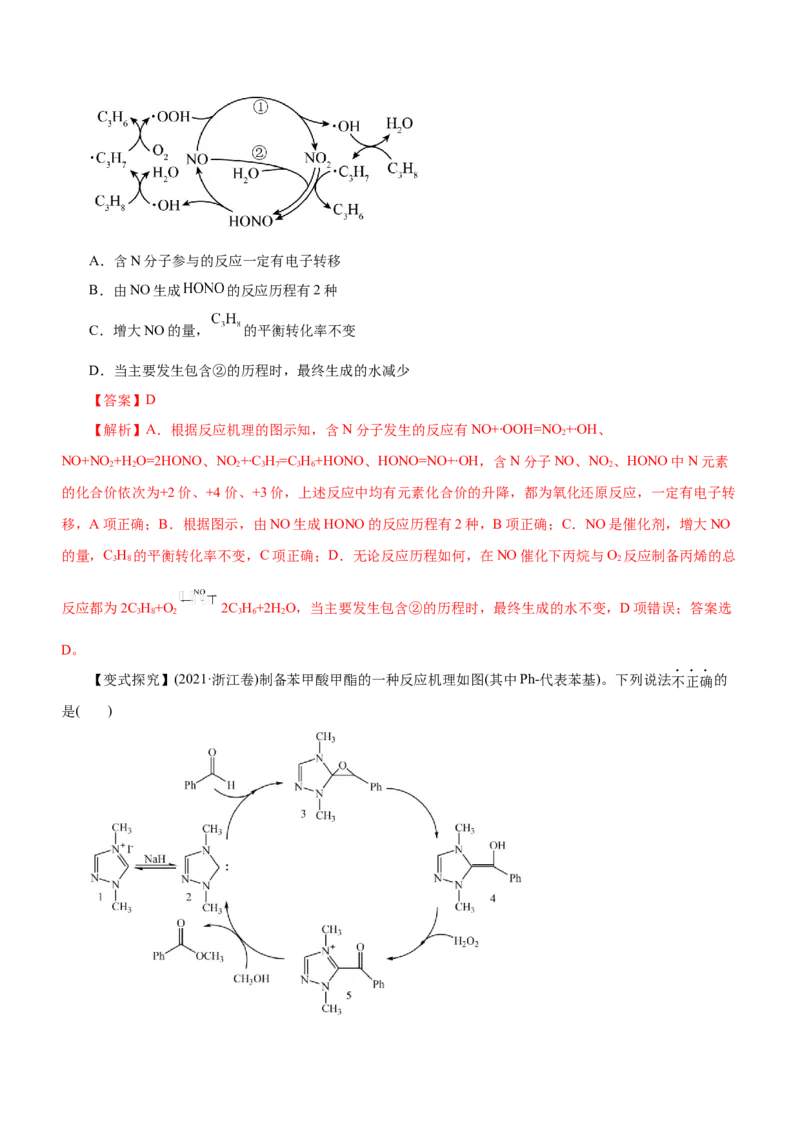
以发生化学反应的体系中,加入有助于反应分子化学键重排的第三种物质(催化剂)其作用可降低反应的活化能。催化剂能改变反应的途径、降低反应的活化能、加快反应速率,但不能改变反应热的符号与数值、不能改
变平衡的移动方向。左图虚线表示催化剂对反应的影响,右图为催化反应历程示意图。
5.催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似乎并没有发生
变化,实则是消耗多少后续又生成了多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看似乎
并没有生成,实则是生成多少后续有消耗多少。
在含少量 I-的溶液中,HO 分解的机理为:
2 2
HO + I- → H O + IO- 慢
2 2 2
HO + IO-→ O + I- +H O 快
2 2 2 2
在该反应中I-为催化剂, IO-为中间产物。
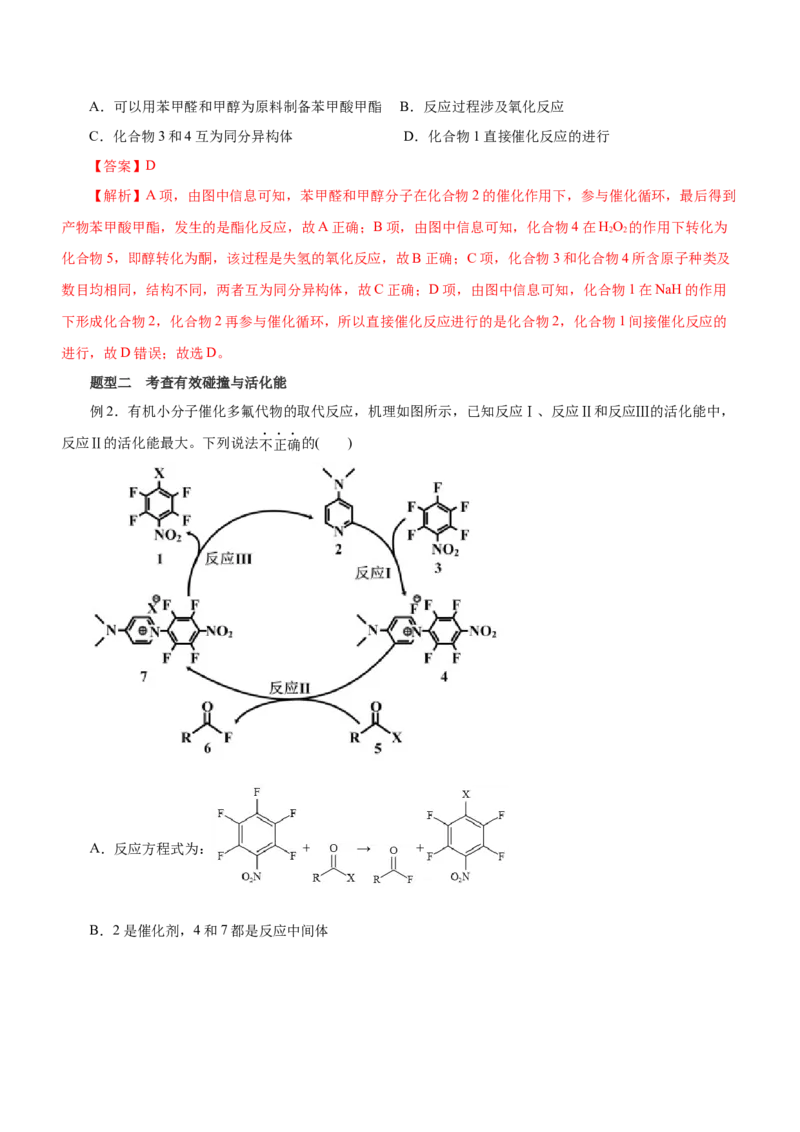
而在机理图中,先找到确定的反应物,反应物一般是通过一个箭头进入整个历程的物质,(产物一般多是
通过一个箭头最终脱离这个历程的物质)与之同时反应的就是催化剂,并且经过一个完整循环之后又会生成;
中间产物则是这个循环中的任何一个环节。如下图中,MoO 则是该反应的催化剂,图中剩余的三个物质均为
3
中间产物:
1,2-丙二醇脱氧脱水反应的催化循环机理
题型一 考查反应机理
例1.【2022·山东卷】在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误
的是A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A.根据反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO +∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中N元素
2 2 2 3 7 3 6 2
的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有电子转
移,A项正确;B.根据图示,由NO生成HONO的反应历程有2种,B项正确;C.NO是催化剂,增大NO
的量,C H 的平衡转化率不变,C项正确;D.无论反应历程如何,在NO催化下丙烷与O 反应制备丙烯的总
3 8 2
反应都为2C H+O 2C H+2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误;答案选
3 8 2 3 6 2
D。
【变式探究】(2021·浙江卷)制备苯甲酸甲酯的一种反应机理如图(其中Ph-代表苯基)。下列说法不正确的
是( )A.可以用苯甲醛和甲醇为原料制备苯甲酸甲酯 B.反应过程涉及氧化反应
C.化合物3和4互为同分异构体 D.化合物1直接催化反应的进行
【答案】D
【解析】A项,由图中信息可知,苯甲醛和甲醇分子在化合物2的催化作用下,参与催化循环,最后得到
产物苯甲酸甲酯,发生的是酯化反应,故A正确;B项,由图中信息可知,化合物4在HO 的作用下转化为
2 2
化合物5,即醇转化为酮,该过程是失氢的氧化反应,故B正确;C项,化合物3和化合物4所含原子种类及
数目均相同,结构不同,两者互为同分异构体,故C正确;D项,由图中信息可知,化合物1在NaH的作用
下形成化合物2,化合物2再参与催化循环,所以直接催化反应进行的是化合物2,化合物1间接催化反应的
进行,故D错误;故选D。
题型二 考查有效碰撞与活化能
例2.有机小分子催化多氟代物的取代反应,机理如图所示,已知反应Ⅰ、反应Ⅱ和反应Ⅲ的活化能中,
反应Ⅱ的活化能最大。下列说法不正确的( )
A.反应方程式为: + → +
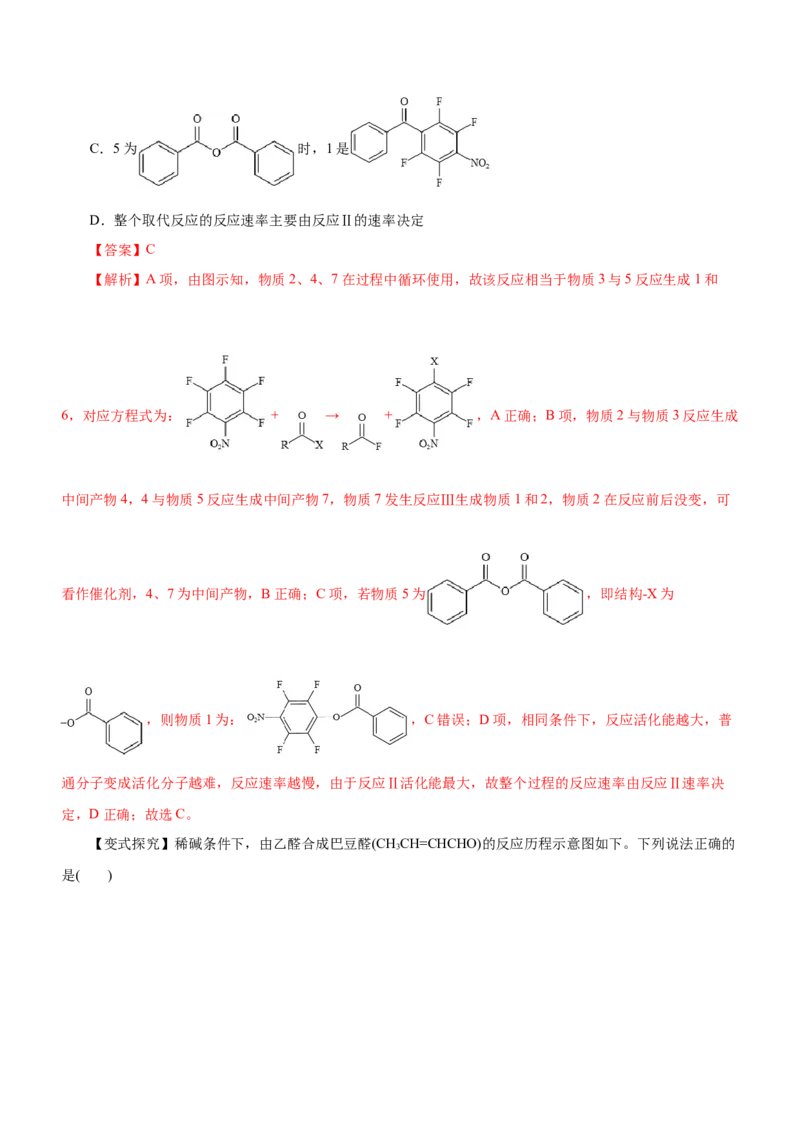
B.2是催化剂,4和7都是反应中间体C.5为 时,1是
D.整个取代反应的反应速率主要由反应Ⅱ的速率决定
【答案】C
【解析】A项,由图示知,物质2、4、7在过程中循环使用,故该反应相当于物质3与5反应生成1和
6,对应方程式为: + → + ,A正确;B项,物质2与物质3反应生成
中间产物4,4与物质5反应生成中间产物7,物质7发生反应Ⅲ生成物质1和2,物质2在反应前后没变,可
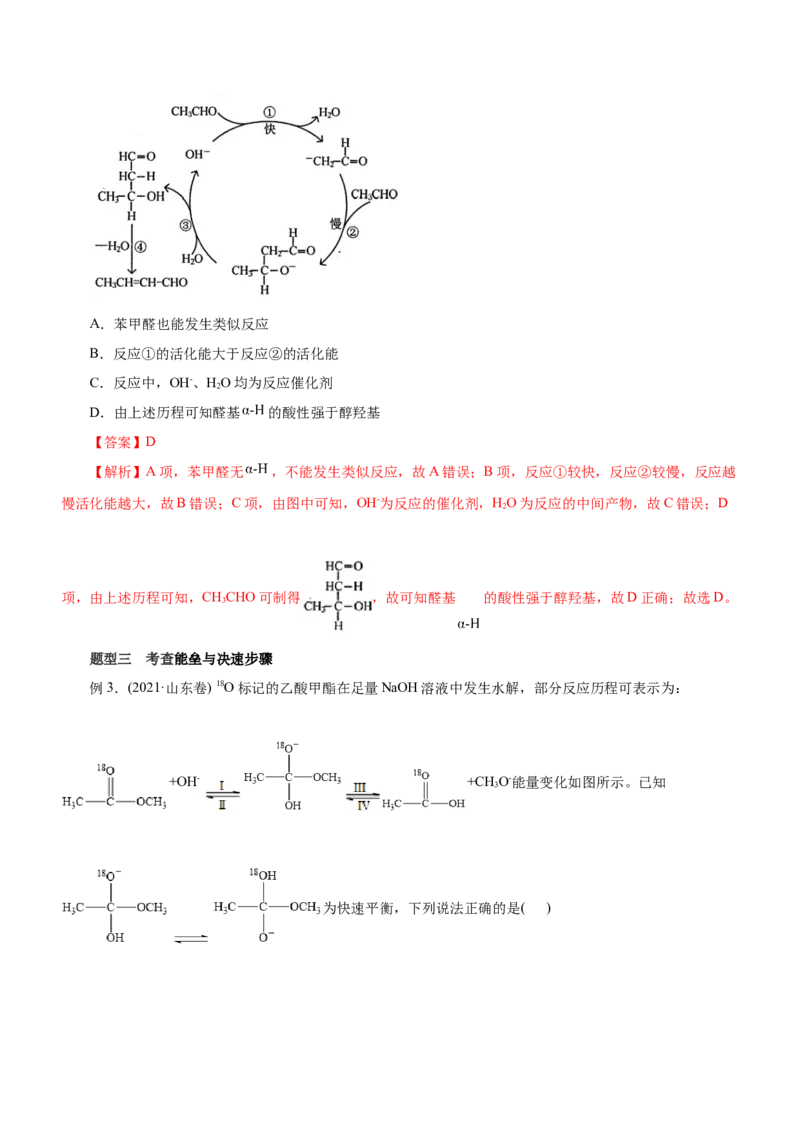
看作催化剂,4、7为中间产物,B正确;C项,若物质5为 ,即结构-X为
,则物质1为: ,C错误;D项,相同条件下,反应活化能越大,普
通分子变成活化分子越难,反应速率越慢,由于反应Ⅱ活化能最大,故整个过程的反应速率由反应Ⅱ速率决
定,D正确;故选C。
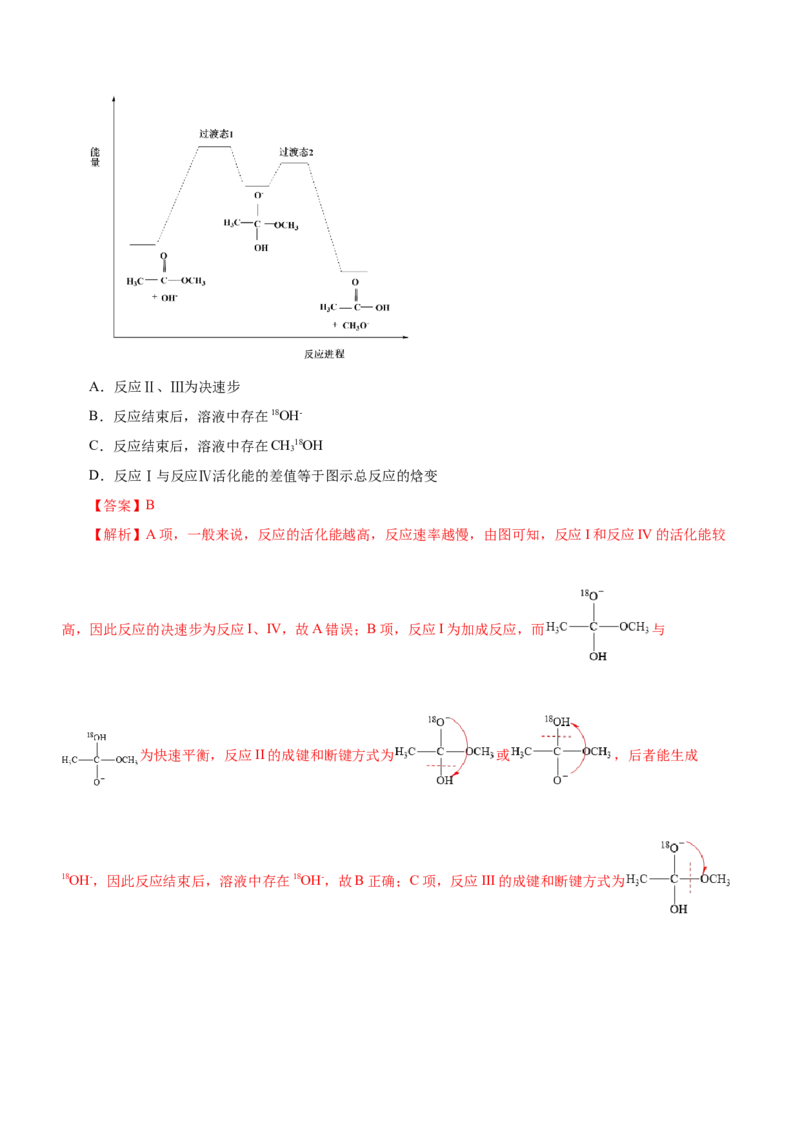
【变式探究】稀碱条件下,由乙醛合成巴豆醛(CHCH=CHCHO)的反应历程示意图如下。下列说法正确的
3
是( )A.苯甲醛也能发生类似反应
B.反应①的活化能大于反应②的活化能
C.反应中,OH-、HO均为反应催化剂
2
D.由上述历程可知醛基 的酸性强于醇羟基
【答案】D
【解析】A项,苯甲醛无 ,不能发生类似反应,故A错误;B项,反应①较快,反应②较慢,反应越
慢活化能越大,故B错误;C项,由图中可知,OH-为反应的催化剂,HO为反应的中间产物,故C错误;D
2
项,由上述历程可知,CHCHO可制得 ,故可知醛基 的酸性强于醇羟基,故D正确;故选D。
3
题型三 考查能垒与决速步骤
例3.(2021·山东卷) 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如图所示。已知
3
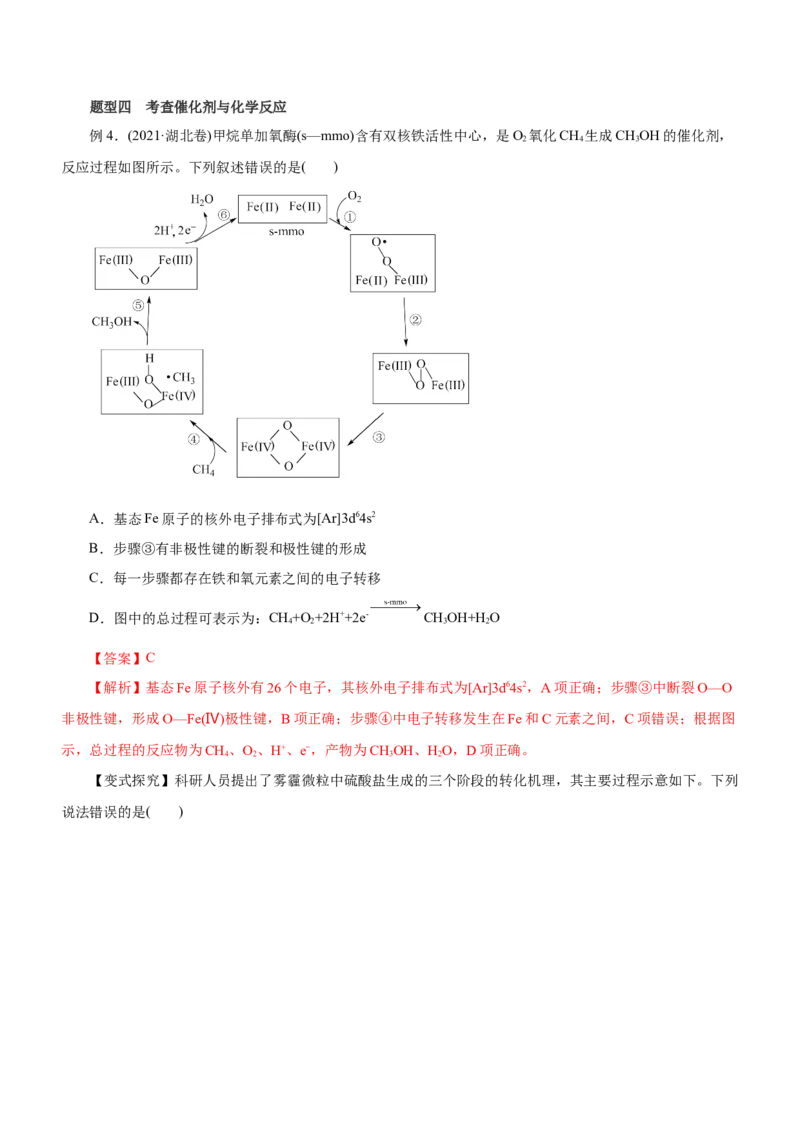
为快速平衡,下列说法正确的是( )A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【解析】A项,一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较
高,因此反应的决速步为反应I、IV,故A错误;B项,反应I为加成反应,而 与
为快速平衡,反应II的成键和断键方式为 或 ,后者能生成
18OH-,因此反应结束后,溶液中存在18OH-,故B正确;C项,反应III的成键和断键方式为或 ,因此反应结束后溶液中不会存在CH18H,故C错误;D项,该总反应对应反应物的总能
3
量高于生成物总能量,总反应为放热反应,因此 和CHO-的总能量与 和OH-的总
3
能量之差等于图示总反应的焓变,故D错误;故选B。
【变式探究】(2021·湖南卷)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量
的变化情况如图所示:
下列说法错误的是( )
A.该过程的总反应为HCOOH CO↑+H ↑
2 2
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】CD
【解析】A项,由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然后
又结合氢离子转化为氢气,所以化学方程式为HCOOH CO↑+H ↑,故A正确;B项,若氢离子浓度过
2 2
低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制加酸的电离,使甲酸根浓
度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减慢,故B正确;C项,由反应
机理可知,Fe在反应过程中,做催化剂,化合价没有发生变化,故C错误;D项,由反应进程可知,反应
Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,故D错误;故选CD。题型四 考查催化剂与化学反应
例4.(2021·湖北卷)甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O 氧化CH 生成CHOH的催化剂,
2 4 3
反应过程如图所示。下列叙述错误的是( )
A.基态Fe原子的核外电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
【答案】C
【解析】基态Fe原子核外有26个电子,其核外电子排布式为[Ar]3d64s2,A项正确;步骤③中断裂O—O
非极性键,形成O—Fe(Ⅳ)极性键,B项正确;步骤④中电子转移发生在Fe和C元素之间,C项错误;根据图
示,总过程的反应物为CH、O、H、e,产物为CHOH、HO,D项正确。
4 2 3 2
【变式探究】科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意如下。下列
说法错误的是( )A.第II、III阶段总反应的离子方程式为:SO -+H O+NO =HNO +H++SO2-
3 2 2 2 4
B.该过程中NO 为催化剂
2
C.第I阶段每1mo1氧化剂参加反应,转移电子数目为N
A
D.还原性SO 2->HNO
3 2
【答案】B
【解析】A项,根据图示,第II、III阶段是SO -、HO、NO 反应生成HNO、HSO - ,总反应的离子方
3 2 2 2 4
程式为SO -+H O+NO =HNO +H++SO2-,故A正确;B项,根据图示,该过程中NO 最终生成>,NO 是反应
3 2 2 2 4 2 2
物,故B错误;C项,根据图示,第I阶段每1个NO 得1个电子生成NO -,每1mo1氧化剂参加反应,转移
2 2
电子数目为N ,故C正确;D项,根据图示,总反应为SO 2-+H O+2NO =2HNO + SO 2-,SO 2-是还原剂、>是
A 3 2 2 2 4 3
还原产物,还原性SO 2->HNO,故D正确;故选B。
3 2