文档内容
专题 13 工艺流程综合题
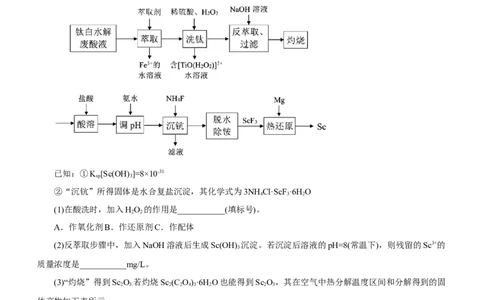
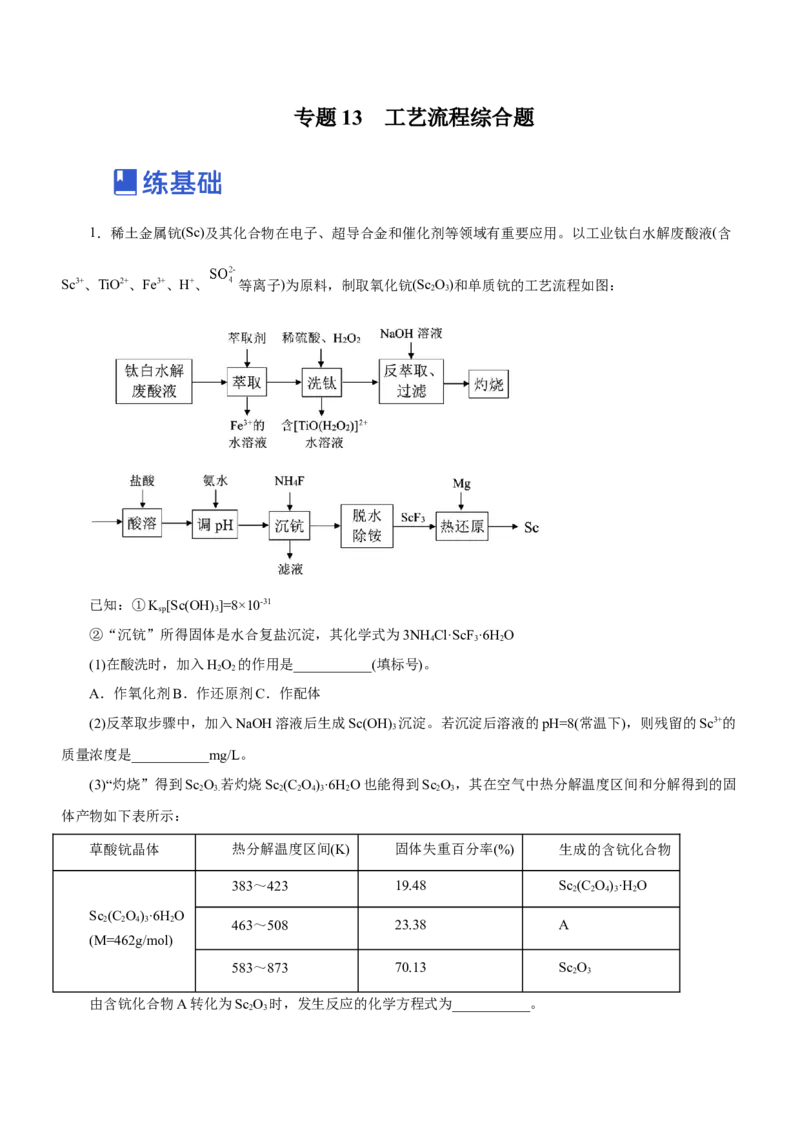
1.稀土金属钪(Sc)及其化合物在电子、超导合金和催化剂等领域有重要应用。以工业钛白水解废酸液(含
Sc3+、TiO2+、Fe3+、H+、 等离子)为原料,制取氧化钪(Sc O)和单质钪的工艺流程如图:
2 3
已知:①K [Sc(OH) ]=8×10-31
sp 3
②“沉钪”所得固体是水合复盐沉淀,其化学式为3NH Cl·ScF ·6H O
4 3 2
(1)在酸洗时,加入HO 的作用是___________(填标号)。
2 2
A.作氧化剂B.作还原剂C.作配体
(2)反萃取步骤中,加入NaOH溶液后生成Sc(OH) 沉淀。若沉淀后溶液的pH=8(常温下),则残留的Sc3+的
3
质量浓度是___________mg/L。
(3)“灼烧”得到Sc O 若灼烧Sc (C O)·6H O也能得到Sc O,其在空气中热分解温度区间和分解得到的固
2 3. 2 2 4 3 2 2 3
体产物如下表所示:
草酸钪晶体 热分解温度区间(K) 固体失重百分率(%) 生成的含钪化合物
383~423 19.48 Sc (C O)·H O
2 2 4 3 2
Sc (C O)·6H O
2 2 4 3 2 463~508 23.38 A
(M=462g/mol)
583~873 70.13 Sc O
2 3
由含钪化合物A转化为Sc O 时,发生反应的化学方程式为___________。
2 3(4)含钪元素的微粒与pF[pF=-lgc(F-)]、pH的关系如图所示,用氨水调节溶液的pH最好小于
___________,“沉钪”所得滤液中c(F-)应大于___________mol·L-1。
(5)传统制备ScF 的方法是先得到ScF·6H O,再高温脱水得到ScF,但所得ScF 通常含有ScOF杂质,原
3 3 2 3 3
因是___________(用化学方程式表示)。该流程中,“脱水除铵”可制得高纯度ScF,原因是___________。
3
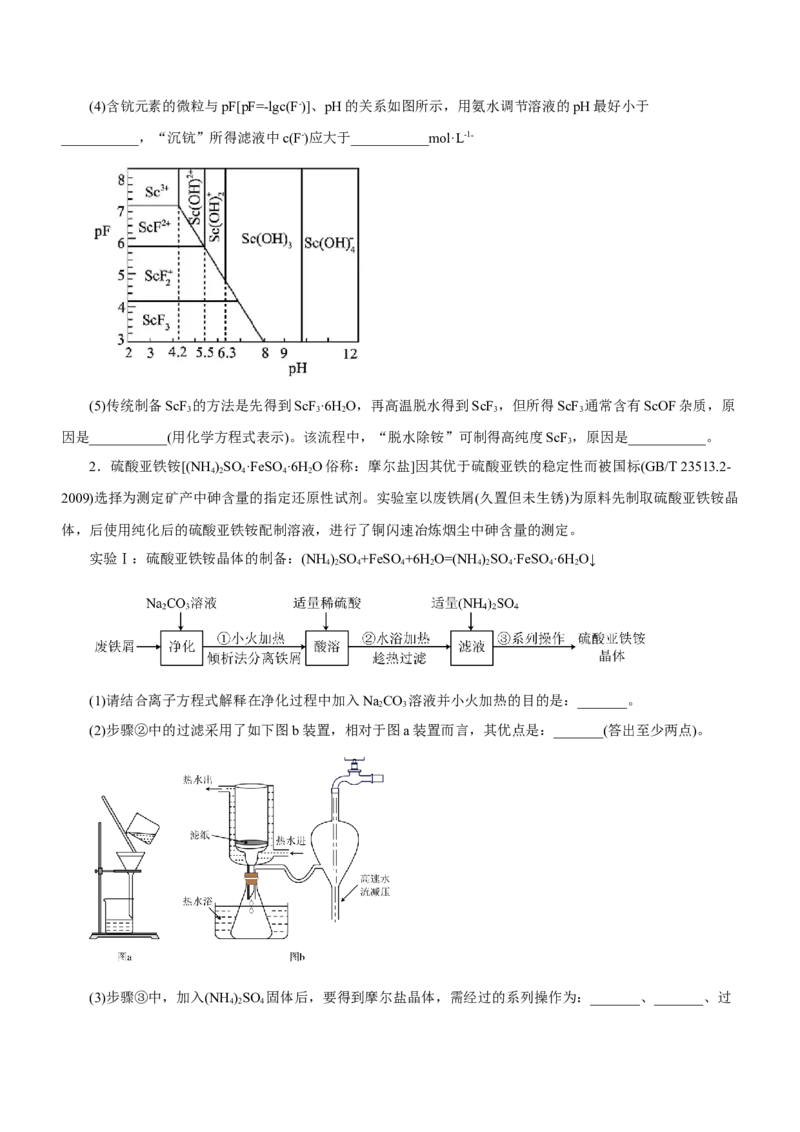
2.硫酸亚铁铵[(NH )SO ·FeSO ·6H O俗称:摩尔盐]因其优于硫酸亚铁的稳定性而被国标(GB/T 23513.2-
4 2 4 4 2
2009)选择为测定矿产中砷含量的指定还原性试剂。实验室以废铁屑(久置但未生锈)为原料先制取硫酸亚铁铵晶
体,后使用纯化后的硫酸亚铁铵配制溶液,进行了铜闪速冶炼烟尘中砷含量的测定。
实验Ⅰ:硫酸亚铁铵晶体的制备:(NH )SO +FeSO+6H O=(NH )SO ·FeSO ·6H O↓
4 2 4 4 2 4 2 4 4 2
(1)请结合离子方程式解释在净化过程中加入NaCO 溶液并小火加热的目的是:_______。
2 3
(2)步骤②中的过滤采用了如下图b装置,相对于图a装置而言,其优点是:_______(答出至少两点)。
(3)步骤③中,加入(NH )SO 固体后,要得到摩尔盐晶体,需经过的系列操作为:_______、_______、过
4 2 4滤、洗涤、干燥;
实验Ⅱ:0.1000 mol/L硫酸亚铁铵标准溶液的配制
准确称取3.92 g硫酸亚铁铵晶体按下图步骤配成100 mL溶液。
(4)该实验中使用到的仪器A的名称为_______;若在上图①过程中晶体溶于水(吸热过程)后就立即转移至
仪器A中,则上述操作会导致配得溶液浓度_______(填“偏高”、“偏低”或“无影响”)。
实验Ⅲ:铜闪速冶炼烟尘中砷的测定
用硝酸、氟化铵和溴水溶解烟尘样品2.0 g,通过系列反应把溶液中的砷离子还原为单质砷。用过量的
0.1000 mol/L酸性KCr O 标准溶液25.00 mL溶解并氧化单质砷为 ,用0.1000 mol/L的硫酸亚铁铵标准
2 2 7
溶液滴定过量的KCr O。
2 2 7
(5)请写出KCr O 氧化单质砷为 的离子反应方程式_______。
2 2 7
(6)若终点时消耗硫酸亚铁铵标准液30.00 mL,则烟尘样品中砷的质量分数为_______。
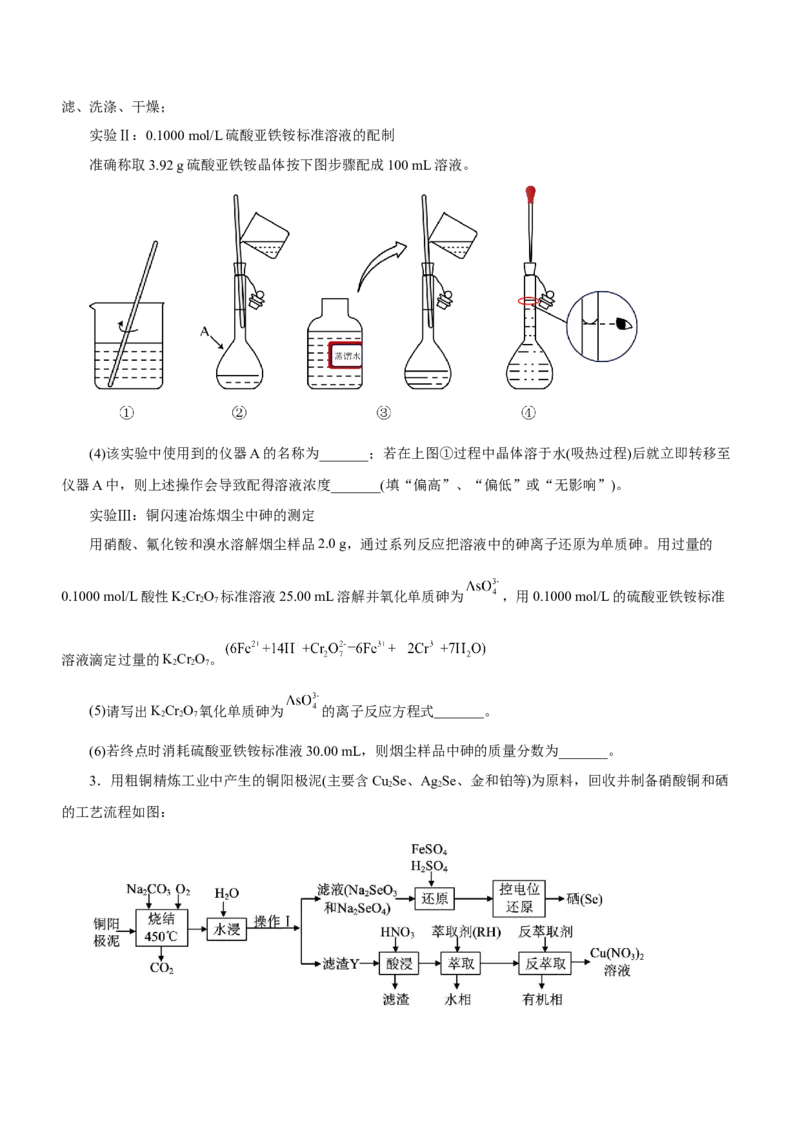
3.用粗铜精炼工业中产生的铜阳极泥(主要含Cu Se、Ag Se、金和铂等)为原料,回收并制备硝酸铜和硒
2 2
的工艺流程如图:(1)工业上,高压氧气与铜阳极泥采用“逆流”的方式通入,其目的是_______。“烧结”时会发生多个反
应,写出其中Cu Se烧结时生成Cu O、NaSeO 反应方程式_______。
2 2 2 3
(2)在实验室,操作Ⅰ的名称为_______。
(3)滤渣Y的成分有Ag O、_______(填化学式,下同);已知萃取与反萃取原理为:2RH+Cu2+
2
R Cu+2H+,则“反萃取”时反萃取剂最好选用_______溶液。
2
(4)Na SeO 中 的空间构型为_______;常温下,HSeO 的K =1.0×10-3,K =1.0×10-7;当常温下溶液
2 4 2 3 a1 a2
的pH=4.5时, 为_______。
(5)“控电位还原”是指在一定电压下,电位高的氧化剂优先被还原,电位低的氧化剂保留在溶液中,以达
到硒与杂质金属的分离;酸性环境下,一些氧化剂的电位如下表(A/B:A代表氧化剂,B代表还原产物)。
名称 Cu2+/Cu Fe2+/Fe Fe3+/Fe2+
电
0.345 -0.440 0.770 0.740
位/V
则 、Fe3+和Cu2+氧化性由强到弱的顺序为_______,在控电位还原时 还原反应(半反应)式为
_______。
4.工业废渣中 的综合利用。
(1)用工业钢渣处理酸性废水
工业钢渣主要含 ,还含有 、 、 、 等。工
业钢渣加水后搅拌得钢渣浆液,向钢渣浆液中逐渐加入硫酸溶液(模拟酸性废水)酸化,浆液pH以及浸出液中
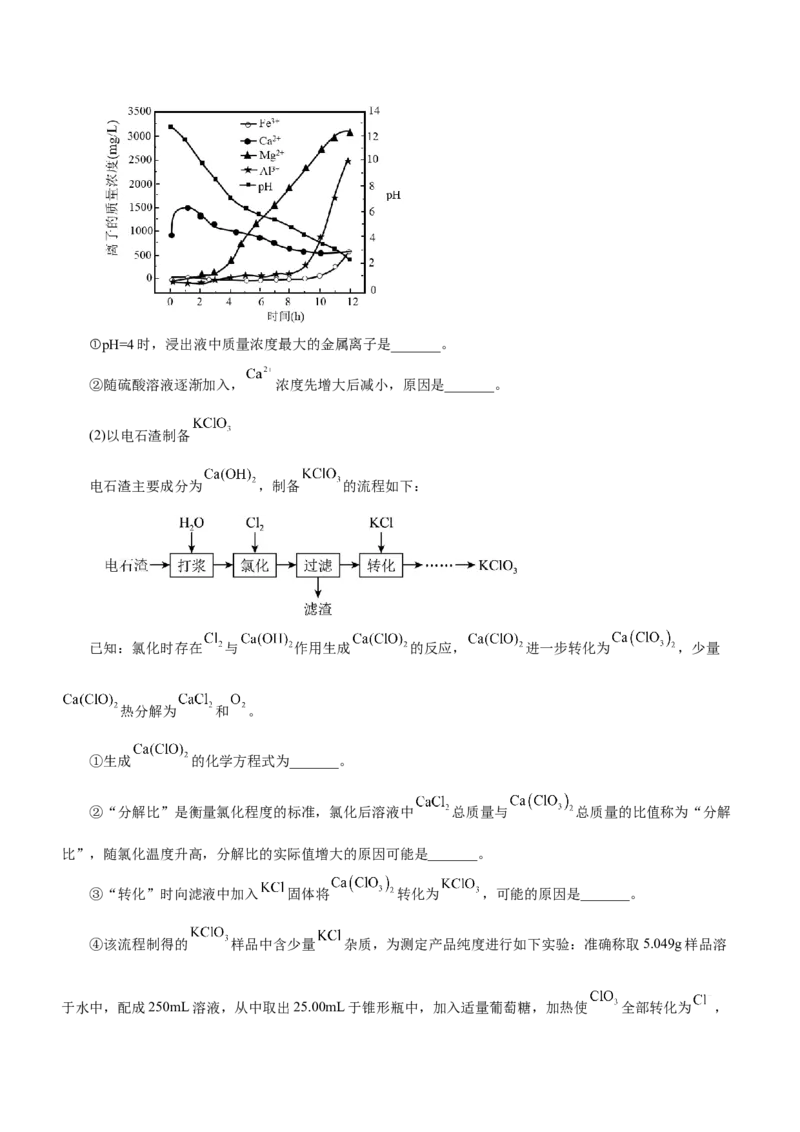
金属离子的质量浓度随时间变化情况如图所示。①pH=4时,浸出液中质量浓度最大的金属离子是_______。
②随硫酸溶液逐渐加入, 浓度先增大后减小,原因是_______。
(2)以电石渣制备
电石渣主要成分为 ,制备 的流程如下:
已知:氯化时存在 与 作用生成 的反应, 进一步转化为 ,少量
热分解为 和 。
①生成 的化学方程式为_______。
②“分解比”是衡量氯化程度的标准,氯化后溶液中 总质量与 总质量的比值称为“分解
比”,随氯化温度升高,分解比的实际值增大的原因可能是_______。
③“转化”时向滤液中加入 固体将 转化为 ,可能的原因是_______。
④该流程制得的 样品中含少量 杂质,为测定产品纯度进行如下实验:准确称取5.049g样品溶
于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使 全部转化为 ,加入少量 溶液作指示剂,用 溶液进行滴定至终点,消耗 溶液体积 。
计算 样品的纯度。(请写出计算过程)_______
5.金属钪 可用作宇航材料、火箭和飞机的制造材料,氧化钪 可提高计算机记忆元件性能。赤
泥中含有丰富的钪元素,另含有 等氧化物。一种从赤泥中提取氧化钪的工艺流程如
图所示( 是一种磷酸酯萃取剂)。
回答下列问题:
(1)写出赤泥经盐酸处理后所得“浸渣”的一种用途:________________________。
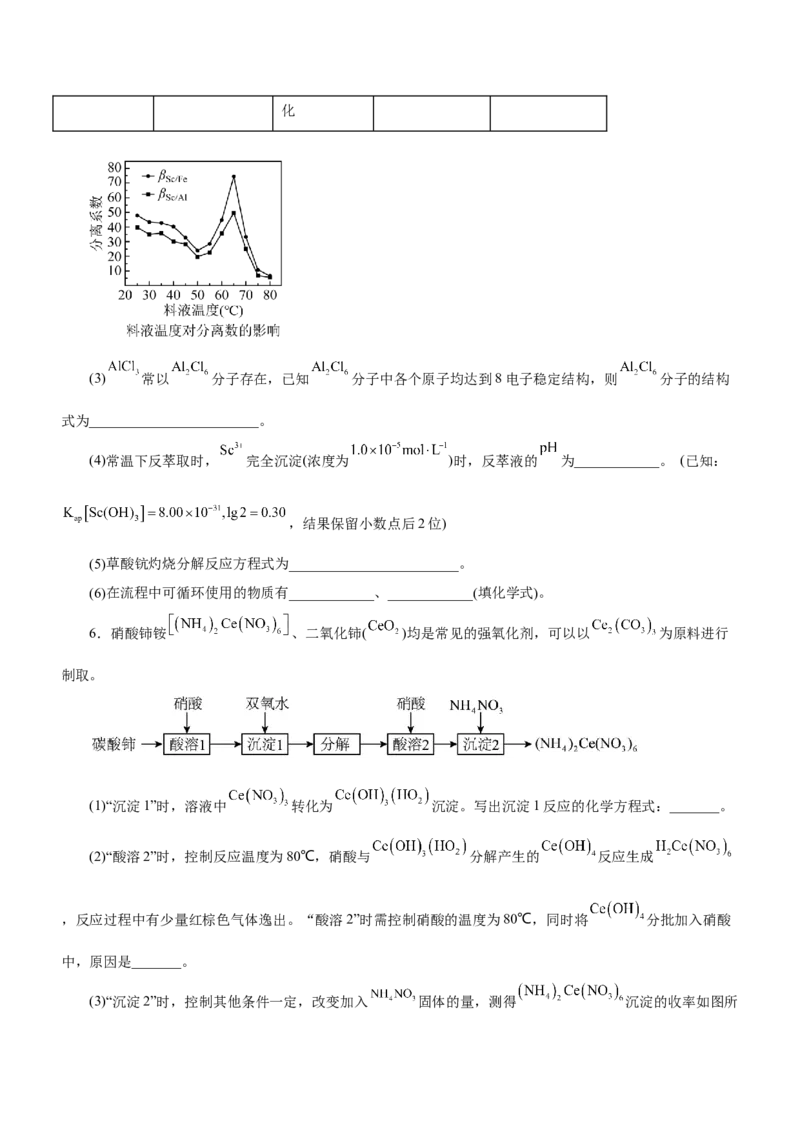
(2) 萃取浸出液,其浓度、料液温度对萃取率的影响如下所示,萃取时 最佳浓度及料液温度分别
为____________、____________。
浓度对萃取率的影响
试验编 分相情
浓度/% 钪萃取率/% 铁萃取率/%
号 况
1-1 1 分相快 90.76 15.82
分相容
1-2 2 91.53 19.23
易
分相容
1-3 3 92.98 13.56
易
有第三
1-4 4 90.69 30.12
相
1-5 5 91.74 39.79
轻微乳化
(3) 常以 分子存在,已知 分子中各个原子均达到8电子稳定结构,则 分子的结构
式为________________________。
(4)常温下反萃取时, 完全沉淀(浓度为 )时,反萃液的 为____________。 (已知:
,结果保留小数点后2位)
(5)草酸钪灼烧分解反应方程式为________________________。
(6)在流程中可循环使用的物质有____________、____________(填化学式)。
6.硝酸铈铵 、二氧化铈( )均是常见的强氧化剂,可以以 为原料进行
制取。
(1)“沉淀1”时,溶液中 转化为 沉淀。写出沉淀1反应的化学方程式:_______。
(2)“酸溶2”时,控制反应温度为80℃,硝酸与 分解产生的 反应生成
,反应过程中有少量红棕色气体逸出。“酸溶2”时需控制硝酸的温度为80℃,同时将 分批加入硝酸
中,原因是_______。
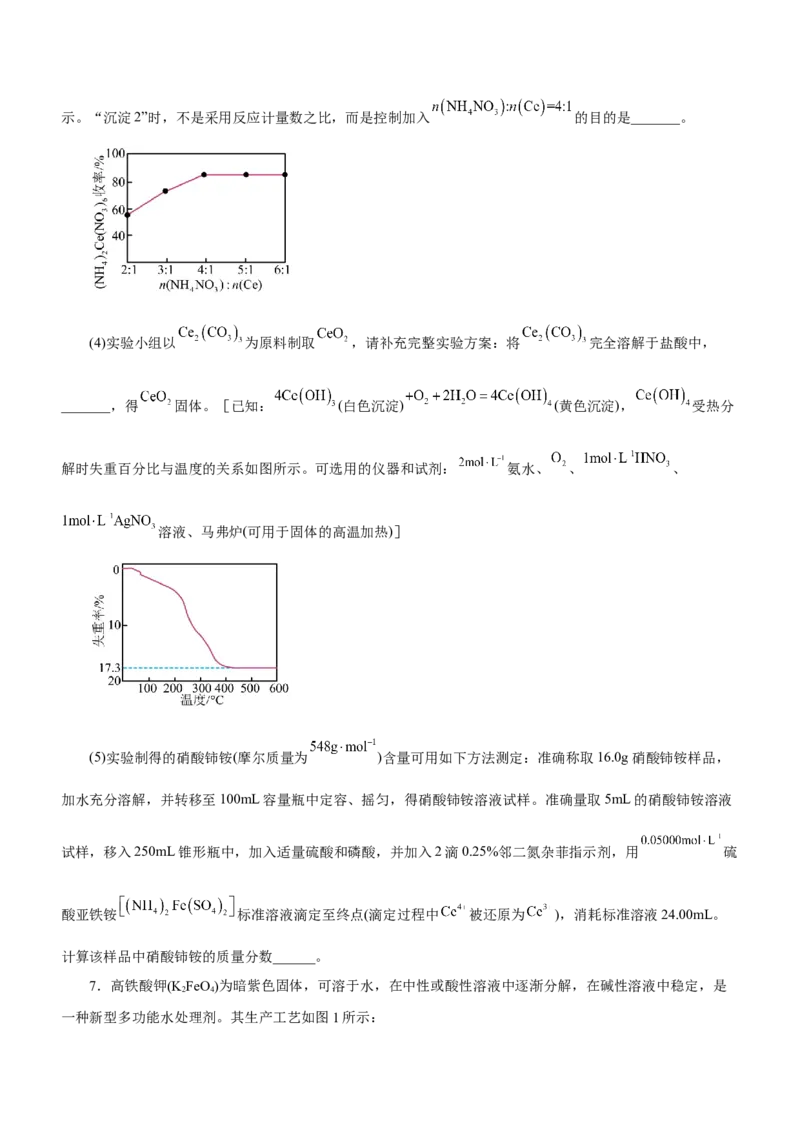
(3)“沉淀2”时,控制其他条件一定,改变加入 固体的量,测得 沉淀的收率如图所示。“沉淀2”时,不是采用反应计量数之比,而是控制加入 的目的是_______。
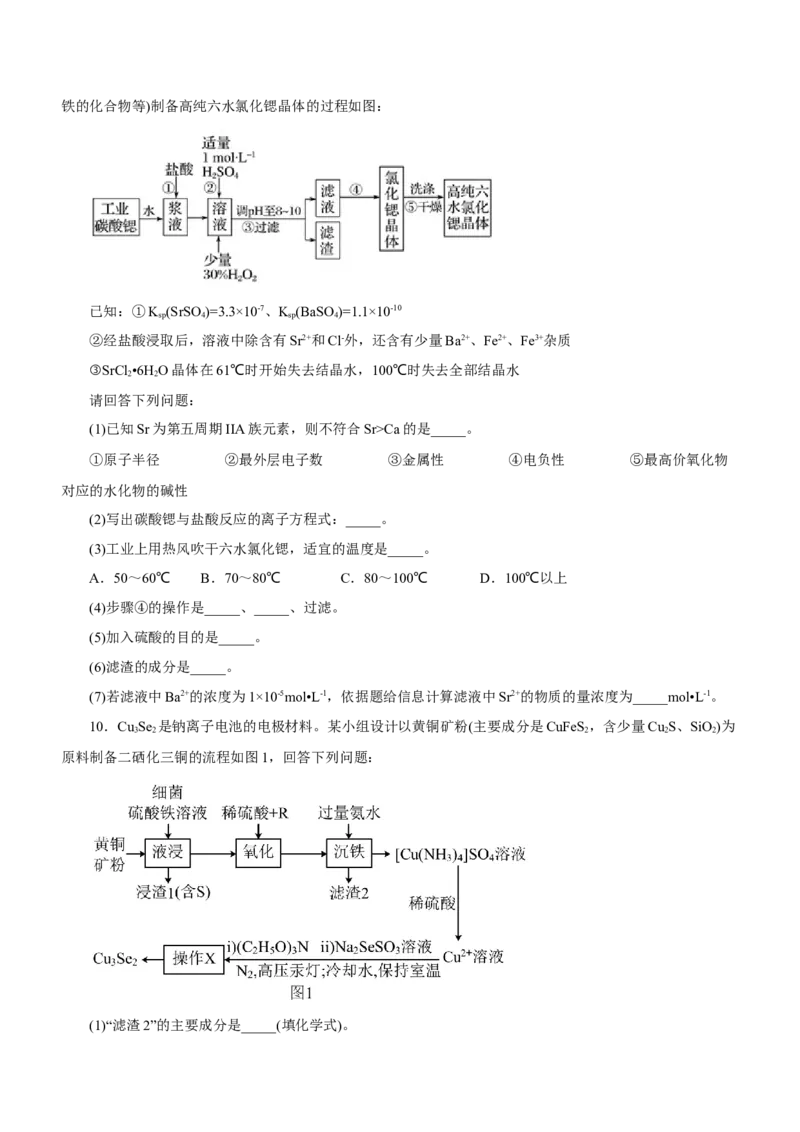
(4)实验小组以 为原料制取 ,请补充完整实验方案:将 完全溶解于盐酸中,
_______,得 固体。[已知: (白色沉淀) (黄色沉淀), 受热分
解时失重百分比与温度的关系如图所示。可选用的仪器和试剂: 氨水、 、 、
溶液、马弗炉(可用于固体的高温加热)]
(5)实验制得的硝酸铈铵(摩尔质量为 )含量可用如下方法测定:准确称取16.0g硝酸铈铵样品,
加水充分溶解,并转移至100mL容量瓶中定容、摇匀,得硝酸铈铵溶液试样。准确量取5mL的硝酸铈铵溶液
试样,移入250mL锥形瓶中,加入适量硫酸和磷酸,并加入2滴0.25%邻二氮杂菲指示剂,用 硫
酸亚铁铵 标准溶液滴定至终点(滴定过程中 被还原为 ),消耗标准溶液24.00mL。
计算该样品中硝酸铈铵的质量分数______。
7.高铁酸钾(K FeO)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是
2 4
一种新型多功能水处理剂。其生产工艺如图1所示:回答下列问题:
(1)Fe(NO ) 中 的空间结构名称为_______氮原子的杂化轨道类型为_______
3 3
(2)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl 反应生成NaClO,取某温度下反应液,
2 3
测得ClO-与 的物质的量浓度之比是2∶1,则Cl 与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子
2
的物质的量之比为_______。
(3)反应③的离子方程式为_______,制备时,两溶液混合的操作为_______。
(4)往溶液II中加入饱和KOH溶液得到湿产品的原因是_______。该工艺流程中可循环使用的物质是
_______(填化学式)。
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:阳极的电极反应式为_______。
8.磷酸铁( )主要用于制造磷酸铁锂电池材料。以硫铁矿烧渣(主要成分是 ,含少量 、
和 )为原料制备磷酸铁的工艺流程如下:
(1)焙烧。将硫铁矿烧渣与蔗糖( )一起焙烧,可生成FeO与 。写出焙烧时 所发生反应的化学方程式:_______。
(2)还原。将焙烧后的固体用稀硫酸浸取,所得溶液主要含 ,还含少量 和 。向
酸浸后所得溶液中加入 固体,充分搅拌至溶液中 全部被还原并生成 。理论上完全反应需要消耗
的 _______。
(3)制备 。向 溶液中加入足量的30% 溶液与 溶液,控制溶液的pH约为
1.5,充分反应可得 沉淀。
①写出生成 反应的化学方程式:_______。
②反应 的平衡常数 _______。[已知: ,
,
, ]
(4)其他条件一定,制备 时测得Fe的有效转化率 与溶液pH的关系如图所示。
①pH<1.5时,pH越大,Fe的有效转化率越大的原因是_______。
②pH>1.5时,pH越大,Fe的有效转化率越低的原因是_______。
9.高纯六水氯化锶晶体(SrCl •6H O)具有很高的经济价值,工业上用碳酸锶(SrCO )粉为原料(含少量钡和
2 2 3铁的化合物等)制备高纯六水氯化锶晶体的过程如图:
已知:①K (SrSO )=3.3×10-7、K (BaSO)=1.1×10-10
sp 4 sp 4
②经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+、Fe2+、Fe3+杂质
③SrCl •6H O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水
2 2
请回答下列问题:
(1)已知Sr为第五周期IIA族元素,则不符合Sr>Ca的是_____。
①原子半径 ②最外层电子数 ③金属性 ④电负性 ⑤最高价氧化物
对应的水化物的碱性
(2)写出碳酸锶与盐酸反应的离子方程式:_____。
(3)工业上用热风吹干六水氯化锶,适宜的温度是_____。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(4)步骤④的操作是_____、_____、过滤。
(5)加入硫酸的目的是_____。
(6)滤渣的成分是_____。
(7)若滤液中Ba2+的浓度为1×10-5mol•L-1,依据题给信息计算滤液中Sr2+的物质的量浓度为_____mol•L-1。
10.Cu Se 是钠离子电池的电极材料。某小组设计以黄铜矿粉(主要成分是CuFeS,含少量Cu S、SiO)为
3 2 2 2 2
原料制备二硒化三铜的流程如图1,回答下列问题:
(1)“滤渣2”的主要成分是_____(填化学式)。(2)从绿色化学角度考虑,纯净物R宜选择______(填化学式)。
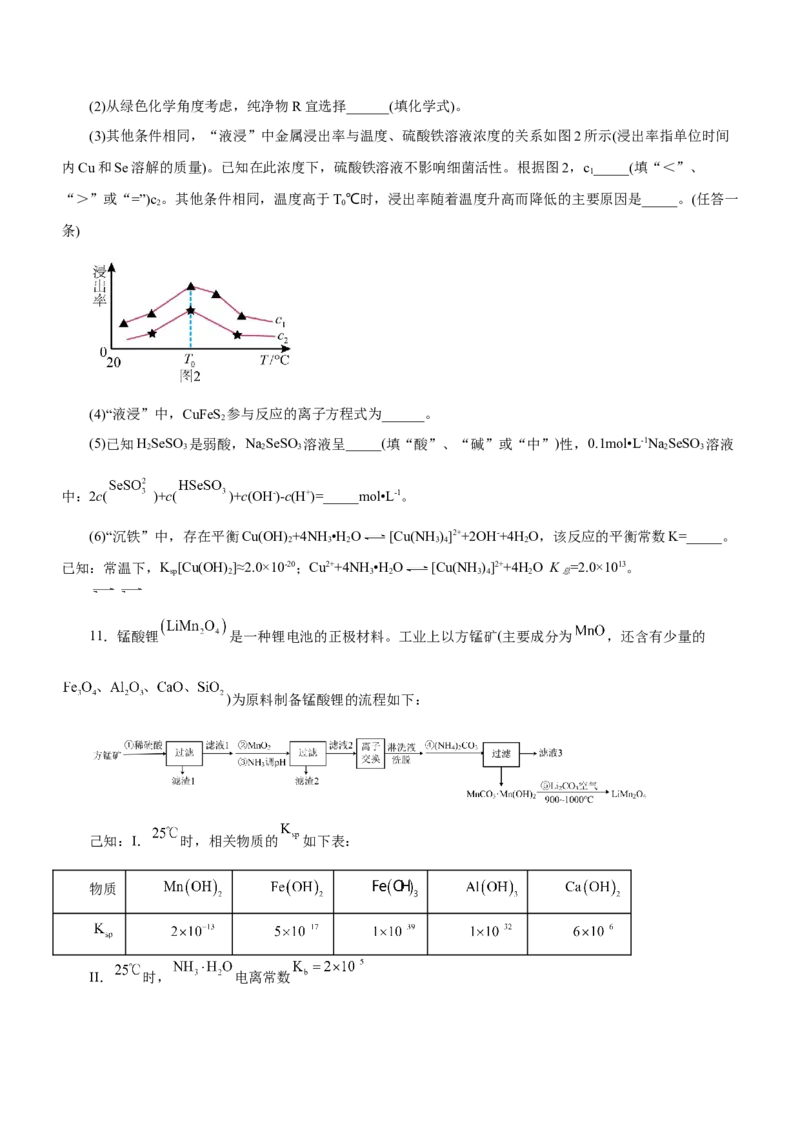
(3)其他条件相同,“液浸”中金属浸出率与温度、硫酸铁溶液浓度的关系如图2所示(浸出率指单位时间
内Cu和Se溶解的质量)。已知在此浓度下,硫酸铁溶液不影响细菌活性。根据图2,c_____(填“<”、
1
“>”或“=”)c。其他条件相同,温度高于T℃时,浸出率随着温度升高而降低的主要原因是_____。(任答一
2 0
条)
(4)“液浸”中,CuFeS 参与反应的离子方程式为______。
2
(5)已知HSeSO 是弱酸,NaSeSO 溶液呈_____(填“酸”、“碱”或“中”)性,0.1mol•L-1NaSeSO 溶液
2 3 2 3 2 3
中:2c( )+c( )+c(OH-)-c(H+)=_____mol•L-1。
(6)“沉铁”中,存在平衡Cu(OH) +4NH•H O [Cu(NH )]2++2OH-+4H O,该反应的平衡常数K=_____。
2 3 2 3 4 2
已知:常温下,K [Cu(OH) ]≈2.0×10-20;Cu2++4NH•H O [Cu(NH )]2++4H O K =2.0×1013。
sp 2 3 2 3 4 2 总
11.锰酸锂 是一种锂电池的正极材料。工业上以方锰矿(主要成分为 ,还含有少量的
)为原料制备锰酸锂的流程如下:
己知:I. 时,相关物质的 如下表:
物质
II. 时, 电离常数III.离子浓度低于 时即为沉淀完全
回答下列问题:
(1)写出步骤①溶于稀疏酸时杂质 反应的离子方程式___________。
(2)滤渣1的成分是_____(填化学式);步骤②加入 的目的是____。
(3)步骤③加入 目的是除去杂质离子,若溶液中 浓度为 ,要确保杂质离子沉淀完全,同
时不降低产品产率,步骤③调控 的范围应该为_______。反应
的平衡常数 ________。
(4)“离子交换”步骤和“洗脱”过程是利用反应: ( 是氢型交换树
脂)的平衡移动将 进一步提纯,为了提高洗脱效率,又不引入其他杂质,淋洗液应选用_____。
(5)步骤④反应未见气体生成,则该反应留存在滤液3中的产物有___________(填化学式)。
(6)步骤⑤反应的化学方程式为___________。
12.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·6H O):
4 2
常温下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L−1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10−5 mol·L−1)的
8.7 4.7 3.2 9.0
pH
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是_______。
(2)为回收金属,向“滤液①”通入足量CO,写出反应生成沉淀的离子方程式_______。“滤液②”中含
2有的金属离子是_______。
(3)若工艺流程改为先“调pH”后“转化”,即 ,“滤液③”中可能含有的杂
质离子为_______。
(4)如果“转化”后的溶液中Ni2+浓度为1.0 mol·L−1,则“调pH”应控制的pH范围是_______。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子
方程式_______。
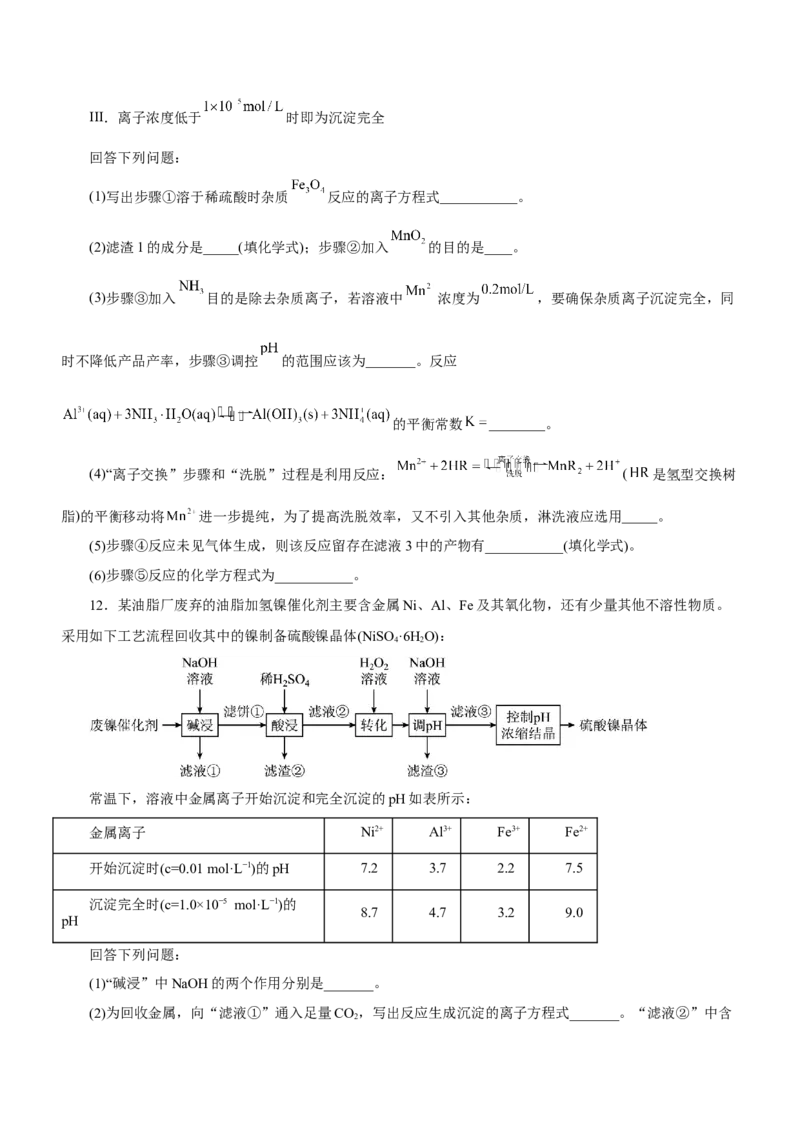
(6)NiSO 质量分数随温度变化情况如图所示,已知当pH控制在3.0时,结晶得到NiSO ·6H O晶体外观最
4 4 2
符合要求。
请补充由滤液③得到NiSO ·6H O晶体的实验方案:_______,得到NiSO ·6H O晶体。(实验中须使用的试
4 2 4 2
剂:1 mol·L−1 HSO ,乙醇)
2 4
13.工业上以黄铁矿(主要成分为FeS)为原料来制备硫酸,产生的含二氧化硫尾气和炉渣(主要成分为
2
Fe O)经过资源化利用可减轻对环境的污染。
2 3
(1)工业制硫酸。沸腾炉中煅烧黄铁矿发生反应的化学方程式为_______,当有6 mol SO 生成时,转移电
2
子_______mol。
(2)生产焦亚硫酸钠(Na SO)。NaSO 常用作食品的抗氧化剂,由NaHSO 过饱和溶液经结晶脱水制得,
2 2 5 2 2 5 3
生产工艺流程如下:
已知:HSO 电离常数分别为K =1.5×10-2、K =1.0×10-7
2 3 a1 a2
HCO 电离常数分别为K =4.3×10-7、K =5.6×10-11
2 3 a1 a2生成NaSO 的化学方程式为2NaHSO=Na SO+H O
2 2 5 3 2 2 5 2
①I中生成一种盐并放出气体,反应的离子方程式为_______。
②工艺中加入NaCO 固体,并再次充入SO 的目的是_______。
2 3 2
③因为NaSO 具有还原性,导致产品中不可避免地存在NaSO ,检验其中是否含有 的方法是
2 2 5 2 4
_______。
(3)由炉渣制备还原铁粉并分析纯度。利用CO与炉渣反应得到还原铁粉,得到的产品可用KCr O 滴定分
2 2 7
析法测定纯度。实验步骤如下:称取0.2240 g样品,加入过量稀硫酸充分溶解,用3.000×10−2 mol·L−1 KCr O
2 2 7
溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗KCr O 溶液20.00 mL,计算该样品中还
2 2 7
原铁粉的质量分数(写出计算过程)_______。
14.中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银铜合金切割废料中回收银并制备铜化
工产品的工艺流程如图所示:
已知: 和 分解温度分别为 和 。
(1)在电解精炼银时,阳极材料为_______。
(2)加快渣料(含少量银)溶于稀 的速率的措施为_______(写出两种)。
(3)滤渣A与稀 反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀 反应的离子方程式为
_______。
(4)过滤操作需要的玻璃仪器除烧杯外还有_______。
(5)固体B的组成为_______;在生成固体B的过程中,需控制 溶液的加入量,若 过量,则因
过量引起的反应的离子方程式为_______。
15.一种从铋冶炼浸渣(浸渣中的铅多数以硫酸铅的形态存在,少量以氧化铅、碳酸铅的形态存在)为原料
生产三盐基硫酸铅( )的工艺流程如图所示。已知常温下, , , ,
回答下列问题:
(1)常温下, 的电离平衡常数 _______。
(2)写出转化过程 发生反应的化学方程式_______,Pb的转化率随着 用量的增加而增加,
醋酸可以促进硫酸铅溶解,但实验表明:Pb的转化率随醋酸用量的增加而减少,这是由于_______。
(3)测得滤液1中 ,则该滤液中 _______ (保留1位小数);滤液2中
可以循环利用的物质是_______;从滤液3可提取出一种含结晶水的钠盐副产品,若测定该晶体中结晶水的含
量,所需的仪器除三脚架、托盘天平、瓷坩埚、干燥器、酒精灯、玻璃棒,还需要的仪器有_______。
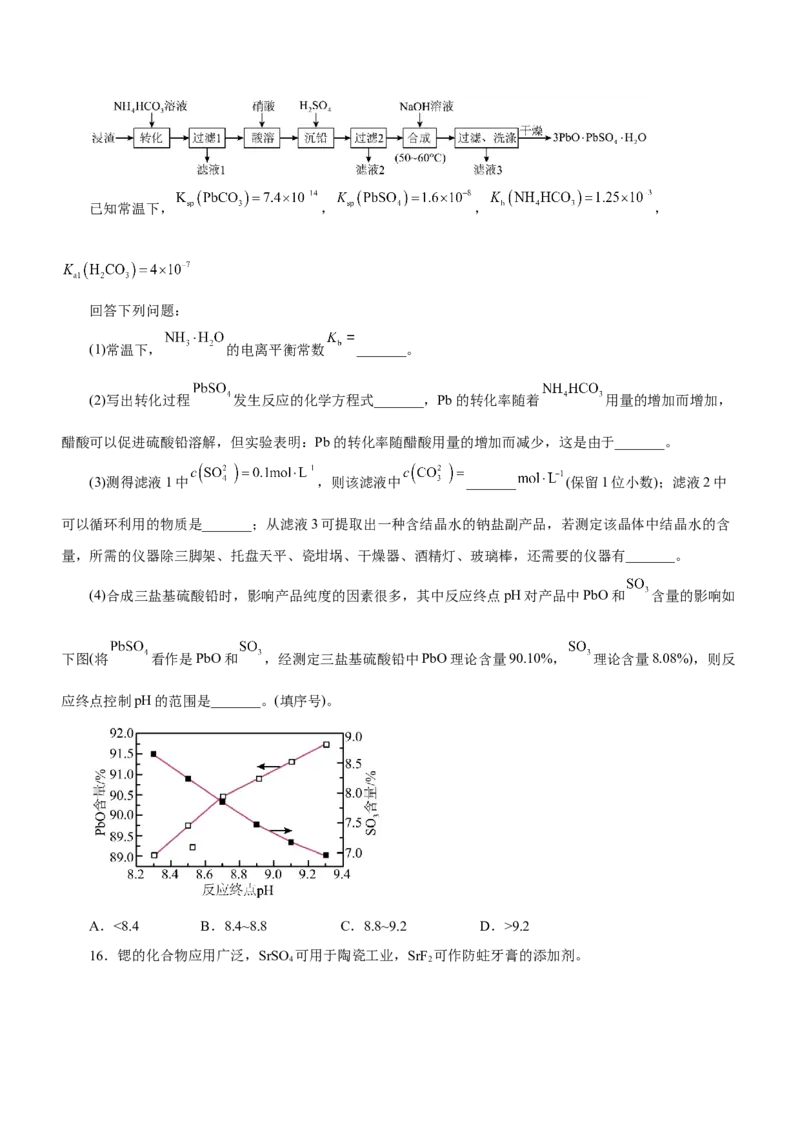
(4)合成三盐基硫酸铅时,影响产品纯度的因素很多,其中反应终点pH对产品中PbO和 含量的影响如
下图(将 看作是PbO和 ,经测定三盐基硫酸铅中PbO理论含量90.10%, 理论含量8.08%),则反
应终点控制pH的范围是_______。(填序号)。
A.<8.4 B.8.4~8.8 C.8.8~9.2 D.>9.2
16.锶的化合物应用广泛,SrSO 可用于陶瓷工业,SrF 可作防蛀牙膏的添加剂。
4 2(1)以天青石精矿(主要含SrSO )为原料制备高纯硫酸锶的部分工艺流程如下:
4
①“转化”中用碳酸氢铵和过量氨水的混合溶液浸取天青石精矿,可制得SrCO 沉淀。写出该过程的离子
3
方程式:_____
②“转化”中维持反应温度70℃且控制氨水过量,氨水过量的主要原因是_____
③该工艺流程中,可循环利用物质是_______ (填化学式) 。
(2)工业上还可用碳还原法制备高纯硫酸锶。将天青石精矿和煤粉按照一定质量比在回转窑中煅烧,生成
SrS,再处理得高纯SrSO 。
4
①煅烧温度对SrSO 转化率的影响如图,最佳煅烧温度为_____
4
②天青石精矿和煤粉质量比对SrSO 转化率的影响如图,天青石精矿和煤粉质量比增大至5.5:1后,SrSO
4 4
转化率下降的可能原因是_______。
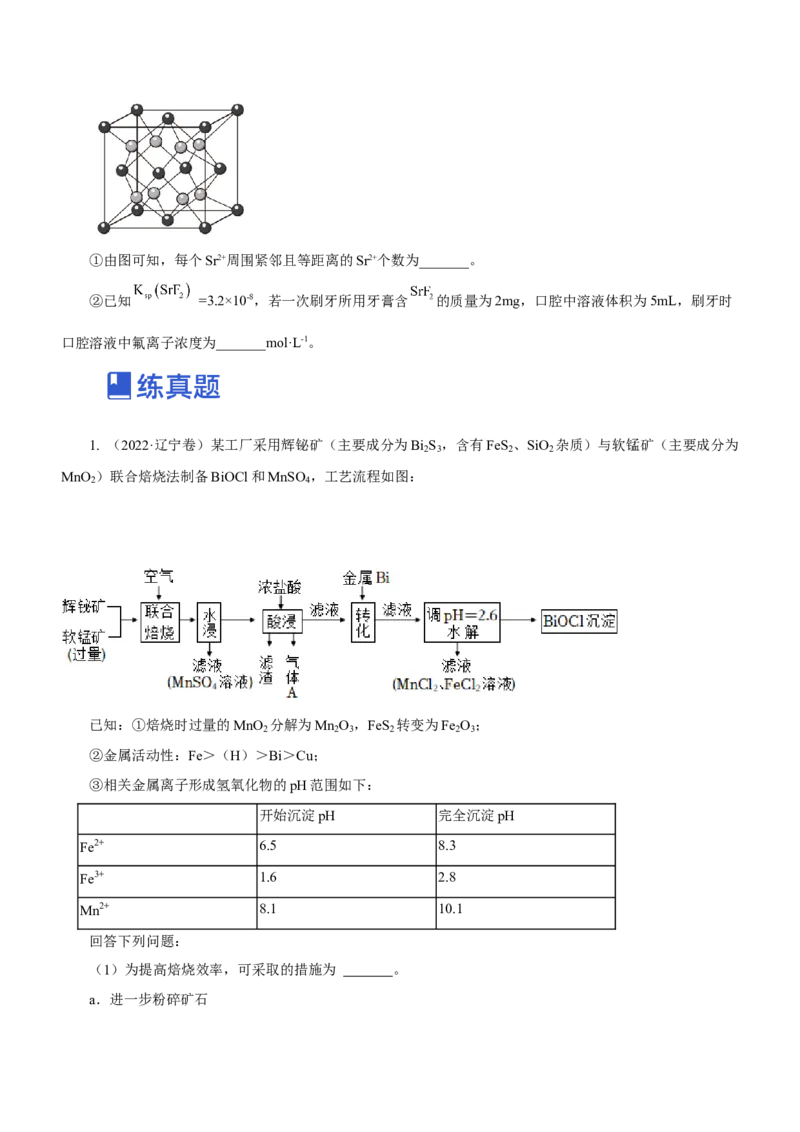
(3)SrF 一种晶体的晶胞结构如图所示。
2①由图可知,每个Sr2+周围紧邻且等距离的Sr2+个数为_______。
②已知 =3.2×10-8,若一次刷牙所用牙膏含 的质量为2mg,口腔中溶液体积为5mL,刷牙时
口腔溶液中氟离子浓度为_______mol·L-1。
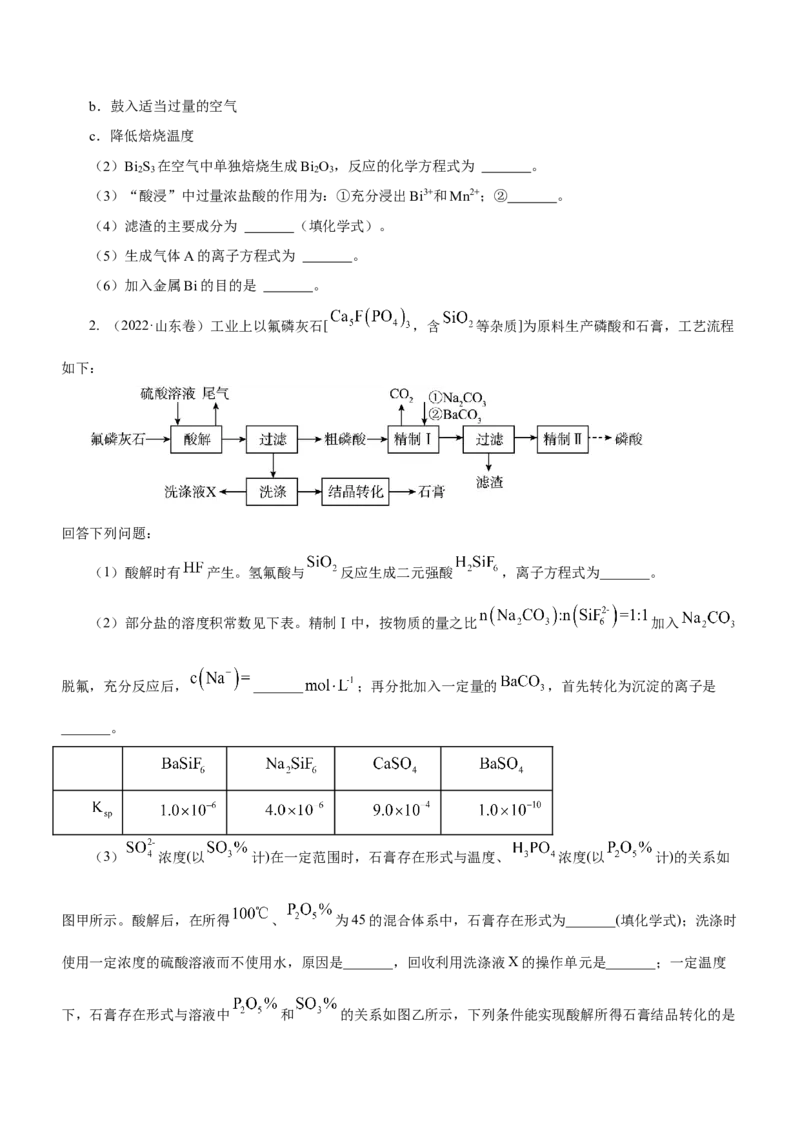
1. (2022·辽宁卷)某工厂采用辉铋矿(主要成分为Bi S ,含有FeS 、SiO 杂质)与软锰矿(主要成分为
2 3 2 2
MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如图:
2 4
已知:①焙烧时过量的MnO 分解为Mn O ,FeS 转变为Fe O ;
2 2 3 2 2 3
②金属活动性:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为 。
a.进一步粉碎矿石b.鼓入适当过量的空气
c.降低焙烧温度
(2)Bi S 在空气中单独焙烧生成Bi O ,反应的化学方程式为 。
2 3 2 3
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+;② 。
(4)滤渣的主要成分为 (填化学式)。
(5)生成气体A的离子方程式为 。
(6)加入金属Bi的目的是 。
2. (2022·山东卷)工业上以氟磷灰石[ ,含 等杂质]为原料生产磷酸和石膏,工艺流程
如下:
回答下列问题:
(1)酸解时有 产生。氢氟酸与 反应生成二元强酸 ,离子方程式为_______。
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比 加入
脱氟,充分反应后, _______ ;再分批加入一定量的 ,首先转化为沉淀的离子是
_______。
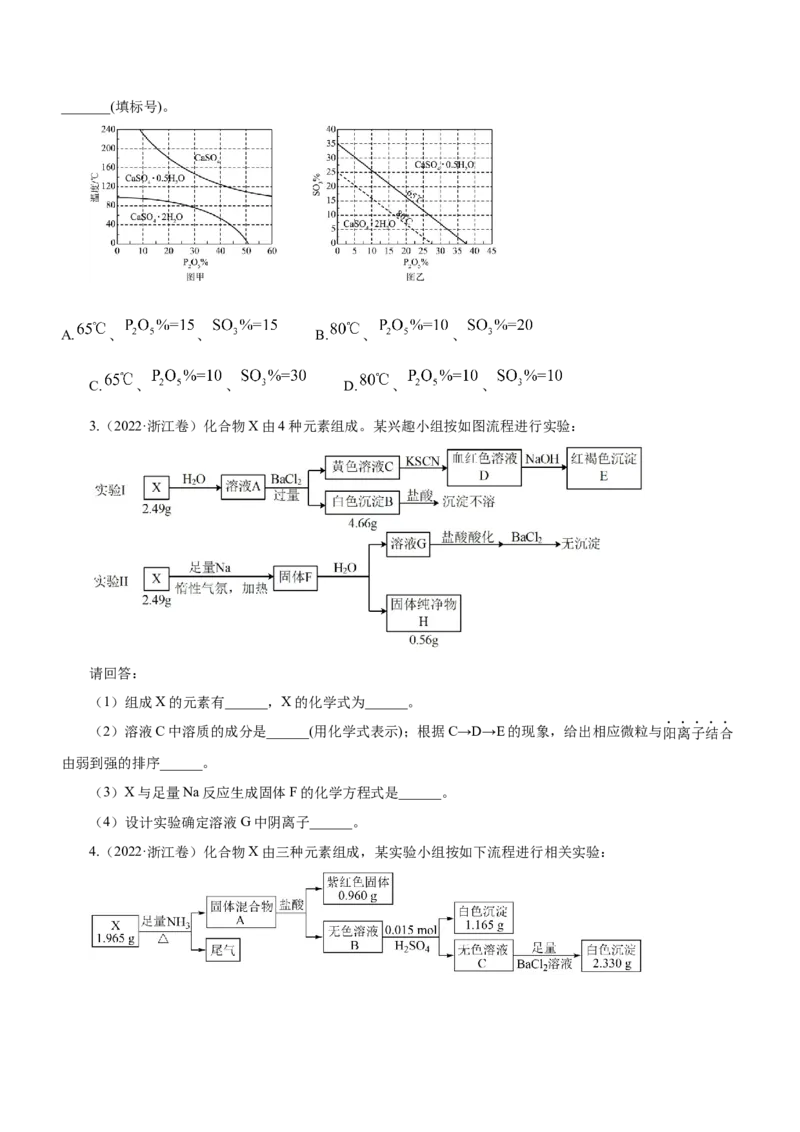
(3) 浓度(以 计)在一定范围时,石膏存在形式与温度、 浓度(以 计)的关系如
图甲所示。酸解后,在所得 、 为45的混合体系中,石膏存在形式为_______(填化学式);洗涤时
使用一定浓度的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是_______;一定温度
下,石膏存在形式与溶液中 和 的关系如图乙所示,下列条件能实现酸解所得石膏结品转化的是_______(填标号)。
A. 、 、 B. 、 、
C. 、 、 D. 、 、
3.(2022·浙江卷)化合物X由4种元素组成。某兴趣小组按如图流程进行实验:
请回答:
(1)组成X的元素有______,X的化学式为______。
(2)溶液C中溶质的成分是______(用化学式表示);根据C→D→E的现象,给出相应微粒与阳离子结合
由弱到强的排序______。
(3)X与足量Na反应生成固体F的化学方程式是______。
(4)设计实验确定溶液G中阴离子______。
4.(2022·浙江卷)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
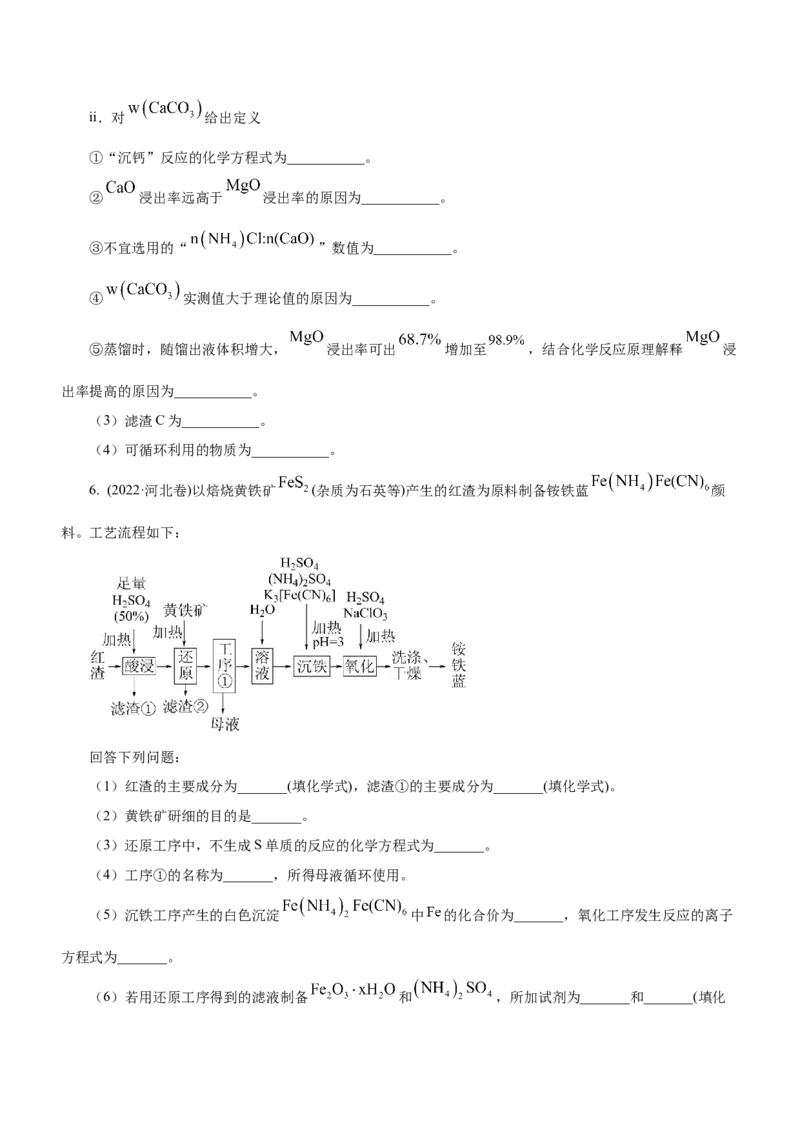
5. (2022·北京卷)铵浸法由白云石[主要成分为 ,含 , 杂质]制备高纯度碳酸钙
和氧化镁。其流程如下:
已知:
物质
(1)煅烧白云石的化学方程式为___________。
(2)根据下表数据分析:
浸出 浸出 理论 实测
率/ 率/ 值/ 值/
98.4 1.1 99.7 -
98.8 1.5 99.2 99.5
98.9 1.8 98.8 99.5
99.1 6.0 95.6 97.6
已知:i.对浸出率给出定义ii.对 给出定义
①“沉钙”反应的化学方程式为___________。
② 浸出率远高于 浸出率的原因为___________。
③不宜选用的“ ”数值为___________。
④ 实测值大于理论值的原因为___________。
⑤蒸馏时,随馏出液体积增大, 浸出率可出 增加至 ,结合化学反应原理解释 浸
出率提高的原因为___________。
(3)滤渣C为___________。
(4)可循环利用的物质为___________。
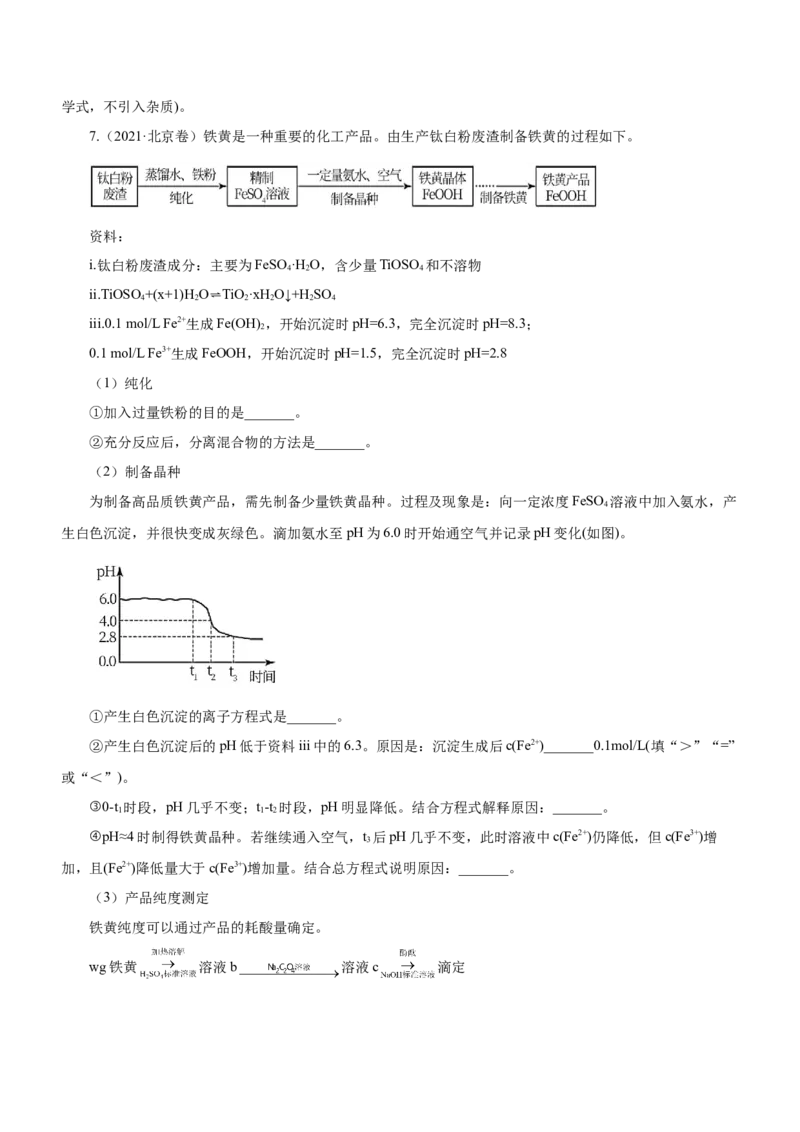
6. (2022·河北卷)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝 颜
料。工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子
方程式为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,不引入杂质)。
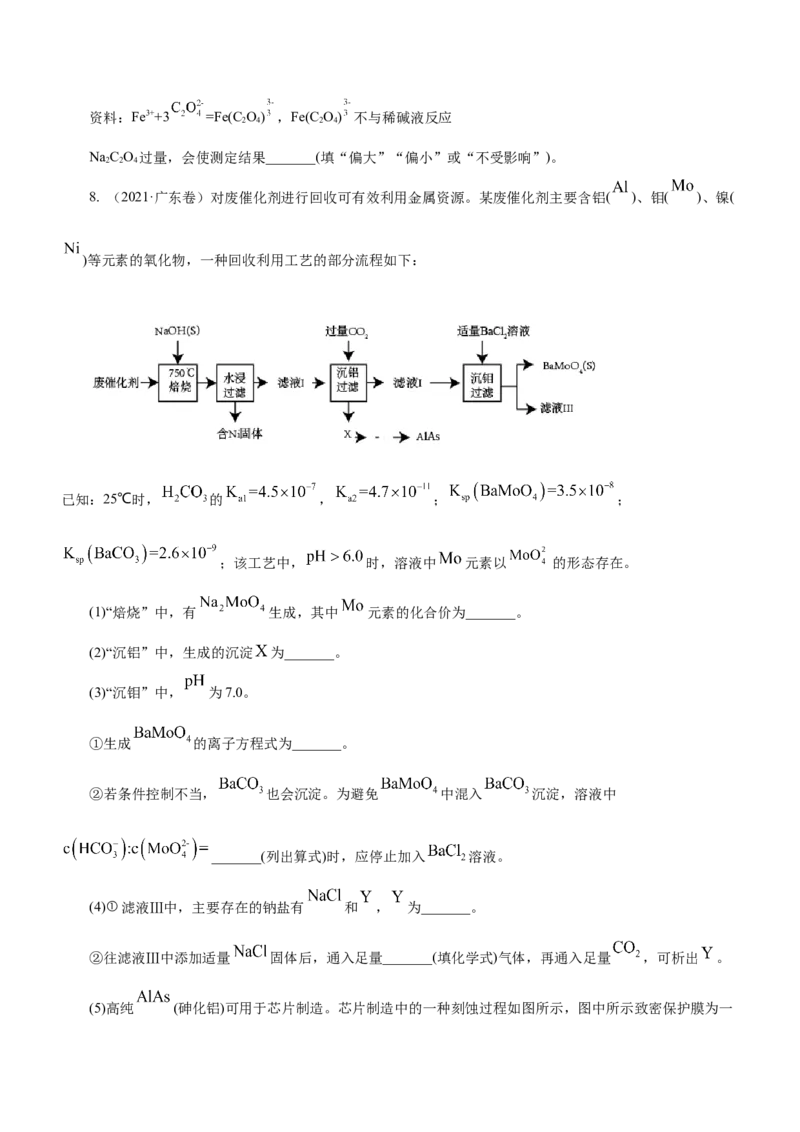
7.(2021·北京卷)铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。
资料:
i.钛白粉废渣成分:主要为FeSO ·H O,含少量TiOSO 和不溶物
4 2 4
ii.TiOSO
4
+(x+1)H
2
O⇌TiO
2
·xH
2
O↓+H
2
SO
4
iii.0.1 mol/L Fe2+生成Fe(OH) ,开始沉淀时pH=6.3,完全沉淀时pH=8.3;
2
0.1 mol/L Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(1)纯化
①加入过量铁粉的目的是_______。
②充分反应后,分离混合物的方法是_______。
(2)制备晶种
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO 溶液中加入氨水,产
4
生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如图)。
①产生白色沉淀的离子方程式是_______。
②产生白色沉淀后的pH低于资料iii中的6.3。原因是:沉淀生成后c(Fe2+)_______0.1mol/L(填“>”“=”
或“<”)。
③0-t 时段,pH几乎不变;t-t 时段,pH明显降低。结合方程式解释原因:_______。
1 1 2
④pH≈4时制得铁黄晶种。若继续通入空气,t 后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)增
3
加,且(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:_______。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
wg铁黄 溶液b 溶液c 滴定资料:Fe3++3 =Fe(C O) ,Fe(C O) 不与稀碱液反应
2 4 2 4
NaC O 过量,会使测定结果_______(填“偏大”“偏小”或“不受影响”)。
2 2 4
8. (2021·广东卷)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、镍(
)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 ,可析出 。
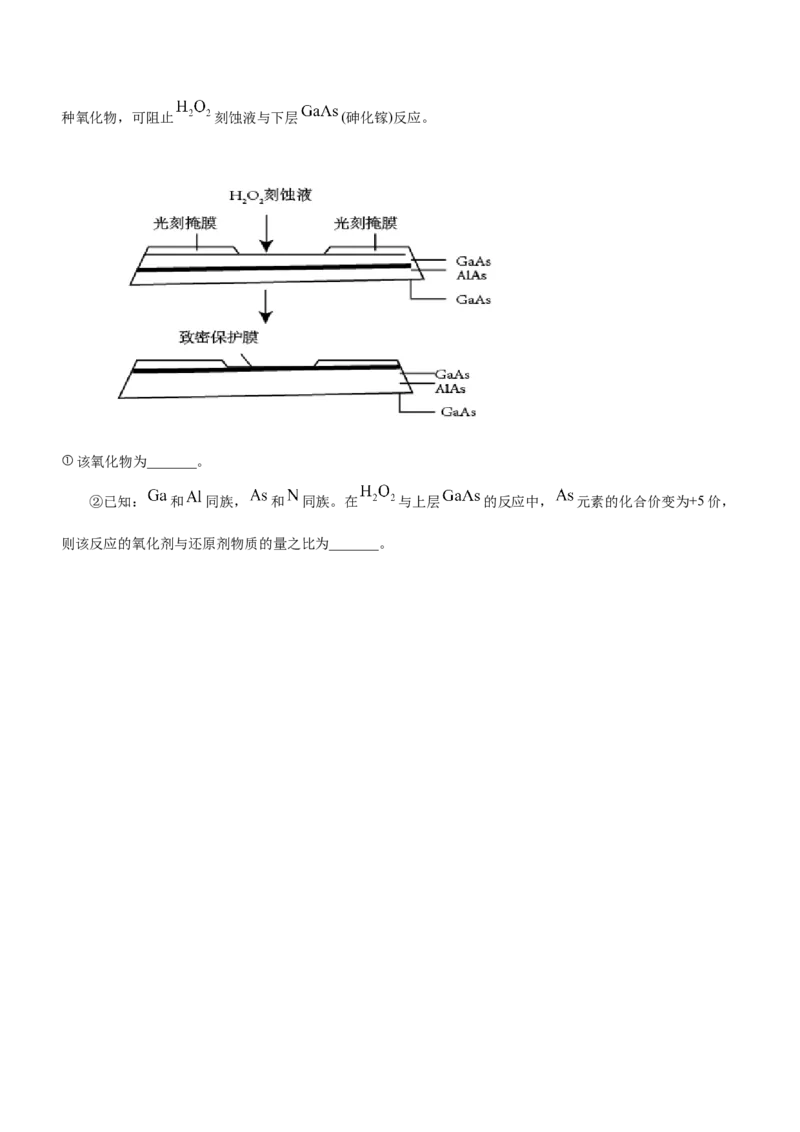
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。
①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价变为+5价,
则该反应的氧化剂与还原剂物质的量之比为_______。