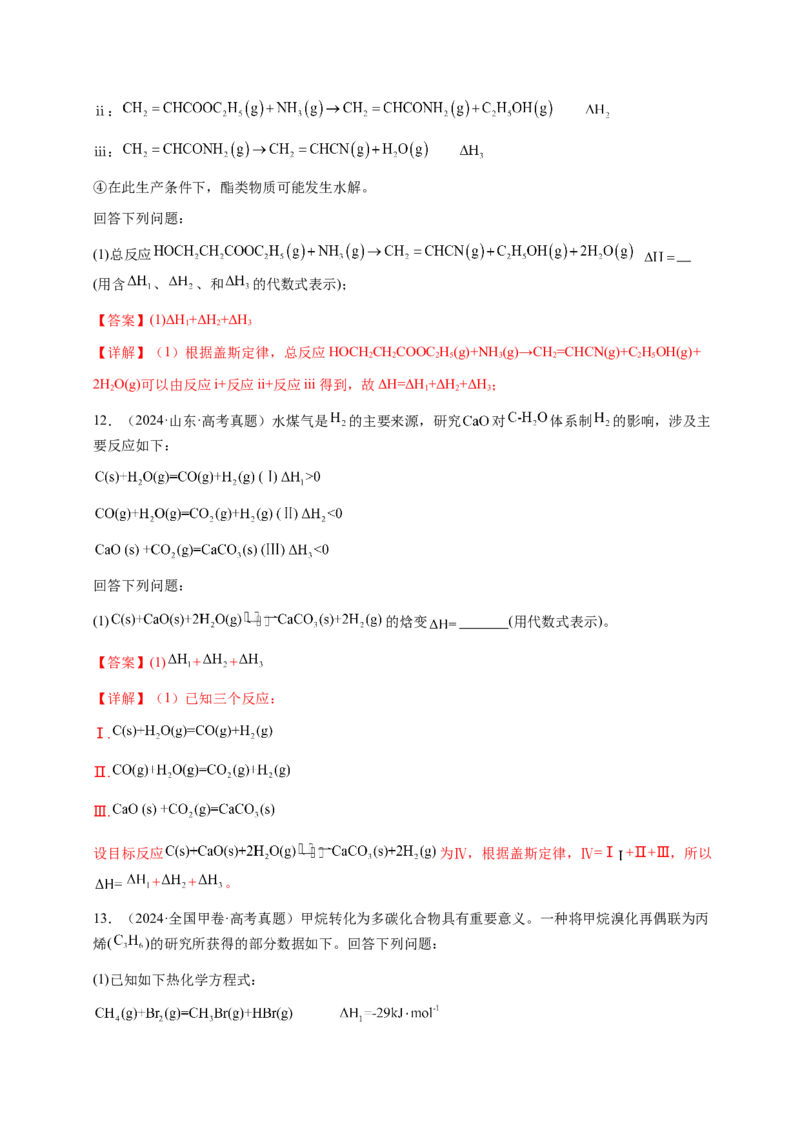文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题19 化学能与热能
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
对于化学反应热效应的考查,主要从三个角度设置题目:
一是在选择题中单独设题,考查反应中的能量变化、反应热的比较及盖斯定律的计算;
二是在选择题中某一选项出现,多与图像分析相结合;
三是在填空题中考查,考查盖斯定律的计算或结合盖斯定律的热化学方程式的书写。
预计2025年仍保持这种命题趋向。
1.(2024·广东·高考真题)“极地破冰”“太空养鱼”等彰显了我国科技发展的巨大成就。下列说法
正确的是
A.“雪龙2”号破冰船极地科考:破冰过程中水发生了化学变化
B.大型液化天然气运输船成功建造:天然气液化过程中形成了新的化学键
C.嫦娥六号的运载火箭助推器采用液氧煤油发动机:燃烧时存在化学能转化为热能
D.神舟十八号乘组带着水和斑马鱼进入空间站进行科学实验:水的电子式为
【答案】C
【详解】A.破冰过程无新物质生成,是物理变化,A错误;
B.天然气液化的过程是气态变为液态,是物理变化,无新的化学键形成,B错误;
C.燃烧放热,是化学能转化为热能,C正确;
D.水是共价化合物,每个H原子都与O原子共用一对电子,电子式为 ,D错误;
本题选C。
2.(2025·浙江·高考真题)下列说法正确的是
A.常温常压下 和 混合无明显现象,则反应 在该条件下不自
发
B. ,升高温度,平衡逆移,则反应的平衡常数减小
C. ,则正反应的活化能大于逆反应的活化能
D. ,则【答案】B
【详解】A.根据复合判据ΔG=ΔH-TΔS,该反应ΔH<0、ΔS<0,温度较低时ΔG<0,故低温能自发
进行,A错误;
B.该反应为放热反应,升高温度,平衡逆移,平衡常数减小,B正确;
C.该反应为放热反应,则 ,则正反应的活化能小于逆反应的活化能,C错误;
D. ,根据盖斯定
律,反应①-反应②得到目标反应Na(s)+ Cl(g)=Na+(g)+Cl−(g),则ΔH= ,由于不能明确
2
相对大小,则ΔH不能确定,D错误;
故选B。
3.(2024·重庆·高考真题)二氧化碳甲烷重整是 资源化利用的重要研究方向,涉及的主要热化学
方程式有:
①
②
③
已知 键能为 , 键能为 , 键能为 ,则 中的碳氧键键能(单
位: )为
A. B. C. D.
【答案】B
【详解】根据盖斯定律反应①+②-③可得反应: ,该反应
,根据 反应物键能和-生成物
键能和可得: 4c+2b-3a- 中的碳氧键键能= , 中的碳氧键键能=( )
,故B正确;
故选:B。
4.(2024·海南·高考真题)已知 时, ,
的临界温度(能够液化的最高温度)为 ,下列说法错误的是
A.氢气燃烧热B.题述条件下 和 ,在燃料电池中完全反应,电功+放热量
C.氢能利用的关键技术在于安全储存与运输
D.不同电极材料电解水所需电压不同,产生 消耗的电功相同
【答案】D
【详解】A.氢气燃烧热为1mol氢气完全燃烧生成液态水放出的热量,则由热化学方程式可知,氢气
燃烧热 ,故A正确;
B.由题意可知,氢氧燃料电池中化学能转化为热能和电能,由能量守恒定律可知, 和
,在燃料电池中完全反应,电功+放热量 ,故B正确;
C.氢气是易燃易爆的气体,难于安全储存与运输,所以氢能利用的关键技术在于安全储存与运输,
故C正确;
D.不同电极材料电解水所需电压不同,说明所需的电流不同,所以产生2g氢气所需时间不同,消耗
的电功不同,故D错误;
故选D。
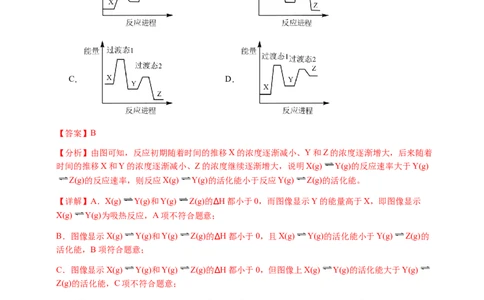
5.(2024·广东·高考真题)对反应 (I为中间产物),相同条件下:
①加入催化剂,反应达到平衡所需时间大幅缩短;
②提高反应温度, 增大, 减小。
基于以上事实,可能的反应历程示意图(——为无催化剂,------为有催化剂)为
A. B. C. D.
【答案】A
【详解】提高反应温度, 增大,说明反应 的平衡逆向移动,即该反应为放热
反应, 减小,说明S生成中间产物I的反应平衡正向移动,属于吸热反应,由此可排除
C、D选项,加入催化剂,反应达到平衡所需时间大幅缩短,即反应的决速步骤的活化能下降,使得
反应速率大幅加快,活化能大的步骤为决速步骤,符合条件的反应历程示意图为A,故A正确,
故选A。
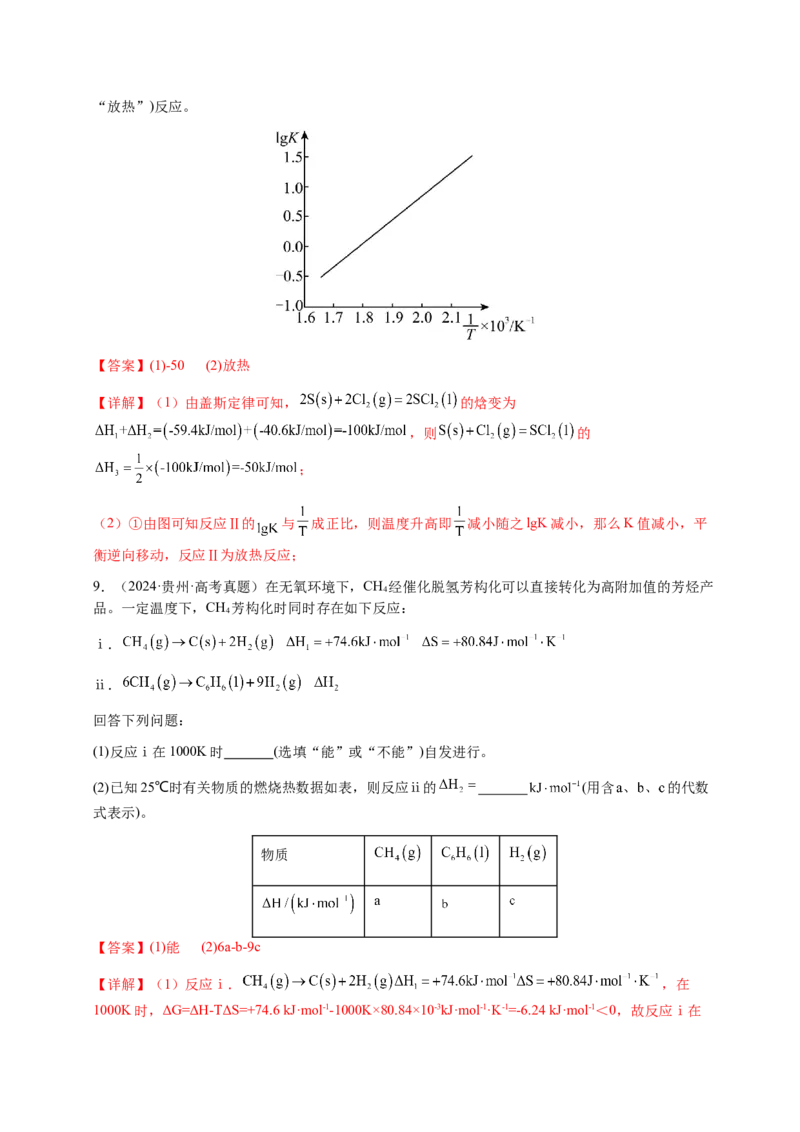
6.(2024·安徽·高考真题)某温度下,在密闭容器中充入一定量的 ,发生下列反应:
, ,测得各气体浓度与反应时间的关系如图所示。下列反
应进程示意图符合题意的是A. B.
C. D.
【答案】B
【分析】由图可知,反应初期随着时间的推移X的浓度逐渐减小、Y和Z的浓度逐渐增大,后来随着
时间的推移X和Y的浓度逐渐减小、Z的浓度继续逐渐增大,说明X(g) Y(g)的反应速率大于Y(g)
Z(g)的反应速率,则反应X(g) Y(g)的活化能小于反应Y(g) Z(g)的活化能。
【详解】A.X(g) Y(g)和Y(g) Z(g)的∆H都小于0,而图像显示Y的能量高于X,即图像显示
X(g) Y(g)为吸热反应,A项不符合题意;
B.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,且X(g) Y(g)的活化能小于Y(g) Z(g)的
活化能,B项符合题意;
C.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,但图像上X(g) Y(g)的活化能大于Y(g)
Z(g)的活化能,C项不符合题意;
D.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都大于0,且X(g) Y(g)的活化能大于Y(g) Z(g)的
活化能,D项不符合题意;
选B。
7.(2024·浙江·高考真题)下列实验装置使用不正确的是A.图①装置用于二氧化锰和浓盐酸反应制氯气
B.图②装置用于标准酸溶液滴定未知碱溶液
C.图③装置用于测定中和反应的反应热
D.图④装置用于制备乙酸乙酯
【答案】A
【详解】A.图①装置没有加热装置,不适用于二氧化锰和浓盐酸反应制氯气,A错误;
B.利用酸式滴定管中装有的标准酸溶液滴定未知碱溶液,装置和操作正确,B正确;
C.图③装置用于测定中和反应的反应热,温度计测温度、玻璃搅拌器起搅拌作用,装置密封、隔热
保温效果好,C正确;
D.图④装置用于制备乙酸乙酯,导管末端不伸入液面下,利用饱和碳酸钠收集乙酸乙酯,D正确;
故选A。
8.(2024·广西·高考真题)二氯亚砜( )是重要的液态化工原料。回答下列问题:
(1)合成 前先制备 。有关转化关系为:
则 的 。
(2)密闭容器中,以活性炭为催化剂,由 和 制备 。反应如下:
Ⅰ
Ⅱ
①反应Ⅱ的 ( 为平衡常数)随 ( 为温度)的变化如图,推断出该反应为 (填“吸热”或“放热”)反应。
【答案】(1)-50 (2)放热
【详解】(1)由盖斯定律可知, 的焓变为
,则 的
;
(2)①由图可知反应Ⅱ的 与 成正比,则温度升高即 减小随之lgK减小,那么K值减小,平
衡逆向移动,反应Ⅱ为放热反应;
9.(2024·贵州·高考真题)在无氧环境下,CH 经催化脱氢芳构化可以直接转化为高附加值的芳烃产
4
品。一定温度下,CH 芳构化时同时存在如下反应:
4
ⅰ.
ⅱ.
回答下列问题:
(1)反应ⅰ在1000K时 (选填“能”或“不能”)自发进行。
(2)已知25℃时有关物质的燃烧热数据如表,则反应ⅱ的 (用含 的代数
式表示)。
物质
【答案】(1)能 (2)6a-b-9c
【详解】(1)反应ⅰ. ,在
1000K时,ΔG=ΔH-TΔS=+74.6 kJ·mol-1-1000K×80.84×10-3kJ·mol-1·K-1=-6.24 kJ·mol-1<0,故反应ⅰ在1000K时能自发进行。
(2)ⅱ.
由题给数据可得出以下热化学方程式:
③CH (g)+2O(g)=CO(g)+2HO(l) ΔH=akJ·mol-1
4 2 2 2
④C H(l)+7.5O(g)=6CO(g)+3HO(l) ΔH=bkJ·mol-1
6 6 2 2 2
⑤H(g)+0.5O (g)=HO(l) ΔH=c kJ·mol-1
2 2 2
依据盖斯定律,将反应③×6-④-⑤×9得,反应ⅱ的 (6a-b-9c) kJ·mol-1。
10.(2024·甘肃·高考真题) 是制备半导体材料硅的重要原料,可由不同途径制备。
(1)由 制备 :
已知
时,由 制备 硅 (填“吸”或“放”)热 。升
高温度有利于制备硅的原因是 。
【答案】(1)吸 587.02 该反应为吸热反应,升高温度,反应正向移动,有利于制备硅
【详解】(1)由题给热化学方程式:① , ;②
, ;则根据盖斯定律可知,①+②,可得热化学
方程式 ,
,则制备56gSi,即2molSi,需要
吸收热量为 ;该反应为吸热反应,升高温度,反应正向移动,有利
于制备硅。
11.(2024·湖南·高考真题)丙烯腈( )是一种重要的化工原料。工业上以 为载气,用
作催化剂生产 的流程如下:
已知:
①进料混合气进入两釜的流量恒定,两釜中反应温度恒定:
②反应釜Ⅰ中发生的反应:
ⅰ:
③反应釜Ⅱ中发生的反应:ⅱ:
ⅲ:
④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应
(用含 、 、和 的代数式表示);
【答案】(1)ΔH +ΔH +ΔH
1 2 3
【详解】(1)根据盖斯定律,总反应HOCH CHCOOC H(g)+NH (g)→CH =CHCN(g)+C HOH(g)+
2 2 2 5 3 2 2 5
2HO(g)可以由反应i+反应ii+反应iii得到,故ΔH=ΔH+ΔH +ΔH ;
2 1 2 3
12.(2024·山东·高考真题)水煤气是 的主要来源,研究 对 体系制 的影响,涉及主
要反应如下:
回答下列问题:
(1) 的焓变 (用代数式表示)。
【答案】(1) + +
【详解】(1)已知三个反应:
Ⅰ.
Ⅱ.
Ⅲ.
设目标反应 为Ⅳ,根据盖斯定律,Ⅳ=Ⅰ +Ⅱ+Ⅲ,所以
+ + 。
13.(2024·全国甲卷·高考真题)甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙
烯( )的研究所获得的部分数据如下。回答下列问题:
(1)已知如下热化学方程式:计算反应 的 。
【答案】(1)-67
【详解】(1)将第一个热化学方程式命名为①,将第二个热化学方程式命名为②。根据盖斯定律,
将方程式①乘以3再加上方程式②,即①×3+②,故热化学方程式3CH(g)+3Br (g)=C H(g)+6HBr(g)的
4 2 3 6
∆H=-29×3+20=-67kJ·mol-1。
14.(2024·安徽·高考真题)乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。
回答下列问题:
【乙烷制乙烯】
(1) 氧化脱氢反应:
计算:
【答案】(1)-566
【详解】(1)将两个反应依次标号为反应①和反应②,反应①-反应②×2可得目标反应,则
ΔH=ΔH -2ΔH =(-209.8-178.1×2)kJ/mol=-566kJ/mol;
3 1 2
15.(2024·吉林·高考真题)为实现氯资源循环利用,工业上采用 催化氧化法处理 废气:
。将 和 分别以不同起始流速
通入反应器中,在 和 下反应,通过检测流出气成分绘制 转化率( )曲线,如下
图所示(较低流速下转化率可近似为平衡转化率)。
回答下列问题:(1) 0(填“>”或“<”); ℃。
(2)结合以下信息,可知 的燃烧热 。
【答案】(1)< 360℃ (2)-285.8
【详解】(1)反应 前后的气体分子数目在减小,所以该反应
<0,该反应为放热反应,由于在流速较低时的转化率视为平衡转化率,所以在流速低的时候,温度越
高,HCl的转化率越小,故T 代表的温度为440℃,T 为360℃。
1 3
(2)表示氢气燃烧热的热化学方程式为④ ,设①
,② ,③ ,则
,因此氢气的燃烧热 -57.2kJ/mol-184.6kJ/mol-44kJ/mol=-285.8
【策略1】记忆常见的放热反应和吸热反应
a.所有的燃烧反应,如:木炭、CH 等在空气或氧气中的燃烧,钠、H 在氯气
4 2
中燃烧,镁条在CO 中燃烧。
2
b.所有的酸碱中和反应,如:HCl+NaOH===NaCl+HO
2
c.大多数的化合反应,如:CaO+HO===Ca(OH)
常见的放热反应 2 2
d.铝热反应,如:2Al+Fe O=====2Fe+Al O
2 3 2 3
e.活泼金属与水、与酸的反应,如:2Na+2HO===2NaOH+H↑
2 2
f.生成沉淀的反应
a.大多数分解反应,如:NH Cl NH ↑+HCl↑、CaCO =====CaO+CO↑
4 3 3 2
b.Ba(OH) ·8H O与NH Cl的反应
2 2 4
c.C和CO 发生的化合反应及C和HO(g)的反应
2 2
常见的吸热反应
d.以碳、CO、H 为还原剂的氧化还原反应:如:H +CuO HO+Cu、C+
2 2 2
HO(g)=====CO+H
2 2
e.盐类的水解反应【策略2】熟练掌握反应焓变的计算方法
(1)根据化学反应过程中的能量变化来计算
ΔH=生成物的总能量-反应物的总能量
ΔH=反应物的总键能-生成物的总键能
ΔH=正反应活化能-逆反应活化能
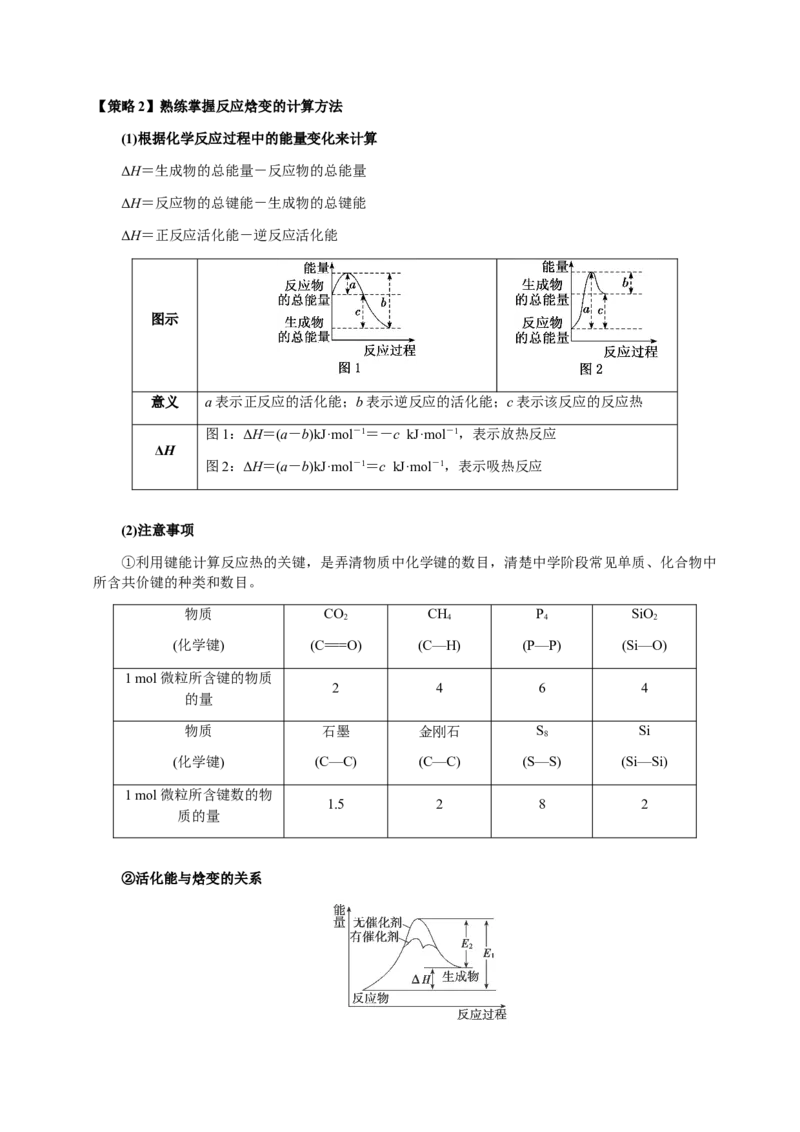
图示
意义 a表示正反应的活化能;b表示逆反应的活化能;c表示该反应的反应热
图1:ΔH=(a-b)kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b)kJ·mol-1=c kJ·mol-1,表示吸热反应
(2)注意事项
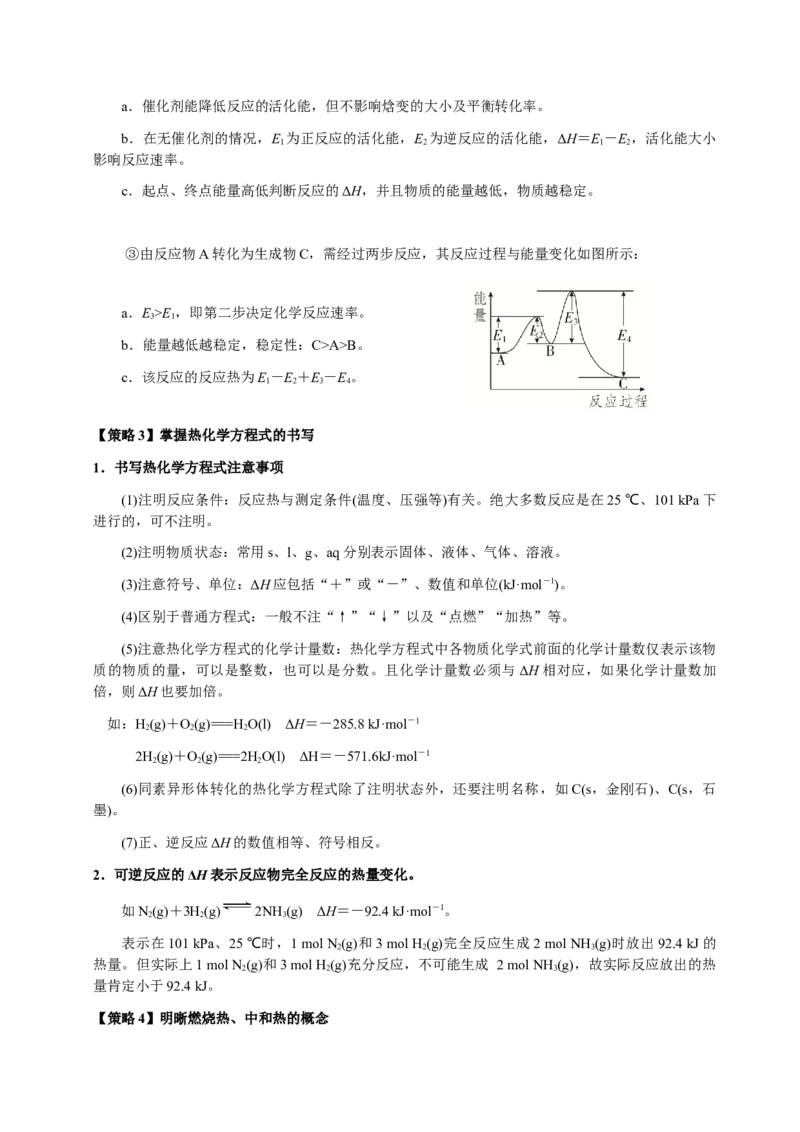
①利用键能计算反应热的关键,是弄清物质中化学键的数目,清楚中学阶段常见单质、化合物中
所含共价键的种类和数目。
物质 CO CH P SiO
2 4 4 2
(化学键) (C===O) (C—H) (P—P) (Si—O)
1 mol微粒所含键的物质
2 4 6 4
的量
物质 石墨 金刚石 S Si
8
(化学键) (C—C) (C—C) (S—S) (Si—Si)
1 mol微粒所含键数的物
1.5 2 8 2
质的量
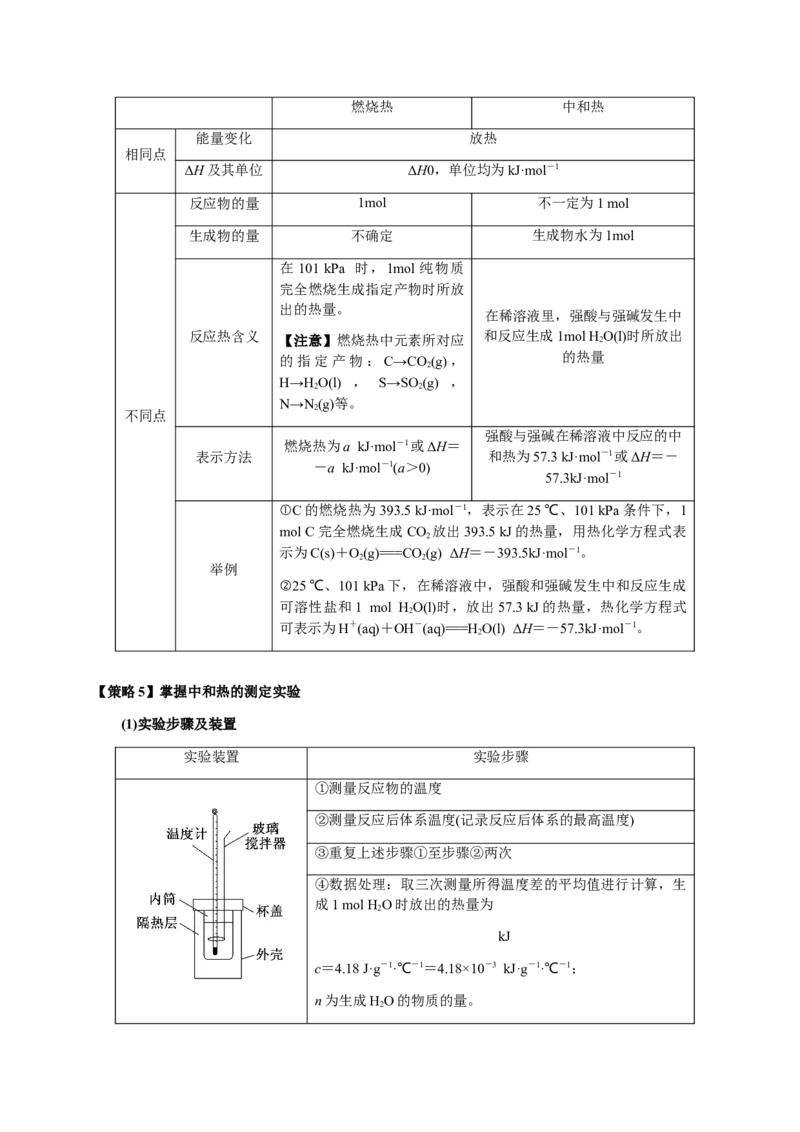
②活化能与焓变的关系a.催化剂能降低反应的活化能,但不影响焓变的大小及平衡转化率。
b.在无催化剂的情况,E 为正反应的活化能,E 为逆反应的活化能,ΔH=E -E ,活化能大小
1 2 1 2
影响反应速率。
c.起点、终点能量高低判断反应的ΔH,并且物质的能量越低,物质越稳定。
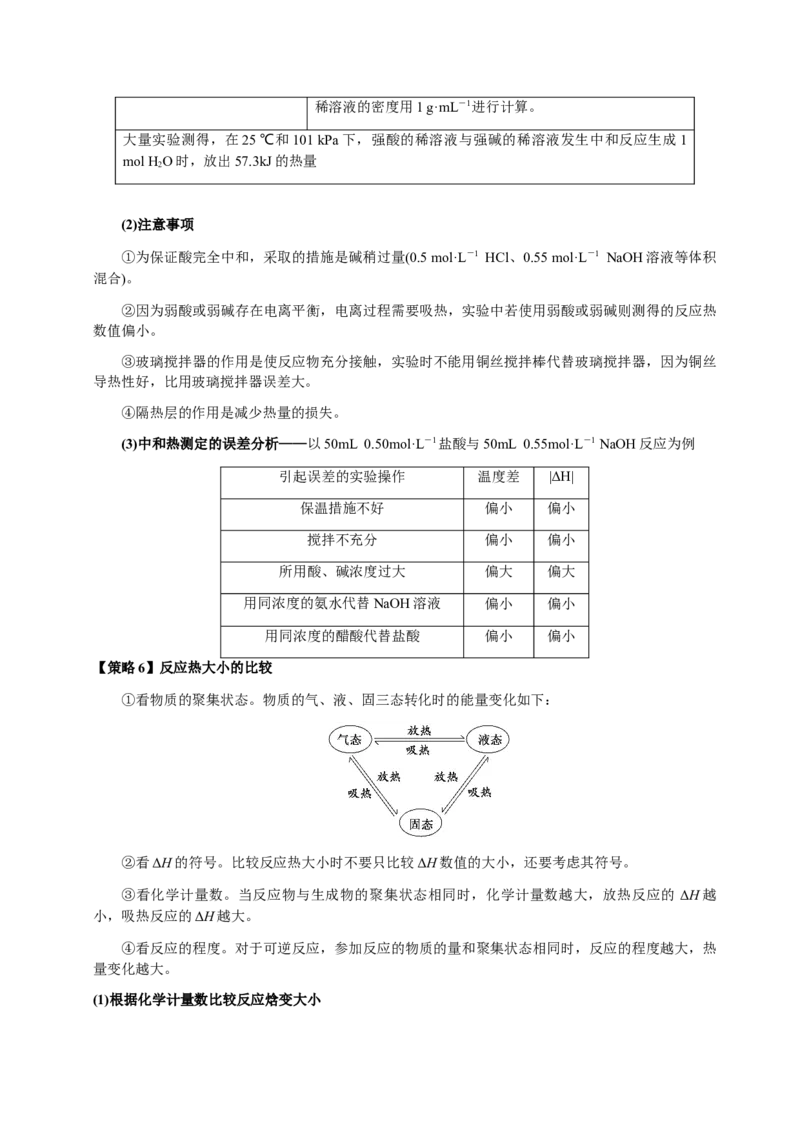
③由反应物A转化为生成物C,需经过两步反应,其反应过程与能量变化如图所示:
a.E>E,即第二步决定化学反应速率。
3 1
b.能量越低越稳定,稳定性:C>A>B。
c.该反应的反应热为E-E+E-E。
1 2 3 4
【策略3】掌握热化学方程式的书写
1.书写热化学方程式注意事项
(1)注明反应条件:反应热与测定条件(温度、压强等)有关。绝大多数反应是在25 ℃、101 kPa下
进行的,可不注明。
(2)注明物质状态:常用s、l、g、aq分别表示固体、液体、气体、溶液。
(3)注意符号、单位:ΔH应包括“+”或“-”、数值和单位(kJ·mol-1)。
(4)区别于普通方程式:一般不注“↑”“↓”以及“点燃”“加热”等。
(5)注意热化学方程式的化学计量数:热化学方程式中各物质化学式前面的化学计量数仅表示该物
质的物质的量,可以是整数,也可以是分数。且化学计量数必须与ΔH相对应,如果化学计量数加
倍,则ΔH也要加倍。
如:H(g)+O(g)===H O(l) ΔH=-285.8 kJ·mol-1
2 2 2
2H(g)+O(g)===2H O(l) ΔH=-571.6kJ·mol-1
2 2 2
(6)同素异形体转化的热化学方程式除了注明状态外,还要注明名称,如C(s,金刚石)、C(s,石
墨)。
(7)正、逆反应ΔH的数值相等、符号相反。
2.可逆反应的ΔH表示反应物完全反应的热量变化。
如N(g)+3H(g) 2NH (g) ΔH=-92.4 kJ·mol-1。
2 2 3
表示在101 kPa、25 ℃时,1 mol N (g)和3 mol H (g)完全反应生成2 mol NH (g)时放出92.4 kJ的
2 2 3
热量。但实际上1 mol N (g)和3 mol H (g)充分反应,不可能生成 2 mol NH (g),故实际反应放出的热
2 2 3
量肯定小于92.4 kJ。
【策略4】明晰燃烧热、中和热的概念燃烧热 中和热
能量变化 放热
相同点
ΔH及其单位 ΔH0,单位均为kJ·mol-1
反应物的量 1mol 不一定为1 mol
生成物的量 不确定 生成物水为1mol
在 101 kPa 时,1mol 纯物质
完全燃烧生成指定产物时所放
出的热量。
在稀溶液里,强酸与强碱发生中
反应热含义 【注意】燃烧热中元素所对应 和反应生成1mol H 2 O(l)时所放出
的指定产物:C→CO(g), 的热量
2
H→H O(l) , S→SO (g) ,
2 2
N→N (g)等。
2
不同点
强酸与强碱在稀溶液中反应的中
燃烧热为a kJ·mol-1或ΔH=
表示方法 和热为57.3 kJ·mol-1或ΔH=-
-a kJ·mol-1(a>0)
57.3kJ·mol-1
①C的燃烧热为393.5 kJ·mol-1,表示在25 ℃、101 kPa条件下,1
mol C完全燃烧生成CO 放出393.5 kJ的热量,用热化学方程式表
2
示为C(s)+O(g)===CO (g) ΔH=-393.5kJ·mol-1。
2 2
举例
②25 ℃、101 kPa下,在稀溶液中,强酸和强碱发生中和反应生成
可溶性盐和1 mol HO(l)时,放出57.3 kJ的热量,热化学方程式
2
可表示为H+(aq)+OH-(aq)===H O(l) ΔH=-57.3kJ·mol-1。
2
【策略5】掌握中和热的测定实验
(1)实验步骤及装置
实验装置 实验步骤
①测量反应物的温度
②测量反应后体系温度(记录反应后体系的最高温度)
③重复上述步骤①至步骤②两次
④数据处理:取三次测量所得温度差的平均值进行计算,生
成1 mol H O时放出的热量为
2
kJ
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;
n为生成HO的物质的量。
2稀溶液的密度用1 g·mL-1进行计算。
大量实验测得,在25 ℃和101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1
mol HO时,放出57.3kJ的热量
2
(2)注意事项
①为保证酸完全中和,采取的措施是碱稍过量(0.5 mol·L-1 HCl、0.55 mol·L-1 NaOH溶液等体积
混合)。
②因为弱酸或弱碱存在电离平衡,电离过程需要吸热,实验中若使用弱酸或弱碱则测得的反应热
数值偏小。
③玻璃搅拌器的作用是使反应物充分接触,实验时不能用铜丝搅拌棒代替玻璃搅拌器,因为铜丝
导热性好,比用玻璃搅拌器误差大。
④隔热层的作用是减少热量的损失。
(3)中和热测定的误差分析——以50mL 0.50mol·L-1盐酸与50mL 0.55mol·L-1 NaOH反应为例
引起误差的实验操作 温度差 |ΔH|
保温措施不好 偏小 偏小
搅拌不充分 偏小 偏小
所用酸、碱浓度过大 偏大 偏大
用同浓度的氨水代替NaOH溶液 偏小 偏小
用同浓度的醋酸代替盐酸 偏小 偏小
【策略6】反应热大小的比较
①看物质的聚集状态。物质的气、液、固三态转化时的能量变化如下:
②看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号。
③看化学计量数。当反应物与生成物的聚集状态相同时,化学计量数越大,放热反应的 ΔH越
小,吸热反应的ΔH越大。
④看反应的程度。对于可逆反应,参加反应的物质的量和聚集状态相同时,反应的程度越大,热
量变化越大。
(1)根据化学计量数比较反应焓变大小①H(g)+O(g)===H O(g) ΔH
2 2 2 1
②2H (g)+O(g)===2H O(g) ΔH
2 2 2 2
反应②中H 的量更多,因此放热更多,|ΔH|<|ΔH|,但ΔH<0,ΔH<0,故ΔH>ΔH。
2 1 2 1 2 1 2
(2)根据反应进行的程度大小比较反应焓变的大小
①C(s)+O(g)===CO(g) ΔH
2 1
②C(s)+O(g)===CO (g) ΔH
2 2 2
反应②中,C完全燃烧,放热更多,|ΔH|<|ΔH|,但ΔH<0,ΔH<0,故ΔH>ΔH。
1 2 1 2 1 2
(3)根据反应物或生成物的状态比较反应焓变的大小
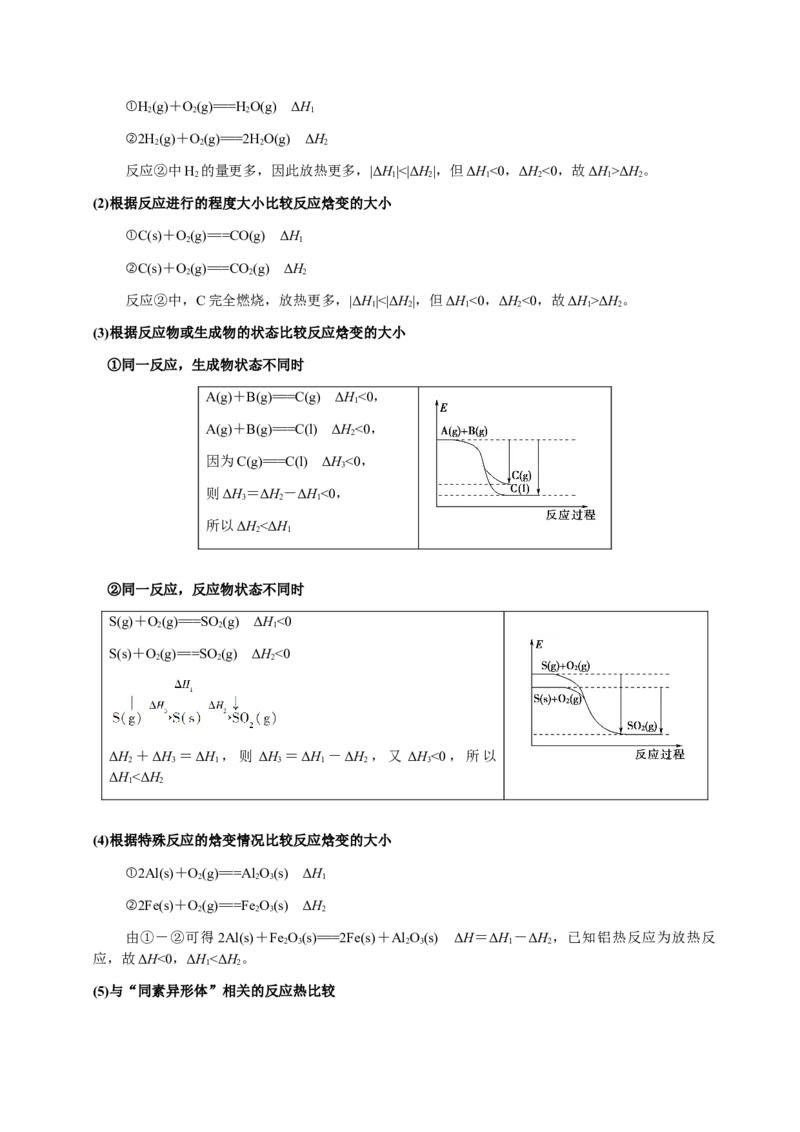
①同一反应,生成物状态不同时
A(g)+B(g)===C(g) ΔH<0,
1
A(g)+B(g)===C(l) ΔH<0,
2
因为C(g)===C(l) ΔH<0,
3
则ΔH=ΔH-ΔH<0,
3 2 1
所以ΔH<ΔH
2 1
②同一反应,反应物状态不同时
S(g)+O(g)===SO(g) ΔH<0
2 2 1
S(s)+O(g)===SO(g) ΔH<0
2 2 2
ΔH +ΔH =ΔH ,则 ΔH =ΔH -ΔH ,又 ΔH<0,所以
2 3 1 3 1 2 3
ΔH<ΔH
1 2
(4)根据特殊反应的焓变情况比较反应焓变的大小
①2Al(s)+O(g)===AlO(s) ΔH
2 2 3 1
②2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 2
由①-②可得2Al(s)+Fe O(s)===2Fe(s)+Al O(s) ΔH=ΔH -ΔH ,已知铝热反应为放热反
2 3 2 3 1 2
应,故ΔH<0,ΔH<ΔH。
1 2
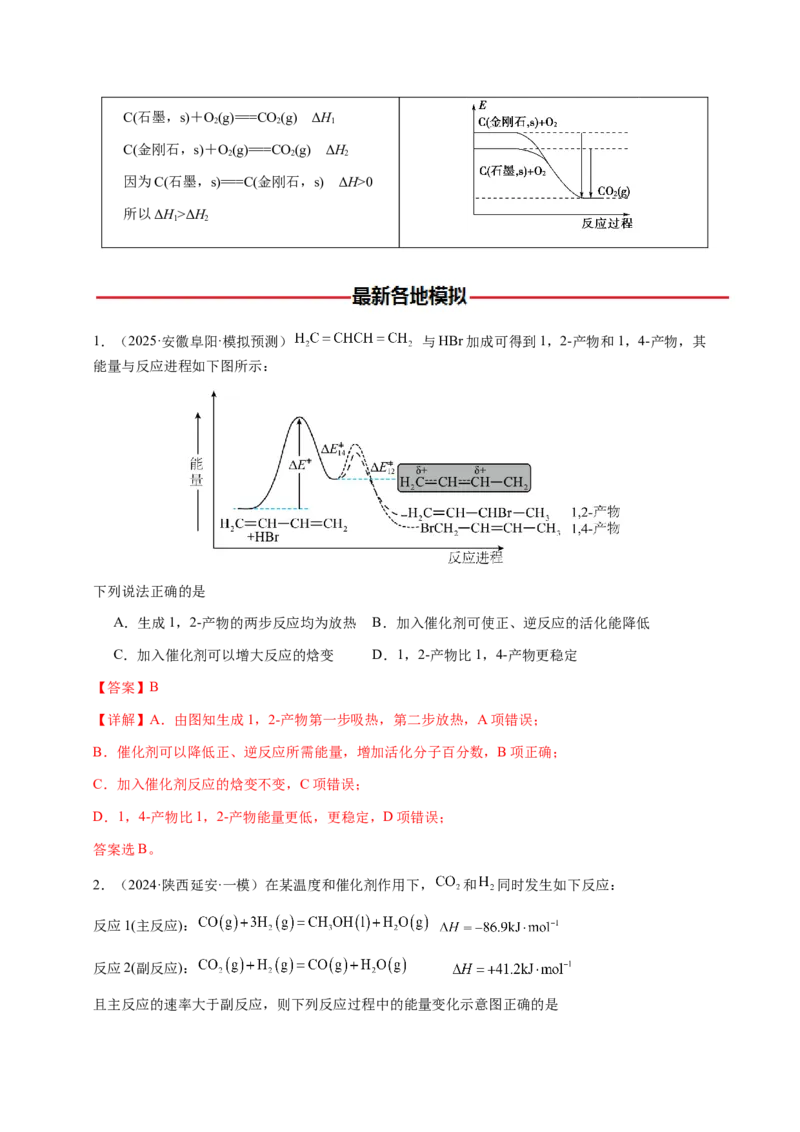
(5)与“同素异形体”相关的反应热比较C(石墨,s)+O(g)===CO (g) ΔH
2 2 1
C(金刚石,s)+O(g)===CO (g) ΔH
2 2 2
因为C(石墨,s)===C(金刚石,s) ΔH>0
所以ΔH>ΔH
1 2
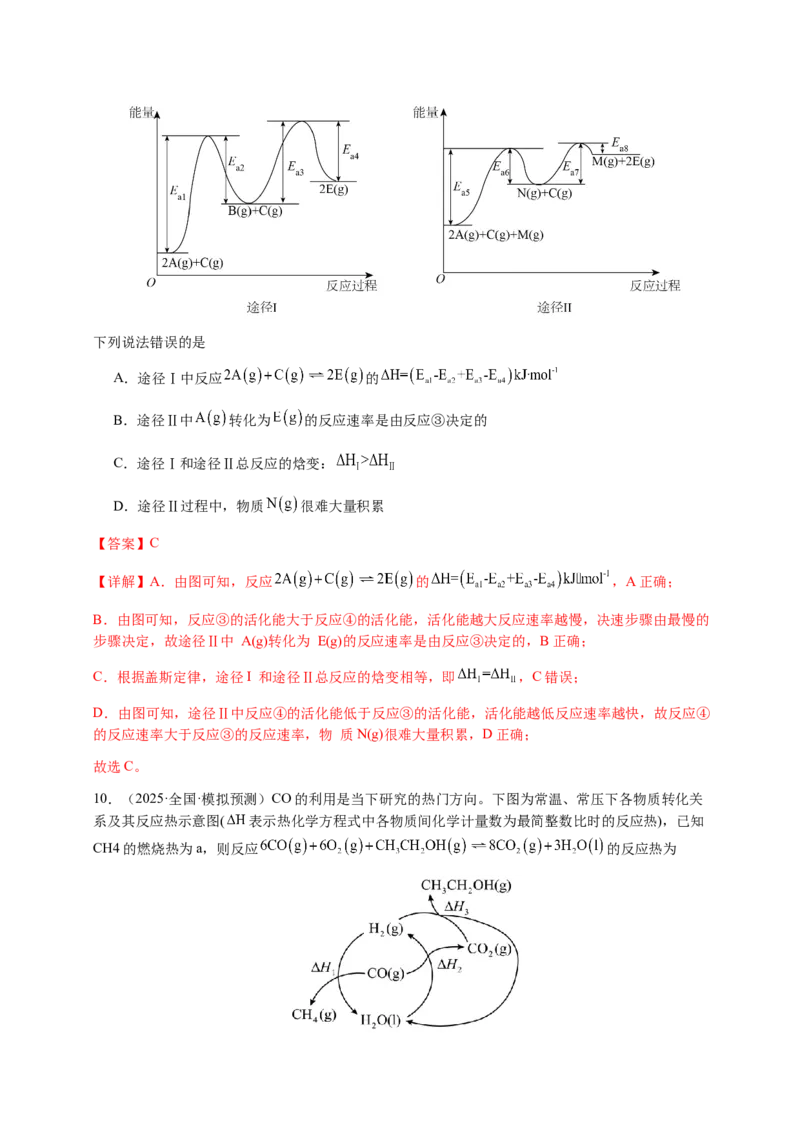
1.(2025·安徽阜阳·模拟预测) 与HBr加成可得到1,2-产物和1,4-产物,其
能量与反应进程如下图所示:
下列说法正确的是
A.生成1,2-产物的两步反应均为放热 B.加入催化剂可使正、逆反应的活化能降低
C.加入催化剂可以增大反应的焓变 D.1,2-产物比1,4-产物更稳定
【答案】B
【详解】A.由图知生成1,2-产物第一步吸热,第二步放热,A项错误;
B.催化剂可以降低正、逆反应所需能量,增加活化分子百分数,B项正确;
C.加入催化剂反应的焓变不变,C项错误;
D.1,4-产物比1,2-产物能量更低,更稳定,D项错误;
答案选B。
2.(2024·陕西延安·一模)在某温度和催化剂作用下, 和 同时发生如下反应:
反应1(主反应):
反应2(副反应):
且主反应的速率大于副反应,则下列反应过程中的能量变化示意图正确的是A. B. C. D.
【答案】A
【详解】反应1为放热反应,则反应物的总能量高于生成物的总能量,反应2为吸热反应,则反应物
的总能量低于生成物的总能量,B、C两项均错误;反应1的速率大于反应2的速率,说明反应1的
活化能小于反应2的活化能,A项正确,D项错误;
答案选A。
3.(2025·吉林长春·模拟预测)下列有关热化学方程式及其叙述正确的是
A.甲烷的燃烧热为 ,则甲烷燃烧的热化学方程式为:
B.若 ,则
C. 、 完全反应,放出热量 ,则
D. ; ,则有
【答案】D
【详解】A.甲烷的燃烧热为 ,燃烧热是在101kPa,1mol纯物质完全燃烧生成指定产物时
放出的热量,氢元素应该变为 ,则甲烷燃烧的热化学方程式为:
,A错误;
B. 还有沉淀生成,生成2mol水时放热大于
114.6kJ, ,B错误;
C.若 和 完全反应放热 ,则2molSO (g)在O 中完全反应放热
2 2
196.6kJ,所以热化学方程式为: ,但是二氧化硫与氧
气的反应是可逆反应,反应不可能完全进行,C错误;
D.氢气与氧气反应是放热反应,焓变小于0, 放出的热量大于
,所以 ,D正确;故选D。
4.(2025·宁夏银川·模拟预测)多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者
发现 时,甲醇与水(各物质均为气态)在铜基催化剂上的反应机理和能量图如下:
下列说法正确的是
A.反应Ⅱ的热化学方程式为:
B. 和 的总能量大于 和 的总能量
C.选择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗
D. 在反应中生成又消耗, 可认为是催化剂
【答案】C
【详解】A.结合能量图可知,反应Ⅱ为放热反应,根据反应机理图可知,反应Ⅱ的热化学方程式
为:CO(g)+HO(g)=H (g)+CO (g) ΔH=-akJ/mol(a>0),A错误;
2 2 2
B.结合反应机理和能量图可知,E >E ,即1molCH OH(g)和1molH O(g)的总能量小于
Ⅱ生 Ⅰ反 3 2
1molCO (g)和3molH (g)的总能量,B错误;
2 2
C.选择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,加快反应速率,减少过程中的能耗,C正确;
D. 在反应机理中先生成后消耗且量相等,因此CO(g)属于中间产物,不是催化剂,D错误;
故选C。
5.(2025·浙江·模拟预测)实验,是化学离不开的主题。下列说法中正确的是
A.图1装置用 和 测定中和反应的反应热
B.图2表示盐酸与 溶液的反应的体系与环境
C.图3装置可用于卤代烃的水解反应D.图4装置可用于简单的电镀实验
【答案】B
【详解】A. 为弱酸,电离吸热,测定中和热会产生误差,A错误;
B.盐酸与 溶液的反应为放热反应,图示为反应的体系和环境,体系与环境之间无物质交换,
但有能量交换,B正确;
C.卤代烃在碱性条件下水解产生醇、盐和水,用酸性高锰酸钾溶液不能检验卤代烃水解产物,C错
误;
D.该装置为电镀装置,与正极相连的为阳极,与负极相连的为阴极,该实验的目的是在铁表面镀
铜,应将铜放在阳极,铁放在阴极,D错误;
故选B。
6.(2025·河北·模拟预测)热力学规定:在298.15K时,由最稳定单质生成1mol化合物时的焓变,
叫做该物质的标准摩尔生成焓 ;最稳定单质的标准摩尔生成焓规定为零。将等物质的量的
和 充入真空恒容密闭容器中,在有催化剂的条件下发生反应:
。相关物质的标准摩尔生成焓数据如下表所示。我国学者通过
计算机模拟进行理论研究,认为在 合金或 合金催化下,该反应以甲烷逐级脱氢开始反
应。脱氢阶段的反应历程如下图所示(*表示吸附在催化剂表面)。下列说法正确的是
物质
0
A.该反应正向为放热反应
B.容器内气体密度不变时,反应达到平衡状态
C.甲烷逐级脱氢历程中最大能垒(活化能)D.两种催化剂比较,脱氢反应阶段催化效果更好的是 合金
【答案】D
【详解】A.由题给数据可知,反应物的标准摩尔生成焓之和为
,生成物的标准摩尔生成焓之和为
,则该反应为反应物总能量小于生成物总能量的吸热反应,A
项错误;
B.该反应在恒容密闭容器中进行,反应中容器体积不变,混合气体的密度始终不变,B项错误;
C.从图中可以看出,正反应的活化能最大的为形成过渡态2的活化能,
,C项错误;
D.据图可知使用 合金作催化剂时,整个过程中的每一步反应的活化能都较小,反应速率较
快,催化效果更好,D项正确;
故答案选D。
7.(2024·陕西延安·一模)已知:
①
②
③
下列说法不正确的是
A.石墨的燃烧热
B.
C.反应①②③均为放热反应
D.若将反应①设计成原电池,则22.4L 在正极反应时转移2mol电子
【答案】D
【详解】A.燃烧热是指1mol可燃物完全燃烧生成稳定氧化物放出的热量,A正确;
B.生成CO时放出的热量减小,故 ,B正确;
C.反应①②③的 均小于0,均为放热反应,C正确;
D.将反应①设计成原电池,1 mol 在正极发生还原反应时转移2 mol电子,但题中没有说明气体
是否在标准状况下,故无法计算,D错误;故选D。
8.(2025·河南·模拟预测)下列热化学方程式中正确的是
A. 在 催化下分解生成 放热 :
B. 和 发生中和反应生成 的反应热为 :
C. 的燃烧热为 , 完全燃烧的热化学方程式:
D.在浓硫酸作用下, 和 发生酯化反应放热25.6kJ:
【答案】C
【详解】A.HO(1)在 MnO 催化下分解生成16gO (g)放热106 kJ,则生成1mol氧气放出热量为
2 2 2 2
212kJ,其热化学方程式为2HO (1)=2HO(1)+O (g) △H=-212kJ·mol-1,A 错误;
2 2 2 2
B.未标明各物质的聚集状态,B 错误;
C.NH (g)的燃烧热为622 kJ·mol-1,则 NH (g)完全燃烧的热化学方程式为NH (g)+O(g)= N (g)
2 4 2 4 2 4 2 2
+2H O(1)△H=-622 kJ·mol-1,C正确;
2
D.酯化反应为可逆反应,反应热应表示完全转化的热效应,D错误;
故选C。
9.(2025·河南·模拟预测)已知 和 经过两种途径转化为 的反应如下:
途径Ⅰ:① ;② ;
途径Ⅱ:③ ;④ 。其反应过程的能量变化如图所
示,已知 的单位为 。下列说法错误的是
A.途径Ⅰ中反应 的
B.途径Ⅱ中 转化为 的反应速率是由反应③决定的
C.途径Ⅰ和途径Ⅱ总反应的焓变:
D.途径Ⅱ过程中,物质 很难大量积累
【答案】C
【详解】A.由图可知,反应 的 ,A正确;
B.由图可知,反应③的活化能大于反应④的活化能,活化能越大反应速率越慢,决速步骤由最慢的
步骤决定,故途径Ⅱ中 A(g)转化为 E(g)的反应速率是由反应③决定的,B正确;
C.根据盖斯定律,途径I 和途径Ⅱ总反应的焓变相等,即 ,C错误;
D.由图可知,途径Ⅱ中反应④的活化能低于反应③的活化能,活化能越低反应速率越快,故反应④
的反应速率大于反应③的反应速率,物 质N(g)很难大量积累,D正确;
故选C。
10.(2025·全国·模拟预测)CO的利用是当下研究的热门方向。下图为常温、常压下各物质转化关
系及其反应热示意图( 表示热化学方程式中各物质间化学计量数为最简整数比时的反应热),已知
CH4的燃烧热为a,则反应 的反应热为A. B.
C. D.
【答案】A
【详解】由题图和题目信息可得以下热化学方程式, ,
,
, ,根据盖斯定律,结合目标热化学方程
式 –可知,总反应的反应热为
;
A符合题意。
11.(2024·四川自贡·一模)碳酸二甲酯 是一种低毒、性能优良的有机合成中
间体,科学家提出了新的合成方案(吸附在固体催化剂表面上的物种用*标注),反应机理如图所
示。
下列说法正确的是
A.反应过程中除固体催化剂外,还使用了 做催化剂
B.反应进程中决速步骤的能垒为
C.第3步的基元反应方程式为:
D.升高温度,合成碳酸二甲酯反应速率增加,平衡向逆反应方向移动
【答案】A
【详解】A.HO·在反应前参与反应,反应后又生成,作催化剂,A正确;
B.反应进程中经过渡态Ⅰ的反应能垒最大,是决速步骤,其能垒为[103.1-
(-22.6)]×102eV=1.257×104eV,B错误;
C.第3步的基元反应方程式为: ,C错误;
D.由图可以看出,2CHOH+CO →CHOCOOCH +H O △H>0,升高温度,合成碳酸二甲酯反应速
3 2 3 3 2率增加,平衡向正反应方向移动,D错误;
故答案为:A。
12.(2024·河南·三模)研究人员提出利用含硫物质的热化学循环实现太阳能的转化与存储,其原理
如图所示。
已知:① 液态 完全分解生成三种气体时吸收热量 ;
② 固态硫完全燃烧放出热量为 。下列叙述错误的是
A.上述循环至少涉及四种能量转化方式
B.反应Ⅰ:
C.反应Ⅲ:
D.反应Ⅱ:
【答案】D
【详解】A.上述循环过程至少涉及四种能量转化方式:太阳能→热能→化学能→热能→电能,A项
正确;
B.结合已知条件可知, 完全分解为二氧化硫、氧气和水蒸气,吸收热量 ,热化
学方程式表示为: ,B项正确;
C. 相当于 ,已知 固态硫完全燃烧放出热量为 ,则 完全燃烧放出热量
,热化学方程式为: ,C项正确;
D.根据盖斯定律,-(反应Ⅰ+反应Ⅲ)=反应Ⅱ, ,D
项错误;
故选:D。
13.(2025·云南昆明·一模)根据伯恩哈勃循环图,部分反应的 如下表所示,K的第一电离能是数值 +89 +121.5 -349 -717 -436.5
A. B.
C. D.
【答案】B
【详解】根据盖斯定律: + + + + = ,解得 = ;
故选B;
14.(2025·重庆·一模)甲醇的用途非常广泛。科学家通过 合成甲醇的反应为:
。
已知:
若合成甲醇的反应中正反应的活化能为 ,逆反应的活化能为 ,则 一定等于
A. B.
C. D.
【答案】B
【详解】反应I ,反应Ⅱ
,根据盖斯定律,反应
可以由反应Ⅰ×3-反应Ⅱ得到,则ΔH=3ΔH -ΔH =(3a-
1 2 3
b)kJ·mol-1,ΔH=E -E =(3a-b)kJ·mol-1,则 ;
1 正 逆
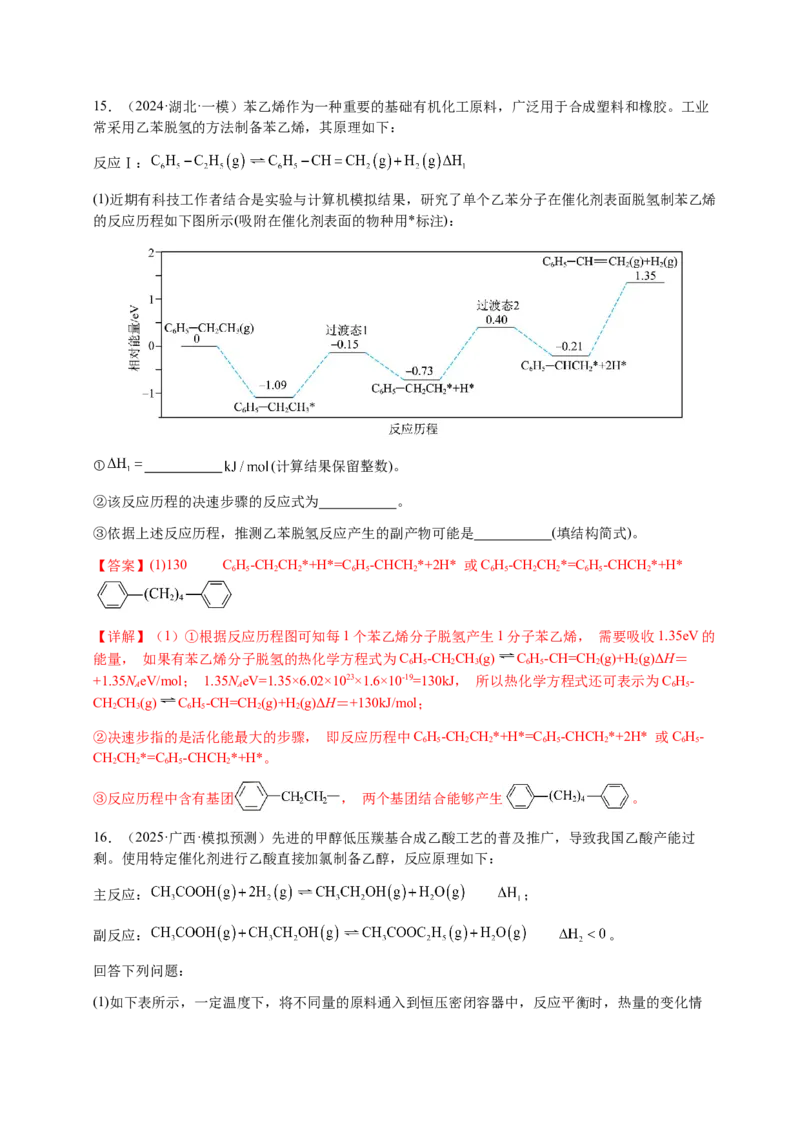
答案选B。15.(2024·湖北·一模)苯乙烯作为一种重要的基础有机化工原料,广泛用于合成塑料和橡胶。工业
常采用乙苯脱氢的方法制备苯乙烯,其原理如下:
反应Ⅰ:
(1)近期有科技工作者结合是实验与计算机模拟结果,研究了单个乙苯分子在催化剂表面脱氢制苯乙烯
的反应历程如下图所示(吸附在催化剂表面的物种用*标注):
① (计算结果保留整数)。
②该反应历程的决速步骤的反应式为 。
③依据上述反应历程,推测乙苯脱氢反应产生的副产物可能是 (填结构简式)。
【答案】(1)130 C H-CHCH*+H*=C H-CHCH *+2H* 或C H-CHCH*=C H-CHCH *+H*
6 5 2 2 6 5 2 6 5 2 2 6 5 2
【详解】(1)①根据反应历程图可知每1个苯乙烯分子脱氢产生1分子苯乙烯, 需要吸收1.35eV的
能量, 如果有苯乙烯分子脱氢的热化学方程式为C H-CHCH(g) C H-CH=CH(g)+H(g)ΔH=
6 5 2 3 6 5 2 2
+1.35N eV/mol; 1.35N eV=1.35×6.02×1023×1.6×10-19=130kJ, 所以热化学方程式还可表示为C H-
A A 6 5
CHCH(g) C H-CH=CH(g)+H(g)ΔH=+130kJ/mol;
2 3 6 5 2 2
②决速步指的是活化能最大的步骤, 即反应历程中C H-CHCH*+H*=C H-CHCH *+2H* 或C H-
6 5 2 2 6 5 2 6 5
CHCH*=C H-CHCH *+H*。
2 2 6 5 2
③反应历程中含有基团 , 两个基团结合能够产生 。
16.(2025·广西·模拟预测)先进的甲醇低压羰基合成乙酸工艺的普及推广,导致我国乙酸产能过
剩。使用特定催化剂进行乙酸直接加氯制备乙醇,反应原理如下:
主反应: ;
副反应: 。
回答下列问题:
(1)如下表所示,一定温度下,将不同量的原料通入到恒压密闭容器中,反应平衡时,热量的变化情况。已知副反应热效应小,可忽略,则该温度下主反应的 。
反应物投入量
实验编号 平衡时,热量变化
Ⅰ 0.5mol 1mol 0 0 放热x kJ
Ⅱ 0 0 1mol 1mol 吸热y kJ
【答案】(1)-(2x+y)
【详解】(1)0.5mol 与1mol 发生反应,达到平衡时放热x kJ,1mol
与1mol 发生反应,达到平衡时吸热y kJ,则1mol 与2mol
完全反应生成1mol 与1mol ,放热 ,即
;
17.(2024·河南·三模)几种物质的燃烧热如下表所示。
可燃物
燃烧热
回答下列问题:
(1)写出表示 燃烧热的热化学方程式: 。
(2) 。
(3)某水煤气含 、 、 和 ,其中 、 体积分数分别为 、 。标准状况下,
这种水煤气完全燃烧生成液态水和二氧化碳时放出的热量为 。该水煤气中 、 的
物质的量分别为 、 。
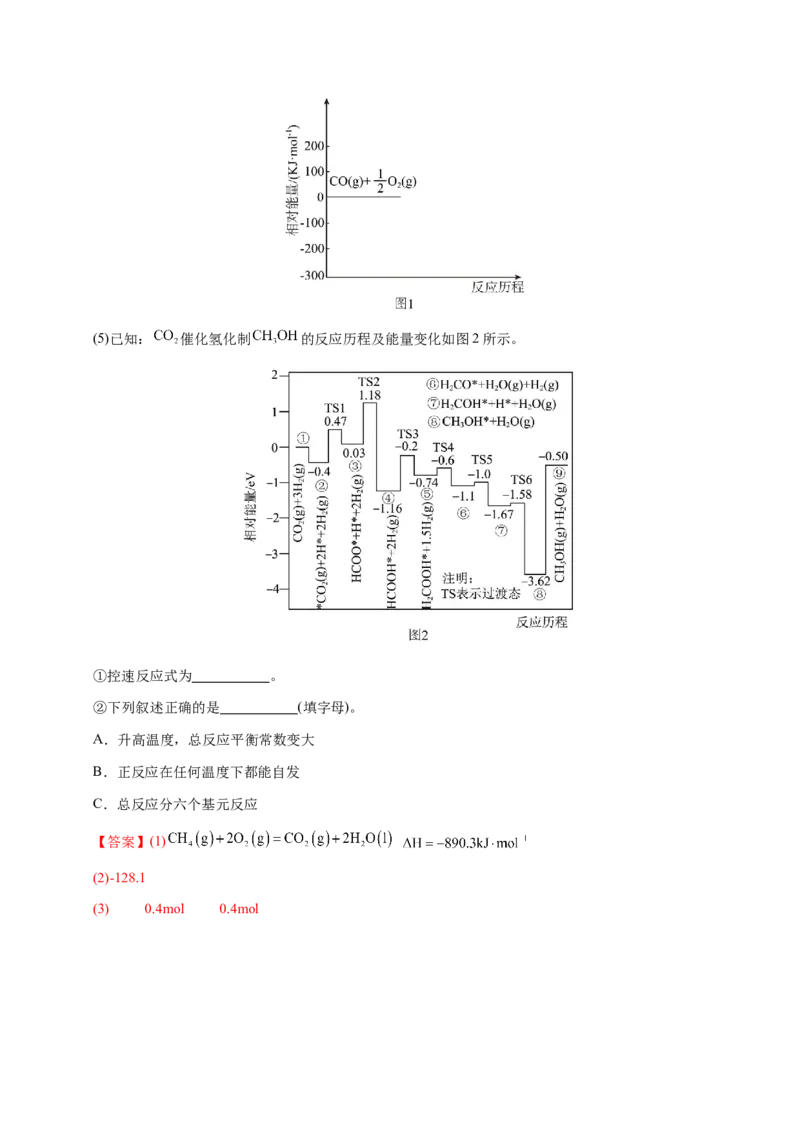
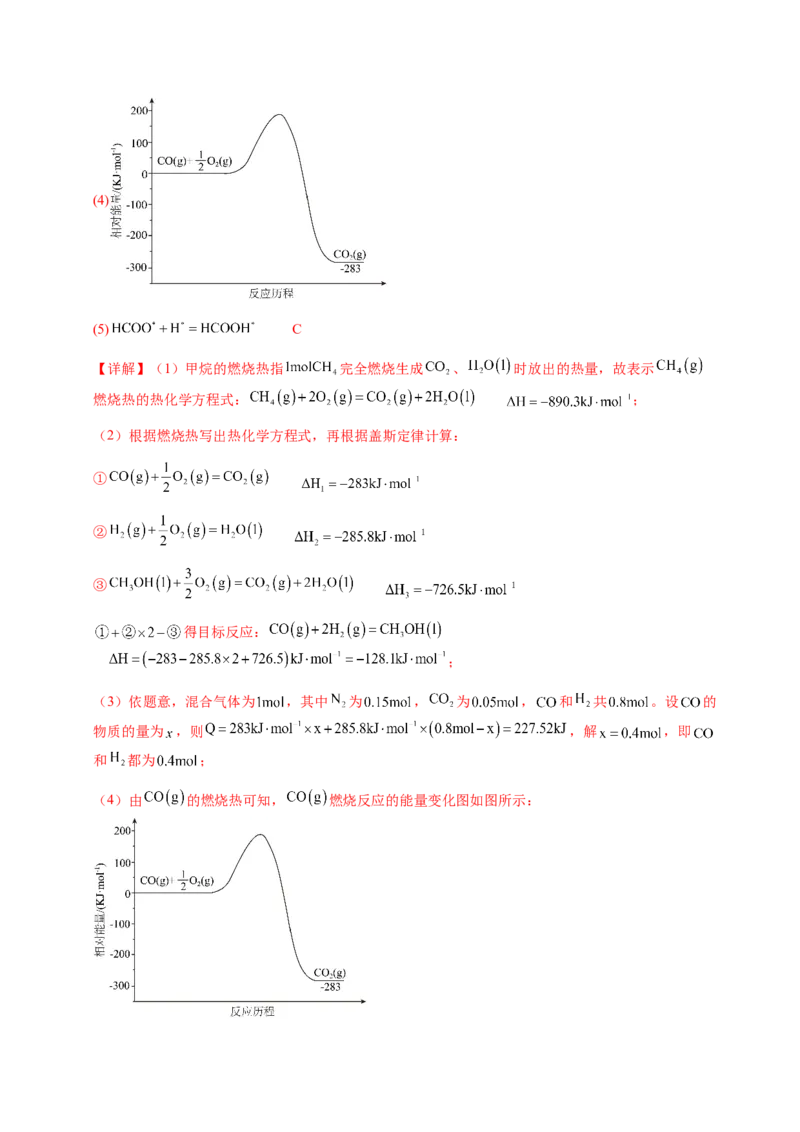
(4)在如图1坐标系中补全 燃烧反应的能量变化图 。(5)已知: 催化氢化制 的反应历程及能量变化如图2所示。
①控速反应式为 。
②下列叙述正确的是 (填字母)。
A.升高温度,总反应平衡常数变大
B.正反应在任何温度下都能自发
C.总反应分六个基元反应
【答案】(1)
(2)-128.1
(3) 0.4mol 0.4mol(4)
(5) C
【详解】(1)甲烷的燃烧热指 完全燃烧生成 、 时放出的热量,故表示
燃烧热的热化学方程式: ;
(2)根据燃烧热写出热化学方程式,再根据盖斯定律计算:
①
②
③
得目标反应:
;
(3)依题意,混合气体为 ,其中 为 , 为 , 和 共 。设 的
物质的量为 ,则 ,解 ,即
和 都为 ;
(4)由 的燃烧热可知, 燃烧反应的能量变化图如图所示:(5)①能垒最大的反应对应的是③到④,最慢反应就是控速反应,反应方程式为
;
②总反应为
A.总反应是放热反应,升温,平衡常数减小,A项错误;
B.正反应是熵减、焓减反应,在较低温度下能自发进行,B项错误;
C.总反应分六个过渡态,即有6个基元反应,C项正确,
故选C。
18.(2024·吉林长春·模拟预测)按要求回答下列问题
Ⅰ.制取甲胺的反应为 。已知该反应中相关化学
键的键能数据如下:
共价键
键能( ) 351 463 393 293
(1)则该反应的 。
Ⅱ.由金红石 制取单质 ,涉及的步骤为 。已知:
①
②
③
(2)则反应 的 (含 、 、 的关系
式表示)。
【答案】(1)-12 (2)ΔH +2ΔH -ΔH
3 1 2
【详解】(1)△H=反应物总键能-生成物总键能,故△H=[3E(C-H)+E(C-O)+E(H-O)+3E(N-H)]-[3
E(C-H)+E(C-N)+2E(N-H)+2E(H-O)]=(351+393-293-463)kJ/mol=-12kJ/mol,故答案为:-12;
(2)根据盖斯定律,由 可得: ,所以
ΔH+2ΔH -ΔH,故答案为:ΔH+2ΔH -ΔH
3 1 2 3 1 2;
19.(2024·辽宁沈阳·三模)回答下列问题。
(1) (反应I)
(反应Ⅱ)假设某温度下,反应I的速率 大于反应Ⅱ的速率 ,则说明I的活化能 Ⅱ的活化能
(填>、<或=),下列反应过程能量变化示意图正确的是 。
(2)已知25℃时中和热的 ,反应
,写出 固体的溶解平衡的热化学方程式: 。
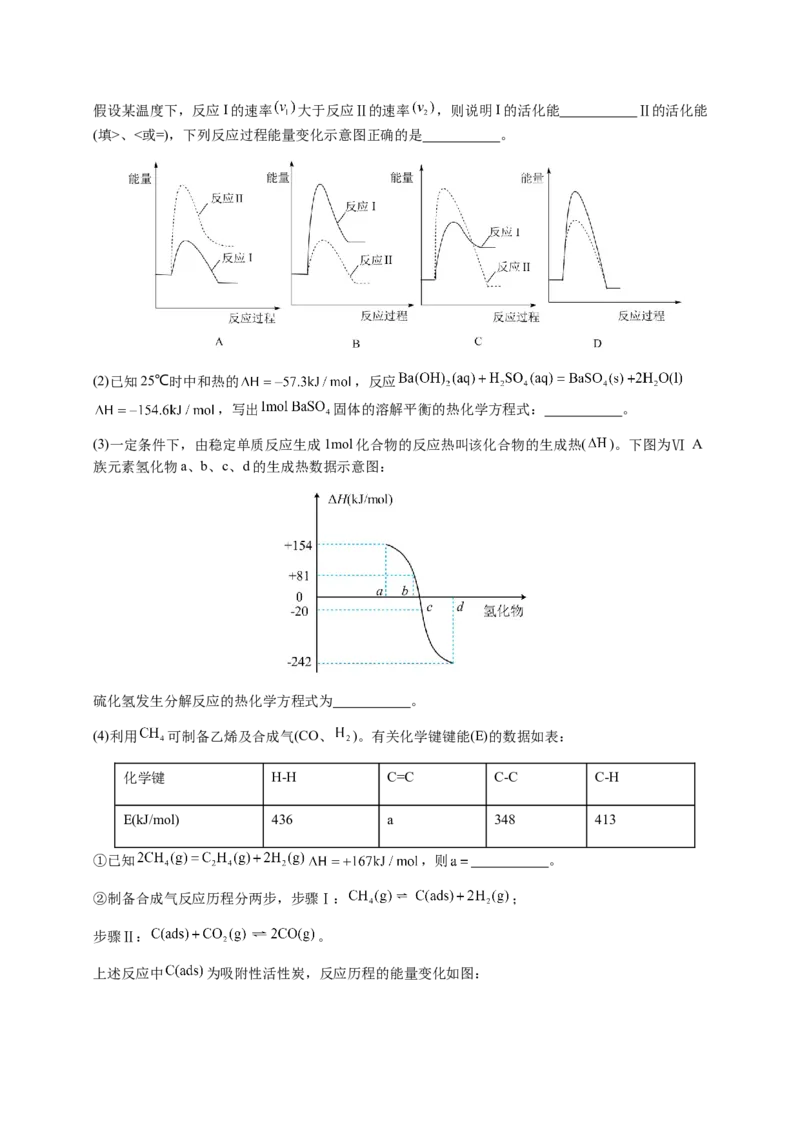
(3)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。下图为Ⅵ A
族元素氢化物a、b、c、d的生成热数据示意图:
硫化氢发生分解反应的热化学方程式为 。
(4)利用 可制备乙烯及合成气(CO、 )。有关化学键键能(E)的数据如表:
化学键 H-H C=C C-C C-H
E(kJ/mol) 436 a 348 413
①已知 ,则 。
②制备合成气反应历程分两步,步骤Ⅰ: ;
步骤Ⅱ: 。
上述反应中 为吸附性活性炭,反应历程的能量变化如图:表示步骤①正反应的 ,决定制备合成气反应速率的是 (填“步骤Ⅰ”
或“步骤Ⅱ”)。
③已知 ,
当放出的热量为nkJ时,该反应转移的电子数为 (用含m、n的代数式表示)。
【答案】
(1)< C
(2)BaSO (s) Ba2+(aq)+ SO (aq) ΔH=+40kJ/mol
4
(3)H S(g)=S(s)+H (g) ΔH=+20 kJ/mol
2 2
(4)613 活化能 步骤Ⅰ
【详解】(1)反应的活化能越大,反应速率越慢,则某温度下,反应I的速率大于反应Ⅱ的速率,
说明反应I的活化能小于反应Ⅱ;反应I是反应物总能量小于生成物总能量的吸热反应,反应Ⅱ是反
应物总能量大于生成物总能量的放热反应,则反应过程能量变化示意图为 ,故
选C,故答案为:<;C;
(2)由题意可得如下热化学方程式:
①H+(aq)+ OH-(aq)=H O(l) ΔH=-57.3kJ/mol
2
②Ba2+(aq) +2OH-(aq)+ SO (aq)+2H+(aq)=BaSO (s)+2 H O(l) ΔH=-154.6kJ/mol
4 2
由盖斯定律可知,反应①×2-反应②得到硫酸钡固体的溶解平衡BaSO(s) Ba2+(aq)+ SO (aq)则
4
ΔH=(-57.3kJ/mol)×2-(-154.6kJ/mol)=+40kJ/mol,固体溶解的热化学方程式为BaSO(s) Ba2+(aq)+ SO
4(aq) ΔH=+40kJ/mol,故答案为:BaSO(s) Ba2+(aq)+ SO (aq) ΔH=+40kJ/mol;
4
(3)同主族元素,从上到下非金属性依次减弱,气态氢化物的热稳定性依次减弱,生成气态氢化物
的焓变ΔH依次增大,则点c表示硫化氢,由图可知,生成硫化氢的热化学方程式为S(s)+H (g)=
2
HS(g) ΔH=-20 kJ/mol,所以硫化氢发生分解反应的热化学方程式为HS(g)=S(s)+H (g) ΔH=+20
2 2 2
kJ/mol,故答案为:HS(g)=S(s)+H (g) ΔH=+20 kJ/mol;
2 2
(4)①反应ΔH=反应物总键能-生成物总键能,则2×4×413kJ/mol-(a+4×413kJ/mol+2×436kJ/
mol)=+167kJ/mol,解得a=613kJ/mol,故答案为:613;
②由图可知,E—E 表示步骤①正反应的活化能;反应的活化能越大,反应速率越慢,慢反应是反应
4 1
的决速步,步骤Ⅰ反应的活化能大于步骤Ⅱ,所以决定制备合成气反应速率的是步骤Ⅰ,故答案为:
步骤Ⅰ;
③由热化学方程式可知,反应转移电子的物质的量为60mol时,反应对应放出的热量为mkJ,则放出
的热量为n kJ时,转移的电子数为 ,故答案为: 。
20.(2025·上海松江·一模)氨是最基本的化工原料之一,用途广泛。自1913年合成氨工业化以来,
科学家一直致力于合成氨技术的研究和发展。已知:
。
(1)有关温度对该反应自发性的影响,下列说法正确的是_______。
A.低温自发 B.高温自发
C.任何温度下均自发 D.任何温度下均不自发
(2)合成氨反应中部分共价键的键能如下表所示:
共价
键能( )
键
H—H 436
946
计算N-H的键能为_______ 。
A.1173 B.782 C.391 D.360
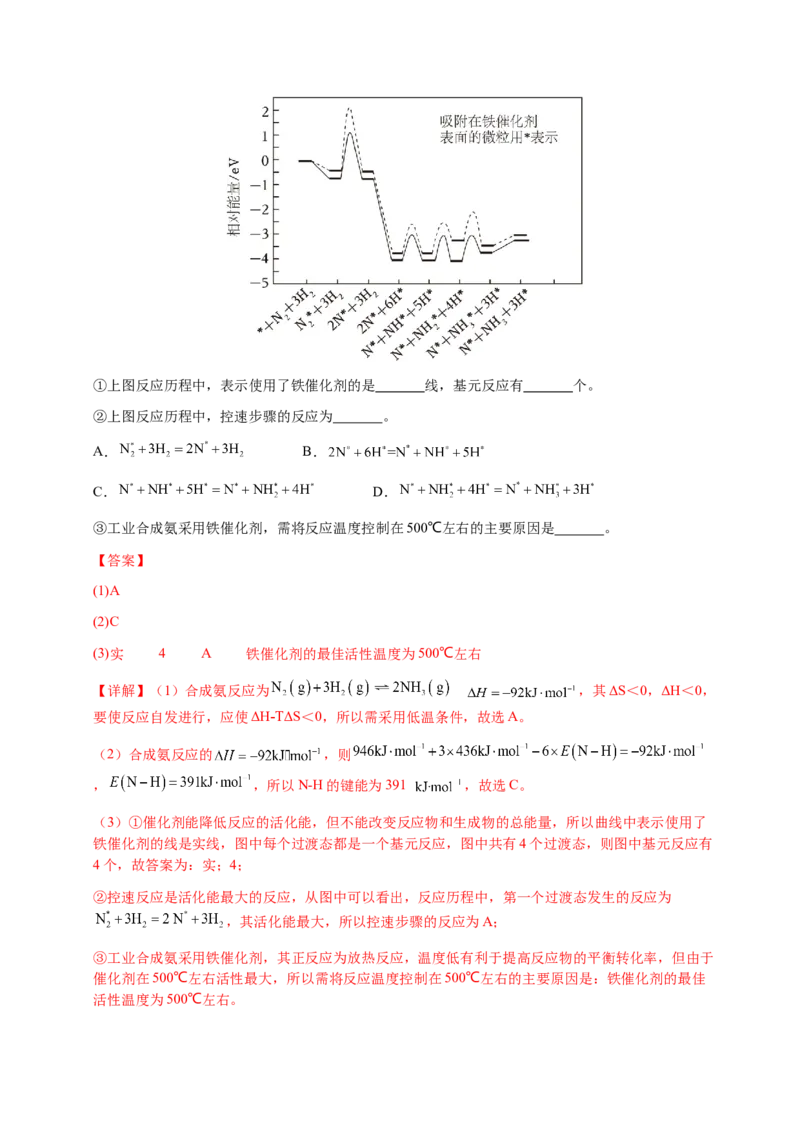
(3)下图为使用铁催化剂和未使用催化剂合成氨反应历程的一部分。①上图反应历程中,表示使用了铁催化剂的是 线,基元反应有 个。
②上图反应历程中,控速步骤的反应为 。
A. B.
C. D.
③工业合成氨采用铁催化剂,需将反应温度控制在500℃左右的主要原因是 。
【答案】
(1)A
(2)C
(3)实 4 A 铁催化剂的最佳活性温度为500℃左右
【详解】(1)合成氨反应为 ,其ΔS<0,ΔH<0,
要使反应自发进行,应使ΔH-TΔS<0,所以需采用低温条件,故选A。
(2)合成氨反应的 ,则
, ,所以N-H的键能为391 ,故选C。
(3)①催化剂能降低反应的活化能,但不能改变反应物和生成物的总能量,所以曲线中表示使用了
铁催化剂的线是实线,图中每个过渡态都是一个基元反应,图中共有4个过渡态,则图中基元反应有
4个,故答案为:实;4;
②控速反应是活化能最大的反应,从图中可以看出,反应历程中,第一个过渡态发生的反应为
,其活化能最大,所以控速步骤的反应为A;
③工业合成氨采用铁催化剂,其正反应为放热反应,温度低有利于提高反应物的平衡转化率,但由于
催化剂在500℃左右活性最大,所以需将反应温度控制在500℃左右的主要原因是:铁催化剂的最佳
活性温度为500℃左右。