文档内容
专题 28 化学平衡常数及转化率的计算
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 化学平衡常数的含义与应用
考点二 化学平衡常数及转化率的计算
考点一 化学平衡常数的含义与应用
1.(2023·安徽·校联考模拟预测)向一个 的绝热刚性容器中通入 和 ,在一定条件下
发生反应 ,正反应速率随时间变化的示意图如下,下列结论正确的是
A.升高温度,该反应的平衡常数将增大
B.从反应开始到达到平衡,逆反应速率先增大后减小
C.体系压强不再变化,说明反应达到平衡
D.从容器中分离出少量 后, 增加, 减小,平衡正向移动
【答案】C
【分析】向一个 的绝热刚性容器中通入 和 ,因此和外界没有热交换,随着反应进行,
容器的温度会发生改变。从图像可以看出,随反应进行,反应物浓度减小,但是正反应速率增大,说明反
应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,该反应为放热反应,即生成
物的总能量低于反应物的总能量。
【解析】A.由分析可知,该反应为放热反应,升高温度,该反应的平衡常数将减小,错误;B.在达到平
衡之前,逆反应速率始终增大,错误;C.反应 是气体体积不变的反
应,反应过程中气体总物质的量不变,根据理想气体状态方程 ,可以看出,压强与温度成正比,
只要反应还在向右进行,容器的温度就会持续升高,压强就会一直增大。因此,压强不变可以说明达到了
平衡状态,正确;D.从容器中分离出少量 后,平衡正向移动, 都减小,错误;故选C。
2.(2023·广东惠州·统考一模)氨气在工业上应用广泛,已知反应
,反应相同时间, 的体积百分数随温度的变化情况如图所示,下列相关描述正确的是
1
原创精品资源学科网独家享有版权,侵权必究!A.线上的点均代表平衡时刻的点 B.逆反应速率:
C.b点时 D.平衡常数值:
【答案】D
【分析】由图可知,c点氨气的体积百分数最大,说明反应达到平衡,则c点以前为平衡的形成过程,c点
以后为平衡的移动过程。
【解析】A.由分析可知,c点以前均未达到平衡,故A错误;B.温度越高,反应速率越快,则d点逆反
应速率大于a点,故B错误;C.由分析可知,b点反应未达到平衡,正反应速率大于逆反应速率,故C错
误;D.该反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,由分析可知,c点以后为
平衡的移动过程,则c点平衡常数大于d点,故D正确;故选D。
3.(2023·江苏·统考一模)硫及其化合物有着广泛的作用。硫元素具有多种化合价,在一定条件下能发生
相互转化。不同温度下硫单质的状态和分子结构不同, 环状分子的结构为 。合理应
用和处理含硫的化合物,在生产生活中有重要意义。利用甲烷可以除去 ,反应为
。下列说法正确的是
A.上述反应的
B.上述反应的化学平衡常数
C.及时分离出 (g),正反应速率增大,平衡向正反应方向移动
D.上述反应中生成1mol ,转移电子的数目约为
【答案】D
【解析】A.反应为气体分子数增大的反应,熵变大于零;A错误;B.由方程式可知,上述反应的化学平
衡常数 ,B错误;C.及时分离出 (g),平衡向正反应方向移动,但是物质
浓度减小,正反应速率减小, C错误;D.反应中硫元素化合价由+6变为0, ,则上述反应中生
成1mol ,转移电子的数目约为 ,D正确;故选D。
4.(2023·辽宁葫芦岛·统考一模)活性炭基材料烟气脱硝技术备受当前研究者关注,其反应原理为
。下列说法不正确的是A.增大压强,平衡向脱硝方向移动
B.上述脱硝反应平衡常数
C.若恒容体系内密度恒定不变,反应达到了平衡
D.每处理标准状况下2.24LNO,转移电子0.2 mol
【答案】A
【解析】A.该反应反应前后气体体积不变,改变压强,不影响平衡状态,A错误;B.上述脱硝反应平衡
常数 ,B正确;C.因C(s)是固体,反应未平衡时,气体的总质量会发生改变,达到平
衡后,气体总质量保持不变,因此若恒容体系内密度恒定不变,反应达到了平衡,C正确;D.处理NO
时,N元素从+2价降至0价,标准状况下2.24LNO的物质的量为0.1mol,因此每处理标准状况下
2.24LNO,转移电子0.2 mol,D正确;故选A。
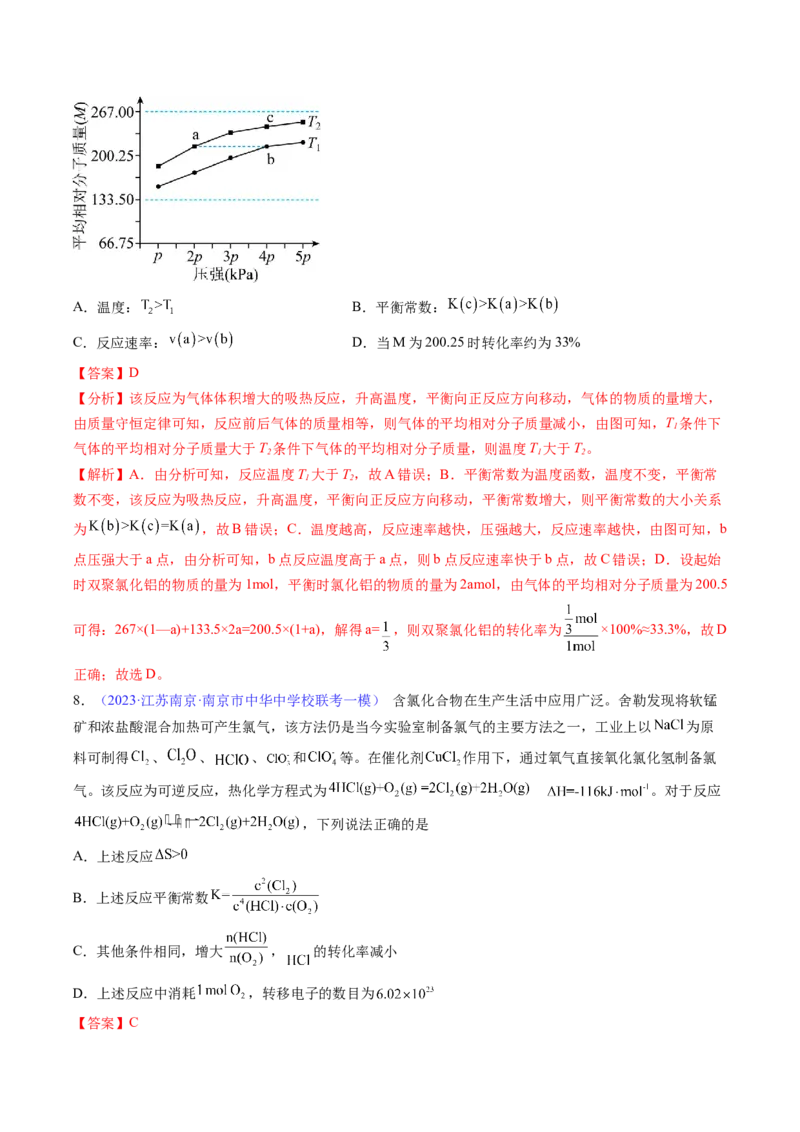
5.(2023·北京朝阳·统考一模)向体积为1L的密闭容器中充入一定量 ,发生反应:
起始物质的量(mol) 平衡物质的量(mol)
编号 温度(℃)
I 0.40 0.16 0.16
II 0.20 0.09 0.09
下列说法不正确的是
A.
B. ℃,该反应的平衡常数K=4
C.II中存在:
D. ℃时,向该容器中充入物质的量均为0.2mol的3种气体,反应将逆向进行
【答案】D
【解析】A.结合已知数据列 温度时三段式:
该温度下平衡常数K=
1
温度时三段式:该温度下平衡常数K=
2
该反应 ,温度升高平衡逆向移动减小, 由K> K 可知, ,故A正确;B.由A中分析可知,
2 1
℃,该反应的平衡常数K=4,故B正确;C.II中存在 的起始物质的量为0.2mol。则其起始
浓度=0.2mol/L,结合物料守恒可知:存在反应 ,故C正确;D.
℃时,向该容器中充入物质的量均为0.2mol的3种气体,则此时Qc=
x
2 1
C.平衡常数K:a>b=c D.净反应速率:a=bx,故B正确;C.平衡常数只与温度有关,a点对应温度较低,K
2 2 1
较大;b、c点对应温度相等,K也相等,故C正确;D.a、b、c都是平衡点,正、逆反应速率相等,净
反应速率等于0,即a、b、c的净反应速率相等,故D错误;选D。
考点二 化学平衡常数及转化率的计算
1.(2023·辽宁沈阳·辽宁实验中学校考模拟预测) 可以和 发生反应:
。一定温度下,向某恒容密闭容器中加入足量铁粉并充入一定量的 气
体,反应过程中 气体和 气体的浓度与时间的关系如图所示。下列说法正确的是
A. 时该化学反应达到平衡状态
B.平衡后向容器内充入 ,重新达到平衡时 增大
C.4 min时, 的转化率约为71.4%
D.4 min内, 的平均反应速率【答案】C
【解析】A.由图可知,tmin时c(CO)=c(CO),相同条件下tmin后c(CO)仍在减小,c(CO)仍在增大,则
1 2 1 2
tmin时该化学反应没有达到平衡状态,故A错误;B.该反应的平衡常数K= ,只与温度有关,温
1
度不变则K不变,所以重新达到平衡时 不变,故B错误;C.由图可知,4min时,CO 的转化率
2
为 ×100%≈71.4%,故C正确;D.由图可知,4min内CO的平均反应速率v(CO)=
=0.125mol⋅L-1⋅min-1,故D错误;故选:C。
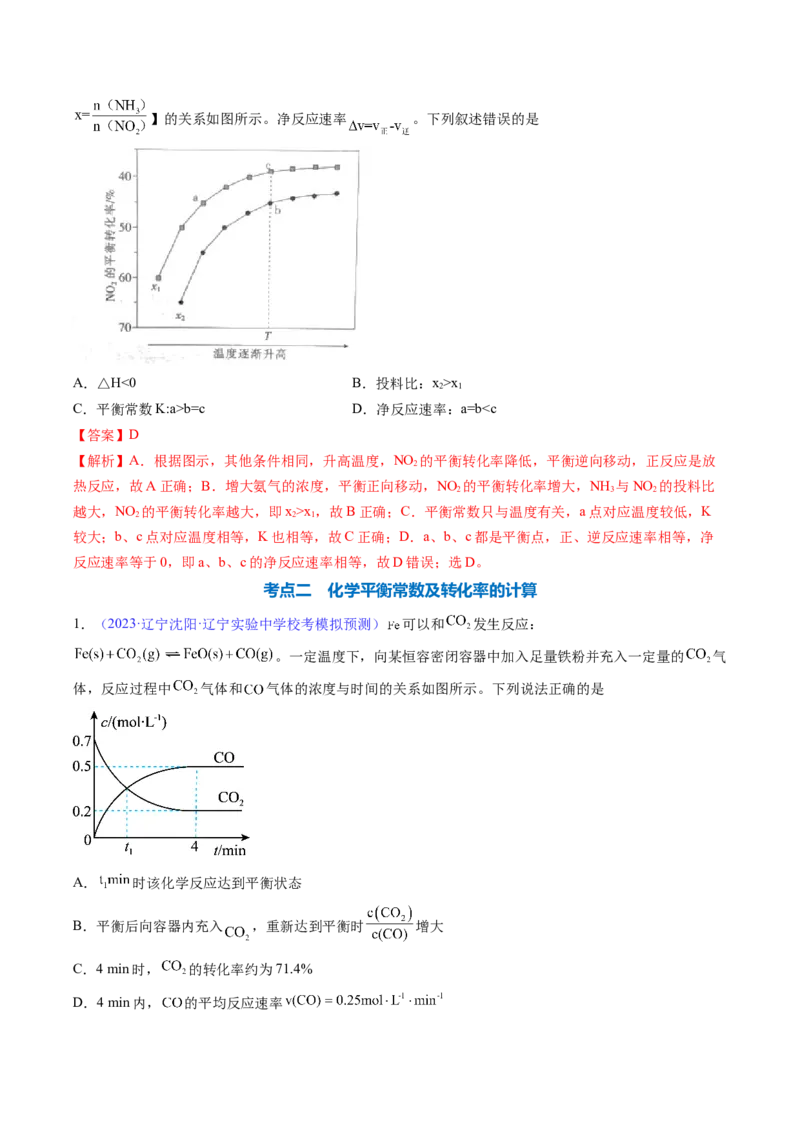
2.(2023·广东·统考二模)某温度下,向恒温、恒压容器中充入3molH 和1molCO ,在催化剂作用下发
2 2
生反应:3H(g)+CO (g) CHOH(g)+H O(g) △H<0,平衡时体系中H、CO 和HO的物质的量分数(x)
2 2 3 2 2 2 2
与平衡总压的关系如图所示。下列说法不正确的是
A.曲线a表示x(H O)随压强的变化情况
2
B.其他条件不变,降低温度会使x(b)和x(c)减小
C.Q点CO 的转化率为75%
2
D.若起始压强为106Pa,将容器改为恒容容器,平衡时x(a)>x
1
【答案】D
【解析】A.由图可知,随着平衡总压的增大,平衡正向移动,水的物质的量分数增大,则曲线a表示
x(H O)随压强的变化情况,A正确;B.由选项A分析可知,a表示x(H O),则x(b)和x(c)应该表示反应物,
2 2
该反应物为放热反应,其他条件不变,降低温度,平衡正向移动,则会使x(b)和x(c)减小,B正确;C.随
着压强增大,反应平衡是正向移动,HO物质的量分数逐渐增大,故a是表示HO (g),H 初始物质的量更
2 2 2
大,故其平衡体系中物质的量分数更大(相比CO),可得b是表示H(g),c是表示CO(g) ,假设Q点时,
2 2 2
转化的CO 是a mol,列三段式,
2
Q点平衡时HO(g) 、H(g)物质的量分数相等,即物质的量相等,可得3-3a=a,a=0.75,则Q点CO 的转
2 2 2化率为 75%,C正确;D.该反应为气体计量系数减小的反应,若起始压强为106Pa,将
容器改为恒容容器,则随着反应进行,压强减小,平衡逆向移动,水的含量减小,即平衡时x(a)80%,
C.30℃、70℃温度下,t min时的 生成速率相等
D.80℃温度下,该反应的平衡常数为2
【答案】B
【解析】A.根据表格数据可知,随着温度升高,速率加快,50℃、30℃ t min未达平衡,70℃、80℃温度
下t min时反应已经达到平衡,为平衡转化率,平衡转化率随升高温度而减小,根据勒夏特列原理知该反
应为放热反应,A错误;A.由选项A中分析和表格数据可知,50℃时NO的转化率大于80%,B正确;
A.30℃、70℃转化率相同,但温度不同,t min时的NO 生成速率不一定相等,C错误;A.80℃温度反
2
应t min时已建立该条件下的平衡,NO、O 的起始浓度分别为1 mol/L,0.5 mol/L,NO的转化率为50%,
2
则NO、O、NO 的平衡浓度分别为0.5 mol/L、0.25mol/L、0.5mol/L,故 ,
2 2
D错误;故答案为:B。
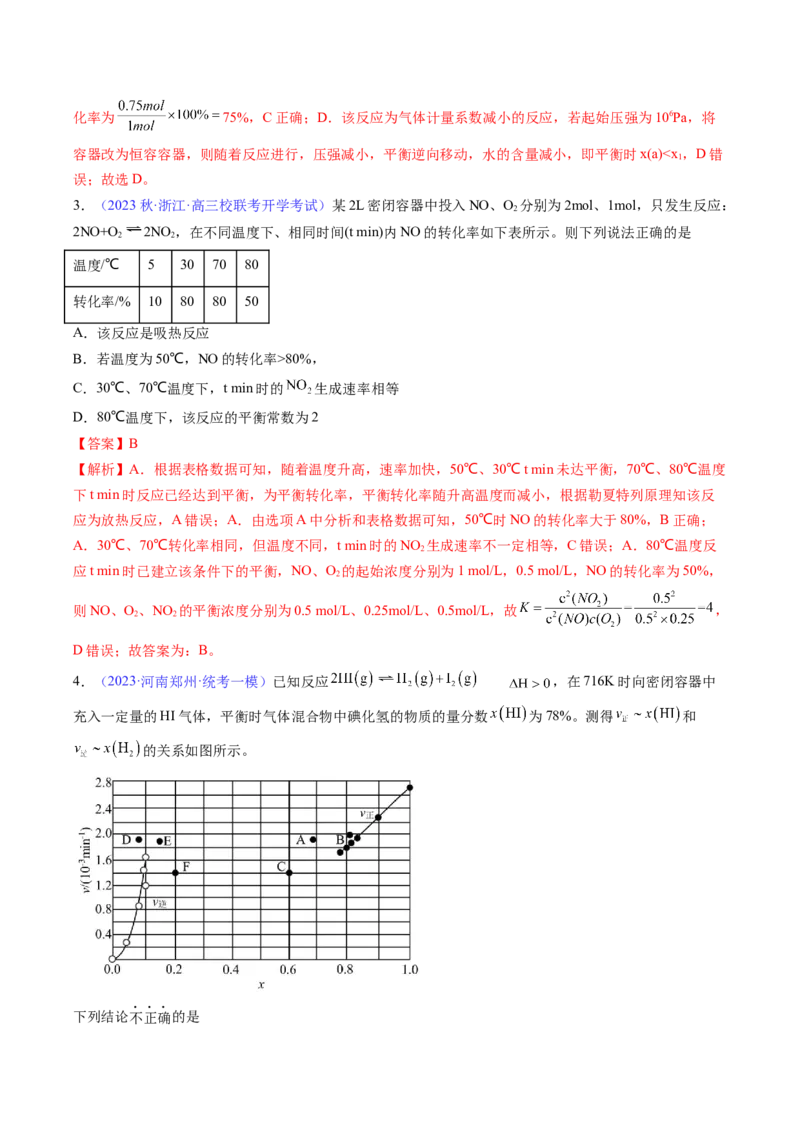
4.(2023·河南郑州·统考一模)已知反应 ,在716K时向密闭容器中
充入一定量的HI气体,平衡时气体混合物中碘化氢的物质的量分数 为78%。测得 和
的关系如图所示。
下列结论不正确的是A.该反应的压力平衡常数 约为0.02
B.增大体系压强,平衡不发生移动,平衡常数 不变
C.温度降低, 、 均减小,平衡向逆反应方向移动
D.温度升高,反应重新达到平衡时,图中表示平衡的点可能是A和D
【答案】D
【解析】A.平衡时气体混合物中碘化氢的物质的量分数 为78%,则 =11%,故HI的
平衡分压为:0.78p总,H、I 的平衡分压为:0.11p总,该反应的压力平衡常数 =
2 2
约为0.02,A正确;B.由反应方程式 可知,反应前
后气体的体积不变,故增大体系压强,平衡不发生移动,平衡常数仅仅是温度的函数,温度不变,平衡常
数 不变,B正确;C.由题干可知,该反应正反应是一个吸热反应,故温度降低, 、 均减小,平
衡向逆反应方向移动,C正确;D.该反应是吸热反应,升高到某一温度时,反应速率加快,平衡向正向
向移动,x(HI)减小,x(H)增大,当升高到某一温度时,反应重新达到平衡,v ~x(HI)和v ~x
2 正 逆
(H)相对应的点可能分别为A、E,D错误;故答案为:D。
2
5.(2023·辽宁葫芦岛·统考模拟预测)在容积均为1L的密闭容器M(500℃,恒温)、N(起始500℃,绝热)
中分别加入 、 和相同催化剂,发生反应: 。
实验测得M、N容器中 的转化率随时间的变化关系如图。下列说法错误的是
A.该反应的ΔH>0
B.500℃该反应的化学平衡常数K约为0.022
C.M容器中 的转化率随时间的变化关系是图中的曲线b
D.反应平衡后,向N容器中再加入 、 , 的平衡转化率减小
【答案】A
【解析】A.两容器的起始温度相同,如图所示,0~100s内,曲线a的NO的平衡转化率较高,则曲线a
2
的反应速率较快,说明曲线a的温度较高,则该反应是放热反应, ,A错误;B.根据曲线b,达到平衡时NO的转化率为25%,则 ,500℃该反
2
应的化学平衡常数K约为 0.022,B正确;C.反应为放热反应,则N(起始500℃,
绝热)容器的温度会升高,反应速率加快,故N容器中NO的转化率随时间的变化关系是图中的曲线a,M
2
(500容器℃,恒温)容器中NO的转化率随时间的变化关系是图中的曲线b,且温度升高,NO的平衡转化
2 2
率降低,C正确;D.反应为气体分子数不变的反应,若为恒温容器,平衡不移动,但N容器为绝热容器,
再加入 、 ,反应放热,平衡逆向移动, 的平衡转化率减小,D正确;答案选A。
6.(2023·广东汕头·金山中学校考一模)还原CoO制备Co可通过下列两个反应实现:
I.CoO(s)+H (g) Co(s)+HO(g)
2 2
II.CoO(s)+CO(g) Co(s)+CO(g)
2
723K下,在初始压强相同(均为12.0kPa)的甲、乙两密闭容器中分别发生反应I、反应II,得到部分气体的
分压随时间的变化关系如图所示。下列说法错误的是
A.甲容器中,10~40min内用H 表示的平均反应速率v(H )=0.15kPa·min-l
2 2
B.增大起始时容器的压强,CoO的平衡转化率增大
C.此条件下,选择CO还原CoO的效率更高
D.723K时,反应Ⅱ的平衡常数K=119
p
【答案】B
【解析】A.甲容器中,10~40min内,氢气分压变化为(7.5-3.0)kPa=4.5kPa,用氢气表示的平均反应速
率为 =0.15kPa/min,故A说法正确;B.根据题所给反应方程式,反应前后气体系数之和相等,增
大起始时压强,平衡不移动,CoO的平衡转化率不变,故B说法错误;C.根据两个图像可知,CO还原
CoO的速率更快,达到平衡时间更短,CO还原CoO达到平衡时,CO 分压为11.9kPa,起始压强为
2
12.0kPa,说明CO还原CoO转化更彻底,因此选择CO还原CoO的效率更高,故C说法正确;D.达到平
衡时,CO 分压为11.9kPa,该反应前后气体系数相等,总压强不变,即CO的分压为0.1kPa,K =
2 p
=119,故D说法正确;答案为B。7.(2023·广东·统考二模)乙酸甲酯催化醇解反应方程式为:
,已知
, ,其中 、 为速率常数,
为物质的量分数。己醇和乙酸甲酯按物质的量之比1∶1投料,测得348K、338K两个温度下乙酸甲酯转化
率 随时间 的变化关系如图所示,下列说法中错误的是
A.曲线①②中,曲线①对应的 更大
B.升高温度,该醇解平衡向正反应方向移动
C.a、b、c、d四点中, 与 差值最大的是b点
D.338K时,该反应的化学平衡常数为1
【答案】C
【分析】根据图像可知,①曲线的反应速率最快,说明温度高,即曲线①对应温度为348K,曲线②对应
温度为338K;
【解析】A.温度越高,反应速率越快, 值越大,根据分析以及图像可知,曲线①对应的 更大,故A
说法正确;B.由图可知,温度越高,乙酸甲酯转化率越高,反应正向进行程度变大,说明反应为吸热反
应,故升高温度,该醇解平衡向正反应方向移动,故B说法正确;C. 、 是温度的函数,该反应为吸
热反应,升高温度,平衡向正反应方向进行, 受温度的影响较大,因此升高温度, 增大程度大于 ,
即 - 的值最大的是曲线①;据图像可知,a点是反应向正方向进行,c点为平衡点,随着反应进行,v
逐渐减小,v 逐渐增大,因此四点中, 与 差值最大的是a点,故C说法错误;D.338K时,令乙酸
正 逆
甲酯的物质的量为1mol,C H OH的物质的量为1mol,则达到平衡时,消耗乙酸甲酯、C H OH的物质的
6 13 6 13
量均为1mol×50%=0.5mol,则生成CHCOOC H 和甲醇的物质的量为0.5mol,K= ,故D说法
3 6 13
正确;故选C。
8.(2023·浙江金华·浙江省丽水中学校联考一模)用CH 还原SO 不仅可以消除污染,而且可以得到单质
4 2
S,反应如下: t℃时,在容积为2L的恒容密闭容器
中测的反应在不同时刻各物质的物质的量如下表:
物质的量(mol)时间(min) 0 2 4 6 8 10物质
SO 4.8 2.64 1.8 1.8 2.1 2.1
2
CO 0 1.08 1.5 1.5 1.75 1.75
2
下列说法不正确的是
A.前2min的平均反应速率v(CH)=0.27mol·L-1·min-1
4
B.6min时SO 的转化率等于10min时SO 的转化率
2 2
C.其它条件不变,在第10min后降低温度,可使容器中的CO 的浓度升高到1.4mol·L-1
2
D.向容器内通入适量的HS,会使平衡逆向移动
2
【答案】C
【解析】A.根据 可知,前2min甲烷物质的量变化
1.08mol,则 ,故A正确;B.根据表中数据可知6min时SO 的
2
转化量为4.8mol-1.8mol=3mol,SO 转化率为 =62.5%;6min后向反应体系中加入二氧化硫,导
2
致平衡发生移动,10min时处于新的平衡,根据硫原子守恒,加入的SO 的物质的量为
2
0.3mol+(1.75mol-1.5mol) 2=0.8mol,则SO 的转化率为 =62.5%;所以转化率相等,故B 正
2
确;C.10min时,二氧化硫浓度1.05mol/L,二氧化碳浓度0.875mol/L,若不改变容器体积,结合方程式,
当二氧化硫全部转化为二氧化碳的浓度1.2mol/L,但该反应为可逆反应,低温平衡正向移动,二氧化碳浓
度不能达到1.4mol/L,故C错误;D.HS会与二氧化硫发生氧化还原反应,导致平衡逆向移动,故D正
2
确;答案选C。
9.(2023·重庆沙坪坝·重庆八中校考二模)一定条件下,在容积为2 L的恒容密闭容器中通入2 mol
发生反应 ,一定温度下,测得 的转化率随时间的变化曲线如图所示,在
60 min时反应达到平衡状态。
下列说法错误的是
A.a点处的逆反应速率小于b点处的正反应速率
B.0~10 min内, 的平均反应速率
C.其他条件不变,若在恒压条件下发生反应,平衡时 的转化率大于50%D.60 min后,保持温度不变,向该容器中再通入0.5 mol 和1 mol ,则反应逆向进行
【答案】D
【分析】据图, ,则 ;
【解析】A.b点仍处于从正反应建立平衡的途中,则b点处的逆反应速率小于b点处的正反应速率,b点
处NO和O 的浓度大于a点处的,则a点处的逆反应速率小于b点处的逆反应速率,更小于b点处的正反
2
应速率,A正确;B. 0~10 min内, 的平均反应速率
,B正确;C. 其他条件不变,若在恒压条件
下发生反应,等效于减压平衡右移,则平衡时 的转化率大于50%,C正确;D. 60 min后,保持温度
不变,向该容器中再通入0.5 mol 和1 mol ,则
,反应正向进行,D错误;答案选D。
10.(2023·湖南·校联考一模)利用反应 可实现从燃煤烟气中
回收硫。向三个体积相同的恒容密闭容器中通入 和 发生反应,反应体系的总压强
随时间的变化如图所示。下列说法错误的是
A.实验b中,40min内CO的平均反应速率
B.与实验a相比,实验b改变的条件是加入催化剂
C.实验b中 的平衡转化率是75%
D.实验abc相应条件下的平衡常数:
【答案】D
【分析】反应为放热反应,三个反应容器体积相同且恒容,反应物起始量相同,实验a、b起始压强相同,
说明反应温度相同,实验b达到平衡快,反应速率大,但两者平衡状态相同,说明实验b使用了催化剂;
与实验a相比,实验c达到平衡快,反应速率大,且平衡时体系压强大,说明实验c的反应温度更高。
【解析】A.对反应 ,反应时混合气体减小的物质的量相同于消耗SO
2的物质的量,根据压强之比等于物质的量之比,实验b中, 40min内体系压强减小了 ,相当于二氧
化硫的分压强减小了40kPa,则CO的分压强减小了80kPa,故CO的平均反应速率为
,A正确;B.根据分析知实验b改变的条件是加入催化剂,B正确;C.设
达到平衡状态时,SO 消耗了 ,列三段式得:
2
40min达到平衡,此时压强为120kPa,根据压强之比等于物质的量之比,得: ,解
得 ,故二氧化硫的转化率为 ,C正确;D.平衡常数只受温度影响,根据分析知
实验a、b反应温度相同,则 。反应 ,说明该反应是放热反应,升高温度,平衡逆向移动,
平衡常数减小,实验c 温度比实验a、b高,则 ,D错误;故选D。