文档内容
新情境下方程式的书写
1.(4分)世界环保联盟将全面禁止在自来水中加氯,取而代之的是安全高效的杀菌消毒剂ClO 。ClO 是一种
2 2
黄绿色、有刺激性气味的气体,熔点:-59 ℃,沸点:11.0 ℃。浓度>10%遇热、光照都会引起爆炸。遇到
有机物也会爆炸。
1
(1)欧洲一些国家用NaClO 氧化浓盐酸来制取ClO ,同时有Cl 生成,且Cl 的体积为ClO 的 。写出反应
3 2 2 2 2 4
的化学方程式: 。
(2)我国广泛采用将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO )的柱内制得ClO 。写出反应的化
2 2
学方程式: 。
2.(4分)氧化还原反应原理在生产、生活中应用广泛。
(1)ClO 可用于污水的杀菌和饮用水的净化。KClO 与SO 在强酸性溶液中反应可制得ClO ,SO 被氧化为
2 3 2 2 2
SO2-,此反应的离子方程式为 。
4
(2)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其
电子转移的方向和数目。
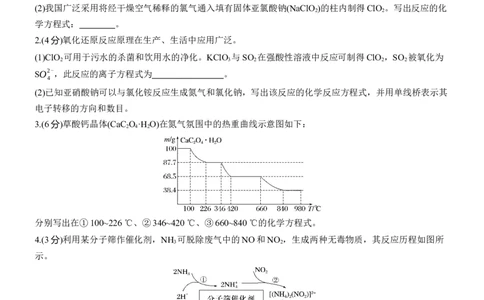
3.(6分)草酸钙晶体(CaC O ·H O)在氮气氛围中的热重曲线示意图如下:
2 4 2
分别写出在①100~226 ℃、②346~420 ℃、③660~840 ℃的化学方程式。
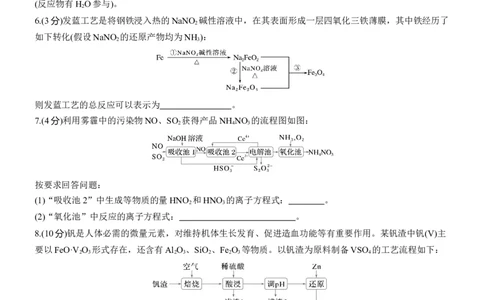
4.(3分)利用某分子筛作催化剂,NH 可脱除废气中的NO和NO ,生成两种无毒物质,其反应历程如图所
3 2
示。
则上述历程的总反应为 。
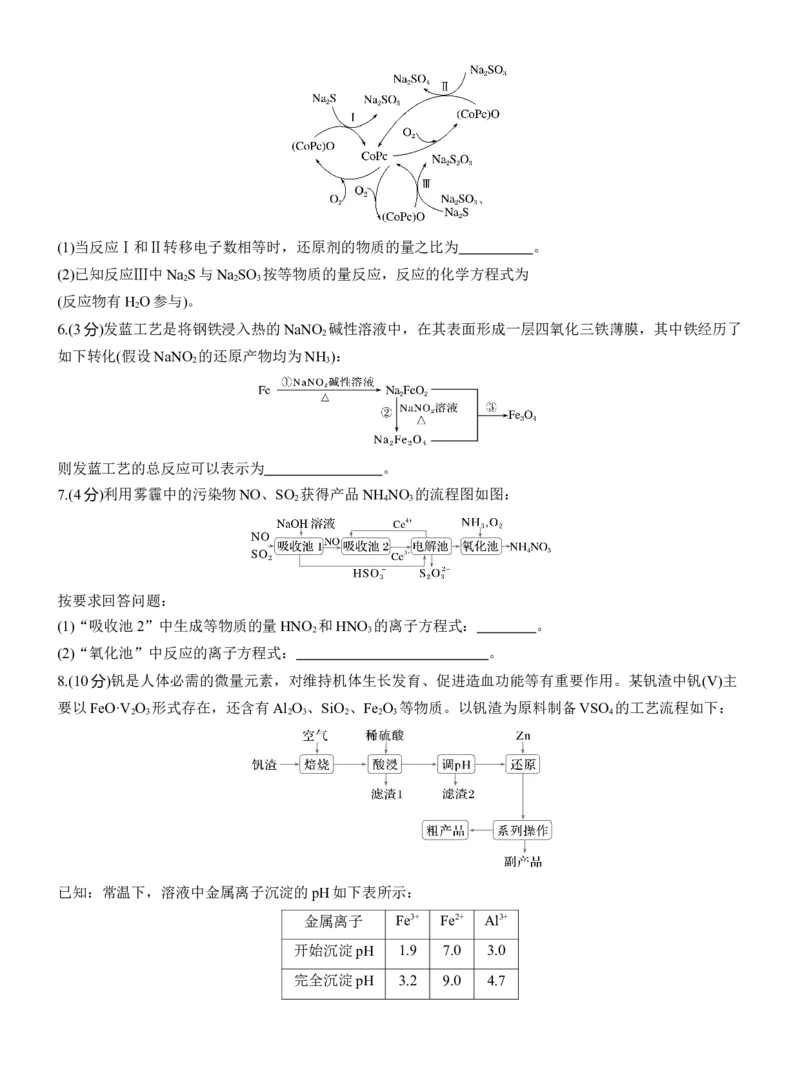
5.(4分)造纸、印刷等工业废水中含有大量的硫化物(主要成分为Na S),可用如图所示转化方式除去。
2(1)当反应Ⅰ和Ⅱ转移电子数相等时,还原剂的物质的量之比为 。
(2)已知反应Ⅲ中Na S与Na SO 按等物质的量反应,反应的化学方程式为
2 2 3
(反应物有H O参与)。
2
6.(3分)发蓝工艺是将钢铁浸入热的NaNO 碱性溶液中,在其表面形成一层四氧化三铁薄膜,其中铁经历了
2
如下转化(假设NaNO 的还原产物均为NH ):
2 3
则发蓝工艺的总反应可以表示为 。
7.(4分)利用雾霾中的污染物NO、SO 获得产品NH NO 的流程图如图:
2 4 3
按要求回答问题:
(1)“吸收池2”中生成等物质的量HNO 和HNO 的离子方程式: 。
2 3
(2)“氧化池”中反应的离子方程式: 。
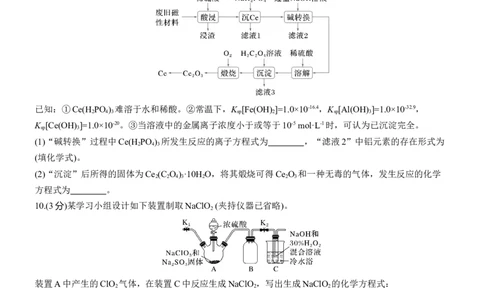
8.(10分)钒是人体必需的微量元素,对维持机体生长发育、促进造血功能等有重要作用。某钒渣中钒(V)主
要以FeO·V O 形式存在,还含有Al O 、SiO 、Fe O 等物质。以钒渣为原料制备VSO 的工艺流程如下:
2 3 2 3 2 2 3 4
已知:常温下,溶液中金属离子沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+
开始沉淀pH 1.9 7.0 3.0
完全沉淀pH 3.2 9.0 4.7(1)“焙烧”过程中发生的主要反应化学方程式为 。
(2)“酸浸”时,V O
转化为VO+
,反应的离子方程式为 。滤渣1的主要成分为 (填化学
2 5 2
式)。
(3)“调pH”时,若溶液中的铝元素恰好沉淀完全,则c(Fe3+)= mol·L-1(当溶液中离子浓度
c≤1.0×10-5mol·L-1时,认为沉淀完全)。
(4)“还原”中,VO+ 逐步被还原成V2+,其中V3+转化为V2+的离子方程式为 。
2
9.(6分)稀土金属(RE)属于战略性金属,我国的稀土提炼技术位于世界领先地位。一种从废旧磁性材料[主要
成分为铈(Ce)、Al、Fe和少量不溶于酸的杂质]中回收稀土金属Ce的工艺流程如图所示。
已知:①Ce(H PO ) 难溶于水和稀酸。②常温下,K [Fe(OH) ]=1.0×10-16.4,K [Al(OH) ]=1.0×10-32.9,
2 4 3 sp 2 sp 3
K [Ce(OH) ]=1.0×10-20。③当溶液中的金属离子浓度小于或等于10-5 mol·L-1时,可认为已沉淀完全。
sp 3
(1)“碱转换”过程中Ce(H PO ) 所发生反应的离子方程式为 ,“滤液2”中铝元素的存在形式为
2 4 3
(填化学式)。
(2)“沉淀”后所得的固体为Ce (C O ) ·10H O,将其煅烧可得Ce O 和一种无毒的气体,发生反应的化学
2 2 4 3 2 2 3
方程式为 。
10.(3分)某学习小组设计如下装置制取NaClO (夹持仪器已省略)。
2
装置A中产生的ClO 气体,在装置C中反应生成NaClO ,写出生成NaClO 的化学方程式:
2 2 2
。
11.(3分)将新制Na SO 溶液和CuSO 溶液按一定量混合,加热至90 ℃并不断搅拌。反应生成Cu O,同时
2 3 4 2
有SO 气体产生。反应结束后,经过滤、洗涤、干燥得到Cu O粉末。制备装置如图所示。
2 2
制备Cu O时,原料理论配比为n(Na SO )∶n(CuSO )=3∶2,该反应的化学方程式为 。
2 2 3 4答案精析
1.(1)11NaClO +18HCl(浓)===11NaCl+3Cl +12ClO +9H O
3 2 2 2
(2)2NaClO +Cl ===2NaCl+2ClO
2 2 2
2.(1)2ClO-
+SO ===2ClO
+SO2-
3 2 2 4
(2)
解析 (1)KClO 和SO 在强酸性条件下反应生成ClO
和SO2- ,离子方程式为2ClO-
+SO ===2ClO
+SO2-
。
3 2 2 4 3 2 2 4
3.①CaC O ·H O CaC O +H O↑、②CaC O CaCO +CO↑、③CaCO
2 4 2 2 4 2 2 4 3 3
CaO+CO ↑
2
解析 ①热重曲线中第一个平台在100 ℃以前为CaC O ·H O;②在100~226 ℃之间第一次出现失重,失去
2 4 2
质量占试样总质量的12.3%,相当于1 mol CaC O ·H O失去1 mol H O,即第二个平台固体组成为
2 4 2 2
CaC O ;③在346~420 ℃之间再次出现失重,失去的质量占试样总质量的19.2%,相当于1 mol CaC O 分
2 4 2 4
解出1 mol CO,即第三个平台固体的组成为CaCO ;④在660~840 ℃之间出现第三次失重,失去的质量占
3
试样总质量的30.1%,相当于1 mol CaCO 分解出1 mol CO ,即第四个平台固体组成为CaO。
3 2
4.2NH +NO+NO 2N +3H O
3 2 2 2
5.(1)1∶3 (2)Na SO +Na S+(CoPc)O+H O===Na S O +CoPc+2NaOH
2 3 2 2 2 2 3
解析 (1)由流程图知,反应Ⅰ中,Na S转化生成Na SO ,还原剂为Na S,且Na S~6e-,反应Ⅱ中,
2 2 3 2 2
Na SO 转化生成Na SO ,还原剂为Na SO ,且Na SO ~2e-,故转移电子数相等时,还原剂的物质的量之
2 3 2 4 2 3 2 3
比为1∶3。(2)结合流程图可知,反应Ⅲ的反应物为Na SO 、Na S、(CoPc)O,生成物为Na S O 和CoPc,
2 3 2 2 2 3
由于Na S与Na SO 按等物质的量反应,反应的化学方程式为Na SO +Na S+
2 2 3 2 3 2
(CoPc)O+H O===Na S O +CoPc+2NaOH。
2 2 2 3
6.9Fe+4NaNO +8H O 3Fe O +4NaOH+4NH ↑
2 2 3 4 3
解析 由图可知,发蓝工艺中Fe和NaNO 碱性溶液反应生成Fe O 和NH ,根据得失电子守恒和元素守恒
2 3 4 3
配平化学方程式为9Fe+4NaNO +8H O 3Fe O +4NaOH+4NH ↑。
2 2 3 4 3
7.(1)2NO+4Ce4++3H O===HNO +NO- +4Ce3++5H+
2 2 3
(2)2NH +O +2HNO
===2NH+ +2NO-
3 2 2 4 3
解析 根据题目信息,吸收池1中,NaOH溶液和SO 反应生成NaHSO ,反应的离子方程式为SO +OH-
2 3 2
===HSO- ;吸收池2中,NO与Ce4+反应生成等物质的量HNO 和HNO ,离子方程式为2NO+4Ce4+
3 2 3
+3H O===HNO +NO- +4Ce3++5H+;电解池中,阴极上HSO- S O2- ,电极反应式为2HSO- +4e-
2 2 3 3 2 3 3
+4H+===S O2- +3H O;“氧化池”中反应的离子方程式:2NH +O +2HNO ===2NH+ +2NO- 。
2 3 2 3 2 2 4 38.(1)4(FeO·V O )+5O 4V O +2Fe O
2 3 2 2 5 2 3
(2)V O +2H+===2VO+ +H O SiO (3)1.0×10-9.5
2 5 2 2 2
(4)2V3++Zn===2V2++Zn2+
解析 钒渣在空气中焙烧,主要成分FeO·V O 在空气中被氧化为V O 与Fe O ;加入稀硫酸酸浸,二氧化
2 3 2 5 2 3
硅不反应成为滤渣1,铁、钒、铝转化为相应盐溶液,调节pH将铁、铝转化为沉淀得到滤渣2,滤液加入
锌单质还原后处理得到粗产品。
(1)在空气中对钒渣进行焙烧,主要成分FeO·V O 在空气中被氧化为V O 与Fe O ,反应的化学方程式为
2 3 2 5 2 3
O+
4(FeO·V
2
O
3
)+5O
2
4V
2
O
5
+2Fe
2
O
3
。(2)“酸浸”时,V
2
O
5
和稀硫酸反应转化为V 2,反应的离子方程式为
V O +2H+===2VO+ +H O;由分析可知,滤渣1的主要成分为SiO 。(3)结合表中数据,溶液中Fe3+ 完全沉
2 5 2 2 2
淀时pH=3.2,即c(OH-)=1.0×10-10.8 mol·L-1,可求得K [Fe(OH) ]=c(Fe3+ )·c3(OH-)=1.0×10-37.4;当溶液中铝离
sp 3
子恰好沉淀完全时,溶液pH为4.7,此时溶液中c(OH-)为1.0×10-9.3 mol·L-1,根据K [Fe(OH) ],可求得溶
sp 3
液中c(Fe3+)=1.0×10-9.5 mol·L-1。
9.(1)Ce(H 2 PO 4 ) 3+9OH-===Ce(OH) 3 +3PO3 4 - +6H 2 O Na[Al(OH) 4 ] (2)2Ce 2 (C 2 O 4 ) 3·10H 2 O+3O 2
2Ce O +12CO +20H O
2 3 2 2
10.2NaOH+H O +2ClO ===2NaClO +O +2H O
2 2 2 2 2 2
解析 在装置C中,ClO 转变为NaClO ,氯元素从+4价降低到+3价,则过氧化氢为还原剂,氧元素从-1
2 2
价升高到0价,根据得失电子守恒、元素守恒得反应的化学方程式:
2NaOH+H O +2ClO ===2NaClO +O +2H O。
2 2 2 2 2 2
11.3Na SO +2CuSO ===Cu O↓+3Na SO +2SO ↑
2 3 4 2 2 4 2