文档内容
专题七 化学反应与能量
核心考点1、反应热及其表示方法
1. 反应热和焓变
(1) 在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反应热。
(2)焓变是化学反应在恒温、恒压条件下放出或吸收的热量。
(3) 研究表明,在等压条件下进行的化学反应,其反应热等于反应的焓变,用符号 ΔH表示,单位为
kJ·mol-1。
2. 理解化学反应热效应的角度
(1)从微观的角度说,是旧化学键断裂吸收的能量与新化学键形成放出的能量的差值,如下图所示:
a表示旧化学键断裂吸收的能量;
b表示新化学键形成放出的能量;
c表示反应热。
(2)从宏观的角度说,是反应物自身的能量与生成物能量的差值,在上图中:
a表示活化能;
b表示活化分子结合成生成物所释放的能量;
c表示反应热。
(3)焓变的计算
①从宏观角度分析:ΔH=H 生成物的总能量-H 反应物的总能量
1 2
②从微观角度分析:ΔH=E 反应物的键能总和-E 生成物的键能总和
1 2
③从活化能角度分析:ΔH=E 正反应活化能-E 逆反应活化能
1 2
3. 对比法理解反应热、燃烧热与中和热
“三热”是指反应热、燃烧热与中和热,可以用对比法深化对这三个概念的理解,明确它们的区别和联系,
避免认识错误。
(1)化学反应吸收或放出的热量称为反应热,符号为ΔH,单位常用kJ·mol-1,它只与化学反应的化学计量
数、物质的聚集状态有关,而与反应条件无关。中学阶段研究的反应热主要是燃烧热和中和热。(2)燃烧热:在101kPa时,1mol物质完全燃烧生成稳定的氧化物时所放出的热量。单位:kJ·mol-1。需注
意:①燃烧热是以1mol物质完全燃烧生成稳定的氧化物放出的热量来定义的,因此在书写燃烧热的热化
学方程式时,一般以燃烧1mol物质为标准来配平其余物质的化学计量数;②燃烧产物必须是稳定的氧化
物,如C→CO、H→HO(l)等。
2 2 2
(3)中和热:在稀溶液中,强酸跟强碱发生中和反应生成 1mol液态HO时的反应热。需注意:①稀溶液是
2
指物质溶于大量水中;②中和热不包括离子在水溶液中的生成热、物质的溶解热、电解质电离时的热效应;
③中和反应的实质是H+和OH-化合生成HO,即H+(aq)+OH-(aq)===H O(l) ΔH=-57.3kJ·mol-1。
2 2
(4)“三热”比较
反应热 燃烧热 中和热
能量变化 放热或吸热(ΔH 放热反应(ΔH<0)
(ΔH) <0或ΔH>0)
单位 单位:kJ·mol-1
反应物的量 不确定 必须为1mol 不确定
生成物的量 不确定 不确定 生成HO必须为1mol
2
【注意】反应热是指反应完全时的热效应,所以对于可逆反应,其热量要小于反应完全时的热量。
4.反应热的表示方法——热化学方程式
(1)定义: 热化学方程式是表示参加反应的物质的量和反应热的关系的化学方程式。
(2)意义: 热化学方程式不仅表示了化学反应中的物质变化,更重要的是表示了一定物质的量的反应物反应
时的能量变化。
例如: 2H ( g) + O ( g)=2HO( l)ΔH =﹣571.6 kJ · mol-1 表示:在25℃,101 kPa的条件下,2mol H 和1 mol
2 2 2 2
O 反应生成2 mol H O时放出571.6 kJ的热量。
2 2
(3)要求:
①热化学方程式和普通化学方程式一样需要配平,需要遵循质量守恒定律。
②热化学方程式的计量系数表示物质的量,所以既可以是整数又可以是分数。
③热化学方程式必须注明,反应物和生成物的状态。一般用括号注明在物质的化学式的右边。固态(s)、
液态(l)、气态(g)、溶液(aq),有的甚至还有注明晶体状态,因为同一种物质,状态改变时会吸收
或放出热量。
④热化学方程式必须在化学方程式的右边注明焓变ΔH。放热反应ΔH<0,吸热反应ΔH>0。ΔH 的值与
方程式的计量系数有一一对应的关系。计量系数改变,ΔH相应改变。逆反应的数值相等,符号相反。
⑤热化学方程式侧重于揭示参加反应的物质的量与反应热的关系,ΔH 的值此条件下一般是在25℃,101kPa 条件测定的数据。所以,热化学方程式如果没有注明反应条件,默认为常温常压下。
注意:a.热化学方程式中的反应热表示反应物完全反应时的热量变化。如3H2(g)+N2(g)
2NH3(g)ΔH=-92.4 kJ/mol是指生成2 mol NH3 时放出92.4 kJ的热量,因反应不能进行完全,3 mol H2(g)和1
mol N2(g)混合反应实际放出的热量小于92.4 kJ。
b.当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
如:①H2(g)+I2(g) 2HI(g) ΔH1 ②2HI(g) H2(g)+I2(g) ΔH2 则有:ΔH1=﹣ΔH2 。
热化学方程式书写或判断的注意事项。
(1)注意ΔH的符号和单位:ΔH的单位为kJ·mol-1。
(3)注意热化学方程式中的化学计量数:热化学方程式化学计量数可以是整数,也可以是分数。
(4)注意物质的聚集状态:气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。热化学方程式中不用
“↑”和“↓”。
(5)注意ΔH的数值与符号:如果化学计量数加倍,则ΔH也要加倍。逆反应的反应热与正反应的反应热数
值相等,但符号相反。
(6)对于具有同素异形体的物质,除了要注明聚集状态外,还要注明物质的名称。
如①S(单斜,s)+O(g)===SO(g) ΔH=-297.16kJ·mol-1
2 2 1
②S(正交,s)+O(g)===SO(g) ΔH=-296.83kJ·mol-1
2 2 2
③S(单斜,s)===S(正斜,s) ΔH=-0.33kJ·mol-1
3
1. (2018北京卷·27(1))近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过
程如下:
反应Ⅰ:2HSO (l) 2SO (g)+2HO(g)+O (g) ΔH =+551 kJ·mol-1
2 4 2 2 2 1
反应Ⅲ:S(s)+O (g) SO (g) ΔH =-297 kJ·mol-1
2 2 3
反应Ⅱ的热化学方程式:________________。
2.【2018天津卷·10(2)】CO 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
2
(2)CO 与CH 经催化重整,制得合成气:CH(g)+ CO (g) 2CO (g)+ 2H (g)
2 4 4 2 2①已知上述反应中相关的化学键键能数据如下:
化学键 C—H C=O H—H C O(CO)
键能/kJ·mol−1 413 745 436 1075
则该反应的ΔH=_________。
1.(2022·上海·统考一模)化学反应 的能量变化如图所示,下列说法错误的是
A.该反应在光照和点燃条件下的反应热效应是相同的
B. 气态氢原子的能量低于 氢气的能量
C. 与 形成 时释放 能量
D.该反应的热化学反应方程式:
2.(2022秋·北京东城·高三北京市第一六六中学校考期中)以CO和 为原料合成甲醇是工业上的成熟
方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要
将 转化为甲醇。
已知:① kJ·mol
② kJ·mol
③ kJ·mol
下列说法不正确的是A.若温度不变,反应①中生成1 mol 时,放出的热量大于90.5 kJ
B. 与 合成甲醇的热化学方程式为:
kJ·mol
C.通过电解制 和选用高效催化剂,可降低 与 合成甲醇反应的焓变
D.以 和 为原料合成甲醇,同时生成 ,该反应需要吸收能量
3.(2022秋·上海普陀·高三上海市宜川中学校考期中)已知:H(g)+F (g)→2HF(g)+270 kJ,下列说法正确
2 2
的是
A.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量小于270 kJ
B.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
C.在相同条件下,1mol氢气与1mol氟气的键能总和大于2mol氟化氢气体的键能
D.2L氟化氢气体分解成1L氢气与1L氟气吸收270 kJ的热量
4.(2022秋·重庆永川·高三重庆市永川北山中学校校考期中)Ni可活化 放出 ,其反应历程如图
所示。下列关于活化历程的说法正确的是
A.决速步骤:中间体1→中间体2
B.在此反应过程中Ni的成键数目没有发生变化
C.涉及非极性键的断裂和生成
D.总反应为 kJ·mol
5.(2022秋·山东德州·高三统考期中)我国科学家研究了不同含金化合物催化乙烯加氢的反应历程如图所
示,下列说法正确的是A.过渡态1比过渡态2更稳定
B.若该反应生成液态 ,则反应的 增大
C.催化剂AuF的催化效果比 的好
D.该反应的热化学方程式为:
6.(2022秋·江苏南京·高三校联考期中)液态CS 是一种溶剂,其燃烧热为1077 。含SeO、SO
2 2 2
的烟气用水吸收后,硒元素全部变为单质硒。工业上制备碲用SO 还原TeCl 溶液或者以石墨为电极,电解
2 4
强碱性NaTeO 溶液。下列化学反应表示正确的是
2 3
A.用SO 水溶液吸收溴蒸气的离子方程式:
2
B.CS 燃烧的热化学方程式:CS(l)+3O (g)=CO (g)+2SO(g)
2 2 2 2 2
C.SO 还原TeCl 反应方程式:2SO +TeCl+4H O=Te+2HSO +4HCl
2 4 2 4 2 2 4
D.电解法制备碲的阴极电极方程式:
核心考点2、盖斯定律的应用
1.定律内容
化学反应不管是一步完成还是分几步完成,其反应热是相同的。也就是说,化学反应的反应热只与物
质的始态和终态有关,而与反应的途径无关。
盖斯定律是能量守恒定律的一种形式,是能量守恒定律在化学能与热能相互转化的一个表现。比如登
山的高度与上山的途径无关,只与起点和终点的相对高度有关。如何更好的理解盖斯定律,可以以下面这个图形。
ΔH=ΔH+ΔH
1 2
2.常用关系式
热化学方程式 焓变之间的关系
aA===B ΔH
1
ΔH=ΔH 或ΔH=aΔH
2 1 1 2
A===B ΔH
2
aA===B ΔH
1
ΔH=-ΔH
1 2
B===aA ΔH
2
ΔH=ΔH+ΔH
1 2
3. 叠加法求焓变
步骤1 “倒”
为了将方程式相加得到目标方程式,可将方程式颠倒过来,反应热的数值不变,但符号相反。这样,就不
用再做减法运算了,实践证明,方程式相减时往往容易出错。
步骤2 “乘”
为了将方程式相加得到目标方程式,可将方程式乘以某个倍数,反应热也要相乘。
步骤3 “加”
上面的两个步骤做好了,只要将方程式相加即可得目标方程式,反应热也要相加。
4. 反应热大小比较
(1)利用盖斯定律比较。
(2)同一反应的生成物状态不同时,如 A(g)+B(g)===C(g) ΔH ,A(g)+B(g)===C(l) ΔH ,则ΔH >
1 2 1ΔH。
2
(3)同一反应的同一反应物状态不同时,如A(s)+B(g)===C(g) ΔH ,A(g)+B(g)===C(g) ΔH ,则ΔH
1 2 1
>ΔH。
2
(4)两个有联系的反应相比较时,如①C(s)+O(g)===CO (g) ΔH,②C(s)+1/2O (g)===CO(g) ΔH。
2 2 1 2 2
比较方法:利用反应①(包括ΔH)乘以某计量数减去反应②(包括ΔH)乘以某计量数,即得出ΔH =ΔH×某
1 2 3 1
计量数-ΔH×某计量数,根据ΔH 大于0或小于0进行比较。
2 3
总之,比较反应热的大小时要注意:①反应中各物质的聚集状态;②ΔH有正负之分,比较时要连同
“+”、“-”一起比较,类似数学中的正、负数大小的比较;③若只比较放出或吸收热量的多少,则只
比较数值的大小,不考虑正、负号。
1. 高考组合(1)【2018新课标2卷·27(1)】CH-CO 催化重整不仅可以得到合成气(CO和H),还对
4 2 2
温室气体的减排具有重要意义。回答下列问题:CH-CO 催化重整反应为:CH(g)+CO (g)=2CO(g)
4 2 4 2
+2H (g)。
2
已知:C(s)+2H(g)=CH (g) ΔH=-75 kJ·mol−1
2 4
C(s)+O(g)=CO (g) ΔH=-394 kJ·mol−1
2 2
C(s)+1/2O (g)=CO(g) ΔH=-111 kJ·mol−1
2
该催化重整反应的ΔH==______ kJ·mol−1。
(2)【2018新课标3卷·28(2)·难度3】三氯氢硅(SiHCl )是制备硅烷、多晶硅的重要原料。回答下列
3
问题:SiHCl 在催化剂作用下发生反应:
3
2SiHCl (g)=SiHCl(g)+ SiCl (g) ΔH =48 kJ·mol−1
3 2 2 4 1
3SiHCl(g)=SiH(g)+2SiHCl (g) ΔH =−30 kJ·mol−1
2 2 4 3 2
则反应4SiHCl (g)=SiH(g)+3SiCl (g)的ΔH=__________kJ·mol−1。
3 4 4
(3)【2018江苏卷·20(1)·难度3】NO(主要指NO和NO )是大气主要污染物之一。有效去除大气中
x 2
的NO 是环境保护的重要课题。
x
(1)用水吸收NO 的相关热化学方程式如下:
x
2NO (g)+H O(l) HNO(aq)+HNO (aq) ΔH=−116.1 kJ·mol−1
2 2 3 2
3HNO(aq) HNO(aq)+2NO(g)+H O(l) ΔH=75.9 kJ·mol−1
2 3 2
反应3NO (g)+H O(l) 2HNO(aq)+NO(g)的ΔH=___________kJ·mol−1。
2 2 32.(2013课标全国卷Ⅱ)在1 200 ℃时,天然气脱硫工艺中会发生下列反应
HS(g)+O(g) SO (g)+HO(g) ΔH
2 2 2 2 1
2HS(g)+SO (g) S(g)+2HO(g) ΔH
2 2 2 2 2
HS(g)+O(g) S(g)+HO(g) ΔH
2 2 2 3
2S(g) S(g) ΔH
2 4
则ΔH 的正确表达式为( )
4
A.ΔH=(ΔH+ΔH-3ΔH) B.ΔH=(3ΔH-ΔH-ΔH)
4 1 2 3 4 3 1 2
C.ΔH=(ΔH+ΔH-3ΔH) D.ΔH=(ΔH-ΔH-3ΔH)
4 1 2 3 4 1 2 3
3.(2014重庆理综) 已知:C(s)+HO(g)==CO(g)+H(g) ΔH=a kJ·mol-1
2 2
2C(s)+O(g)==2CO(g) ΔH=-220 kJ·mol-1
2
H-H、O=O和O-H键的键能分别为436、496和462 kJ·mol-1,则a为( )
A.-332 B.-118 C.+350 D.+130
1.(2022秋·北京石景山·高三统考期末) 、 下,①
②
下列说法不正确的是
A.液态水变为水蒸气破坏的是分子间作用力
B.水分解为氢气和氧气,断键吸收的总能量大于成键放出的总能量
C.标准状况下, 水中含共用电子对总数约为
D. 、 下,
2.(2022秋·江苏扬州·高三统考期末)碘及其化合物有着多方面的用途,一碘甲烷(CHI)热裂解可制取乙
3
烯等低碳烯烃化工原料。CHI热裂解时主要反应有:
3
反应I:2CHI(g) C H(g)+2HI(g) ΔH
3 2 4 1反应II:3C H(g) 2C H(g) ΔH
2 4 3 6 2
反应III:2C H(g) C H(g) ΔH (298K)
2 4 4 8 3
实验测得,反应I、II的ΔH随温度的变化如图1所示,在1L密闭的容器中,起始投料1molCH I(g),反应
3
温度对平衡时体系中乙烯、丙烯和丁烯物质的量分数的影响如图2所示。
下列说法正确的是
A.298K时,反应3CHI(g) C H(g)+3HI(g) ΔH=-66.3kJ•mol-1
3 3 6
B.图中曲线X表示乙烯的物质的量分数随温度的变化
C.A、B是曲线Y上两点,曲线Y对应反应的平衡转化率:α(A)<α(B)
D.当平衡体系温度从600K升高到800K时,三条曲线对应的反应:X和Y正向移动,Z逆向移动
3.(2022·浙江·模拟预测)晶格能(U)是气态离子形成1mol离子晶体释放的能量。 是离子晶体,其晶
格能的实验值可通过玻恩-哈伯热力学循环图计算得到。
已知: ,
下列说法不正确的是A. B.O—O键键能为
C. D.
4.(2022秋·安徽安庆·高三校考期末)已知反应:①2H(g)+O(g)=2HO(g) ΔH
2 2 2 1
②N(g)+2O(g)=2NO (g) ΔH
2 2 2 2
③N(g)+3H(g)=2NH (g) ΔH,
2 2 3 3
则反应4NH (g)+7O(g)=4NO (g)+6HO(g)的ΔH为
3 2 2 2
A.2ΔH+2ΔH-2ΔH B.ΔH+ΔH-ΔH
1 2 3 1 2 3
C.3ΔH+2ΔH-2ΔH D.3ΔH+2ΔH+2ΔH
1 2 3 1 2 3
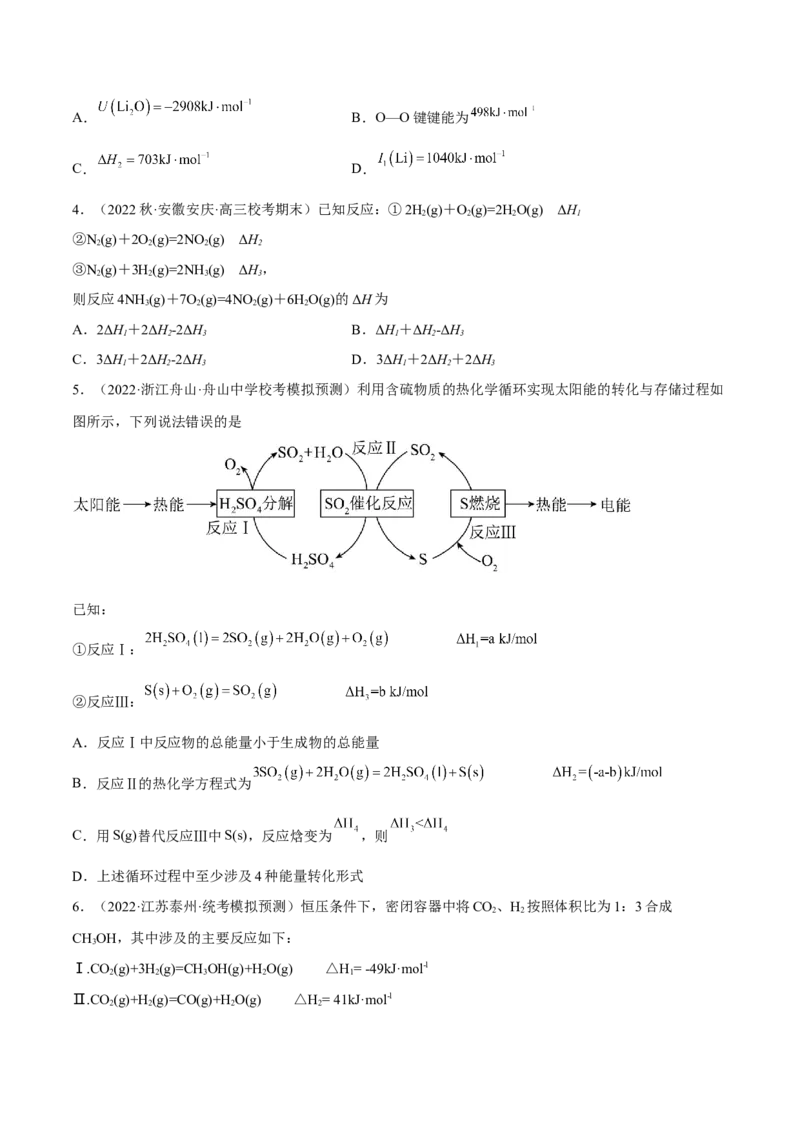
5.(2022·浙江舟山·舟山中学校考模拟预测)利用含硫物质的热化学循环实现太阳能的转化与存储过程如
图所示,下列说法错误的是
已知:
①反应Ⅰ:
②反应Ⅲ:
A.反应Ⅰ中反应物的总能量小于生成物的总能量
B.反应Ⅱ的热化学方程式为
C.用S(g)替代反应Ⅲ中S(s),反应焓变为 ,则
D.上述循环过程中至少涉及4种能量转化形式
6.(2022·江苏泰州·统考模拟预测)恒压条件下,密闭容器中将CO、H 按照体积比为1:3合成
2 2
CHOH,其中涉及的主要反应如下:
3
Ⅰ.CO (g)+3H(g)=CH OH(g)+H O(g) △H= -49kJ·mol-l
2 2 3 2 1
Ⅱ.CO (g)+H(g)=CO(g)+HO(g) △H= 41kJ·mol-l
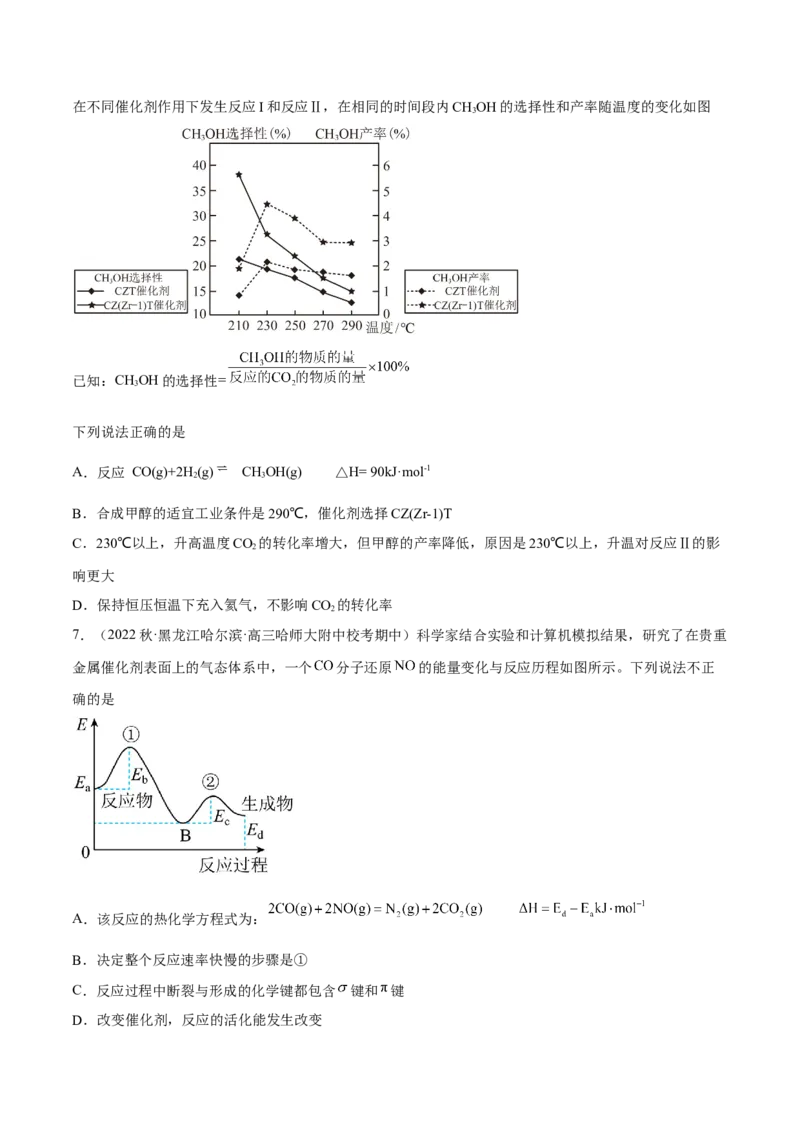
2 2 2 2在不同催化剂作用下发生反应I和反应Ⅱ,在相同的时间段内CHOH的选择性和产率随温度的变化如图
3
已知:CHOH的选择性=
3
下列说法正确的是
A.反应 CO(g)+2H(g) CHOH(g) △H= 90kJ·mol-1
2 3
B.合成甲醇的适宜工业条件是290℃,催化剂选择CZ(Zr-1)T
C.230℃以上,升高温度CO 的转化率增大,但甲醇的产率降低,原因是230℃以上,升温对反应Ⅱ的影
2
响更大
D.保持恒压恒温下充入氦气,不影响CO 的转化率
2
7.(2022秋·黑龙江哈尔滨·高三哈师大附中校考期中)科学家结合实验和计算机模拟结果,研究了在贵重
金属催化剂表面上的气态体系中,一个 分子还原 的能量变化与反应历程如图所示。下列说法不正
确的是
A.该反应的热化学方程式为:
B.决定整个反应速率快慢的步骤是①
C.反应过程中断裂与形成的化学键都包含 键和 键
D.改变催化剂,反应的活化能发生改变