文档内容
多平衡体系中的规范解答题
1.平衡移动类文字说理题答题模板
叙特点(反应特点或容器特点)→变条件→定方向→得结论(或结果)
(1)温度:该反应正向为×××(放热或吸热)反应,其他条件不变,升高(或降低)温度,平衡×××(正向或逆
向)移动,因此×××(得结论)。
(2)压强:反应的正反应是气体分子数减小(或增大)的反应,当温度一定时,增大压强,平衡正向(或逆
向)移动,因此×××(得结论)。
2.工业生产图像中转化率、产率变化文字说理题答题要领
(一)最佳反应条件的判断
例1 甲烷还原可消除NO污染。将NO、O 、CH 混合物按一定体积比通入恒容容器中,发生如下主
2 4
要反应:
①CH (g)+2NO(g)+O (g)===N (g)+CO (g)+2H O(g) ΔH <0
4 2 2 2 2 1
②CH (g)+4NO(g)===2N (g)+CO (g)+2H O(g) ΔH <0
4 2 2 2 2
③CH (g)+2O (g)===CO (g)+2H O(g) ΔH <0
4 2 2 2 3
在催化剂A和B的分别作用下,NO的还原率和CH 的转化率分别与温度的关系如图所示。
4
由图可知,消除NO的最佳条件是 和催化剂 。
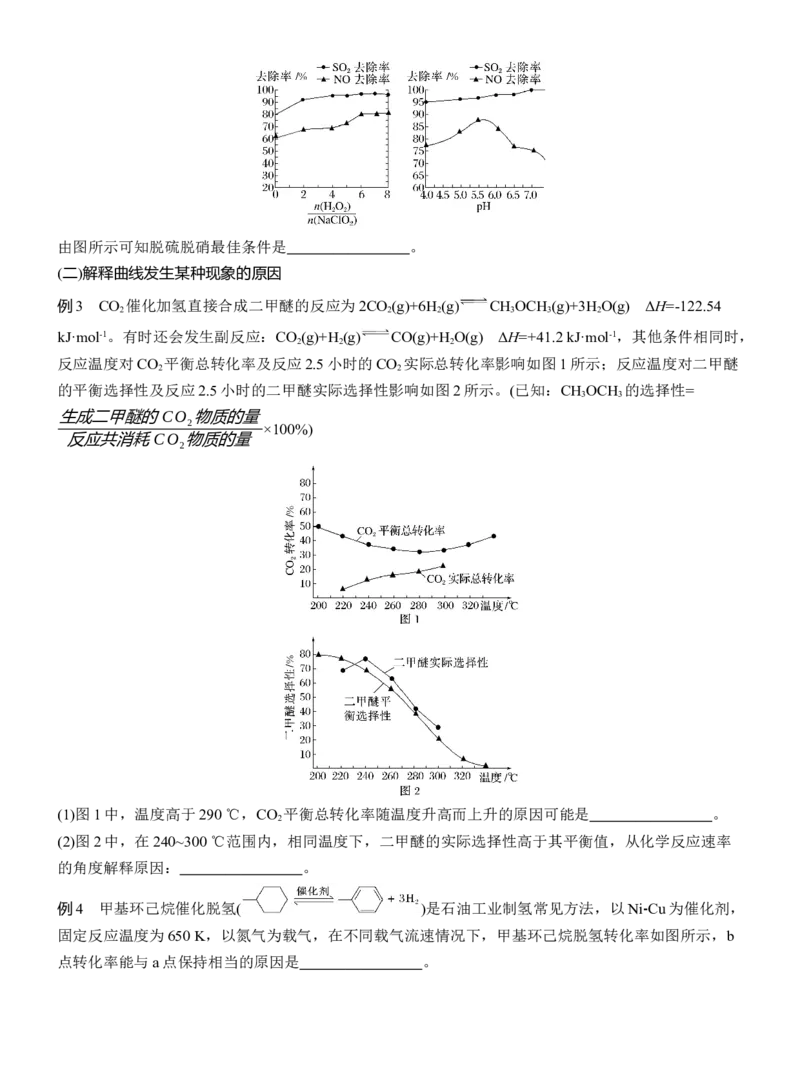
例2 利用NaClO /H O 酸性复合吸收剂可同时对NO、SO 进行氧化得到硝酸和硫酸而除去。在温度一
2 2 2 2
n(H O )
2 2
定时, 、溶液pH对脱硫脱硝的影响如图所示:
n(NaClO )
2由图所示可知脱硫脱硝最佳条件是 。
(二)解释曲线发生某种现象的原因
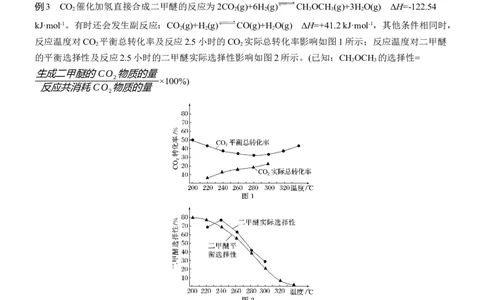
例3 CO 催化加氢直接合成二甲醚的反应为2CO (g)+6H (g) CH OCH (g)+3H O(g) ΔH=-122.54
2 2 2 3 3 2
kJ·mol-1。有时还会发生副反应:CO (g)+H (g) CO(g)+H O(g) ΔH=+41.2 kJ·mol-1,其他条件相同时,
2 2 2
反应温度对CO 平衡总转化率及反应2.5小时的CO 实际总转化率影响如图1所示;反应温度对二甲醚
2 2
的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知:CH OCH 的选择性=
3 3
生成二甲醚的CO 物质的量
2
×100%)
反应共消耗CO 物质的量
2
(1)图1中,温度高于290 ℃,CO 平衡总转化率随温度升高而上升的原因可能是 。
2
(2)图2中,在240~300 ℃范围内,相同温度下,二甲醚的实际选择性高于其平衡值,从化学反应速率
的角度解释原因: 。
例4 甲基环己烷催化脱氢( )是石油工业制氢常见方法,以Ni⁃Cu为催化剂,
固定反应温度为650 K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图所示,b
点转化率能与a点保持相当的原因是 。1.[2024·湖南,18(2)]丙烯腈(CH ==CHCN)是一种重要的化工原料。工业上以N 为载气,用TiO 作催化
2 2 2
剂生产CH ==CHCN的流程如下:
2
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定;
②反应釜Ⅰ中发生的反应:
ⅰ:HOCH CH COOC H (g)―→CH ==CHCOOC H (g)+H O(g) ΔH
2 2 2 5 2 2 5 2 1
③反应釜Ⅱ中发生的反应:
ⅱ:CH ==CHCOOC H (g)+NH (g)―→CH ==CHCONH (g)+C H OH(g) ΔH
2 2 5 3 2 2 2 5 2
ⅲ:CH ==CHCONH (g)―→CH ==CHCN(g)+H O(g) ΔH
2 2 2 2 3
④在此生产条件下,酯类物质可能发生水解。
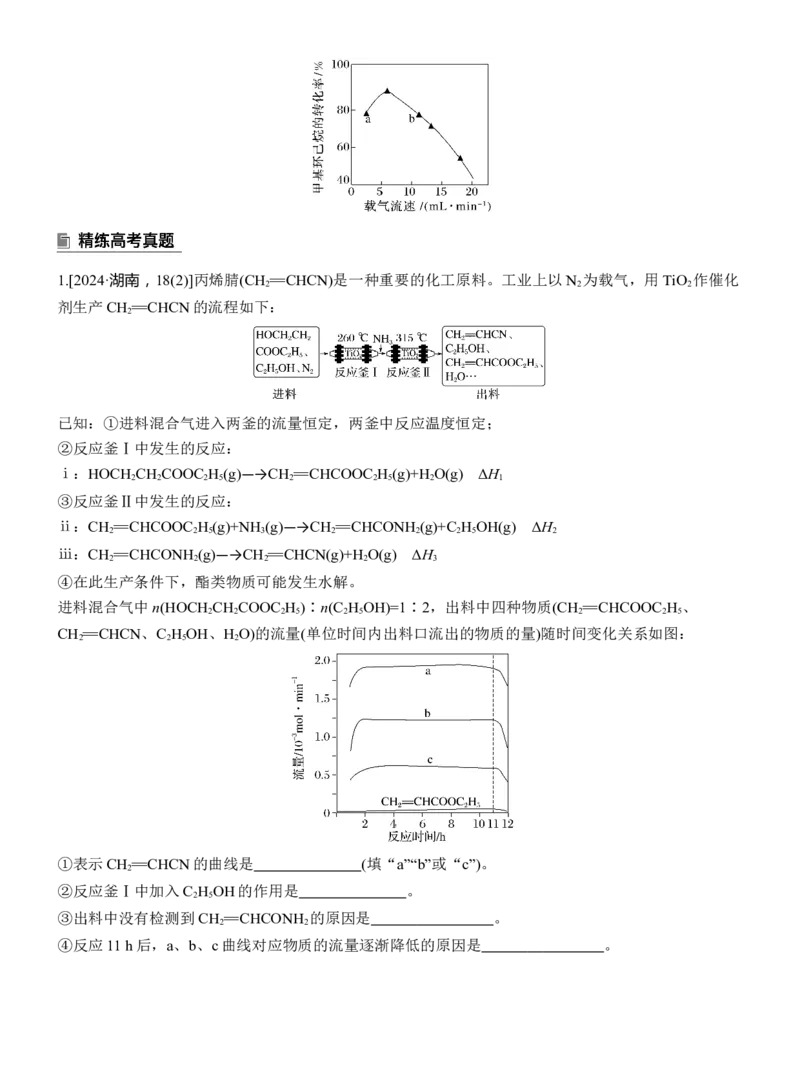
进料混合气中n(HOCH CH COOC H )∶n(C H OH)=1∶2,出料中四种物质(CH ==CHCOOC H 、
2 2 2 5 2 5 2 2 5
CH ==CHCN、C H OH、H O)的流量(单位时间内出料口流出的物质的量)随时间变化关系如图:
2 2 5 2
①表示CH ==CHCN的曲线是 (填“a”“b”或“c”)。
2
②反应釜Ⅰ中加入C H OH的作用是 。
2 5
③出料中没有检测到CH ==CHCONH 的原因是 。
2 2
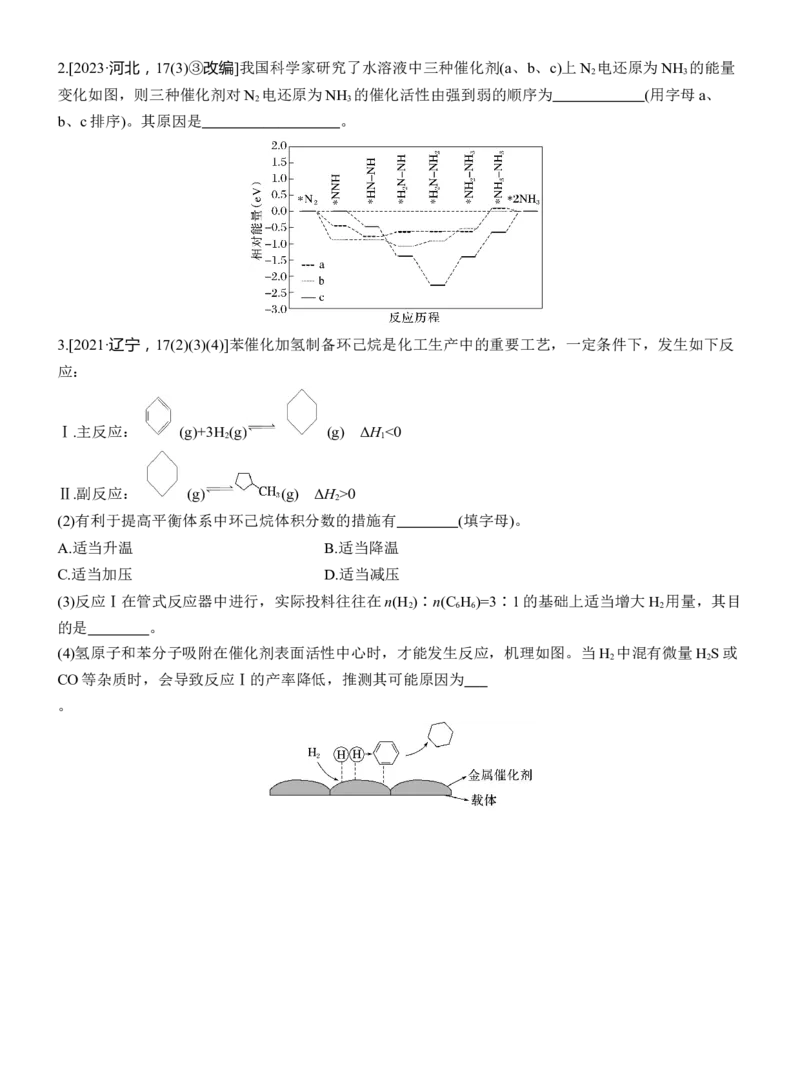
④反应11 h后,a、b、c曲线对应物质的流量逐渐降低的原因是 。2.[2023·河北,17(3)③改编]我国科学家研究了水溶液中三种催化剂(a、b、c)上N 电还原为NH 的能量
2 3
变化如图,则三种催化剂对N 电还原为NH 的催化活性由强到弱的顺序为 (用字母a、
2 3
b、c排序)。其原因是 。
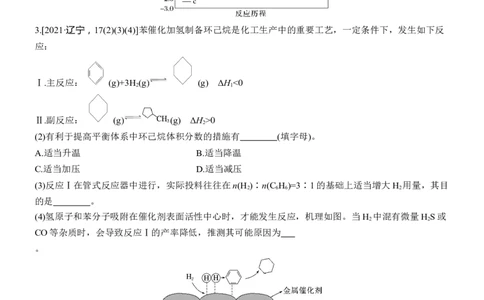
3.[2021·辽宁,17(2)(3)(4)]苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反
应:
Ⅰ.主反应: (g)+3H (g) (g) ΔH <0
2 1
Ⅱ.副反应: (g) (g) ΔH >0
2
(2)有利于提高平衡体系中环己烷体积分数的措施有 (填字母)。
A.适当升温 B.适当降温
C.适当加压 D.适当减压
(3)反应Ⅰ在管式反应器中进行,实际投料往往在n(H )∶n(C H )=3∶1的基础上适当增大H 用量,其目
2 6 6 2
的是 。
(4)氢原子和苯分子吸附在催化剂表面活性中心时,才能发生反应,机理如图。当H 中混有微量H S或
2 2
CO等杂质时,会导致反应Ⅰ的产率降低,推测其可能原因为
。答案精析
类型分析
例1 500 ℃ A
解析 由图可知,500 ℃时,在催化剂A的作用下NO还原率最高,是消除NO的最佳条件。
n(H O )
2 2
例2 pH在5.5~6.0、 =6
n(NaClO )
2
例3 (1)温度高于290 ℃,随着温度升高,CO (g)+H (g) CO(g)+H O(g)平衡向右移动的程度大于
2 2 2
2CO (g)+6H (g) CH OCH (g)+3H O(g)平衡向左移动的程度,使CO 的平衡总转化率上升 (2)CO 催化
2 2 3 3 2 2 2
加氢直接合成二甲醚的反应活化能较低,而合成二甲醚时的副反应CO (g)+H (g) CO(g)+H O(g)活化能
2 2 2
较高,所以二甲醚的实际选择性高于其平衡值
例4 a点载气流速较小,甲基环己烷的浓度较大,其在催化剂表面吸附及发生脱氢反应的百分率较小,故
其转化率较小;适当加快载气流速可以减小反应物的浓度,使反应物在催化剂表面吸附及发生脱氢反应的
百分率变大,故甲基环己烷转化率随载气流速适当加快而提高;b点载气流速过快,会使甲基环己烷在催
化剂表面的反应时间减少,导致甲基环己烷转化率降低,因此,b点转化率能与a点保持相当
精练高考真题
1.①c ②降低分压,有利于反应ⅰ平衡正向移动,且提高醇的浓度可以使酯的水解程度降低,从而提高产
率
③CH CHCONH 在反应釜Ⅱ的温度下发生分解
2 2
④反应时间过长,催化剂中毒,活性降低,反应速率降低,故产物减少
解析 ①将反应ⅰ、ⅱ、ⅲ相加得总反应HOCH CH COOC H (g)+NH (g) CH ==CHCN(g)+C H OH(g)
2 2 2 5 3 2 2 5
+2H O(g),设进料混合气中n(HOCH CH COOC H )=1 mol,n(C H OH)=2 mol,出料气中
2 2 2 2 5 2 5
CH ==CHCOOC H 含量很少,则生成CH ==CHCN(g)、C H OH(g)物质的量约为1 mol,生成H O(g)的物
2 2 5 2 2 5 2
质的量约为2 mol,故出料气中C H OH(g)物质的量共约3 mol,故出料气中CH ==CHCN、C H OH、H O
2 5 2 2 5 2
物质的量之比约为1∶3∶2,故曲线c表示CH ==CHCN的曲线。
2
2.bac 催化剂通过降低反应活化能提高反应速率
3.(2)BC (3)提高苯的转化率 (4)金属催化剂会与H S或CO反应从而失去催化活性
2