文档内容
专题十三 水的电离与溶液的pH 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
选择题(本题含20小题,每题5分,共100分。每题只有一个选项符合题意)
1.(2022秋·浙江舟山·高二舟山中学校考期中)NaHSO 在水中的电离方程式为
4
。某温度下,向c(H+)=1×10-6 mol/L的蒸馏水中加入NaHSO
4
晶体,保持温度不变,测得溶液c(H+)=1×10-2 mol/L。下列对该溶液的叙述不正确的是
A.该温度高于25℃
B.由水电离出来的H+的浓度为1×10-10 mol/L
C.加入NaHSO 晶体抑制了水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
2.(2022·上海嘉定·统考一模)2022年11月30日,天气阴冷。嘉定区某化学教师在
讲水的电离时,为了求证水电离的热效应,她做了一个对比实验,甲烧杯放60℃蒸馏
水,乙烧杯蒸馏水仍保持室温,分别测其导电性,下列有关该条件下纯水的说法错误
的是
A.水的电离可表示为: 简写成
B.甲中
C.乙中
D.甲中
3.(2022·上海金山·统考二模)常温下,等体积等浓度的盐酸与下列溶液分别恰好完
全中和。
①V mL pH=9的氨水;②V mL pH=10的氨水
1 2下列判断正确的是
A.10V>V B. 的比值:②>①
2 1
C.水的电离程度:②>① D.反应后溶液的pH:①>②
4.(2022·浙江宁波·统考一模)下列说法正确的是
A.25℃时,将pH=5的醋酸溶液与pH=5的盐酸等体积混合,混合后溶液pH>5
B.25℃时,等浓度的盐酸与醋酸分别稀释相同倍数,稀释后溶液pH:盐酸<醋酸
C.25℃时,等体积、等pH的盐酸与醋酸分别用等浓度的NaOH溶液中和,盐酸消耗
NaOH溶液多
D.25℃时,pH=3的一元酸HA溶液与pH=11的一元碱MOH溶液等体积混合后溶液
呈酸性,则HA是强酸
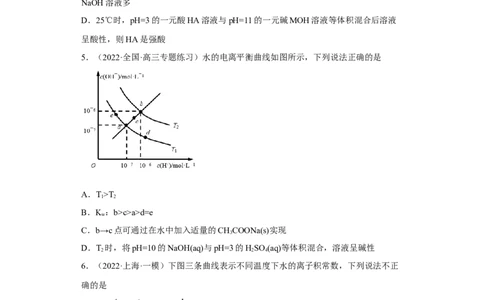
5.(2022·全国·高三专题练习)水的电离平衡曲线如图所示,下列说法正确的是
A.T>T
1 2
B.K :b>c>a>d=e
w
C.b→c点可通过在水中加入适量的CHCOONa(s)实现
3
D.T 时,将pH=10的NaOH(aq)与pH=3的HSO (aq)等体积混合,溶液呈碱性
2 2 4
6.(2022·上海·一模)下图三条曲线表示不同温度下水的离子积常数,下列说法不正
确的是
A.图中温度: B.图中 的关系:
试卷第2页,共9页C.C点物质可能是盐酸 D.图中五点 间的关系:
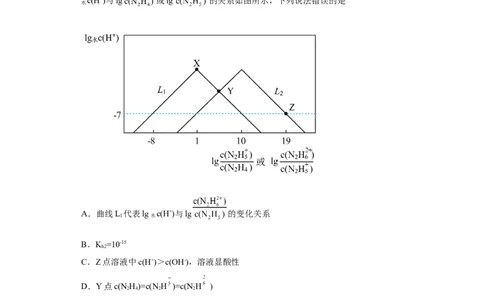
7.(2023秋·山东日照·高三统考期末)NH 为二元弱碱,在水中的电离方式与NH 相
2 4 3
似。室温下,通过调节pH,使混合溶液中c(NH)+c(N H )+c(N H )=0.01mol•L-1,lg
2 4 2 2
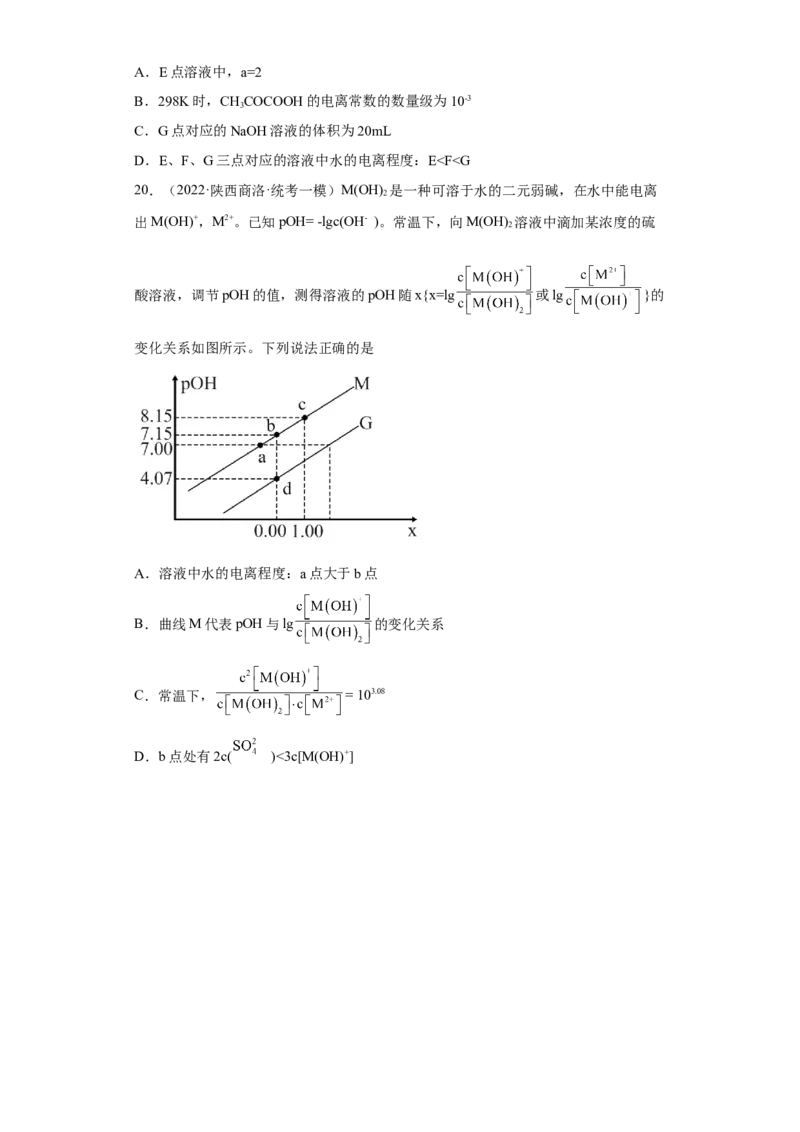
c(H+)与lg 或lg 的关系如图所示,下列说法错误的是
水
A.曲线L 代表lg c(H+)与lg 的变化关系
1 水
B.K =10-15
b2
C.Z点溶液中c(H+)>c(OH-),溶液显酸性
D.Y点c(NH)=c(N H )=c(N H )
2 4 2 2
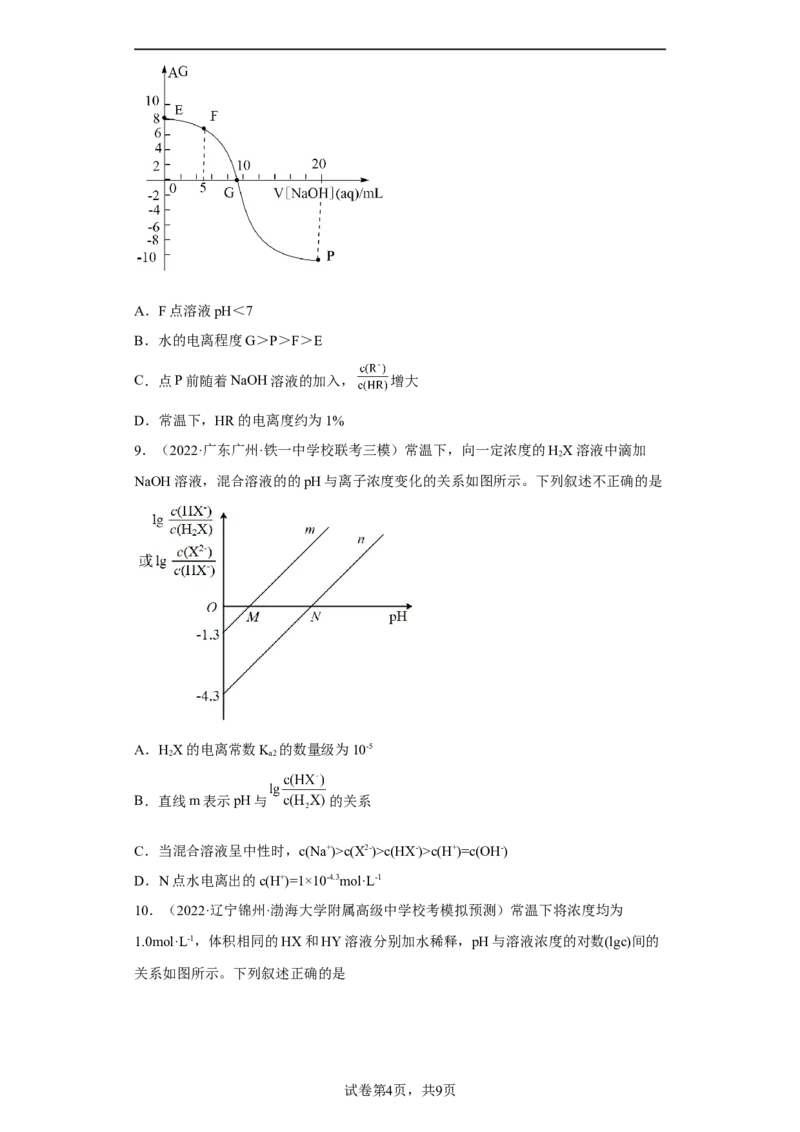
8.(2022·全国·高三专题练习)已知AG=lg ,电离度(α)=
×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液
中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是A.F点溶液pH<7
B.水的电离程度G>P>F>E
C.点P前随着NaOH溶液的加入, 增大
D.常温下,HR的电离度约为1%
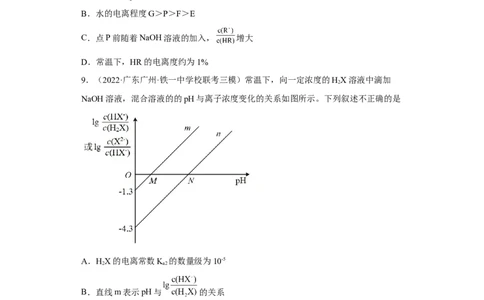
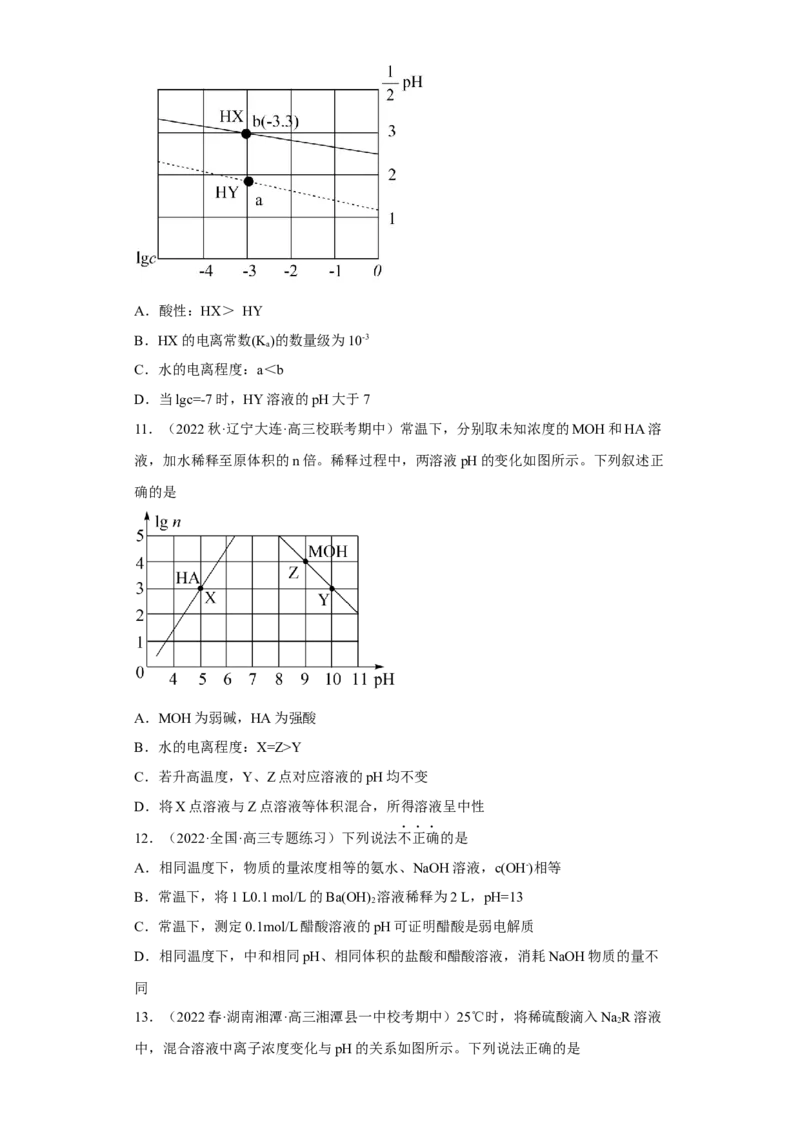
9.(2022·广东广州·铁一中学校联考三模)常温下,向一定浓度的HX溶液中滴加
2
NaOH溶液,混合溶液的的pH与离子浓度变化的关系如图所示。下列叙述不正确的是
A.HX的电离常数K 的数量级为10-5
2 a2
B.直线m表示pH与 的关系
C.当混合溶液呈中性时,c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-)
D.N点水电离出的c(H+)=1×10-4.3mol·L-1
10.(2022·辽宁锦州·渤海大学附属高级中学校考模拟预测)常温下将浓度均为
1.0mol·L-1,体积相同的HX和HY溶液分别加水稀释,pH与溶液浓度的对数(lgc)间的
关系如图所示。下列叙述正确的是
试卷第4页,共9页A.酸性:HX> HY
B.HX的电离常数(K)的数量级为10-3
a
C.水的电离程度:a<b
D.当lgc=-7时,HY溶液的pH大于7
11.(2022秋·辽宁大连·高三校联考期中)常温下,分别取未知浓度的MOH和HA溶
液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述正
确的是
A.MOH为弱碱,HA为强酸
B.水的电离程度:X=Z>Y
C.若升高温度,Y、Z点对应溶液的pH均不变
D.将X点溶液与Z点溶液等体积混合,所得溶液呈中性
12.(2022·全国·高三专题练习)下列说法不正确的是
A.相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
B.常温下,将1 L0.1 mol/L的Ba(OH) 溶液稀释为2 L,pH=13
2
C.常温下,测定0.1mol/L醋酸溶液的pH可证明醋酸是弱电解质
D.相同温度下,中和相同pH、相同体积的盐酸和醋酸溶液,消耗NaOH物质的量不
同
13.(2022春·湖南湘潭·高三湘潭县一中校考期中)25℃时,将稀硫酸滴入NaR溶液
2
中,混合溶液中离子浓度变化与pH的关系如图所示。下列说法正确的是A.M点对应溶液中存在c(Na+)>3c(R2-)
B.B.HR的第二步电离常数K 的数量级为10-4
2 a2
C.NaHR溶液能使酚酞溶液变红
D.L 表示-lg 与pH的关系曲线
1
14.(2022秋·黑龙江哈尔滨·高三黑龙江实验中学校考期中)室温下,向10mL
的 溶液中加入下列物质,对所得溶液的分析正确的是
加入的物质 对所得溶液的分析
A 溶液加水稀释到100mL
由水电离出的
B 0.1mol 固体 比原 溶液中的大
C 10mLpH=1的 溶液 的电离程度不变
D 10mLpH=11的NaOH溶液
A.A B.B C.C D.D
15.(2022秋·河南濮阳·高三濮阳一高校考期中)向10 mL 0.1 molL 溶液
⋅
中滴加0.1 molL 溶液,溶液的导电能力随滴入 溶液体积变化的曲
⋅
线如图所示。下列说法正确的是
试卷第6页,共9页A.a点对应的溶液呈碱性 B. mL
C.水的电离程度:a>b D.b点后的溶液满足
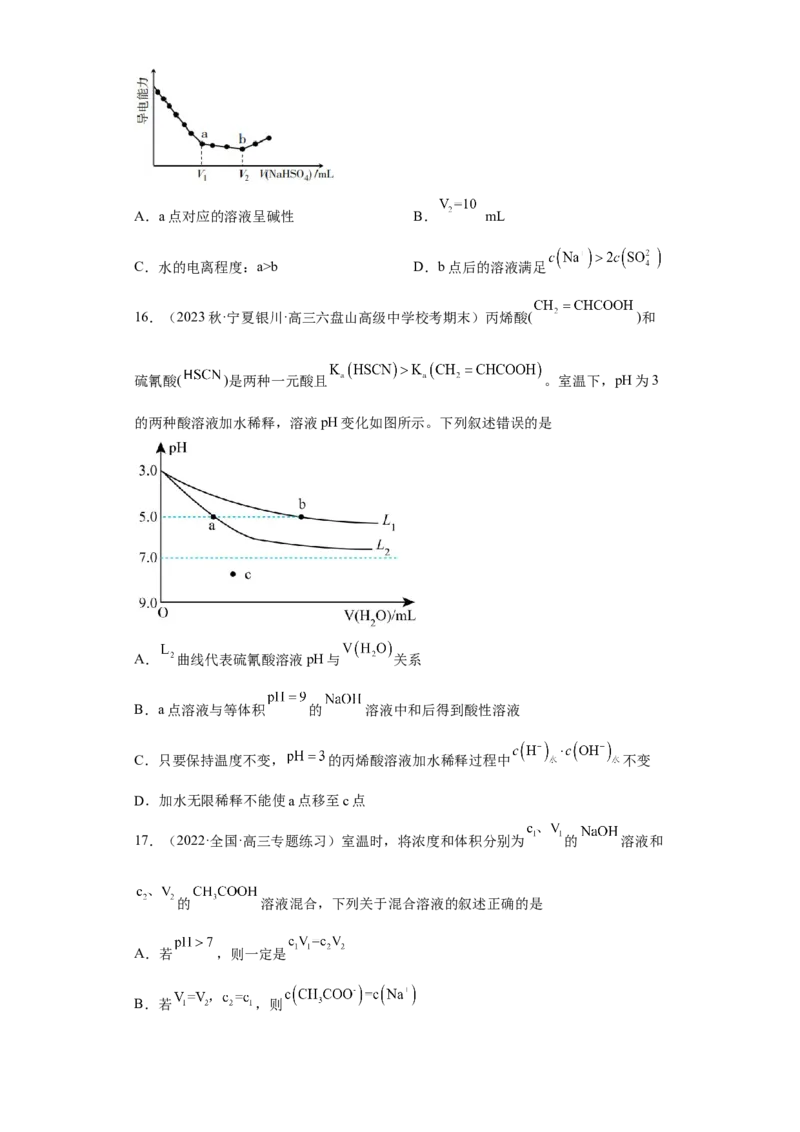
16.(2023秋·宁夏银川·高三六盘山高级中学校考期末)丙烯酸( )和
硫氰酸( )是两种一元酸且 。室温下,pH为3
的两种酸溶液加水稀释,溶液pH变化如图所示。下列叙述错误的是
A. 曲线代表硫氰酸溶液pH与 关系
B.a点溶液与等体积 的 溶液中和后得到酸性溶液
C.只要保持温度不变, 的丙烯酸溶液加水稀释过程中 不变
D.加水无限稀释不能使a点移至c点
17.(2022·全国·高三专题练习)室温时,将浓度和体积分别为 的 溶液和
的 溶液混合,下列关于混合溶液的叙述正确的是
A.若 ,则一定是
B.若 ,则C.当 时,若 ,则一定是
D.当 时,
18.(2022秋·浙江杭州·高二浙江大学附属中学校考期中)常温下,将KOH溶液滴加
到某二元弱酸(H R )中,混合溶pH与 或 的变化关系如图所示,下
2
列叙述正确的是。
A.K (H R)的数量级为10-7
a2 2
B.常温时,NaHR溶液显酸性
C.曲线N表示pH与 的变化关系
D.当混合溶液呈中性时,c(K+ )>c(R2- )>(HR- )>(OH- )=(H+)
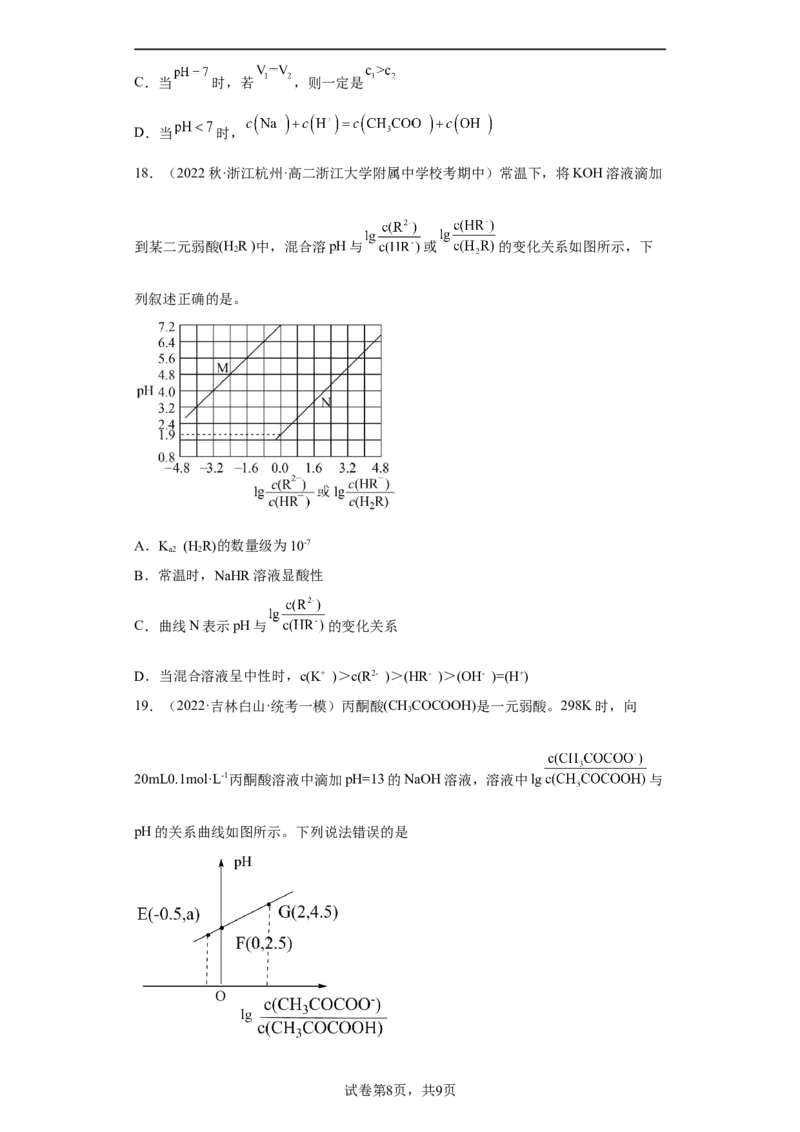
19.(2022·吉林白山·统考一模)丙酮酸(CHCOCOOH)是一元弱酸。298K时,向
3
20mL0.1mol·L-1丙酮酸溶液中滴加pH=13的NaOH溶液,溶液中lg 与
pH的关系曲线如图所示。下列说法错误的是
试卷第8页,共9页A.E点溶液中,a=2
B.298K时,CHCOCOOH的电离常数的数量级为10-3
3
C.G点对应的NaOH溶液的体积为20mL
D.E、F、G三点对应的溶液中水的电离程度:E