文档内容
专题十四 弱电解质的电离 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
选择题(本题含20小题,每题5分,共100分。每题只有一个选项符合题意)
1.(2023秋·山东潍坊·高三统考期末)肼(N H)主要用作导弹、火箭的燃料。已知:
2 4
NH 在水中与NH 性质相似。下列关于NH 的说法错误的是
2 4 3 2 4
A.肼溶于水,发生的第一步电离可表示为:
B.常温下,向0.1mol·L-1的NH 溶液中加水稀释时, 会增大
2 4
C.1molN H 分子中含有5molσ键
2 4
D.NH 和NO 用作火箭推进剂的主要原因是反应放出大量的热且反应后气体体积增
2 4 2 4
大
【答案】B
【详解】A. 在水中与 性质相似,在水中电离与 相似,所以 在水
中发生的第一步电离可表示为: ,A正确;
B. 在水溶液中发生二级电离: ,
, ,加水稀释, 不变, 减小,
减小,B错误;C. 的结构式为: ,1mol 分子中含有5molσ键,C正确;
D. 和 发生反应: ,用作火箭推进剂的
主要原因是反应放出大量的热且反应后气体体积增大,D正确;
故选B。
2.(2023·四川绵阳·二模)已知含磷废水中的磷以磷酸及其盐的形式存在。某温度下,
磷酸的 与溶液的 的关系如下图,该温度下向初始 的含磷废水中加入
可以得到 沉淀而实现废水除磷。下列叙述错误的是
A.该温度下,磷酸的
B.若逐渐增大该废水的 ,溶液中 将随之不断增大
C. 的该废水中离子浓度存在关系:
D.该废水除磷的离子反应有:
【答案】B
【分析】由磷酸的 与溶液的 的关系图可知 、 、
。
【详解】A.该温度下,由关系图可知pH=p =7.21,即 ,A正确;
B.逐渐增大该废水的 过程中,含磷微粒的变化是
,因此溶液中 将先增大后减
小,B错误;
试卷第2页,共21页C. 时,因为 ,所以
,即 ,因为
,所以 ,即
,故 ,C正确;
D.因为向含磷废水中加入 可以得到 沉淀,因此废水除磷过程中
存在离子反应 ,D正确;
故答案为:B。
3.(2022·浙江·模拟预测) 时,下列说法正确的是
A. 为5的氯水和 为5的 溶液混合, 仍为5
B.物质的量浓度相同的 溶液和 溶液, 的数值前者大
C. 相同的醋酸和盐酸,分别与足量的锌粒反应,前者产生的氢气一定大于后者
D.某溶液中水电离出的 ,则该溶液中的溶质可能为酸、碱或盐
【答案】D
【详解】A.氯水与亚硫酸混合发生反应 ,弱酸生成强
酸,故混合后 将会小于5,A错误;
B.由于温度一定时, 的 、 为定值,且 ,由于
铵根离子会水解产生 ,故物质的量浓度相同的 中 大于 溶液中 , 溶液中 数值小,B错误;
C.由于两溶液体积未知,则无法判断产生氢气的多少,C错误;
D.常温下某溶液中水电离出的 ,说明水的电离受到了抑制,则
溶质为自身可电离出氢离子或氢氧根离子的物质,可以是酸、碱或盐(如 ),D
正确;
故选D。
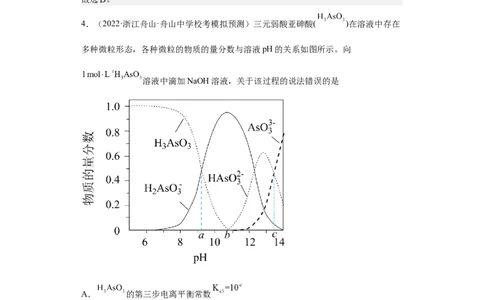
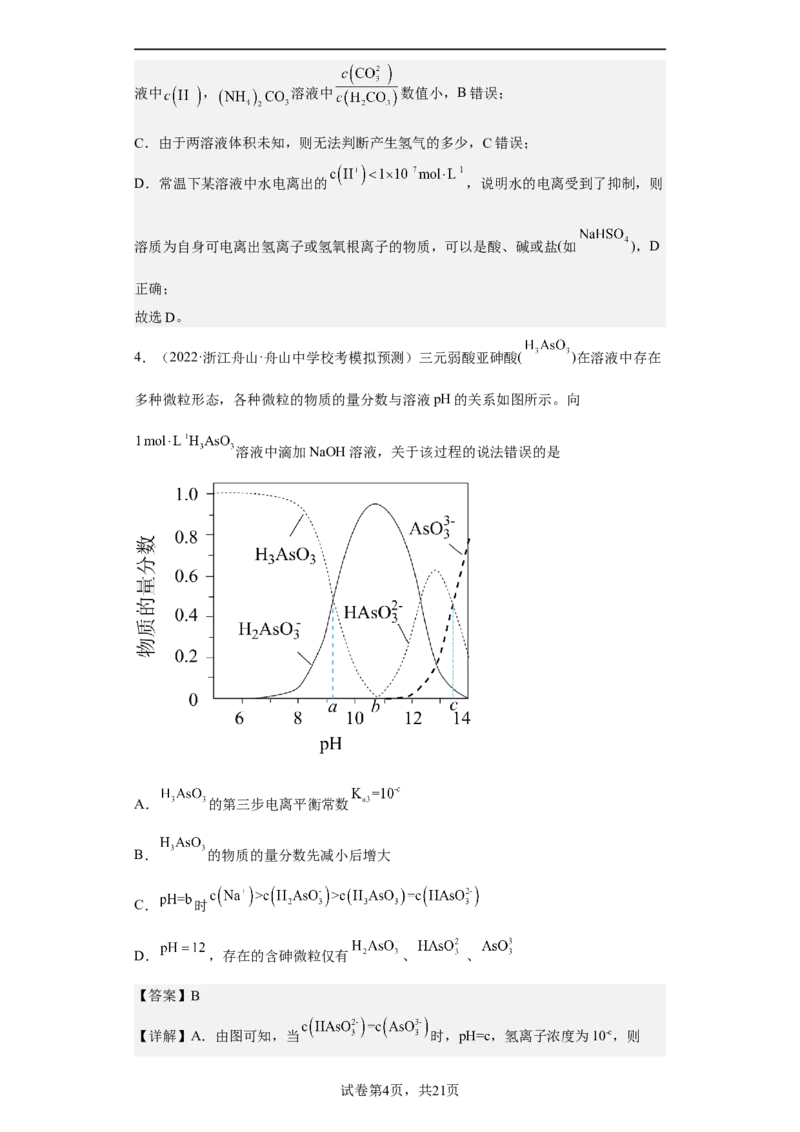
4.(2022·浙江舟山·舟山中学校考模拟预测)三元弱酸亚砷酸( )在溶液中存在
多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示。向
溶液中滴加NaOH溶液,关于该过程的说法错误的是
A. 的第三步电离平衡常数
B. 的物质的量分数先减小后增大
C. 时
D. ,存在的含砷微粒仅有 、 、
【答案】B
【详解】A.由图可知,当 时,pH=c,氢离子浓度为10-c,则
试卷第4页,共21页的第三步电离平衡常数 ,A正确;
B.由图可知, 的物质的量分数一直在减小,B错误;
C.由图可知, 时 浓度最大且 ,则此时溶质主
要为 ,故有 ,C正确;
D.由图可知, , 已经不存在,此时存在的含砷微粒仅有 、
、 ,D正确;
故选B。
5.(2023秋·吉林长春·高三长春市第二中学校考期末) (亚磷酸)为二元弱酸。
298K时,向一定浓度的 溶液中滴加NaOH溶液,溶液的pH与 或
的变化关系如图所示。下列叙述不正确的是
A.直线a代表 与pH的关系
B.d点对应的溶液呈碱性
C. 时,D. 的平衡常数
【答案】B
【详解】A.根据上述分析,a代表 ,A正确;
B.根据上述分析, 代表曲线b,d点 =0, ,温
度不变,K=10-6.7不变,则c(H+)=10-6.7mol/L,pH=6.7,溶液显酸性,B错误;
2
C.根据电荷守恒, ,pH=7,溶液显中
性, ,则
,因为d显酸性,所以c点显酸性,如果溶液显示中性,
则对于曲线a, >0, , ,
,C正确;
D. 的平衡常数 =105.3,D正确;
故选B。
【点睛】根据结构式分析,HPO 为二元弱酸,在水中两步电离,
3 3
, ,当横坐标为0时,
c(H+)=1mol/L,曲线a>曲线b, > ,曲线a
代表 ,曲线b代表 ,则K=10-1.4、K=10-6.7;
1 2
6.(2023秋·北京通州·高三统考期末)某温度下,四种不同一元酸溶液在不同浓度时
试卷第6页,共21页的pH如下表所示,下列推测不合理的是
酸HX的 酸HY的 酸HM的 酸HN的
酸浓度(mol/L)
pH pH pH pH
0.010 3.44 2.00 2.92 2.20
0.10 2.94 1.00 2.42 1.55
A.该温度下电离出H+的能力:HY>HN>HM>HX
B.该温度下将HY溶液加入NaX溶液中,发生反应为HY+NaX=HX+NaY
C.该温度下当HX的浓度为0.10mol/L时,c(HX)>c(X—)>c(H+)>c(OH—)
D.该温度下用同种方法测定,相同体积的0.10mol/LHM溶液比0.010mol/LHM溶液导
电能力强
【答案】C
【详解】A.由表格数据可知,等浓度的四种一元酸溶液的pH大小顺序为
HX>HM>HN>HY,则该温度下四种酸溶液电离出氢离子的能力大小顺序为
HY>HN>HM>HX,故A正确;
B.由表格数据可知,等浓度的HY溶液的pH小于HX溶液,说明HY的酸性强于
HX,由强酸制弱酸的原理可知,HY溶液加入NaX溶液中发生的反应为
HY+NaX=HX+NaY,故B正确;
C.由表格数据可知,HX为一元弱酸,在溶液中部分电离出氢离子和X—离子,则溶
液中微粒的大小顺序为c(HX>c(H+))>c(X—)>c(OH—),故C错误;
D.由表格数据可知,HM为一元弱酸,则相同体积的0.10mol/LHM溶液中离子浓度
大于0.010mol/LHM溶液,导电能力强于0.010mol/LHM溶液,故D正确;
故选C。
7.(2022·河北衡水·河北衡水中学校考模拟预测)t ℃时,向蒸馏水中不断加入NaA
溶液,溶液中c2( )与c( )的变化关系如图所示。下列叙述错误的是A.当溶液中c( )=2× mol/L时,有c( ) > 5× mol/L
B.该温度下, 的水解常数K 的数量级为
h
C.溶液中:c(HA)+c( ) = c( )
D.x点溶液中:c( ) > c( ) > c(HA) > c( )
【答案】B
【详解】A.由图可知,t℃时,没有加入NaA的水中c2( )为1× mol2 · ,
蒸馏水中氢离子浓度等于氢氧根离子浓度,都为1× mol· ,则水的离子积常数
K =1× 。由图可知,溶液中 浓度为2× mol· 时,溶液中c2( )为3×
w
mol2 · ,溶液中氢氧根离子浓度为 × mol· ,则溶液中的氢离子浓度为
mol·L-1≈ 5.8×10-8mol·L-1 > 5×10-8mol·L-1,A项正确;
B.NaA溶液中存在 的水解平衡和水的电离平衡,溶液中 浓度越大,溶液中
与HA的浓度越接近, 的水解常数K ≈ ,由图可知,
h
浓度较大时K ≈ 1×10-10,数量级为10-10,B项错误;
h
C.NaA溶液中存在质子守恒关系c(HA)+c( ) = c( ),C项正确;
D.由图可知,x点溶液中 浓度为3× mol· ,溶液中氢氧根离子浓度为2×
mol·L-1,由C项分析可知NaA溶液中c(HA)+c( ) = c( ),溶液中HA的浓
度小于氢氧根离子浓度,氢离子浓度为5× mol·L-1,则溶液中各微粒浓度的大小顺
序为c( ) > c( ) > c(HA) > c( ),D项正确;
答案选B。
8.(2023秋·新疆·高三校联考期末)室温下,pH=3的HR 溶液、HR 溶液各V mL,
1 2 0
分别加入蒸馏水稀释至V mL。稀释过程中溶液pH与lg 的关系如图所示。下列推断
试卷第8页,共21页错误的是
A.HR 溶液中存在5种粒子
2
B.0.1 mol•L-1 HR 、HR 溶液中,前者酸根离子浓度更大
1 2
C.c(OH-):a=b
D.若起始HR 浓度为0.1 mol•L-1,则起始时HR 的电离度约为0.1%
2 2
【答案】D
【详解】A.pH=3的HR 溶液,c(H+)=10-3 mol/L,当其溶液稀释10倍,溶液pH增大
2
不到1个单位,说明HR 为弱酸,在HR 溶液中存在HR 的电离平衡及H2O的电离平
2 2 2
衡,溶液中存在HR 、H2O、H+、OH-、 ,共5种粒子,A正确;
2
B.根据开始时溶液pH=3,c(H+)=10-3 mol/L,当HR 、HR 溶液稀释相同倍数后溶液
1 2
pH增大值:HR >HR ,所以酸性:HR >HR ,因此0.1 mol•L-1 HR 、HR 溶液中,前
1 2 1 2 1 2
者电离程度比后者大,故前者溶液中酸根离子浓度更大,B正确;
C.根据图示可知:a、b两点的pH相等,而两种溶液中c(H+)相等,根据水的离子积
常数可知两种溶液中OH-的浓度大小关系为:a=b,C正确;
D.若起始HR 浓度为0.1 mol•L-1,c(HR )=0.1 mol/L,开始时溶液pH=3,c(H+)=10-3
2 2
mol/L,故起始时HR 的电离度约为 ,
2
故合理选项是D。
9.(2022秋·北京石景山·高三统考期末)某温度下,水溶液中 和
的物质的量分数随 变化如图所示。下列说法不正确的是A.碳酸的电离方程式为: ,
B.该温度下,
C.该温度下,
D. 溶液中,
【答案】D
【详解】A.碳酸为二元弱酸,分两步电离,其电离方程式为: ,
,A正确;
B.由图可知 时, ,
,B正确;
C.由图可知 时, ,
,C正确;
D.根据电荷守恒有 ,D错误;
故选D。
10.(2022秋·山东济宁·高三统考期末)根据酸碱质子理论,给出质子( )的物质是
试卷第10页,共21页酸,给出质子的能力越强,酸性越强。相同温度下,HCl和 在冰醋酸中存在
,
,(知 )下列说法正确
的是
A.把HCl通入 水溶液中:
B.酸性强弱顺序为:
C. 在HCOOH中的
D.接受质子的能力:
【答案】BD
【详解】A.在冰醋酸中才存在 ,在水中是生成
CHCOOH,故反应为 ,选项A错误;
3
B.在冰醋酸中,HCl和 的 :HCl< ,故 :HCl< ,酸性:
HCl> ,在冰醋酸中 给出质子(H+),CHCOOH结合H+,给出H+能力:
3
>CH COOH,故酸性: ,选项B正确;
3
C.酸性HCOOH> CH COOH,给出H+能力HCOOH> CH COOH,结合H+能力
3 3
HCOOH< CH COOH, 在HCOOH的电离程度小于在冰醋酸中的电离程度,
3
<10-9.4, >9.4,选项C错误;
D.HCl在水中完全电离,在冰醋酸中电离程度较小,说明结合HCl电离出的H+能力
HO> CH COOH,选项D正确;
2 3
答案选BD。
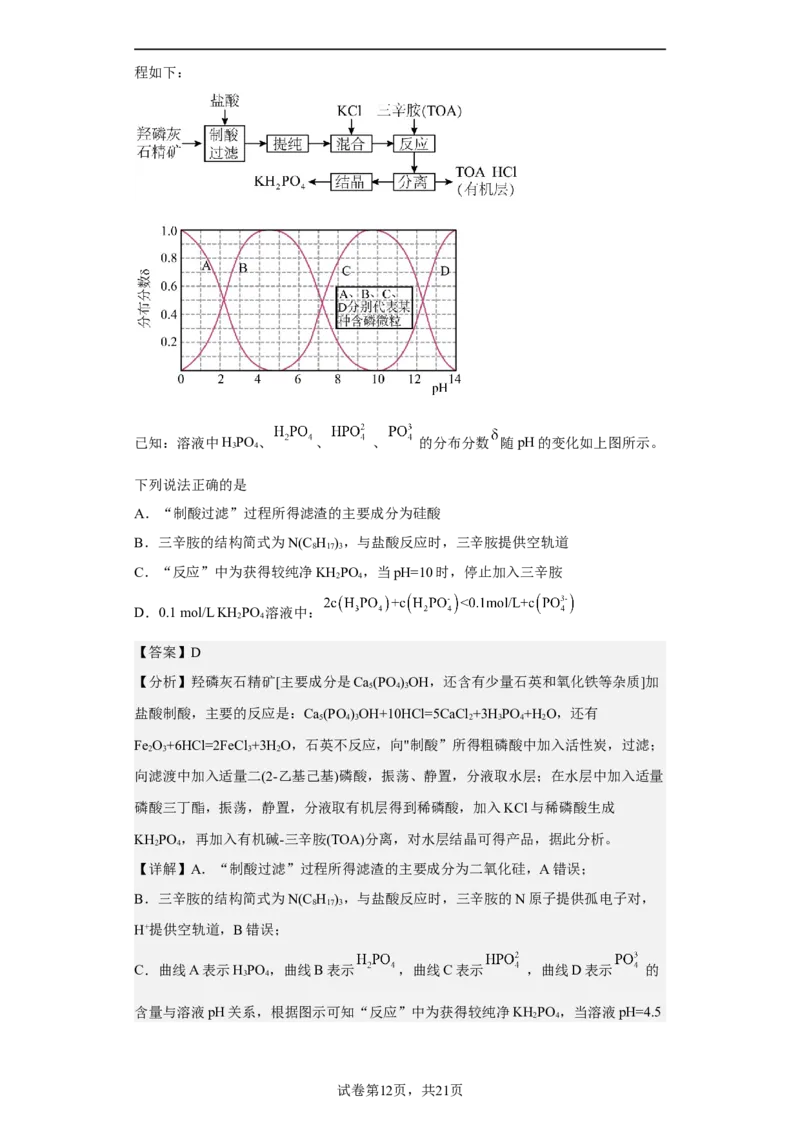
11.(2023秋·江苏南通·高三统考期末)工业上以羟磷灰石精矿[主要成分是
Ca (PO )OH,还含有少量石英和氧化铁等杂质]为原料,生产磷酸二氢钾(KH PO )的流
5 4 3 2 4程如下:
已知:溶液中HPO 、 、 、 的分布分数 随pH的变化如上图所示。
3 4
下列说法正确的是
A.“制酸过滤”过程所得滤渣的主要成分为硅酸
B.三辛胺的结构简式为N(C H ),与盐酸反应时,三辛胺提供空轨道
8 17 3
C.“反应”中为获得较纯净KH PO ,当pH=10时,停止加入三辛胺
2 4
D.0.1 mol/L KH PO 溶液中:
2 4
【答案】D
【分析】羟磷灰石精矿[主要成分是Ca (PO )OH,还含有少量石英和氧化铁等杂质]加
5 4 3
盐酸制酸,主要的反应是:Ca (PO )OH+10HCl=5CaCl +3H PO +H O,还有
5 4 3 2 3 4 2
Fe O+6HCl=2FeCl +3H O,石英不反应,向"制酸”所得粗磷酸中加入活性炭,过滤;
2 3 3 2
向滤渡中加入适量二(2-乙基己基)磷酸,振荡、静置,分液取水层;在水层中加入适量
磷酸三丁酯,振荡,静置,分液取有机层得到稀磷酸,加入KCl与稀磷酸生成
KH PO ,再加入有机碱-三辛胺(TOA)分离,对水层结晶可得产品,据此分析。
2 4
【详解】A.“制酸过滤”过程所得滤渣的主要成分为二氧化硅,A错误;
B.三辛胺的结构简式为N(C H ),与盐酸反应时,三辛胺的N原子提供孤电子对,
8 17 3
H+提供空轨道,B错误;
C.曲线A表示HPO ,曲线B表示 ,曲线C表示 ,曲线D表示 的
3 4
含量与溶液pH关系,根据图示可知“反应”中为获得较纯净KH PO ,当溶液pH=4.5
2 4
试卷第12页,共21页时, 的含量最大,此时应该停止加入三辛胺,C错误;
D.对于0.1 mol/L KH PO 溶液,根据质子守恒可得:①c(H+)=c(OH-)+c( )+2c(
2 4
)-c(H PO );根据物料守恒可得②c(K+)=c(H PO )+c( )+c( )+c( ),
3 4 3 4
将②-①整理可得c(K+)-c(H+)= 2c(H PO )+c( )-c( )-c(OH-),c(H+)-
3 4
c(OH-)=c(K+)-2c(H PO )-c( )-c( ), 水解大于电离,溶液显酸性,所以
3 4
c(H+)-c(OH-)>0,根据溶液组成可知c(K+)=0.1 mol/L,所以2c(H PO )+ c( )<0.1
3 4
mol/L+ c( ),D正确;
故合理选项是D。
12.(2023秋·吉林长春·高三长春市第二中学校考期末)常温下,向20 mL0.1 mol/L
氨水中滴加盐酸,溶液中由水电离出的c(H+)随加入盐酸体积的变化如图所示。则下列
说法正确的是
A.常温下,0.1 mol/L氨水的电离常数K约为
B.c点溶液中,c(Cl-)=c( )
C.a、b之间的任意一点:c(Cl-)>c( ),c(H+)>c(OH-)
D.b、d两点均为中性
【答案】A
【分析】向20 mL 0.1 mol/L氨水中滴加0. l mol/L盐酸,根据图象可知:水的电离程度
由小逐渐变大,后又逐渐变小,则a点溶液中溶质只有氨水,b点溶质为一水合氨和氯化铵,c点 的水解程度达到最大,也是恰好完全反应点,溶质为NH Cl;再继续加
4
入盐酸,盐酸过量抑制水的电离,溶质为氯化铵和盐酸。
【详解】A.由图可知,常温下,0.l mol/L的氨水溶液中c(H+) =10-11 mol/L,则
c(OH-)= ,0.1 mol/L氨水的电离常数K =
,A正确;
B.根据分析可知c点为氨水与盐酸完全反应点,溶液中溶质为氯化铵,铵根离子会水
解而消耗,所以c( )<c(Cl-),B错误;
C.a到b过程中,水电离程度不断增大,氨水不断被中和生成氯化铵,b点溶质应为
氯化铵与氨水混合溶液,溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(H+)+c( ),溶液从
碱性到中性,则a~b之间任意一点有c(H+)<c(OH-),结合电荷守恒得c(Cl-)<c( ),
C错误;
D.b点溶质为氯化铵与氨水,溶液呈中性,d点溶质为氯化铵与过量的盐酸,溶液显
酸性,D错误;
故合理选项是A。
13.(2023秋·江苏南通·高三统考期末)化学常用图像直观地描述化学反应的进程或
结果。下列与NH 有关的图像描述正确的是
3
A.图①表示 在t 时刻扩大容器体积,v 随时间变化的曲
1 逆
线
试卷第14页,共21页B.图②表示 平衡时NH 体积分数随起始 变化的曲线,
3
则转化率:a (H )=a (H )
A 2 B 2
C.图③表示25℃时分别稀释pH=1的NaOH溶液和氨水时溶液pH的变化,曲线Ⅰ表
示氨水
D.图④可表示CHCOOH溶液中通入NH 至过量的过程中溶液导电性的变化
3 3
【答案】A
【详解】A. 的正反应是气体体积减小的反应,在t 时刻扩
1
大容器体积,导致NH 气体的浓度降低,体系的压强减小,v 减小,化学平衡向气体
3 逆
体积增大的逆反应方向移动,导致NH 的浓度进一步减小,v 减小,后到t 时反应达
3 逆 2
到平衡状态,故可以表示v 随时间变化的曲线,A正确;
逆
B.A、B两点NH 的平衡含量相同,但反应体系中 越大反应的H 的物质的量就
3 2
越多, H 的转化率就越大,所以转化率:a (H )<a (H ),B错误;
2 A 2 B 2
C.开始时溶液pH相等,溶液中c(OH-)相等,但NaOH是强电解质完全电离,而氨水
中存在电离平衡,所以开始时浓度c(NH ·H O)>c(NaOH),当二者稀释相同倍数时,
3 2
稀释使溶液中c(OH-)减小,氨水中电离平衡正向移动,最终达到平衡时氨水中c(OH-)
比NaOH大,溶液pH更大,故曲线Ⅰ表示NaOH溶液,曲线Ⅱ表示氨水,C错误;
D.CHCOOH溶液中存在电离平衡:CHCOOH CHCOO-+H+,溶液中含有自由移
3 3 3
动的离子,因此能够导电,向溶液中通入NH ,反应产生盐CHCOONH,导致溶液中
3 3 4
自由移动的离子浓度增大,溶液导电性增强,当二者恰好反应时离子浓度最大,溶液
导电能力最强,后溶液中自由移动的离子浓度几乎不变,因此图示不能表示
CHCOOH溶液中通入NH 至过量的过程中溶液导电性的变化,D错误;
3 3
故合理选项是A。
14.(2023秋·北京昌平·高三统考期末)已知物质的相关数据如下表,下列说法正确
的是
物质
相关数
据
A. 不与盐酸溶液反应B. 溶液中存在的所有微粒有:
C. 与碳酸钠溶液反应,可能产生气体
D.向石灰水悬浊液中加入 溶液,溶液可能变澄清
【答案】C
【详解】A.HF为弱酸,NaF与盐酸反应生成 ,符合强酸制
弱酸,A错误;
B. ,则溶液中的微粒有,
,B错误;
C.根据电离平衡常数, , 。
符合强酸制弱酸,C正确;
D.根据Ksp可知, ,Ca(OH) 转化为CaF 沉淀,D错误;
2 2
故答案为:C。
15.(2022秋·广东汕尾·高三统考期末)实验室粗配 0.1 mol/L NaOH 溶液,用邻苯二
甲酸氢钾(用 KHP 表示)标定其精确浓度。取 20.00 mL 0.1000 mol/L KHP 标准液于锥
形瓶中,滴入所配NaOH 溶液,滴定曲线如图。下列说法错误的是
A.a点有:
B.b点有:
C.c点有:
D.该NaOH实际浓度为0.09524mol/L,可能是称量时潮解了
【答案】A
【详解】A.HP-水解和电离方程式分别为HP-+H O HP+OH-,HP- H++P2-,则有
2 2
c(H+)+c(H P)=c(P2-)+c(OH-),A错误;
2
试卷第16页,共21页B.该NaOH实际浓度为0.09524mol/L,10.5mLNaOH溶液的物质的量为0.001mol,根
据物料守恒可知,n(P2-)+n(HP-)+n(HP)=0.002mol,则b点有:
2
,B正确;
C.根据电荷守恒 ,c点pH=7,
c(OH-)=c(H+),则 ,C正确;
D.NaOH固体具有吸水性,容易吸水而潮解,导致NaOH实际浓度降低,D正确;
故答案选A。
16.(2022·浙江·模拟预测)二甲胺的水合物 是一元弱碱,在水中
的电离与 相似,可与盐酸反应生成 。下列说法错误的是
A.常温下, 二甲胺溶液的
B.往二甲胺溶液中加入NaOH固体会抑制 的电离
C.加水稀释 溶液, 增大
D. 溶液中:
【答案】C
【详解】A. 是一元弱碱,在水溶液中部分电离,则常温下,
二甲胺溶液中 , ,A正确;
B.二甲胺溶液中存在平衡: ,加入NaOH固体
后,OH-浓度增大,二甲胺电离平衡逆向移动,从而抑制了 的电离,B
正确;
C. 溶液中存在水解平衡: ,加水稀释,水解平衡正向移动,但H+浓度减小,则 ,由
K 只与温度有关,加水稀释不变,所以 减小,C错误;
h
D. 溶液中存在电荷守恒: ,D
正确;
故选C。
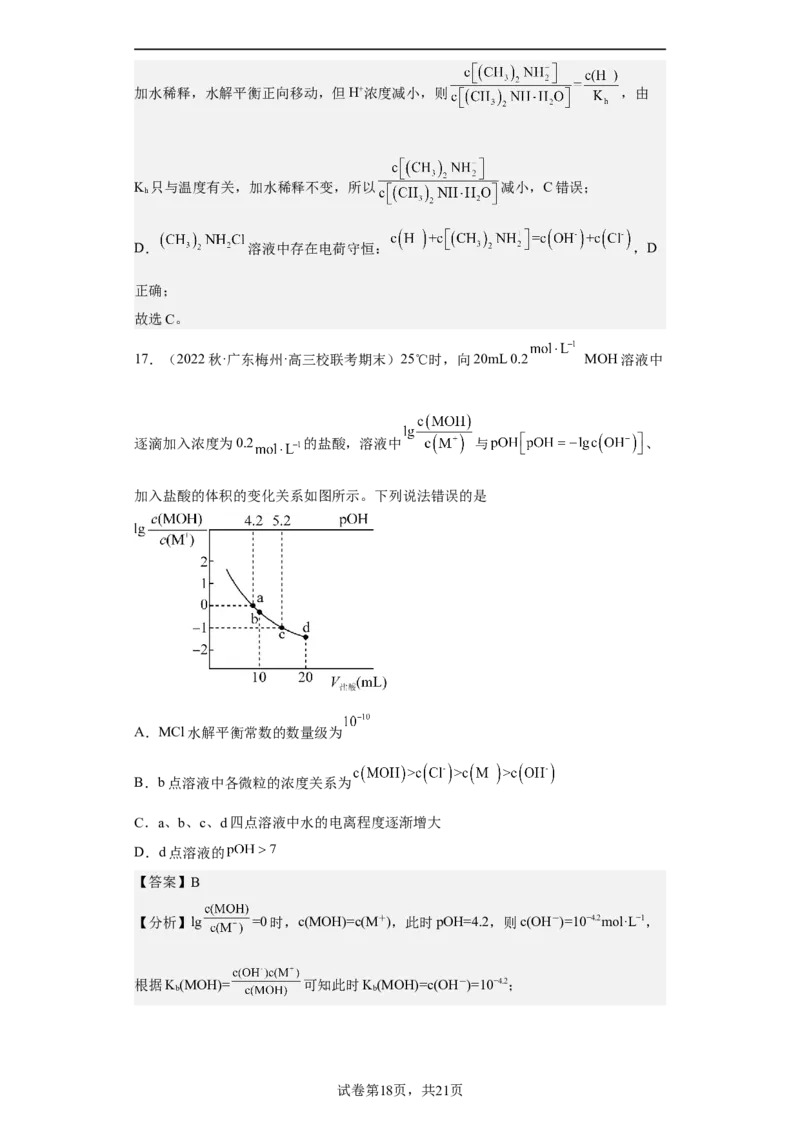
17.(2022秋·广东梅州·高三校联考期末)25℃时,向20mL 0.2 MOH溶液中
逐滴加入浓度为0.2 的盐酸,溶液中 与 、
加入盐酸的体积的变化关系如图所示。下列说法错误的是
A.MCl水解平衡常数的数量级为
B.b点溶液中各微粒的浓度关系为
C.a、b、c、d四点溶液中水的电离程度逐渐增大
D.d点溶液的
【答案】B
【分析】lg =0时,c(MOH)=c(M+),此时pOH=4.2,则c(OH-)=10−4.2mol·L−1,
根据K(MOH)= 可知此时K(MOH)=c(OH-)=10−4.2;
b b
试卷第18页,共21页【详解】A.由分析可知,MCl的水解常数为 ,数量级为
10−10,A正确;
B.b点加入10mL0.2 的盐酸,溶质为等量的MOH和MCl,溶液呈碱性,
c(OH-)>c(H+),则MOH的电离程度大于M+水解程度,所以离子浓度大小顺序为
c(M+)>c(Cl-)>c(MOH)>c(OH-)>c(H+),B错误;
C.酸和碱都会抑制水的电离,开始未加入HCl溶液,原碱溶液电离出的氢氧根离子
抑制水的电离,加入HCl溶液到中和率100%时生成可以水解的MCl,促进水的电离,
即中和率从0至100%的过程水的电离程度一直增大,所以水的电离程度:a