文档内容
2025新教材化学高考第一轮
专题四 氧化还原反应
1.劳动开创未来。下列劳动项目与所述化学知识没有关联的是( )
选项 劳动项目 化学知识
A 利用工业合成氨实现人工固氮 N 具有还原性
2
B 用石灰乳除去烟气中的SO SO 是酸性氧化物
2 2
C 将锌块镶嵌在轮船底部防腐 锌的金属性比铁强
D 用HNO 除去试管中的银镜 HNO 具有强氧化性
3 3
2.化学品在生活、生产中应用广泛。下列有关物质的应用与氧化还原反应无关的是(
)
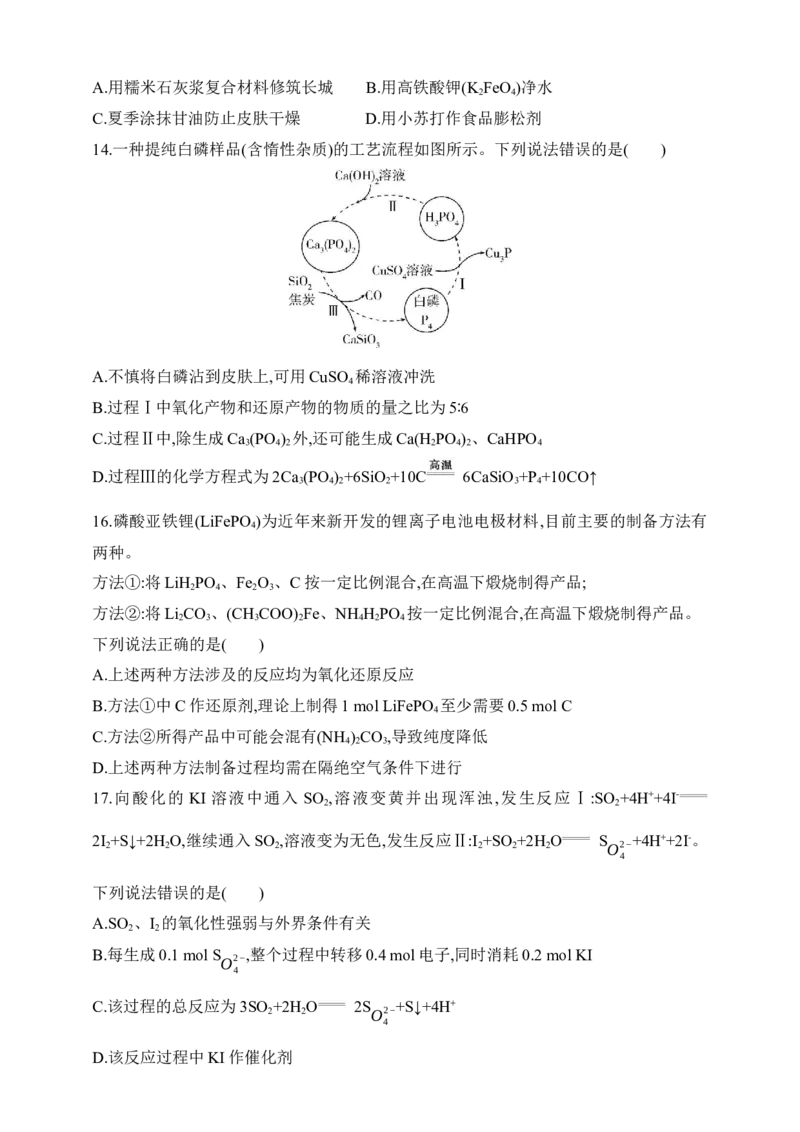
A.工业上用硫铁矿(FeS )为原料生产发烟硫酸
2
B.用Na O 作潜水器的供氧剂
2 2
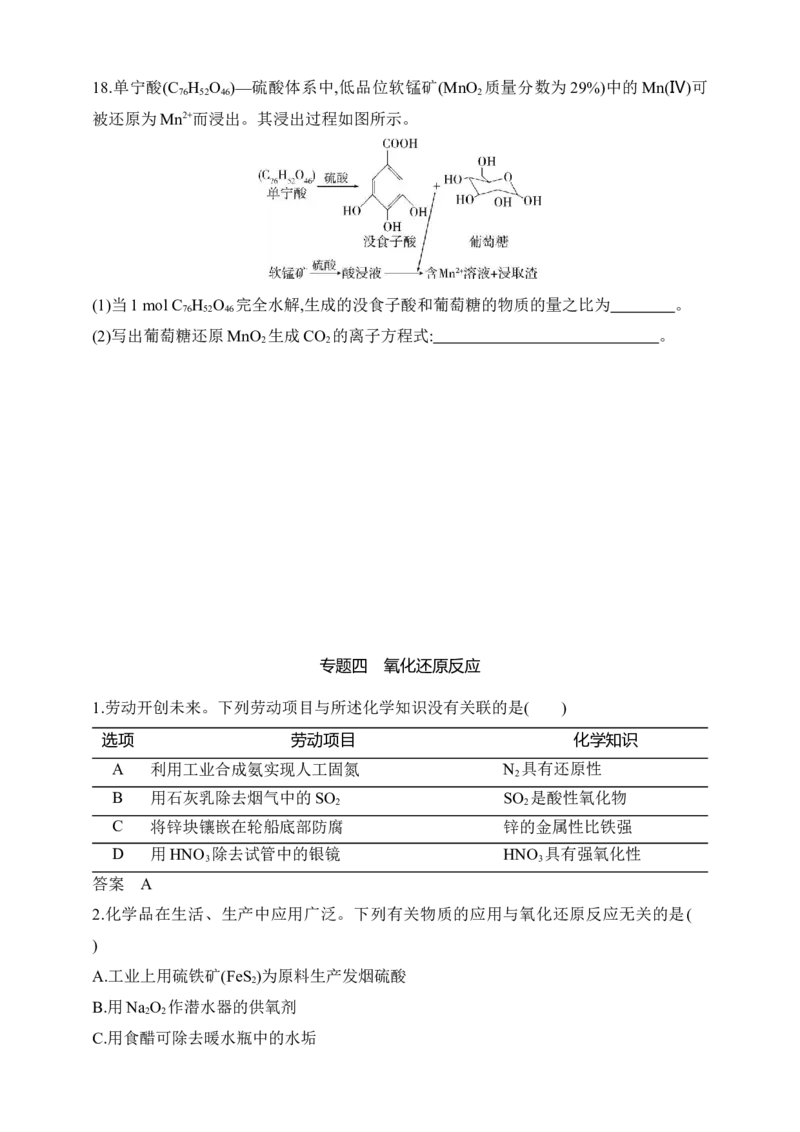
C.用食醋可除去暖水瓶中的水垢
D.用优质糯米为原料酿制白酒
3.氯及其化合物在生活、生产中用途广泛。下列相关的离子方程式正确的是( )
A.漂白粉投入水中:ClO-+H O HClO+OH-
2
B.用Cl 使电路板刻蚀废液再生:Cl +Fe2+ 2Cl-+Fe3+
2 2
C.Cl 与NaOH溶液制“84消毒液”:Cl +2OH- Cl-+ClO-+H O
2 2 2
D.浓盐酸和MnO 制Cl :4HCl(浓)+MnO Cl ↑+2H O+2Cl-+Mn2+
2 2 2 2 2
4.纯净物状态下的标准电极电势,可用来比较对应氧化剂的氧化性强弱,现有5组标准电极
电势数据如下表所示:
氧化还原电对 标准电极电
电极反应式
(氧化型/还原型) 势(φθ/V)
Fe3+/Fe2+ Fe3++e- Fe2+ 0.77
I /I- I +2e- 2I- 0.54
2 2
Cr O2−+6e-+14H+
Cr O2−/Cr3+ 2 7 1.36
2 7 2Cr3++7H O
2
Br /Br- Br (l)+2e- 2Br- 1.07
2 2
Sn4+/Sn2+ Sn4++2e- Sn2+ 0.151
下列分析不正确的是( )
A.氧化性:Cr >Br >Fe3+
2O2− 2
7B.往淀粉KI溶液中滴加SnCl 溶液,溶液不变蓝
4
C.往含有KSCN的FeI 溶液中滴加少量溴水,溶液变红色
2
D.K Cr O 溶液与 FeCl 溶液反应的离子方程式为 Cr +6Fe2++14H+ 2Cr3++6Fe3+
2 2 7 2 2O2−
7
+7H O
2
5.钛酸亚铁(FeTiO )在高温下经氯化得到四氯化钛,再制取金属钛的流程如图所示(已知电
3
负性Ti:1.54,F:3.98,Cl:3.16)。
下列说法正确的是( )
A.氯化过程中,每消耗6 mol碳单质,转移电子14 mol
B.氯化过程中,FeTiO 既是氧化剂也是还原剂
3
C.相对分子质量:TiCl >TiF ,熔点:TiCl >TiF
4 4 4 4
D.制取金属钛时也可以选用CO 隔绝空气
2
6.《本草纲目》中记载:“(火药)乃焰硝(KNO )、硫黄、杉木炭所合,以为烽燧铳机诸药
3
者。”火药燃烧爆炸时发生的反应为S+2KNO +3C K S+N ↑+3CO ↑。下列有关说法
3 2 2 2
错误的是( )
A.氧化产物与还原产物的物质的量之比为3∶2
B.反应每转移6 mol电子,则能生成11.2 L N
2
C.该反应过程中有极性键、非极性键和离子键的形成
D.该反应中分别被S和硝酸钾氧化的碳原子数之比为1∶5
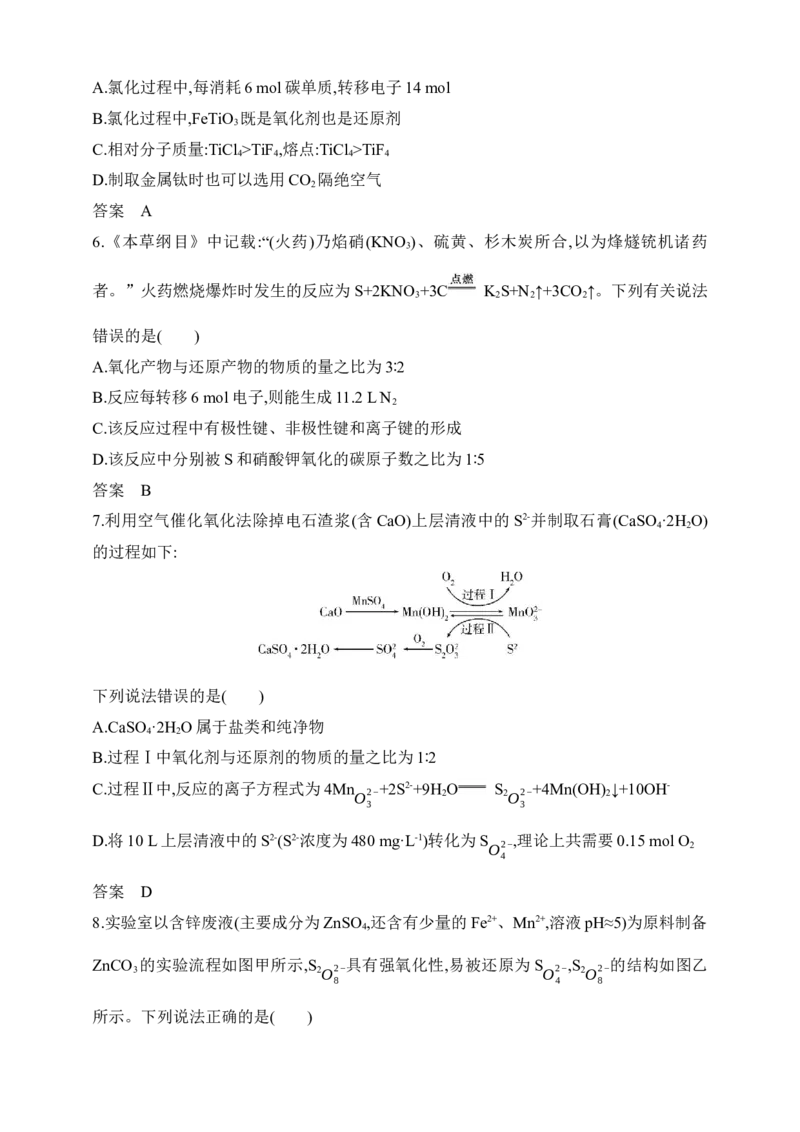
7.利用空气催化氧化法除掉电石渣浆(含CaO)上层清液中的S2-并制取石膏(CaSO ·2H O)
4 2
的过程如下:
下列说法错误的是( )
A.CaSO ·2H O属于盐类和纯净物
4 2
B.过程Ⅰ中氧化剂与还原剂的物质的量之比为1∶2C.过程Ⅱ中,反应的离子方程式为4Mn +2S2-+9H O S +4Mn(OH) ↓+10OH-
O2− 2 2O2− 2
3 3
D.将10 L上层清液中的S2-(S2-浓度为480 mg·L-1)转化为S ,理论上共需要0.15 mol O
O2− 2
4
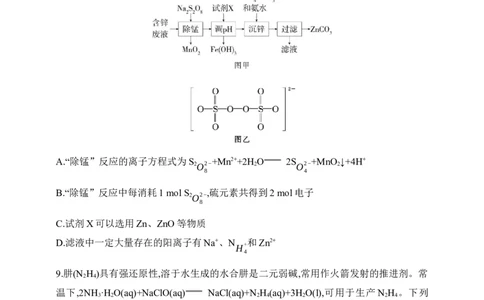
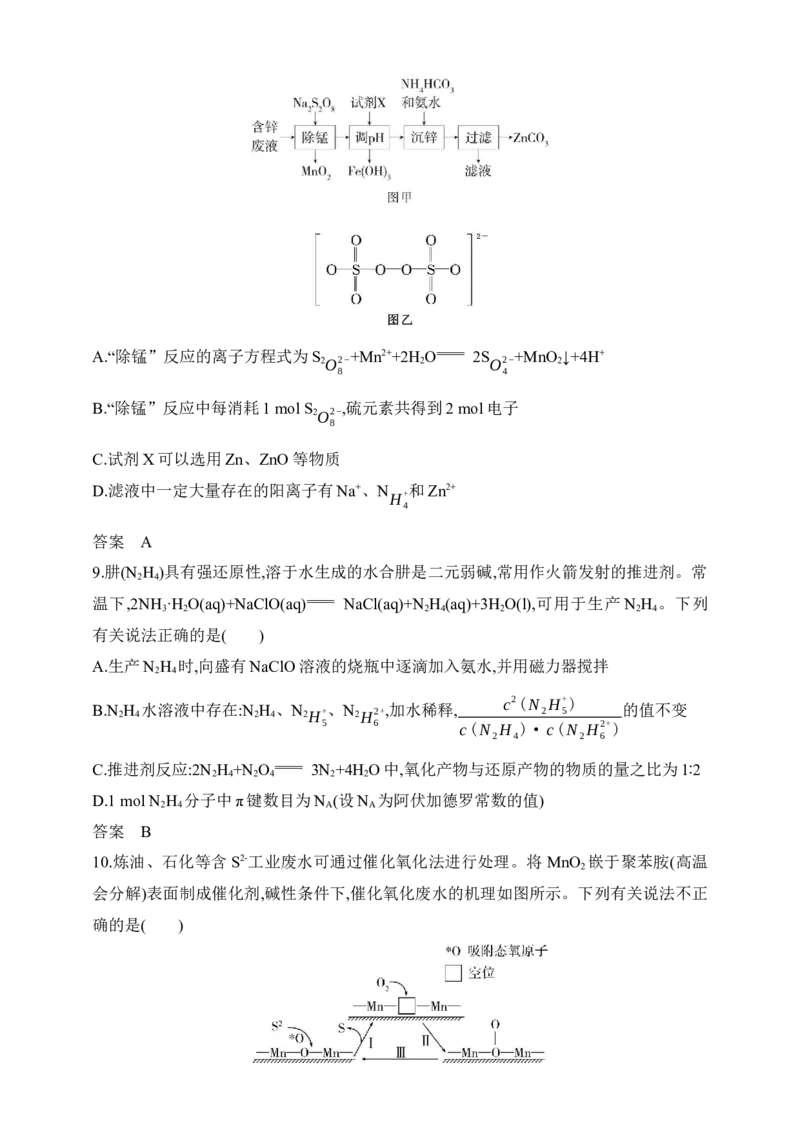
8.实验室以含锌废液(主要成分为ZnSO ,还含有少量的Fe2+、Mn2+,溶液pH≈5)为原料制备
4
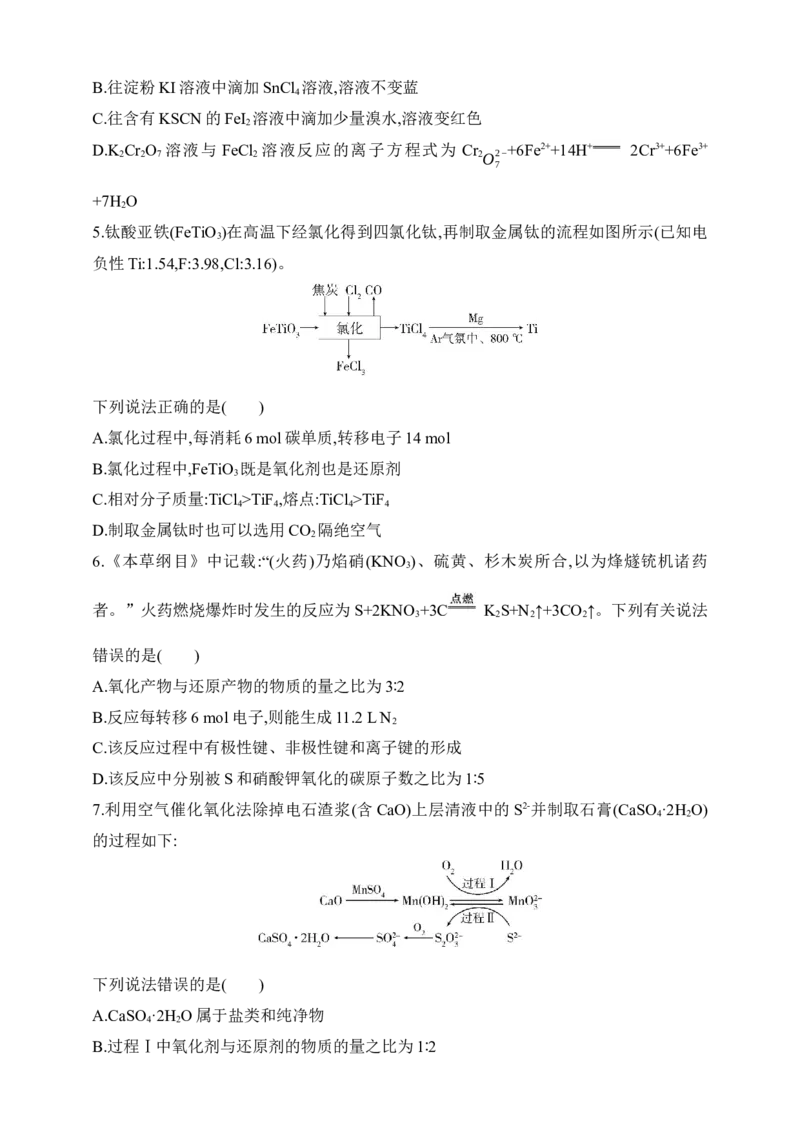
ZnCO 的实验流程如图甲所示,S 具有强氧化性,易被还原为S ,S 的结构如图乙
3 2O2− O2− 2O2−
8 4 8
所示。下列说法正确的是( )
A.“除锰”反应的离子方程式为S +Mn2++2H O 2S +MnO ↓+4H+
2O2− 2 O2− 2
8 4
B.“除锰”反应中每消耗1 mol S ,硫元素共得到2 mol电子
2O2−
8
C.试剂X可以选用Zn、ZnO等物质
D.滤液中一定大量存在的阳离子有Na+、N 和Zn2+
H+
4
9.肼(N H )具有强还原性,溶于水生成的水合肼是二元弱碱,常用作火箭发射的推进剂。常
2 4
温下,2NH ·H O(aq)+NaClO(aq) NaCl(aq)+N H (aq)+3H O(l),可用于生产 N H 。下列
3 2 2 4 2 2 4
有关说法正确的是( )
A.生产N H 时,向盛有NaClO溶液的烧瓶中逐滴加入氨水,并用磁力器搅拌
2 4
c2(N H+)
B.N 2 H 4 水溶液中存在:N 2 H 4 、N 2H+ 、N 2H2+,加水稀释, 2 5 的值不变
5 6 c(N H )·c(N H2+)
2 4 2 6
C.推进剂反应:2N H +N O 3N +4H O中,氧化产物与还原产物的物质的量之比为1∶2
2 4 2 4 2 2
D.1 mol N H 分子中π键数目为N (设N 为阿伏加德罗常数的值)
2 4 A A
10.炼油、石化等含S2-工业废水可通过催化氧化法进行处理。将 MnO 嵌于聚苯胺(高温
2
会分解)表面制成催化剂,碱性条件下,催化氧化废水的机理如图所示。下列有关说法不正确的是( )
A.催化剂因S覆盖表面或进入空位而失效,高温灼烧后也不可继续使用
B.该反应过程的总反应方程式为O +2H O+2S2- 4OH-+2S↓
2 2
C.反应过程中只有硫元素被氧化
D.反应Ⅲ的ΔH>0
11.以废弃锌锰干电池(主要成分是 Zn 和 MnO ,还含有少量炭黑)为原料制取 ZnSO 、
2 4
MnSO 溶液,进而得到复合微肥的流程如下:
4
下列说法正确的是( )
A.浸取时,MnO 与FeS(不溶于水)反应的离子方程式为8MnO +2FeS+16H+ 8Mn2++2S
2 2
+2Fe2++8H O
O2− 2
4
B.浸取液中主要存在的离子有H+、Fe3+、Zn2+、S2-、Mn2+、S
O2−
4
C.过滤Ⅱ所得的滤渣为ZnCO
3
D.过滤所得ZnSO 、MnSO 溶液中:c(Zn2+)+c(Mn2+)Br >Fe3+
2O2− 2
7
B.往淀粉KI溶液中滴加SnCl 溶液,溶液不变蓝
4
C.往含有KSCN的FeI 溶液中滴加少量溴水,溶液变红色
2
D.K Cr O 溶液与 FeCl 溶液反应的离子方程式为 Cr +6Fe2++14H+ 2Cr3++6Fe3+
2 2 7 2 2O2−
7
+7H O
2
答案 C
5.钛酸亚铁(FeTiO )在高温下经氯化得到四氯化钛,再制取金属钛的流程如图所示(已知电
3
负性Ti:1.54,F:3.98,Cl:3.16)。
下列说法正确的是( )A.氯化过程中,每消耗6 mol碳单质,转移电子14 mol
B.氯化过程中,FeTiO 既是氧化剂也是还原剂
3
C.相对分子质量:TiCl >TiF ,熔点:TiCl >TiF
4 4 4 4
D.制取金属钛时也可以选用CO 隔绝空气
2
答案 A
6.《本草纲目》中记载:“(火药)乃焰硝(KNO )、硫黄、杉木炭所合,以为烽燧铳机诸药
3
者。”火药燃烧爆炸时发生的反应为S+2KNO +3C K S+N ↑+3CO ↑。下列有关说法
3 2 2 2
错误的是( )
A.氧化产物与还原产物的物质的量之比为3∶2
B.反应每转移6 mol电子,则能生成11.2 L N
2
C.该反应过程中有极性键、非极性键和离子键的形成
D.该反应中分别被S和硝酸钾氧化的碳原子数之比为1∶5
答案 B
7.利用空气催化氧化法除掉电石渣浆(含CaO)上层清液中的S2-并制取石膏(CaSO ·2H O)
4 2
的过程如下:
下列说法错误的是( )
A.CaSO ·2H O属于盐类和纯净物
4 2
B.过程Ⅰ中氧化剂与还原剂的物质的量之比为1∶2
C.过程Ⅱ中,反应的离子方程式为4Mn +2S2-+9H O S +4Mn(OH) ↓+10OH-
O2− 2 2O2− 2
3 3
D.将10 L上层清液中的S2-(S2-浓度为480 mg·L-1)转化为S ,理论上共需要0.15 mol O
O2− 2
4
答案 D
8.实验室以含锌废液(主要成分为ZnSO ,还含有少量的Fe2+、Mn2+,溶液pH≈5)为原料制备
4
ZnCO 的实验流程如图甲所示,S 具有强氧化性,易被还原为S ,S 的结构如图乙
3 2O2− O2− 2O2−
8 4 8
所示。下列说法正确的是( )A.“除锰”反应的离子方程式为S +Mn2++2H O 2S +MnO ↓+4H+
2O2− 2 O2− 2
8 4
B.“除锰”反应中每消耗1 mol S ,硫元素共得到2 mol电子
2O2−
8
C.试剂X可以选用Zn、ZnO等物质
D.滤液中一定大量存在的阳离子有Na+、N 和Zn2+
H+
4
答案 A
9.肼(N H )具有强还原性,溶于水生成的水合肼是二元弱碱,常用作火箭发射的推进剂。常
2 4
温下,2NH ·H O(aq)+NaClO(aq) NaCl(aq)+N H (aq)+3H O(l),可用于生产 N H 。下列
3 2 2 4 2 2 4
有关说法正确的是( )
A.生产N H 时,向盛有NaClO溶液的烧瓶中逐滴加入氨水,并用磁力器搅拌
2 4
c2(N H+)
B.N 2 H 4 水溶液中存在:N 2 H 4 、N 2H+ 、N 2H2+,加水稀释, 2 5 的值不变
5 6 c(N H )·c(N H2+)
2 4 2 6
C.推进剂反应:2N H +N O 3N +4H O中,氧化产物与还原产物的物质的量之比为1∶2
2 4 2 4 2 2
D.1 mol N H 分子中π键数目为N (设N 为阿伏加德罗常数的值)
2 4 A A
答案 B
10.炼油、石化等含S2-工业废水可通过催化氧化法进行处理。将 MnO 嵌于聚苯胺(高温
2
会分解)表面制成催化剂,碱性条件下,催化氧化废水的机理如图所示。下列有关说法不正
确的是( )A.催化剂因S覆盖表面或进入空位而失效,高温灼烧后也不可继续使用
B.该反应过程的总反应方程式为O +2H O+2S2- 4OH-+2S↓
2 2
C.反应过程中只有硫元素被氧化
D.反应Ⅲ的ΔH>0
答案 C
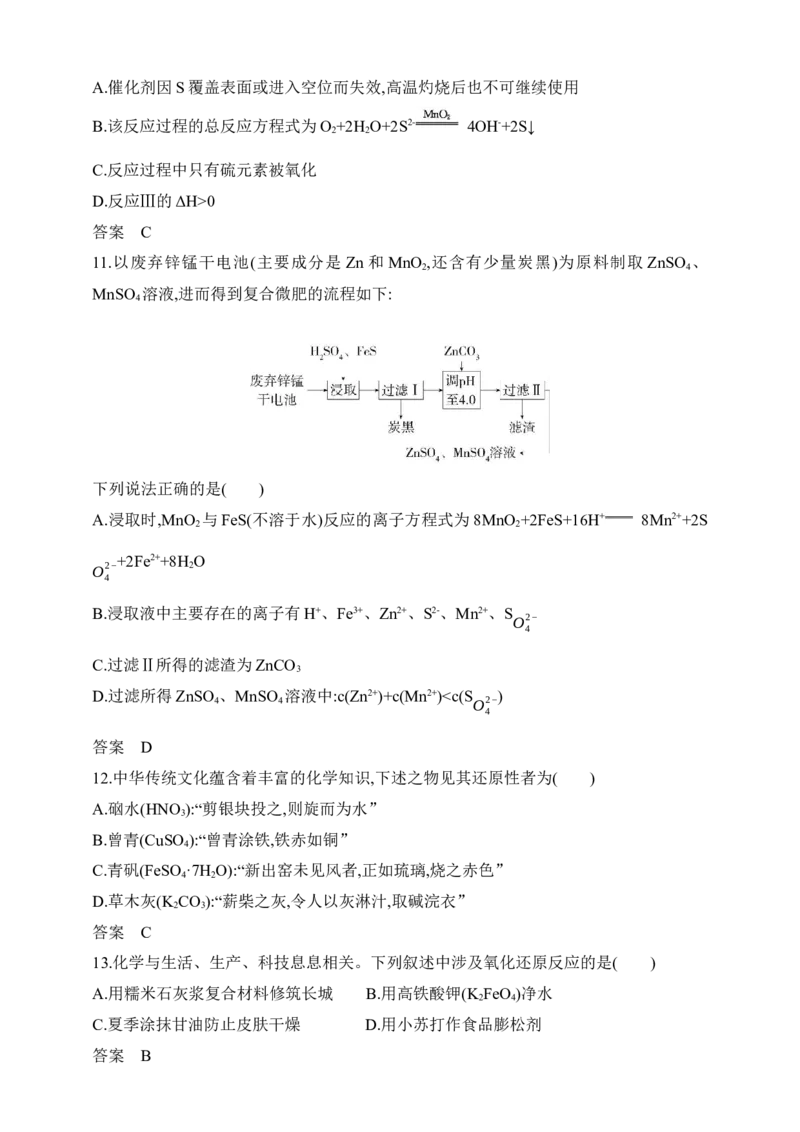
11.以废弃锌锰干电池(主要成分是 Zn 和 MnO ,还含有少量炭黑)为原料制取 ZnSO 、
2 4
MnSO 溶液,进而得到复合微肥的流程如下:
4
下列说法正确的是( )
A.浸取时,MnO 与FeS(不溶于水)反应的离子方程式为8MnO +2FeS+16H+ 8Mn2++2S
2 2
+2Fe2++8H O
O2− 2
4
B.浸取液中主要存在的离子有H+、Fe3+、Zn2+、S2-、Mn2+、S
O2−
4
C.过滤Ⅱ所得的滤渣为ZnCO
3
D.过滤所得ZnSO 、MnSO 溶液中:c(Zn2+)+c(Mn2+)