文档内容
专题突破卷 01 化学物质及其变化
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2024·湖北武汉第二中学高三6月模拟)化学与人类生活、生产、科技等密切相关。下列说法正确的
是
A.豆浆中加入石膏,使蛋白质变性制得豆腐
B.以淀粉为原料,可得到多种产品如白酒和食醋等
C.2023年诺贝尔化学奖授予量子点研究,直径为 硅量子点属于胶体
D.“神州十七号”使用砷化镓 太阳能电池,供电时 发生了电子转移
【答案】B
【解析】豆浆中加入石膏,发生聚沉制得豆腐,A错误;以淀粉为原料,水解得到葡萄糖,在酒化酶的作
用下可以得到白酒,发酵之后可以得到食醋,B正确;胶体属于混合物,直径为2~20nm硅量子点属于纯
净物,不是胶体,C错误;“神州十七号”使用砷化镓(GaAs)太阳能电池,供电时将太阳能转化为电能,
没有电子的转移,D错误。
2.(2023·江苏盐城期末)分类是科学研究的一种重要方法。下列物质分类正确的是( )
A.淀粉溶液和烟都是胶体
B.碱石灰、冰水混合物都是混合物
C.硫酸、纯碱、石膏是按酸、碱、盐排列的
D.NaCl、盐酸都是电解质
【答案】A
【解析】冰水混合物是纯净物,故B 错误;纯碱是碳酸钠,属于盐,故C 错误;盐酸是混合物,不是电
解质,故D 错误。
3.(2024·辽宁沈阳第一二〇中学高三第十次质量监测)下列关于物质的性质、用途等描述错误的是
A.工业上,用氯气和热的石灰乳制备漂白粉、漂粉精
B.在葡萄酒中添加适量的SO 能杀灭微生物并防止葡萄酒的氧化变质
2
C.储氢合金是一类能大量吸收H,并与H 结合成金属氢化物的材料
2 2
D.高铁酸钾(K FeO)在水处理过程中涉及的变化过程有:氧化还原反应、蛋白质变性、盐类水解、胶体聚
2 4
沉等
【答案】A【解析】工业上用氯气与冷的石灰乳作用制成漂白粉或漂粉精,方程式为:
2Ca(OH) +2Cl═CaCl +Ca(ClO) +2H O,A错误;二氧化硫具有还原性,并且可以杀菌、抗氧化,在葡萄酒
2 2 2 2 2
中添加适量的二氧化硫能杀灭微生物并防止葡萄酒的氧化变质,B正确;储氢合金是一类能大量吸收H,
2
并与H 结合成金属氢化物的材料,C正确;高铁酸钾具有强氧化性,能使蛋白质发生变性达到杀菌消毒的
2
作用,被还原生成铁离子在溶液中水解成生成氢氧化铁胶体,胶体吸附水中悬浮杂质聚沉而达到净水的作
用,则水处理过程中涉及的变化有氧化还原反应、蛋白质的变性、盐类的水解、胶体的聚沉等,D正确。
4.钛酸钙(CaTiO )材料制备原理之一是CaCO +TiO=====CaTiO +CO↑。下列有关判断不正确的是( )
3 3 2 3 2
A.TiO 和CO 属于酸性氧化物
2 2
B.CaCO 、CaTiO 均属于含氧酸盐
3 3
C.CaCO 属于强电解质
3
D.CO 溶于水可以导电,CO 为电解质
2 2
【答案】D
【解析】A项,TiO 和CO 与NaOH溶液反应只生成盐和水,故属于酸性氧化物,正确;D项,CO 与
2 2 2
HO反应生成电解质HCO,CO 属于非电解质,错误。
2 2 3 2
5.(2024·广东广州联考)下列事实与胶体性质无关的是( )
A.水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
B.向Fe(OH) 胶体中滴入稀硫酸,先看到红褐色沉淀生成,而后沉淀溶解
3
C.一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的“通路”
D.将植物油倒入水中用力搅拌形成油水混合物
【答案】D
【解析】烟尘属于胶体,直流电除尘是利用胶体的电泳性质,A不符合题意;向氢氧化铁胶体中滴入稀硫
酸,先发生胶体的聚沉,然后沉淀发生化学反应而溶解,B不符合题意;蛋白质溶液属于胶体,可以产生
丁达尔效应,C不符合题意;将植物油倒入水中,用力搅拌可以形成乳浊液,不是胶体,D符合题意。
6.(2024·江苏徐州睢宁第一中学高三大联考)在给定条件下,下列选项所示的物质间转化能实现的是
A.
B.
C.
D.
【答案】A【解析】氯化镁溶液可以与石灰乳反应得到氢氧化镁沉淀,煅烧氢氧化镁可以分解生成氧化镁,A符合题
意; 氯气与氢氧化钙反应生成次氯酸钙,次氯酸钙与过量SO 发生氧化还原反应,生成硫酸根和氯离子,
2
B不符合题意;铁与稀盐酸反应只能生成氯化亚铁,且氯化铁溶液蒸发过程中彻底水解得不到氯化铁固
体,C不符合题意;硫酸铜与氢氧化钠反应生成新制氢氧化铜,但是蔗糖中不含醛基是非还原糖,无法用
新制氢氧化铜检验,D不符合题意。
7.(2023·山东威海期末)下列有关物质分类正确的是( )
选项 A B C D
电解 Cu HClO NaCl NaOH
质
强电 HCl Ba(OH) Na O BaSO
2 2 4
解质
弱电 CH COOH SO Fe(SCN) 氨水
3 2 3
解质
非电 CO 蔗糖 NH 酒精
3
解质
【答案】C
【解析】Cu 是单质,不属于电解质,A错误;SO 属于非电解质,B错误;NaCl是电解质,Na O属于
2 2
强电解质,Fe(SCN) 属于弱电解质,NH 是非电解质,C正确;氨水属于混合物,D错误。
3 3
8.(2024·河南七市重点高中高三5月联合模拟)随着经济稳定发展,我国科学技术水平突飞猛进。下列
有关我国最新成果解读错误的是
选
最新成果摘录 化学解读
项
中国科学技术大学陈维教授团队成功构建可充电氢氯电池,电池能 放电时, 在负极区发生氧
A
在-70~40℃下运行 化反应
同济大学材料科学与工程学院许维教授团队首次合成由10个碳原 环型碳( )与 互为同素异
B
子组成的环型碳( ) 形体且含非极性键
南开大学材料科学与工程学院孙忠明教授课题组成功制备了全金属
金属富勒烯所含元素都是过渡
C
富勒烯 元素
中国科学院深圳先进技术研究院合成生物学研究所于涛研究员团队
D 合成过程发生了化学变化
实现用二氧化碳合成葡萄糖和蔗糖
【答案】C
【解析】放电时, 在负极区失去电子发生氧化反应,A正确;环型碳( )与 是C元素构成的不同单质,互为同素异形体且含C-C非极性键,B正确;金属富勒烯中的K、Sb都不是过渡元素,C错误;用二
氧化碳合成葡萄糖和蔗糖,合成过程发生了化学变化,D正确。
9.有些离子方程式能表示一类反应,有些离子方程式却只能表示一个反应。下列离子方程式中,只能表
示一个化学反应的是( )
①2Na+Cu2++2H O 2Na++Cu(OH) +H ↑
2 2 2
②SO +H O 2H++SO2−
3 2 4
③Ba2++2OH−+Cu2++SO2− BaSO ↓+Cu(OH) ↓
4 4 2
④CO2−+2H+ CO ↑+H O
3 2 2
⑤Ag++Cl− AgCl↓
A.③④ B.②③ C.③⑤ D.①④
【答案】B
【解析】①2Na+Cu2++2H O 2Na++Cu(OH) +H ↑ 可以表示Na 与可溶性铜盐
2 2 2
发生的一类反应;②SO +H O 2H++SO2−只能表示SO 与水发生的反应;
3 2 4 3
③Ba2++2OH−+Cu2++SO2− BaSO ↓+Cu(OH) ↓只能表示Ba(OH) 与CuSO
4 4 2 2 4
发生的反应;④CO2−+2H+ CO ↑+H O可以表示可溶性碳酸盐与强酸发生的一类
3 2 2
反应;⑤Ag++Cl− AgCl↓可以表示AgNO 与可溶性盐酸盐发生的一类反应。综合
3
以上分析,只有②③表示一个化学反应,故选B。
10.(2024·浙江金华第一中学高三模拟)在溶液中能大量共存的离子组是
A. 、 、 、
B. 、 、 、C. 、 、 、
D. 、 、 、
【答案】D
【解析】 和 生成弱电解质甲酸而不能大量共存,A不符合题意; 和 反应生成铬酸银
沉淀,B不符合题意; 和 反应生成氢氧化钙沉淀而不能大量共存,C不符合题意;选项中所给离
子相互都不反应,可以大量共存,D符合题意。
11.(2023·湖北荆州联考)某无色溶液中可能含有 、 、 、 、 、 中的一种或若干
Na+ Ba2+ Cl− Br− SO2− SO2−
3 4
种,依次进行下列实验(每一步所加试剂均过量),观察到的现象如下:
步骤 操作 现象
(1) 向溶液中滴加新制氯水,再加入CCl 振荡、静置 下层液体呈橙红
4
色
(2) 分液,向水溶液中加入Ba(NO ) 溶液和稀硝酸 有白色沉淀产生
3 2
(3) 过滤,向滤液中加入AgNO 稀溶液和稀硝酸 有白色沉淀产生
3
下列结论正确的是( )
A.肯定含有的离子是Na+、Br−
B.肯定没有的离子是 、
Ba2+ SO2−
4
C.如果步骤(2)中没有加入稀硝酸,白色沉淀中可能含有BaSO
3
D.如果将步骤(1)中新制氯水换成H O 溶液,对结论没有影响
2 2
【答案】A
【解析】由步骤(1)可知,溶液中一定存在 ;由步骤(2)可知,白色沉淀为 ,但 能被
Br− BaSO SO2−
4 3
氧化为 ,则 、 至少有一种,因 、 均与 不能大量共存,则一定没有 ;
SO2− SO2− SO2− SO2− SO2− Ba2+ Ba2+
4 3 4 3 4
由步骤(3)可知,白色沉淀为AgCl,步骤(1)中引入Cl−,不能确定原溶液是否含有Cl−,又因为溶液
呈电中性,一定存在阳离子,则一定存在 。综上所述,一定存在 、 , 、 至少存在一
Na+ Na+ Br− SO2− SO2−
3 4种,一定不存在Ba2+,不能确定的离子为Cl−,故选A。
12.(2024·广西贺州昭平部分学校高三一模)某安全气囊装置如图所示,其气体发生剂主要含有 、
、 等。已知产气时发生的反应为 ,该反应放出大量的热。下列说法错误
的是
A. 中含有离子键和极性共价键
B. 参与分解反应转移的电子数为
C. 在分解过程中既作氧化剂又作还原剂
D. 作氧化剂,消耗生成的金属钠
【答案】B
【解析】 是由铵根离子和硝酸根离子构成的,含有离子键,还含有氮氢、氮氧极性共价键,A正
确;反应中钠化合价由+1变为0,电子转移关系为 , (为0.2mol)参与分解反应转移
的电子数为0.1N ,B错误; 在分解过程中钠化合价降低、氮化合价升高,故既作氧化剂又作还原
A
剂,C正确;钠具有强还原性,会和氧化铁发生氧化还原反应,反应中 作氧化剂,消耗生成的金属
钠,D正确。
13.(2024·湖南长沙阶段练)“类比”与“类推”都是化学研究与推测物质性质的重要方法。下列有关
“类比”“类推”不正确的是( )A.NH 与HCl反应生成NH Cl,则H N —NH 可与HCl反应生成N H Cl
3 4 2 2 2 6 2
B.Na CO 溶液显碱性,则Na CS 溶液也显碱性
2 3 2 3
C.CH CH OH的沸点比CH CH 的沸点高,则苯酚的沸点比苯的沸点高
3 2 3 3
D.乙醇与足量酸性高锰酸钾溶液反应生成乙酸,则乙二醇与足量酸性高锰酸钾溶液反应生成乙二酸
【答案】D
【解析】NH 与HCl 反应生成NH Cl,H N —NH 相当于由2分子NH 脱去2个H 原子形成的,也
3 4 2 2 3
具有类似氨的性质,则 可与 反应生成 , 正确; 和 均能发生水
H N —NH HCl N H Cl A CO2− CS2−
2 2 2 6 2 3 3
解反应产生OH−,使溶液显碱性,B正确;乙醇的沸点高于乙烷的沸点是因为乙醇存在分子间氢键,而乙
烷不能形成氢键,同理苯酚也能形成分子间氢键,而苯不能形成氢键,因此苯酚的沸点比苯高,C正确;
乙醇与足量酸性高锰酸钾溶液反应生成乙酸,乙酸与高锰酸钾不反应,乙二醇与足量酸性高锰酸钾溶液反
应生成乙二酸,乙二酸具有还原性,可以继续与高锰酸钾反应最终生成二氧化碳,D错误。
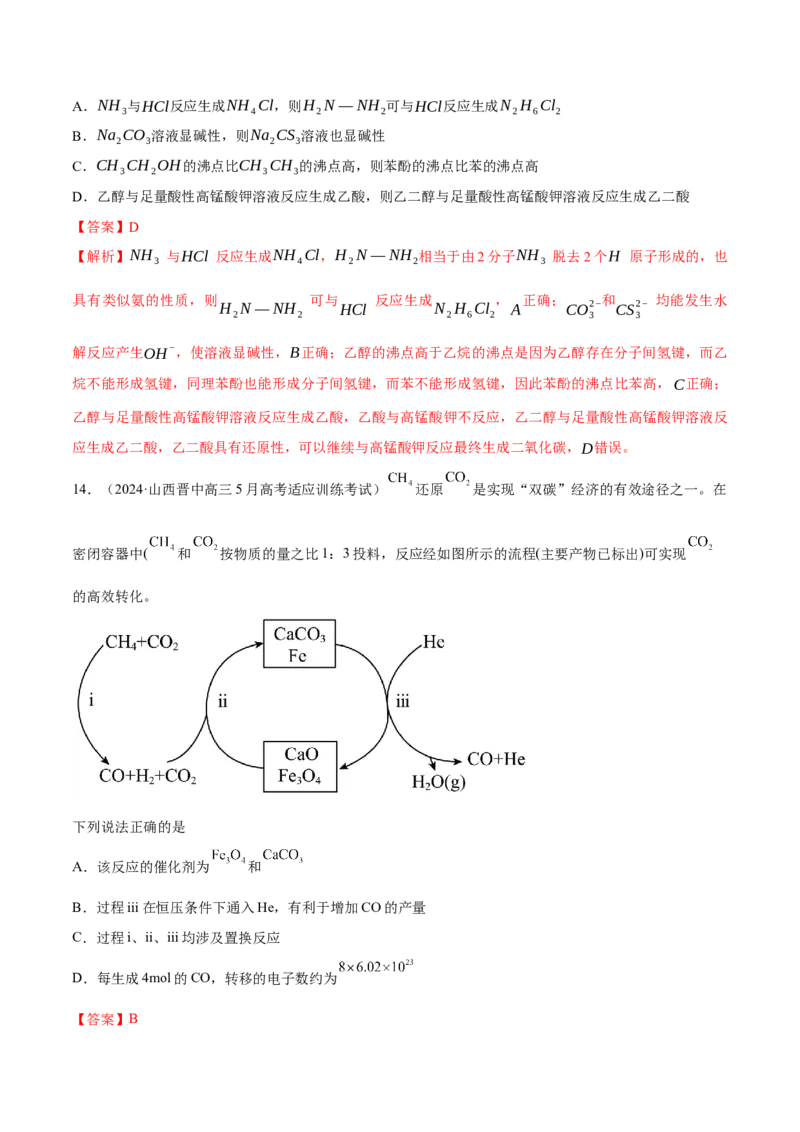
14.(2024·山西晋中高三5月高考适应训练考试) 还原 是实现“双碳”经济的有效途径之一。在
密闭容器中( 和 按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现
的高效转化。
下列说法正确的是
A.该反应的催化剂为 和
B.过程iii在恒压条件下通入He,有利于增加CO的产量
C.过程i、ii、iii均涉及置换反应
D.每生成4mol的CO,转移的电子数约为
【答案】B【解析】 是催化剂, 是中间产物,A错误;恒压条件下通入He, 分解平衡正向移动,
导致 增大,促进Fe还原CO 平衡正向移动,有利于增加CO的产量,B正确;过程i、iii中没有发
2
生置换反应,C错误;依流程图可知,该反应为 ,生成物CO既是氧化产物,
又是还原产物,每生成4mol的CO,转移的电子数约为 ,D错误。
15.某同学设计完成了以下两个实验:
①向盛有KI溶液的试管中加入少许CCl 后滴加氯水,CCl 层变成紫色。继续向试管中滴加氯水,振荡,
4 4
CCl 层会逐渐变浅,最后变成无色(生成了HIO )。
4 3
②向盛有KBr溶液的试管中加入少许CCl 后滴加氯水,CCl 层变成红棕色。继续向试管中滴加氯水,振
4 4
荡,CCl 层的颜色没有变化。
4
下列说法不正确的是( )
A.实验①生成HIO 时发生的反应为
3
I+5Cl+6HO===2HIO+10HCl
2 2 2 3
B.实验②中当CCl 层变成红棕色时可通过分液的方法获得Br 的CCl 溶液
4 2 4
C.由上述实验得出Cl、Br 、I 的氧化性由强到弱的顺序是Cl>Br >I
2 2 2 2 2 2
D.由上述实验得出Cl、HIO 、HBrO 的氧化性由强到弱的顺序是HBrO >Cl>HIO
2 3 3 3 2 3
【答案】C
【解析】①向盛有KI溶液的试管中加入少许CCl 后滴加氯水,CCl 层变成紫色,发生的反应为Cl+2I-
4 4 2
===I +2Cl-;继续向试管中滴加氯水,振荡,CCl 层会逐渐变浅,最后变成无色(生成了HIO ),说明氯气
2 4 3
可氧化碘单质,故A正确;向盛有KBr溶液的试管中加入少许CCl 后滴加氯水,CCl 层变成红棕色,发
4 4
生反应:Cl+2Br-===Br +2Cl-,溴单质易溶于四氯化碳,则可通过萃取分液的方法获得Br 的CCl 溶
2 2 2 4
液,故B正确;由氧化剂的氧化性强于氧化产物的氧化性可知,①中的氧化性强弱为Cl>I ,②中的氧化
2 2
性强弱为Cl>Br ,但不能比较Br 和I 的氧化性强弱,故C错误;由①②中的反应及氧化剂的氧化性强于
2 2 2 2
氧化产物的氧化性可知,Cl 能将I 氧化为HIO 而不能将Br 氧化为HBrO ,所以氧化性由强到弱的顺序是
2 2 3 2 3
HBrO >Cl>HIO,故D正确。
3 2 3
二、非选择题(本题包括4小题,共55分)
16.(13分)(2024·江苏南京高三阶段练习)四川广汉三星堆遗址发现了大量青铜器,如青铜面具、青铜神
树等。由于时间久远,青铜器表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、
O、CO 作用产生的,其化学式为Cu (OH) CO,请用学过的方法对其展开探究。
2 2 2 2 3(1)根据以上信息,可以获知Cu (OH) CO 的物理性质有________、________(选取其中两点)。
2 2 3
(2)从不同的物质分类标准角度分析,“铜绿”不属于________(填字母)。
A.铜盐 B.碳酸盐
C.碱式盐 D.碱
E.含氧酸盐 F.无氧酸盐
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式表达(注:
选写两个你认为可以实现的化学方程式,并且尽可能使得到的产物形态不同)。
①________________________________________________________________,
②________________________________________________________________。
(4)以“铜绿”为反应物可以实现以下物质转化:
铜绿――→CuCl ――→Cu(OH) ――→CuO――→Cu
2 2
反应④使用的是气体还原剂,且得到的产物之一可以使澄清石灰水变浑浊。请写出反应④的化学方程式:
___________________________________________。
【答案】(1)绿色 固体(答案合理即可)(2分)
(2)DF(2分)
(3)Cu (OH) CO=====2CuO+CO↑+HO(3分)
2 2 3 2 2
Cu (OH) CO+4HCl===2CuCl +3HO+CO↑(答案合理即可) (3分)
2 2 3 2 2 2
(4)CO+CuO=====Cu+CO(3分)
2
【解析】(1)由于时间久远,青铜器表面有一层“绿锈”,故 Cu (OH) CO 的物理性质有绿色、固体等。
2 2 3
(2)“铜绿”是碱式碳酸铜的俗称,Cu (OH) CO 中含有铜离子、碳酸根离子、氢氧根离子,故其属于铜盐、
2 2 3
碳酸盐、碱式盐、含氧酸盐。(3)Cu (OH) CO 中含有碳酸根离子、氢氧根离子,则其具有不稳定、受热易
2 2 3
分 解 的 化 学 性 质 , 能 和 盐 酸 等 酸 性 物 质 反 应 生 成 盐 和 水 , 相 应 反 应 的 化 学 方 程 式 为
Cu (OH) CO=====2CuO+CO↑+HO、Cu (OH) CO+4HCl===2CuCl +3HO+CO↑。(4)反应④为氧化铜
2 2 3 2 2 2 2 3 2 2 2
与CO反应生成单质铜和CO,反应的化学方程式为CO+CuO=====Cu+CO。
2 2
17.(13分)雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下离子中的若干种:NH、Ba2
+、Fe2+、Cl-、NO、CO、SO。某同学收集了该地区的雾霾,经必要的预处理后得到试样溶液,设计并完
成如下实验:
试回答下列问题:
(1)实验①中加入稀盐酸后,有无色气体A生成,溶液B依然澄清,且溶液中阴离子种类不变,据此可知原
溶液中一定不含________(填离子符号)。
(2)实验①中发生反应的离子方程式为___________________________________。
(3)实验②中逐滴加入碳酸氢钠溶液,立即有气泡产生,一段时间后又有沉淀出现,生成沉淀的离子方程式
为________________________________________________________。(4)气体F的成分为________(填化学式)。
(5)根据实验③现象该同学认为原溶液中一定含有 SO,有其他同学认为其结论不合理,又进行了后续实验
④,最终确认原溶液中含有SO,试写出实验④可行的操作方法及现象:
________________________________________________________________________。
【答案】(1)CO(2分)
(2)3Fe2++NO+4H+===3Fe3++NO↑+2HO(3分)
2
(3)Fe3++3HCO===Fe(OH) ↓+3CO↑(3分)
3 2
(4)NH (2分)
3
(5)向沉淀G中加入足量的稀硝酸,若沉淀部分溶解,则证明原溶液中含有SO(3分)
【解析】(1)实验①中加入稀盐酸后,有无色气体A生成,该气体可能为CO 或NO,由于稀盐酸过量且反
2
应后溶液中阴离子种类不变,则生成的气体为NO,则溶液中一定不存在CO,一定含有Fe2+、Cl-、NO,
且NO过量。(2)实验①中Fe2+与稀硝酸反应生成Fe(NO ) 、NO和HO,离子方程式为3Fe2++NO+4H+
3 3 2
===3Fe3++NO↑+2HO。(3)实验①加入足量稀盐酸,则溶液B中含有过量的H+,逐滴加入NaHCO 溶液
2 3
时,先发生的反应为H++HCO===H O+CO↑;H+反应完全后,此时溶液B中还含有Fe3+,继续滴加
2 2
NaHCO 溶液,铁离子与碳酸氢根离子发生相互促进的水解反应生成Fe(OH) 沉淀和CO 气体,离子方程式
3 3 2
为Fe3++3HCO===Fe(OH) ↓+3CO↑。(4)向溶液D中加入足量Ba(OH) 溶液后生成气体F、沉淀G和溶液
3 2 2
H,则气体F为NH 。(5)由于实验②中NaHCO 溶液足量,则实验③的沉淀G中一定含有BaCO 沉淀,不
3 3 3
能确定是否含有BaSO ,需要进行后续实验④,可向沉淀G中加入足量的稀硝酸,若沉淀部分溶解,则证
4
明原溶液中含有SO。
18.(14分)(2024·辽宁抚顺一中月考)钒性能优良,用途广泛,有“金属维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分为VO)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应
2 5
的化学方程式是_____________________________________。
(2)向上述所得溶液中加入KClO 溶液,完善并配平反应的离子方程式:
3
ClO+VO2++__________===Cl-+VO+__________。
(3)V O 能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与NaSO 溶液反应从而被吸收,则SO、Cl
2 5 2 3
-、VO2+还原性由大到小的顺序是________________。
(4)在20.00 mL c(VO)=0.1 mol·L-1的溶液中,加入 0.195 g锌粉,恰好完全反应,则还原产物可能是
__________(填标号)。
a.VO2+ b.V2+ c.V
【答案】(1)V O+KSO +2HSO ===2VOSO +KSO +2HO(2分)
2 5 2 3 2 4 4 2 4 2
(2)1(1分) 6(1分) 3(1分) HO(1分) 1(1分) 6(1分) 6(1分) H+(1分)
2
(3)SO、Cl-、VO2+(2分)(4)b(2分)
【解析】(1)由题意知,VO 与稀硫酸、亚硫酸钾反应可生成VOSO 和KSO ,根据质量守恒知生成物中还
2 5 4 2 4
有水,化学反应方程式为VO +KSO +2HSO ===2VOSO +KSO +2HO。(2)ClO与VO2+反应生成Cl-
2 5 2 3 2 4 4 2 4 2
和VO,氯元素的化合价由+5降低到-1,V元素的化合价由+4升高到+5,由得失电子守恒知,ClO和
Cl-的化学计量数为1,VO2+和VO的化学计量数为6,结合电荷守恒和元素守恒配平该离子方程式为ClO
+6VO2++3HO===Cl-+6VO+6H+。(3)V O 与盐酸反应生成VO2+,V元素的化合价降低,则HCl中Cl
2 2 5元素的化合价升高,产生的黄绿色气体为Cl ,由还原剂的还原性大于还原产物的还原性知,还原性Cl-
2
>VO2+,氯气与NaSO 反应生成NaCl、NaSO ,NaSO 作还原剂,则还原性SO>Cl-,故SO、Cl-、VO2
2 3 2 4 2 3
+还原性由大到小的顺序为SO>Cl->VO2+。(4)0.195 g锌粉的物质的量为=0.003 mol,设V元素在还原产
物中的化合价为x,根据氧化剂得电子总数等于还原剂失电子总数得 0.003×2=0.02×0.1×(5-x),解得x=
+2,则还原产物为V2+。
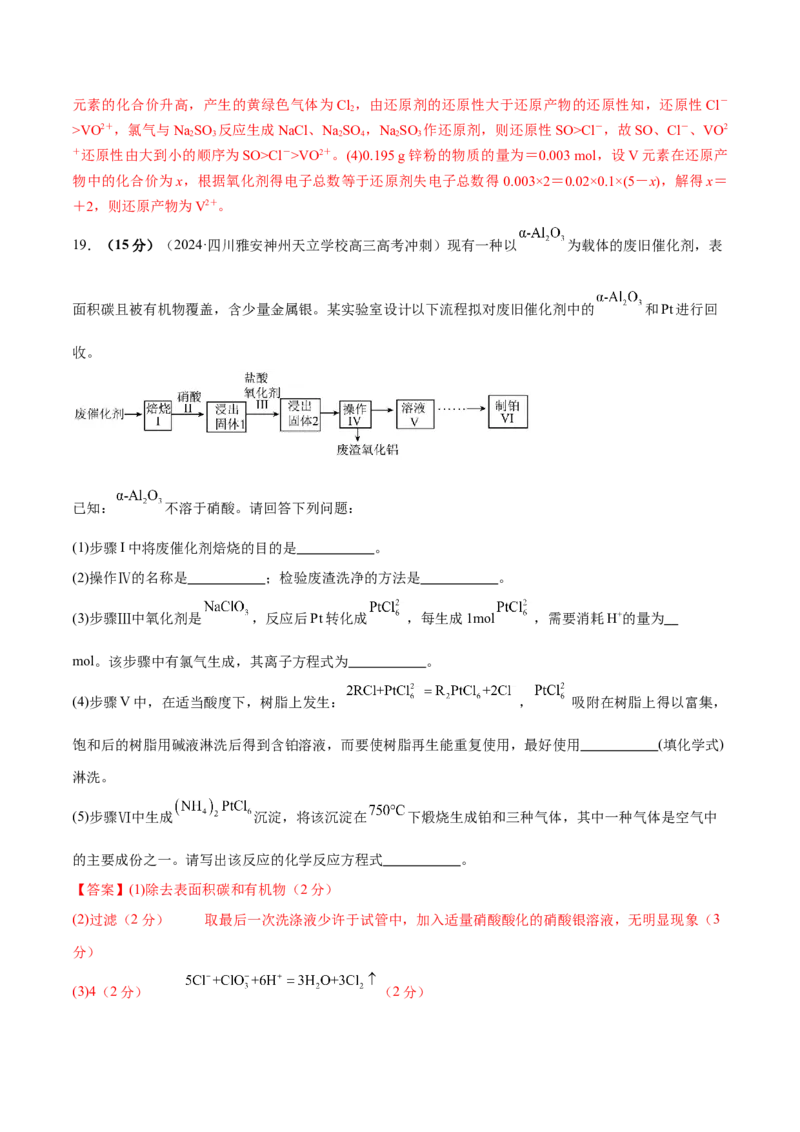
19.(15分)(2024·四川雅安神州天立学校高三高考冲刺)现有一种以 为载体的废旧催化剂,表
面积碳且被有机物覆盖,含少量金属银。某实验室设计以下流程拟对废旧催化剂中的 和Pt进行回
收。
已知: 不溶于硝酸。请回答下列问题:
(1)步骤I中将废催化剂焙烧的目的是 。
(2)操作Ⅳ的名称是 ;检验废渣洗净的方法是 。
(3)步骤Ⅲ中氧化剂是 ,反应后Pt转化成 ,每生成1mol ,需要消耗H+的量为
mol。该步骤中有氯气生成,其离子方程式为 。
(4)步骤V中,在适当酸度下,树脂上发生: , 吸附在树脂上得以富集,
饱和后的树脂用碱液淋洗后得到含铂溶液,而要使树脂再生能重复使用,最好使用 (填化学式)
淋洗。
(5)步骤Ⅵ中生成 沉淀,将该沉淀在 下煅烧生成铂和三种气体,其中一种气体是空气中
的主要成份之一。请写出该反应的化学反应方程式 。
【答案】(1)除去表面积碳和有机物(2分)
(2)过滤(2分) 取最后一次洗涤液少许于试管中,加入适量硝酸酸化的硝酸银溶液,无明显现象(3
分)
(3)4(2分) (2分)(4)HCl(2分)
(5) (2分)
【解析】废旧催化剂(含有 、Pt、Ag)进行焙烧Ⅰ,除去表面的积炭和有机物;然后加硝酸进行浸
取,Ag溶于硝酸, 、Pt不溶,过滤后得到浸出固体1;加入盐酸和氧化剂 ,反应后Pt转化
成 ,过滤后得到废渣氧化铝和含有 的溶液;用树脂提取 , 吸附在树脂上得以富
集,饱和后的树脂用碱液淋洗后得到含铂溶液,经过一系列处理生成 沉淀,将该沉淀在
下煅烧生成铂等。(1)废旧催化剂,表面积碳且被有机物覆盖,则步骤I中将废催化剂焙烧的目的
是:除去表面积碳和有机物。(2)由分析可知,操作Ⅳ用于分离氧化铝和含有 的溶液,名称是过
滤;检验废渣是否洗净时,也就是检验洗涤液中是否溶有Cl-,方法是:取最后一次洗涤液少许于试管中,
加入适量硝酸酸化的硝酸银溶液,无明显现象。(3)步骤Ⅲ中氧化剂是 ,反应后Pt转化成
,发生反应的离子方程式为2 +3Pt+12H++16Cl-=3 +6H O,则每生成1mol ,需要消耗H+的
2
量为4mol。该步骤中有氯气生成,则Cl 来自 与Cl-在酸性条件下的反应,其离子方程式为
2
。(4)步骤V中,在适当酸度下,树脂上发生:
, 吸附在树脂上得以富集,饱和后的树脂用碱液淋洗后得到含铂溶液,
而要使树脂再生能重复使用,需将ROH转化为RCl,最好使用HCl淋洗。(5) 在 下煅
烧生成铂和三种气体,其中一种气体是空气中的主要成份之一,则其为N,从得失电子守恒考虑,
2中的N元素只能有一部分转化为N,另一部分价态不变,所以产物中有NH ,则另一种气体
2 3
为HCl,该反应的化学反应方程式为 。